Neuronavegação e Endoscopia como Ferramentas Adjuvantes na Revisão do Implante do Assoalho Orbital: Tratamento Cirúrgico do Implante do Assoalho Orbital Infectado e Mal Colocado com Fístula Palpebral Crônica e Sinusite
Main Text
Table of Contents
As fraturas do assoalho orbitário representam sequelas comuns de trauma facial que podem resultar em consequências funcionais e estéticas significativas. Este artigo apresenta uma visão abrangente do manejo de um caso de revisão envolvendo uma fratura do assoalho orbital, com foco nas complicações relacionadas ao hardware orbital extrudado e infectado. Além disso, erros comuns que envolvem colocação inadequada do implante do assoalho orbital, dimensionamento inadequado do implante e falta de fixação adequada do implante são discutidos.
O caso apresentado envolve cicatrização tardia de feridas e uma fístula cutânea sino-orbital (SOCF) devido a hardware orbital infectado de um reparo anterior de fratura do assoalho orbital. A discussão gira em torno do planejamento pré-operatório, incluindo a escolha da abordagem cirúrgica (transconjuntival com cantotomia lateral) e do material do implante. A neuronavegação intraoperatória foi utilizada como uma ferramenta adjuvante para confirmar a posição do implante orbital recém-colocado. Este caso fornece informações valiosas sobre complicações evitáveis para este procedimento, nuances na abordagem cirúrgica e desafios incomuns enfrentados pelos profissionais que realizam reparo cirúrgico de trauma facial.
Fratura orbital; assoalho orbital; abordagem transconjuntival; infecção de hardware; implante orbital; Medpor; polietileno; titânio; fístula palpebral.
A pneumo-órbita, envolvendo ar na cavidade orbital, geralmente decorre de conexões seio-órbita após trauma orbital. Embora esses casos geralmente cicatrizem espontaneamente após o reparo da fratura, as fístulas persistentes indicam problemas subjacentes. Os relatos de casos destacam a fístula cutânea sino-orbital (SOCF) de implantes de trauma orbital não autólogo. 1–3 Nesse caso, o deslocamento incorreto do hardware no complexo osteomeatal maxilar levou à obstrução contínua do seio nasal, criando uma passagem anômala para a pele da pálpebra inferior enfraquecida pelo hardware infectado. Abordar esse cenário desafiador é crucial para restaurar a anatomia óssea normal e prevenir complicações semelhantes no futuro.
Um homem de 34 anos inicialmente procurou atendimento para drenagem recorrente crônica sob o olho direito, decorrente de uma fratura orbital direita há sete anos devido a agressão. A fratura foi inicialmente reparada com redução aberta e fixação interna em outra instituição. Desde então, ele experimentou drenagem purulenta intermitente da cavidade nasal direita e uma fístula da pálpebra inferior. Ele também observou movimento de ar através do local da incisão anterior ao assoar o nariz e diplopia de início tardio com enoftalmia. Após a cirurgia inicial, o paciente foi submetido a vários cursos de antibióticos com melhora dos sintomas crescentes e minguantes.
O exame físico revelou uma deiscência de pele de 3 cm na borda infraorbitária com crostas e drenagem purulenta à palpação. Eritema leve foi observado ao longo da pele da borda infraorbital direita no local da fístula. O paciente relatou discreta diminuição da sensibilidade da V2 direita. Diplopia foi observada nos olhares primário e direcional, e os movimentos extraoculares estavam intactos com acuidade visual preservada. A endoscopia nasal revelou drenagem purulenta do meato médio direito.
A imagem maxilofacial por tomografia computadorizada (TC) revelou hardware anterior deslocado ao longo do assoalho orbital direito (Figura 1-3). O seio maxilar direito exibia opacificação completa, indicando sinusite maxilar crônica presumida e obstrução do complexo osteomeatal. Defeitos ósseos persistentes foram observados na parede orbital medial e no assoalho orbitário. Na incidência sagital, o implante foi deslocado para o seio maxilar, não reconstruindo o defeito do assoalho orbitário posterior. A incidência axial mostrou o implante do assoalho orbital estendendo-se além da borda infraorbital, com uma bolsa de ar ao redor de um parafuso, sugerindo falha de hardware com infecção.
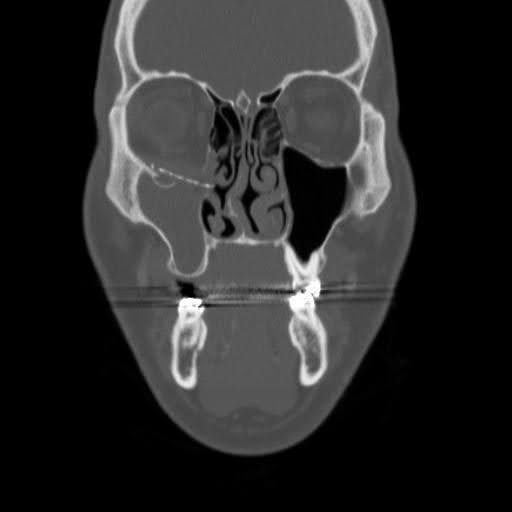
Figura 1. Tomografia computadorizada coronal pré-operatória sem contraste. Imagem de TC demonstrando deslocamento inferior da face medial do implante do assoalho orbital e a conexão entre os seios paranasais e a cavidade orbitária.
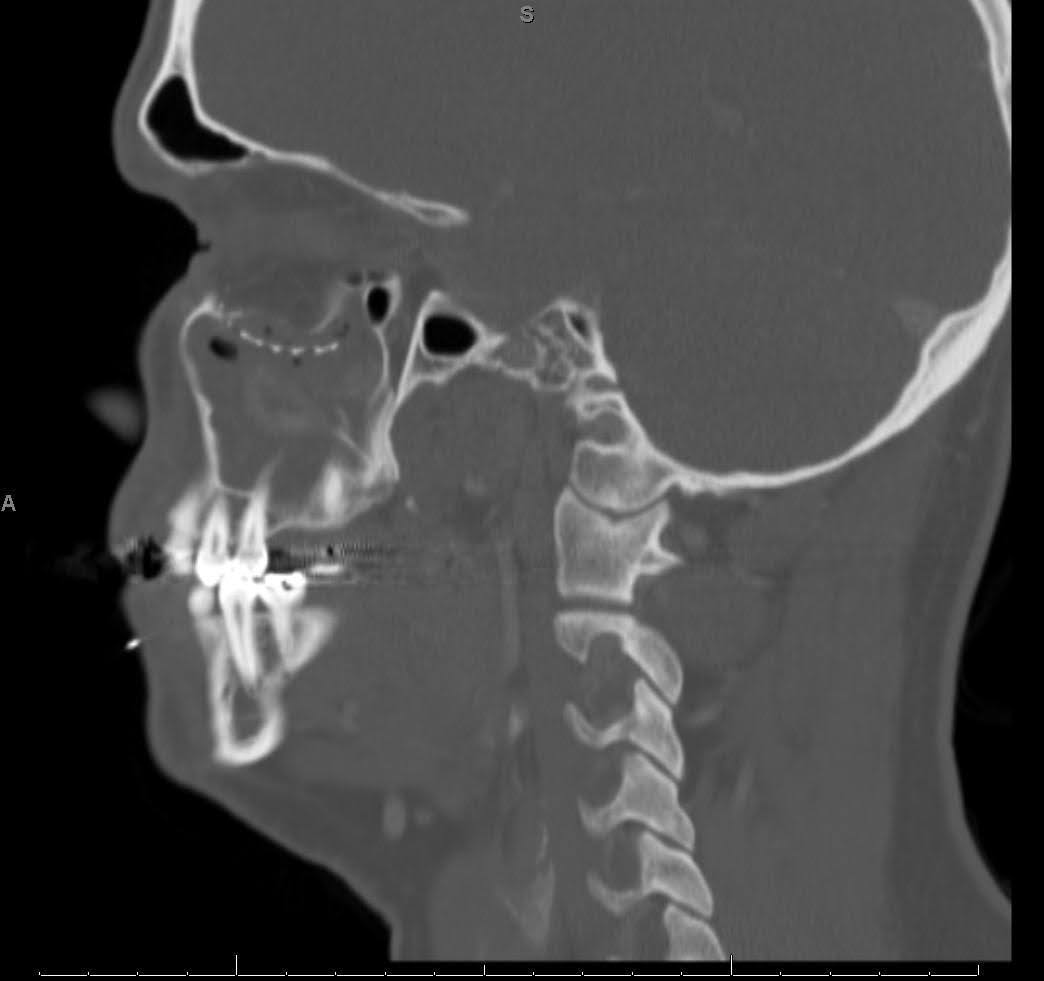
Figura 2. Tomografia computadorizada sagital sem contraste pré-operatória.Imagem de TC demonstrando deslocamento inferior do implante do assoalho orbitário para o seio maxilar, bem como assentamento posterior inadequado no assoalho orbital residual.
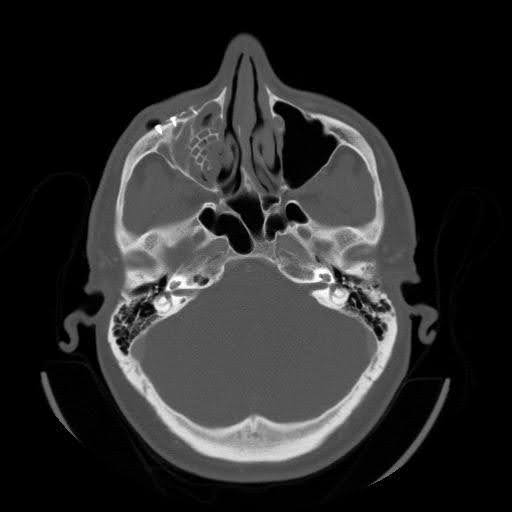
Figura 3. Tomografia computadorizada axial sem contraste pré-operatória.Imagem de TC demonstrando ar livre adjacente ao parafuso lateral na borda orbital.
A investigação do trauma orbital requer um exame físico completo com foco nas deformidades externas, juntamente com um exame oftalmológico e neurológico abrangente. A imagem pré-operatória com tomografia computadorizada sem contraste de corte fino auxilia na tomada de decisão intraoperatória. Quando integrada à neuronavegação, a TC auxilia na diferenciação de pontos de referência, particularmente na anatomia distorcida.
A principal prioridade era eliminar a fonte de infecção em andamento, removendo o hardware comprometido. Em seguida, abordar a diplopia persistente restaurando o volume orbital pré-mórbido foi crucial. A terceira prioridade concentrou-se na resolução do bloqueio da via de drenagem do seio maxilar que leva à sinusite maxilar persistente. O objetivo final abrangeu abordar a cicatriz palpebral resultante da fístula e melhorar a estética.
Os pacientes que apresentam infecções por hardware após mais de um mês de pós-operatório, especialmente aqueles que falharam em vários ciclos de antibióticos, geralmente se beneficiam da remoção completa do hardware devido à potencial formação de biofilme. 4 A intervenção cirúrgica é frequentemente recomendada para pacientes com diplopia persistente e mau posicionamento do globo ocular com duração superior a 1 a 3 meses, conforme recomendado por autores seniores (TL, DS).
A cirurgia orbital de revisão pode não ser necessária se a infecção do hardware responder a antibióticos no primeiro mês após a cirurgia, antes da formação do biofilme. Em casos de trauma orbital grave, como hemorragia intraconal ou descolamento de retina, a cirurgia é contraindicada para minimizar o risco de lesão orbital intraoperatória adicional por retração do globo ocular.
O paciente, neste caso, foi submetido a 1) remoção de hardware orbital com abordagem pós-septal, transconjuntival e cantotomia lateral, 2) substituição do implante de assoalho orbital usando implante de Medpor-titânio com neuronavegação, 3) antrostomia maxilar conservadora com remoção de tecido e 4) excisão de fístula palpebral com fechamento de avanço tecidual local.
A região facial do paciente foi coberta com a órbita contralateral exposta para avaliar a simetria. Lidocaína e epinefrina foram injetadas para hemostasia e hidrodissecção dos planos teciduais, particularmente na borda orbitária, onde ocorreu a amarração ao redor da fístula. O autor sênior (TL), por uma questão de preferência, opera com um escudo corneano. Posteriormente, foi realizada uma cantotomia lateral para aumentar a exposição e mobilizar a pálpebra inferior.
As fraturas do assoalho orbitário são geralmente abordadas por meio de abordagens transconjuntivais ou transcutâneas. Incisões transcutâneas, como as abordagens subciliar, subtarsal e da borda orbital, representam um risco maior de ectrópio pós-operatório. 5–8 Em contraste, a abordagem transconjuntival é preferida devido à sua evitação de incisões externas, resultando em taxas mais baixas de ectrópio ou retração, preservando a inervação do músculo orbicular. 9, 10
Os autores seniores (TL, DS) favorecem uma incisão transconjuntival em um plano pós-septal até a borda orbital. Embora esse plano de dissecção seja considerado mais simples, não há diferença estatisticamente significativa nas taxas de entrópio, ectrópio, sensação de corpo estranho e formação de cicatrizes. 9 Na abordagem transconjuntival, a preservação da placa tarsal é crucial. A incisão deve ser feita próxima à borda infraorbitária, com a pálpebra inferior retraída com afastador de Desmarres. Se a incisão for medial ao punctum, é necessário cuidado para evitar lesões no canalículo e no sistema lacrimal. Ficar perto da carúncula ou fazer a transição para uma incisão transcaruncular pode ajudar a mitigar o risco de danos.
Neste caso, a identificação do plano do tecido subperiosteal através da incisão transconjuntival foi difícil devido à fibrose e aderências da infecção prévia ao longo da borda infraorbitária. Para resolver isso, o local da cantotomia lateral foi usado para identificar inicialmente o plano do tecido subperiosteal ao longo da parede orbital lateral, que foi então transportado centralmente para a incisão transconjuntival. Mais profundamente no plano pós-septal, a pálpebra de Jaeger e os afastadores maleáveis facilitaram a retração da gordura orbital posteriormente durante a dissecção até a borda infraorbital. O implante do assoalho orbital foi descoberto dentro do seio maxilar, e um elevador periosteal # 9 foi usado para levantar o conteúdo orbital, dissecando imediatamente superficialmente ao implante deslocado. Essa manobra permitiu que um maleável varresse o conteúdo orbital herniado superiormente, identificando o osso orbital periférico estável. O desbridamento dos fragmentos ósseos do seio maxilar foi realizado com cuidado para preservar o nervo infraorbital e os músculos extraoculares.
A endoscopia nasal revelou extrusão de hardware medialmente abaixo do processo uncinado, formando uma fístula anormal conectando as cavidades nasal, maxilar e orbital. A consideração da megaantrostomia maxilar ipsilateral foi debatida, mas foi adiada devido às preocupações com o aumento da comunicação orbitonasal e exposição do implante. Em vez disso, uma sinusotomia maxilar conservadora foi realizada estendendo a abertura natural do seio maxilar inferiormente para evitar a recirculação com planos de tomografia computadorizada seriada para possível futura cirurgia definitiva do seio maxilar se a sinusite recorrer.
Após a remoção do implante anterior, foi observada herniação significativa do conteúdo orbital no seio a partir do assoalho orbital e defeito da parede orbital medial. Um novo implante de assoalho orbital foi colocado, estabilizado pela identificação de bordas ósseas posteriores e mediais sólidas com neuronavegação.
Um implante de titânio revestido com polietileno (Medpor) foi escolhido para evitar contratura cicatricial periorbital associada a titânio nu. O implante foi embebido em Betadine, contornado para se ajustar à curvatura natural da órbita e aparado para estabilidade sem se estender além da borda infraorbital. A neuronavegação na visão coronal garantiu o posicionamento adequado. Os parafusos e o implante foram colocados atrás da borda infraorbital, com um parafuso normalmente suficiente, ancorado através do implante do assoalho orbital. Devido ao defeito quase total do assoalho orbital, uma ponta que se estende do implante foi usada para prender o implante. Nos casos de assoalho orbitário estável inadequado, os parafusos devem ser colocados em regiões com pele mais espessa, como ao longo da parede lateral nasal ou borda orbital lateral. A endoscopia nasal pós-reimplante confirmou o posicionamento adequado, resolvendo o deslocamento medial inicial bloqueando a via de drenagem do seio maxilar.
Antes do fechamento, as bordas da fístula palpebral cutânea foram excisadas e o avanço tecidual local levantou a contratura da cicatriz palpebral da borda infraorbitária. O tendão cantal lateral foi reaproximado ao tubérculo de Whitnall com náilon transparente 4-0.
Para reduzir o risco de entrópio, a sutura absorvível (intestino absorvível rápido 5-0 neste caso) foi usada pelo autor sênior (TL) para o fechamento da incisão transconjuntival, que é uma questão de preferência do cirurgião.
O paciente foi observado durante a noite e recebeu alta no dia seguinte. A tomografia computadorizada pós-operatória imediata (Figuras 4–6) confirmou o posicionamento adequado do hardware orbital. Precauções sinusais (evitar assoar o nariz, pressionar ou aumentar a pressão intratorácica) foram aconselhadas para evitar possíveis comprometimentos vasculares e visuais devido ao ar orbital aprisionado involuntariamente, e Augmentin foi prescrito por 7 dias. Devido à fístula naso-orbitária pré-existente, as irrigações sinusais foram adiadas.
No seguimento de 8 meses, o paciente relatou melhora significativa da diplopia, com movimentos extraoculares intactos e sem recorrência de fístula palpebral ou sinusite. O progresso clínico será monitorado com imagens seriadas de tomografia computadorizada dos seios paranasais para possível recorrência da sinusite maxilar.
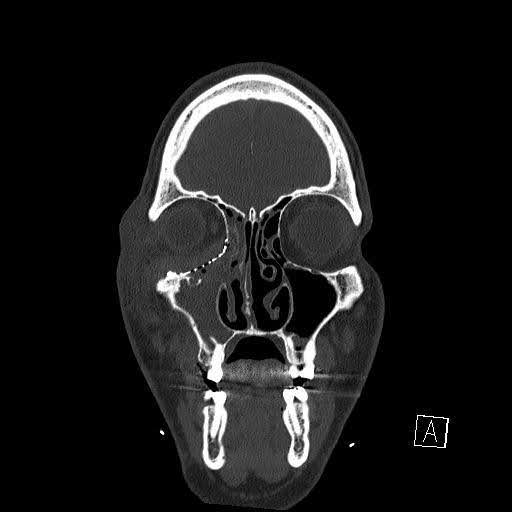
Figura 4. Tomografia computadorizada coronal sem contraste no 1º dia de pós-operatório imediato. Imagem de TC demonstrando a presença de opacificação persistente precoce no seio maxilar direito.
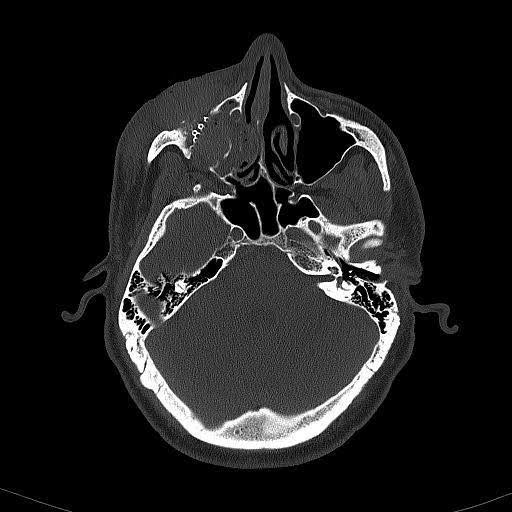
Figura 5. Pós-operatório imediato 1º dia de tomografia computadorizada axial sem contraste. Imagem de TC demonstrando o novo implante de assoalho orbital, que não se estende além da borda infraorbitária.
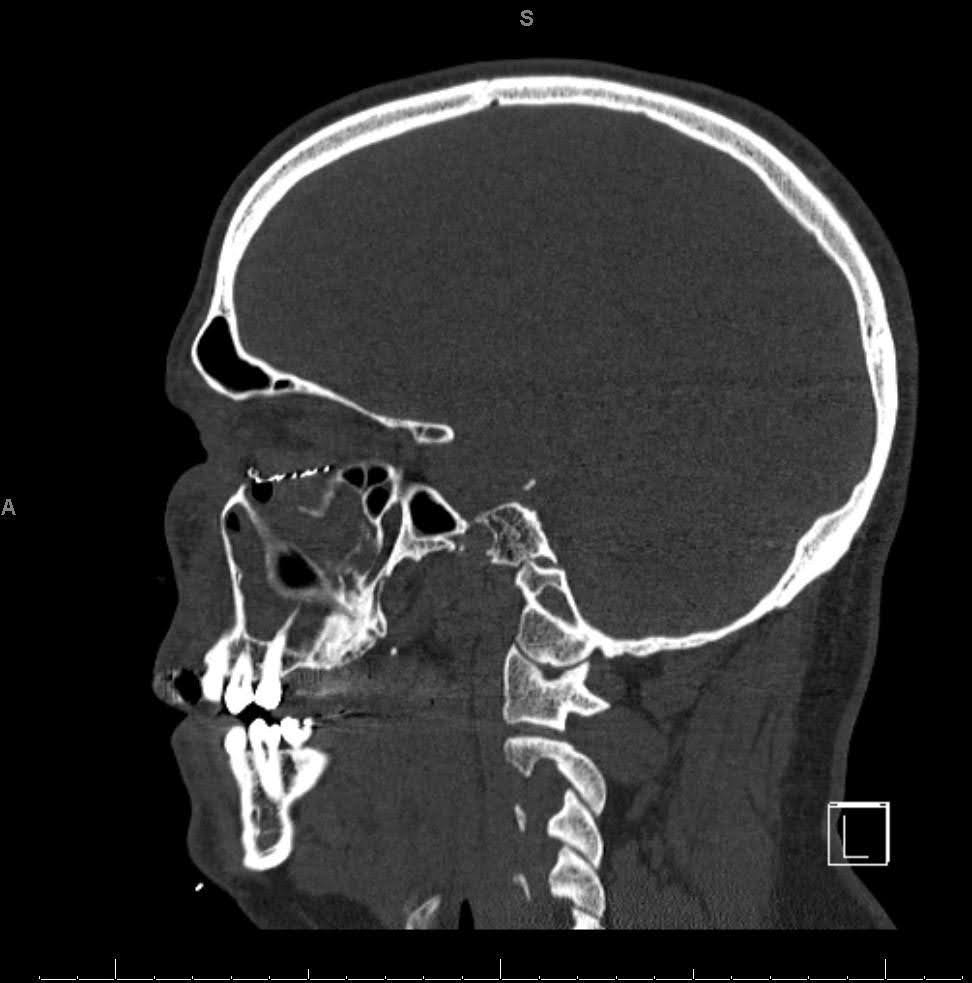
Figura 6. Tomografia computadorizada sagital sem contraste no 1º dia de pós-operatório imediato. Imagem de TC demonstrando o posicionamento adequado do implante do assoalho orbitário com a porção posterior apoiada acima de uma borda estável do osso orbital posterior.
Este caso apresentou uma SOCF tardia resultante de mau posicionamento de hardware, exigindo remoção de hardware infectado, restauração da anatomia nativa e correção de diplopia.
As indicações cirúrgicas para reparo do assoalho orbital incluem: 1) aprisionamento do músculo extraocular com ou sem reflexo oculocardíaco, 2) globo ocular mal posicionado com diplopia persistente, 3) diplopia com defeito orbital (maior que 2–3 cm2 com pelo menos 3 mm de deslocamento) e enoftalmia resultante ou fratura envolvendo mais de 50% do assoalho orbital, 4) hardware orbital extrudado ou infectado, e 5) uma SOCF persistente que não se resolve com o tratamento conservador. 11–15
As complicações tardias da cirurgia orbital, decorrentes do atraso na cicatrização da ferida, fibrose e contratura cicatricial, abrangem um espectro de problemas que geralmente requerem cirurgia de revisão. Essas complicações incluem ectrópio, entrópio, falha de hardware, infecções crônicas, formação de fístula, parestesias persistentes e lagoftalmia. A contratura cicatricial e o encurtamento lamelar de várias abordagens cirúrgicas podem causar ectrópio e entrópio. 16 A abordagem transconjuntival, preservando o tarso, é preferida para pacientes com vetor negativo, reduzindo o risco de formação de ectrópio.
A diplopia persistente, ocorrendo em 8 a 52% dos casos durante semanas de pós-operatório, é exacerbada por edema pré-operatório, fibrose intrínseca, isquemia muscular, inflamação e colocação inadequada do implante, causando impacto do músculo extraocular. 5,7,17 Os exames de imagem auxiliam na identificação das causas da diplopia. Se o volume orbital pós-operatório for normal, a observação permite uma possível compensação do sistema nervoso central. Nesse caso, a diplopia persistente resultou da colocação, forma e tamanho inadequados do implante, causando volume orbital inadequado. Diferente do mau posicionamento do globo ocular, lesões traumáticas nos nervos cranianos ou músculos extraoculares também podem causar diplopia prolongada com estrabismo. Depois de restaurar o volume orbital adequado e a posição do globo, um especialista em estrabismo é essencial para avaliar e tratar a diplopia dessas lesões.
Outra complicação tardia inclui enoftalmia tardia (ocorrendo em 7–27% dos casos no pós-operatório) e hipoglobus, que podem surgir gradualmente devido a déficits teciduais de desvascularização e isquemia prévias. 5,12,18 No entanto, uma causa mais comum, como observado neste caso, é a expansão aberrante da cavidade orbitária com deslocamento do implante ou dimensionamento inadequado. O tratamento eficaz da enoftalmia tardia apresenta desafios e pode exigir a substituição ou aumento do implante para restaurar o volume orbital adequado. 5
Estudos recentes enfatizam as vantagens dos implantes individualizados criados por meio de impressão 3D seletiva com resultados aprimorados e taxas de revisão mais baixas comparáveis à neuronavegação intraoperatória. 19,20 As desvantagens incluem aumento de custo e atrasos de fabricação de algumas semanas. 20 A decisão entre implantes individualizados e não individualizados deve ser adaptada. O autor sênior (TL) normalmente reserva implantes de assoalho orbital personalizados para pacientes com fraturas zigomático-maxilares complexas e fraturas concomitantes do assoalho orbital que requerem correção simultânea do achatamento malar.
Para evitar complicações orbitais, é crucial evitar erros comuns durante a cirurgia inicial. Descreveremos brevemente os fatores potenciais que podem ter contribuído para as complicações observadas neste paciente. A exposição inadequada pode ter desempenhado um papel significativo para este paciente. O implante orbital deve idealmente repousar sobre o assoalho orbital posterior e/ou lateral estável e uma parede orbital medial estável. O defeito significativo da parede orbital medial de nosso paciente, estendendo-se posteriormente, provavelmente não foi exposto adequadamente. Em casos como esse, uma incisão transcaruncular posterior ao ducto nasolacrimal, além de uma abordagem transconjuntival, pode ser necessária para a exposição adequada da parede orbital medial. A dissecção subperiosteal cautelosa minimiza a lesão durante a dissecção superior ao longo da parede orbital medial, onde a identificação de artérias como a etmoidal anterior e a etmoidal posterior é crucial. Permanecer no plano subperiosteal também é fundamental para preservar estruturas como o músculo oblíquo inferior durante a dissecção intraorbital.
Da mesma forma, a fratura se estende extensivamente posteriormente ao longo do assoalho orbital, e essa região provavelmente permaneceu inadequadamente exposta. Isso é evidente a partir do deslocamento inferior do implante para o seio maxilar. Dada a presença de nervos cranianos cruciais e músculos extraoculares no ápice orbital, há uma hesitação e ansiedade naturais associadas à dissecação nessa área. O uso da neuronavegação, particularmente em casos de revisão, adiciona uma camada adicional de segurança e certeza, especialmente ao lidar com anatomia significativamente alterada. A exposição insuficiente da fratura leva à redução incompleta e a possíveis complicações, incluindo o deslocamento dos implantes para o seio, resultando em mau posicionamento do globo ocular ou aprisionamento do tecido orbital. Isso, por sua vez, pode levar a limitações na motilidade extraocular devido à amarração dos músculos extraoculares.
Ao projetar a forma do implante, é importante estar atento à curva em S suave do assoalho orbital natural quando visto em um plano sagital. O piso desce imediatamente posterior à borda e, em seguida, sobe suavemente para cima, mais perto do ápice orbital. Ao longo do assoalho orbital medial, há uma transição suave para a parede orbital medial. Infelizmente, parece que o implante do assoalho orbital original não seguiu esses contornos, resultando na reconstrução de uma parte do defeito do assoalho orbital sem o componente da parede orbital medial. Isso provavelmente contribuiu ainda mais para a sinusite crônica e a formação de fístula palpebral depois que o componente medial do implante orbital obstruiu o complexo osteomeatal natural que permite a drenagem adequada do seio maxilar. Uma vez que a sinusite crônica se desenvolveu, a colonização bacteriana se desenvolveu ao longo do aspecto orbital do implante e contribuiu ainda mais para a infecção periorbital contínua.
Em relação ao dimensionamento do implante, é importante moldá-lo de forma que o implante fique posterior à borda infraorbital para evitar a erosão do hardware através da pálpebra inferior. É melhor evitar a colocação excessiva de hardware ao longo da superfície anterior da borda infraorbital para evitar a palpabilidade do implante, cicatrizes indesejáveis e/ou exposição do hardware como observado neste paciente em particular. Em relação às dimensões anterior e posterior do implante do assoalho orbital, o implante deve ser suficientemente longo para alcançar o osso estável localizado posteriormente, tomando cuidado para evitar colidir com o conteúdo do ápice orbital. Durante o processo de dimensionamento e modelagem do implante, a neuronavegação pode ajudar a identificar o osso orbital medial, posterior e lateral estável para implantação. Após a colocação de um novo implante de assoalho orbital, uma sonda de neuronavegação pode ser usada para traçar o contorno do novo hardware do assoalho orbital para garantir a forma, o posicionamento e a estabilidade adequados no intraoperatório. O uso intraoperatório da neuronavegação pode ser particularmente benéfico em um caso complexo de revisão orbital como este ou em pacientes com problemas concomitantes de seios nasais ou base do crânio.
Uma opção mais cara é a tomografia computadorizada intraoperatória, onde o implante do assoalho orbital é colocado e escaneado para confirmar o posicionamento do implante. Isso permite ajustes imediatos sem a necessidade de viagens adicionais à sala de cirurgia. É importante notar que, apesar de muitos estudos compararem os resultados cirúrgicos com o olho contralateral, nem sempre pode haver uma simetria 3D exata em ambas as órbitas. 21
Para evitar a migração tardia do hardware, a fixação do implante do assoalho orbital é crucial. Idealmente, o parafuso de fixação deve passar pelo implante, prendendo-o a um segmento estável do assoalho orbital. Nos casos com um defeito quase total do assoalho orbital, o hardware pode ser preso ao osso estável ao longo da borda infraorbital. A colocação ideal do parafuso é ao longo dos extremos medial ou lateral da órbita, onde a pele sobrejacente é mais espessa (pele nasal ou regiões cantais laterais). Nesse caso, o excesso de titânio do hardware original foi colocado ao longo do segmento central da borda infraorbital subjacente à pele fina da pálpebra inferior, contribuindo para o problema de falha do hardware.
Os autores seniores (TL, DS) recomendam implantes híbridos de polietileno poroso (Medpor) ou Medpor-titânio para minimizar cicatrizes anormais, crescimento interno de tecidos moles e contratura cicatricial. Os implantes de titânio Medpor têm radiopacidade para facilitar a identificação em tomografias computadorizadas, ao contrário do Medpor radiolúcido sozinho. Estudos mostram consistentemente taxas mais baixas de síndrome de aderência orbital com implantes Medpor em comparação com placas de titânio nuas. 22–25 O revestimento de polietileno promove o crescimento fibrovascular sem amarração cicatricial, crucial em casos de revisão de diplopia. 17,23
Depois de remover o hardware original em caso de infecção persistente, a decisão de colocar outro implante de assoalho orbital depende da capacidade de manter a posição do globo. Nesse paciente, hipoglobus e enoftalmia graves foram previstos devido ao aumento do volume orbital e à falta de apoio ao longo do assoalho orbital e da parede medial. Como não havia infecção purulenta macroscópica e havia tecido circundante saudável, foi realizada uma reconstrução aloplástica imediata do assoalho orbital. Nos casos de infecção ativa, pode-se considerar o desbridamento e o uso de material de enxerto autógeno vascularizado. Uma opção que tem sido empregada com sucesso pelo autor sênior (TL) é um enxerto ósseo ilíaco envolto em um retalho pericraniano vascularizado da abóbada craniana (Figura 7). Se houver algum potencial de contaminação nasossinusal ou infecção persistente, envolver todo o enxerto ósseo com um retalho pericraniano é essencial para evitar a falha total do enxerto ósseo.
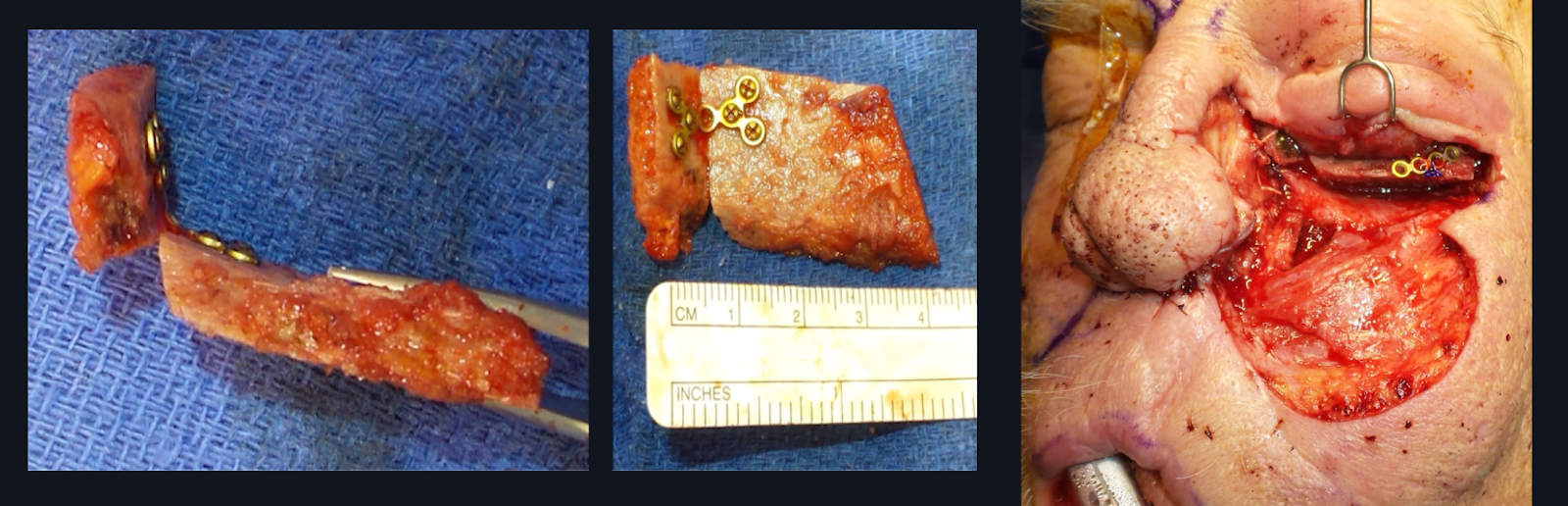
Figura 7. Enxerto ósseo ilíaco utilizado para reconstruir defeito do assoalho medial e orbital. Esta é uma fotografia intraoperatória de um enxerto ósseo ilíaco (esquerdo e central) envolto em um retalho pericraniano vascularizado da abóbada craniana; pode ser usado para reconstruir o assoalho orbital (direita). Este paciente em particular tinha um implante de assoalho orbital infectado com histórico prévio de radiação. Devido à preocupação de que a pele irradiada não tolerasse o implante orbital de Medpor, a órbita do paciente foi reconstruída com enxerto ósseo ilíaco. Este tipo de reconstrução óssea não vascularizada deve ser envolto em retalho pericraniano vascularizado se houver algum potencial de comunicação nasossinusal ou infecção.
Em conclusão, os casos de fratura do assoalho orbital de revisão podem apresentar um conjunto único de complicações que requerem que vários fatores sejam considerados para o sucesso do tratamento. O uso de uma combinação de ferramentas adjuvantes, como neuronavegação intraoperatória e endoscopia nasal, pode ser útil no manejo de um caso complexo de fratura orbital com sinusite concomitante. A consideração cuidadosa da abordagem cirúrgica e do material de hardware orbital também pode contribuir para o sucesso a longo prazo da cirurgia.
- Neuronavegação Medtronic StealthStation.
- Implante orbital Stryker Medpor-Titanium.
Nada a divulgar.
O paciente referido neste artigo em vídeo deu seu consentimento informado para ser filmado e está ciente de que informações e imagens serão publicadas online.
References
- Anabtawi M, Tompkins H, Salvi SM, Lee NJ. Manejo da pneumo-órbita recorrente secundária à fístula sino-orbital pós-traumática usando um implante de titânio impresso em 3D personalizado guiado por navegação: relato de caso e revisão da literatura. Cirurgia Oral. 2021; 14(3):285-294. DOI:10.1111/ors.12577.
- Huelse R, Freuschle A, Hörmann K, Stuck BA. [Fístula orbitocutânea após reconstrução orbitária]. HNO. 2013; 61(4):344-346. DOI:10.1007/S00106-012-2529-7.
- Kim JI, Cheon TU, Kim TK, Nam JG. Fístula sinocutânea após o uso do implante Medpor na fratura orbital blowout. J Craniofac Surg. 2020; 31(6):1766-1767. DOI:10.1097/SCS.00000000000006549.
- Lee TS, Appelbaum EN, Sheen D, Han R, Wie B. Perfuração esofágica devido à colocação de hardware da coluna cervical anterior: série de casos. Int J Otolaringol. 2019;2019:7682654. DOI:10.1155/2019/7682654.
- Boyette JR, Pemberton JD, Bonilla-Velez J. Manejo de fraturas orbitais: desafios e soluções. Clin Oftalmol. 2015;9:2127-2137. DOI:10.2147/OPTH. S80463.
- Ridgway EB, Chen C, Colakoglu S, Gautam S, Lee BT. A incidência de mau posicionamento da pálpebra inferior após reparo de fratura facial: um estudo retrospectivo e meta-análise comparando incisões subtarsais, subciliares e transconjuntivais. Plast Reconstr Surg. 2009; 124(5):1578-1586. DOI:10.1097/PRS.0b013e3181babb3d.
- Roth FS, Koshy JC, Goldberg JS, Soparkar CNS. Pérolas do gerenciamento de trauma orbital. Cirurgia de Semin Plast. 2010; 24(4):398-410. DOI:10.1055/s-0030-1269769.
- Shin JW, Lim JS, Yoo G, Byeon JH. Uma análise de fraturas puras e sintomas oculares associados. J Craniofac Surg. 2013; 24(3):703-707. DOI:10.1097/SCS.0b013e31829026ca.
- Barcic S, Blumer M, Essig H, et al. Comparação das abordagens transconjuntivais pré-septal e retrosseptal em pacientes com fraturas isoladas do assoalho orbitário. J Craniomaxilofaque Surg. 2018; 46(3):388-390. DOI:10.1016/j.jcms.2017.12.013.
- Korchia D, Braccini F, Paris J, Thomassin J. Abordagem transconjuntival em blefaroplastia de pálpebra inferior. Pode J Plast Surg. 2003; 11(3):166-170. DOI:10.1177/229255030301100311.
- Bonsembiante A, Valente L, Ciorba A, Galiè M, Pelucchi S. Abordagem endoscópica transnasal para o tratamento de fraturas da parede orbital medial. Ann Maxillofac Surg. 2019; 9(2):411-414. DOI:10.4103/ams.ams_173_19.
- Clauser L, Galiè M, Pagliaro F, Tieghi R. Enoftalmia pós-traumática: etiologia, princípios de reconstrução e correção. J Craniofac Surg. 2008; 19(2):351-359. DOI:10.1097/SCS.0b013e3180534361.
- de Silva DJ, Rose GE. Fraturas orbitais e raça. Oftalmologia. 2011; 118(8):1677-1680. DOI:10.1016/j.ophtha.2011.05.001.
- Kunz C, Sigron GR, Jaquiéry C. Resultado funcional após tratamento não cirúrgico de fraturas orbitais - o viés da tomada de decisão de acordo com o tamanho do defeito: revisão crítica de 48 pacientes. Br J Oral Maxillofac Surg. 2013; 51(6):486-492. DOI:10.1016/j.bjoms.2012.09.016.
- Sung YS, Chung CM, Hong IP. A correlação entre o grau de enoftalmia e a extensão da fratura na fratura da parede medial da órbita deixada sem tratamento por mais de seis meses: uma análise retrospectiva de 81 casos em uma única instituição. Arco Explosão Surg. 2013; 40(4):335-340. DOI:10.5999/aps.2013.40.4.335.
- Kesselring AG, Promes P, Strabbing EM, van der Wal KGH, Koudstaal MJ. Mau posicionamento da pálpebra inferior após cirurgia de fratura orbital: uma análise retrospectiva baseada em 198 cirurgias. Reconstrução de Trauma Craniomaxilofaco. 2016; 9(2):109-112. DOI:10.1055/s-0035-1567813.
- Diplopia residual em fraturas ósseas orbitais tratadas. Ann Maxillofac Surg. 2013; 3(1):40-45. DOI:10.4103/2231-0746.110078.
- Chen CT, Huang F, Chen YR. Manejo da enoftalmia pós-traumática. Chang Gung Med J. 2006; 29(3):251-261.
- Tavassol F, Gellrich NC. [Competência e comunicação na implementação do planejamento cirúrgico assistido por computador]. Chirurg. 2021; 92(3):194-199. DOI:10.1007/S00104-020-01348-8.
- Zimmerer RM, Ellis E, Aniceto GS, et al. Um estudo multicêntrico prospectivo para comparar a precisão da reconstrução orbital interna pós-traumática com implantes orbitais pré-formados e individualizados padrão. J Craniomaxilofaque Surg. 2016; 44(9):1485-1497. DOI:10.1016/j.jcms.2016.07.014.
- Felding UNA. Fraturas por explosão - clínica, imagem e anatomia aplicada da órbita. Dan Med J. 2018; 65(3).
- Síndrome de aderência orbital após o uso de malha orbital pré-contornada de titânio para a reconstrução de defeitos pós-traumáticos do assoalho orbital. Reconstrução de Trauma Craniomaxilofaco. 2017; 10(1):77-83. DOI:10.1055/s-0036-1584398.
- Bênção NW, Rong AJ, Tse BC, Erickson BP, Lee BW, Johnson TE. Reconstrução óssea orbital com implantes porosos de polietileno-titânio pré-dimensionados e pré-contornados. Cirurgia de reconstrução de plastos oftálmicos. 2021 maio-junho 01; 37(3):284-289. DOI:10.1097/IOP.00000000000001829.
- Lee HBH, Nunery WR. Síndrome de aderência orbital secundária ao material de implante de titânio. Cirurgia de reconstrução de plastos oftálmicos. 2009; 25(1):33-36. DOI:10.1097/IOP.0b013e3181929b6e.
- Sleem H, Wahdan W. Síndrome de adesão orbital: caracterização clínica e rastreamento de fatores de risco (pesquisa clínica retrospectiva). Egípcia J Cirurgia Oral e Maxilofacial. 2018;9:17-21. DOI:10.21608/OMX.2018.5622.
Cite this article
Sheen D, Yu C, Debs S, Yu KM, Calder AN, Quinn KJ, Sismanis D, Lee T. Neuronavegação e endoscopia como ferramentas adjuvantes na revisão do implante do assoalho orbital: tratamento cirúrgico de implante de assoalho orbital infectado e mal posicionado com fístula palpebral crônica e sinusite. J Med Insight. 2024; 2024(410). DOI:10.24296/jomi/410.







