Neuronavigation et endoscopie en tant qu’outils d’appoint dans la révision des implants du plancher orbitaire : prise en charge chirurgicale d’un implant de plancher orbitaire infecté et mal placé avec fistule chronique des paupières et sinusite
Main Text
Table of Contents
Les fractures du plancher orbitaire représentent des séquelles courantes de traumatisme facial qui peuvent entraîner des conséquences fonctionnelles et esthétiques importantes. Cet article présente un aperçu complet de la prise en charge d’un cas de révision impliquant une fracture du plancher orbitaire, en mettant l’accent sur les complications liées au matériel orbitaire extrudé et infecté. De plus, les erreurs courantes qui impliquent un mauvais placement de l’implant du plancher orbital, un mauvais dimensionnement de l’implant et un manque de fixation adéquate de l’implant sont discutées.
Le cas présenté implique un retard de cicatrisation de la plaie et une fistule cutanée sino-orbitale (SOCF) due à un matériel orbitaire infecté provenant d’une réparation antérieure d’une fracture du plancher orbitaire. La discussion porte sur la planification préopératoire, y compris le choix de l’approche chirurgicale (transconjonctivale avec cantatomie latérale) et du matériau de l’implant. La neuronavigation peropératoire a été utilisée comme outil d’appoint pour confirmer la position de l’implant orbitaire nouvellement placé. Ce cas fournit des informations précieuses sur les complications évitables de cette procédure, les nuances de l’approche chirurgicale et les défis peu communs auxquels sont confrontés les prestataires de soins qui effectuent des réparations chirurgicales de traumatismes faciaux.
Fracture orbitaire ; plancher orbital ; approche transconjonctivale ; infection matérielle ; implant orbitaire ; Medpor ; polyéthylène; titane; fistule des paupières.
La pneumo-orbite, impliquant de l’air dans la cavité orbitaire, provient souvent de connexions sinus-orbitale après un traumatisme orbitaire. Alors que de tels cas guérissent généralement spontanément après une réparation post-fracture, les fistules persistantes indiquent des problèmes sous-jacents. Des rapports de cas mettent en évidence une fistule cutanée sino-orbitaire (SOCF) provenant d’implants de traumatisme orbitaire non autologues. 1 à 3 Dans ce cas, un mauvais positionnement du matériel dans le complexe ostéoméal maxillaire a entraîné une obstruction continue des sinus, créant un passage anormal vers la peau de la paupière inférieure affaiblie par du matériel infecté. Il est essentiel de s’attaquer à ce scénario difficile pour rétablir une anatomie osseuse normale et prévenir des complications similaires à l’avenir.
Un homme de 34 ans a d’abord cherché à se faire soigner pour un drainage chronique récurrent sous son œil droit, résultant d’une fracture de l’orbite droite il y a sept ans à la suite d’une agression. La fracture a d’abord été réparée par réduction ouverte et fixation interne dans un autre établissement. Depuis, il souffre d’un écoulement purulent intermittent de la cavité nasale droite et d’une fistule de la paupière inférieure. Il a également noté un mouvement d’air à travers le site d’incision antérieur lorsqu’il s’est mouché et une diplopie d’apparition retardée avec énophtalmie. Après la chirurgie initiale, le patient a subi plusieurs traitements antibiotiques avec une amélioration des symptômes.
L’examen physique a révélé une déhiscence cutanée de 3 cm au bord infra-orbitaire avec croûte et écoulement purulent à la palpation. Un léger érythème a été noté le long de la peau du bord infraorbitaire droit au site de la fistule. Le patient a signalé une légère diminution de la sensation V2 droite. Une diplopie a été observée dans les regards primaires et directionnels, et les mouvements extraoculaires étaient intacts avec une acuité visuelle préservée. L’endoscopie nasale a révélé un écoulement purulent du méat moyen droit.
L’imagerie maxillo-faciale par tomodensitométrie (TDM) a révélé un déplacement du matériel antérieur le long du plancher orbitaire droit (Figure 1–3). Le sinus maxillaire droit présentait une opacification complète, indiquant une sinusite maxillaire chronique présumée et une obstruction du complexe ostéoméatal. Des défauts osseux persistants ont été notés dans la paroi orbitaire médiale et le plancher orbitaire. En vue sagittale, l’implant a été déplacé dans le sinus maxillaire, ne parvenant pas à reconstruire l’anomalie du plancher orbitaire postérieur. La vue axiale a montré que l’implant du plancher orbitaire s’étendait au-delà du bord infraorbitaire, avec une poche d’air autour d’une vis, suggérant une défaillance matérielle avec infection.
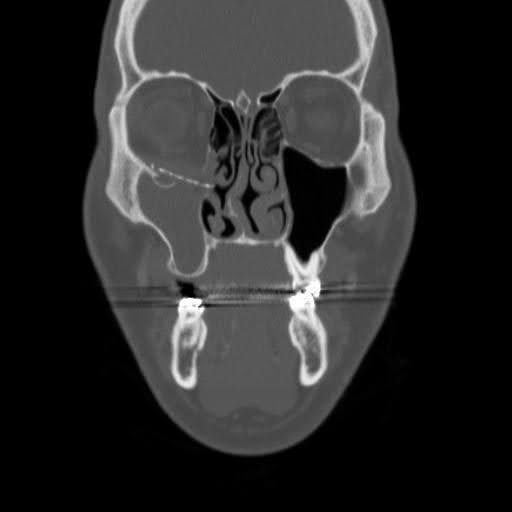
Graphique 1. TDM coronaire préopératoire sans contraste. Image CT montrant un déplacement inférieur de la face médiale de l’implant du plancher orbitaire et la connexion entre les sinus paranasaux et la cavité orbitaire.
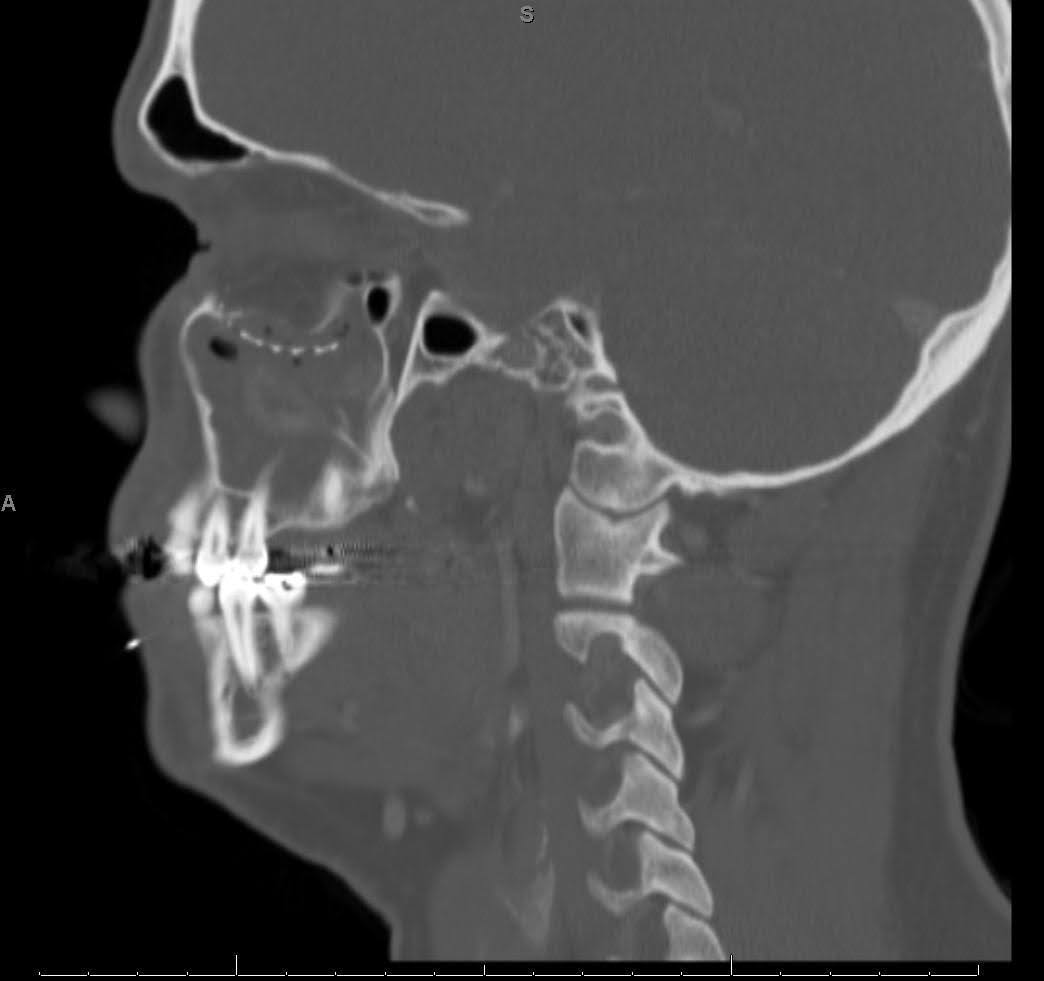
Graphique 2. TDM sagittale préopératoire sans contraste. L’image TDM montrant un déplacement inférieur de l’implant du plancher orbitaire dans le sinus maxillaire ainsi qu’une position postérieure inadéquate sur le plancher orbitaire résiduel.
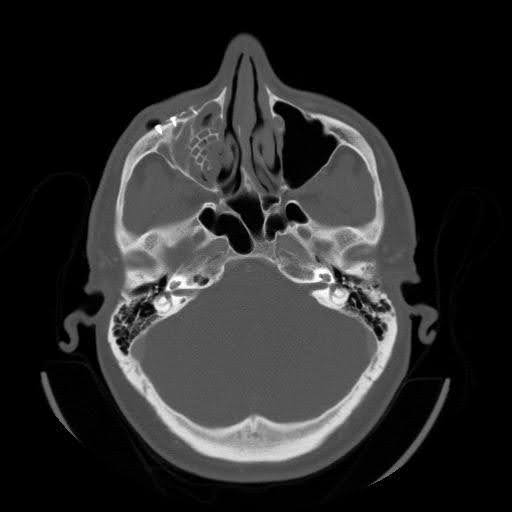
Graphique 3. Tomodensitométrie axiale préopératoire sans contraste. Image CT montrant de l’air libre adjacent à la vis latérale dans le bord orbital.
Le bilan d’un traumatisme orbitaire nécessite un examen physique approfondi axé sur les déformations externes, ainsi qu’un examen ophtalmique et neurologique complet. L’imagerie préopératoire avec des tomodensitogrammes fins sans contraste aide à la prise de décision peropératoire. Lorsqu’elle est intégrée à la neuronavigation, la tomodensitométrie aide à différencier les points de repère, en particulier dans l’anatomie déformée.
La priorité absolue était d’éliminer la source de l’infection en cours en supprimant le matériel compromis. Ensuite, il était crucial de s’attaquer à la diplopie persistante en restaurant le volume orbitaire prémorbide. La troisième priorité portait sur la résolution du blocage de la voie de drainage du sinus maxillaire conduisant à une sinusite maxillaire persistante. L’objectif final englobait le traitement de la cicatrice de la paupière résultant de la fistule et l’amélioration de l’esthétique.
Les patients présentant des infections matérielles au-delà d’un mois postopératoire, en particulier ceux qui ont échoué à plusieurs traitements antibiotiques, bénéficient généralement d’un retrait complet du matériel en raison de la formation potentielle d’un biofilm. 4 L’intervention chirurgicale est souvent recommandée pour les patients présentant une diplopie persistante et un malpositionnement du globe durant plus de 1 à 3 mois, comme le conseillent les auteurs principaux (TL, DS).
La chirurgie orbitaire de révision peut ne pas être nécessaire si l’infection matérielle répond aux antibiotiques dans le premier mois suivant la chirurgie, avant la formation du biofilm. En cas de traumatisme orbitaire grave, tel qu’une hémorragie intraconale ou un décollement de la rétine, la chirurgie est contre-indiquée pour minimiser le risque de lésion orbitale peropératoire supplémentaire due à la rétraction du globe.
Dans ce cas, le patient a subi 1) une ablation du matériel orbitaire par voie postseptale, transconjonctivale et une canthatomie latérale, 2) un remplacement de l’implant du plancher orbitaire à l’aide d’un implant Medpor-titanium avec neuronavigation, 3) une antrostomie maxillaire conservatrice avec ablation de tissu, et 4) une excision de la fistule de la paupière avec fermeture locale de l’avancement tissulaire.
La région faciale du patient a été drapée avec l’orbite controlatérale exposée pour évaluer la symétrie. De la lidocaïne et de l’épinéphrine ont été injectées pour l’hémostase et l’hydrodissection des plans tissulaires, en particulier au niveau du bord orbitaire où l’attache autour de la fistule s’était produite. L’auteur principal (TL), de préférence, opère avec un bouclier cornéen. Par la suite, une canthatomie latérale a été pratiquée afin d’améliorer l’exposition et de mobiliser la paupière inférieure.
Les fractures du plancher orbitaire sont généralement abordées par des approches transconjonctivales ou transcutanées. Les incisions transcutanées, telles que les approches sous-ciliaire, sous-tarsienne et orbitaire, présentent un risque plus élevé d’ectropion postopératoire. 5 à 8 En revanche, l’approche transconjonctivale est préférée en raison de son évitement des incisions externes, ce qui entraîne des taux plus faibles d’ectropion ou de rétraction, tout en préservant l’innervation du muscle orbiculaire. 9, 10
Les auteurs principaux (TL, DS) privilégient une incision transconjonctivale dans un plan postseptal jusqu’au bord orbitaire. Bien que ce plan de dissection soit considéré comme plus simple, il n’y a pas de différence statistiquement significative dans les taux d’entropion, d’ectropion, de sensation de corps étranger et de formation de cicatrices. 9 Dans l’approche transconjonctivale, la préservation de la plaque tarsienne est cruciale. L’incision doit être pratiquée près du bord infra-orbitaire, avec la paupière inférieure rétractée à l’aide d’un écarteur de Desmarres. Si l’incision est médiale au punctum, des précautions sont nécessaires pour éviter de lésion du canalicule et du système lacrymal. Rester près de la caroncule ou passer à une incision transcarunculaire peut aider à atténuer le risque de dommages.
Dans ce cas, l’identification du plan du tissu sous-périosté à travers l’incision transconjonctivale était difficile en raison de la fibrose et des adhérences de l’infection précédente le long du bord infra-orbitaire. Pour résoudre ce problème, le site de cangotomie latérale a été utilisé pour identifier initialement le plan du tissu sous-périosté le long de la paroi orbitaire latérale, qui a ensuite été transporté au centre de l’incision transconjonctivale. Plus profondément dans le plan postseptal, la paupière de Jaeger et les écarteurs malléables ont facilité la rétraction de la graisse orbitaire postérieurement lors de la dissection jusqu’au bord infraorbitaire. L’implant du plancher orbitaire a été découvert dans le sinus maxillaire, et un élévateur périosté #9 a été utilisé pour soulever le contenu orbitaire en disséquant immédiatement superficiellement l’implant déplacé. Cette manœuvre a permis à un malléable de balayer le contenu orbitaire hernié de manière supérieure tout en identifiant l’os orbitaire périphérique stable. Le débridement des fragments osseux du sinus maxillaire a été effectué avec soin pour préserver le nerf infra-orbitaire et les muscles extraoculaires.
L’endoscopie nasale a révélé une extrusion matérielle médialement sous le processus unciné, formant une fistule anormale reliant les cavités nasale, maxillaire et orbitaire. L’examen d’une méga-antrostomie maxillaire ipsilatérale a été débattu, mais a été reporté en raison des préoccupations concernant l’augmentation de la communication orbitale-nasale et l’exposition aux implants. Au lieu de cela, une sinusotomie maxillaire conservatrice a été réalisée en étendant l’ouverture naturelle du sinus maxillaire vers le bas pour empêcher la recirculation avec des plans d’imagerie CT en série pour une éventuelle chirurgie définitive des sinus si la sinusite récidive.
Après le retrait de l’implant précédent, une hernie significative du contenu orbitaire dans le sinus à partir du plancher orbitaire et une anomalie de la paroi orbitaire médiale ont été notées. Un nouvel implant orbitaire a été placé, stabilisé en identifiant les rebords osseux postérieurs et médiaux solides avec neuronavigation.
Un implant en titane recouvert de polyéthylène (Medpor) a été choisi pour éviter la contracture cicatricielle périorbitaire associée au titane nu. L’implant a été trempé dans de la bétadine, profilé pour s’adapter à la courbure naturelle de l’orbite et taillé pour plus de stabilité sans s’étendre au-delà du bord infra-orbitaire. La neuronavigation en vue coronale a assuré un bon positionnement. Les vis et l’implant ont été placés derrière le bord infraorbitaire, avec une vis généralement suffisante, ancrée à travers l’implant du plancher orbitaire. En raison d’un défaut presque total du plancher orbitaire, une broche s’étendant de l’implant a été utilisée pour fixer l’implant. En cas de plancher orbitaire stable inadéquat, les vis doivent être placées dans les régions où la peau est plus épaisse, comme le long de la paroi latérale nasale ou du bord orbitaire latéral. L’endoscopie nasale post-réimplantation a confirmé le bon positionnement, résolvant le déplacement médial initial bloquant la voie de drainage du sinus maxillaire.
Avant la fermeture, les bords de la fistule cutanée de la paupière ont été excisés et l’avancement local des tissus a soulevé la contracture cicatricielle de la paupière du bord infra-orbitaire. Le tendon canthal latéral a été rapproché sur le tubercule de Whitnall avec du nylon transparent 4-0.
Pour réduire le risque d’entropion, une suture résorbable (5-0 fast absorbable gut dans ce cas) a été utilisée par l’auteur principal (TL) pour la fermeture de l’incision transconjonctivale, ce qui est une question de préférence du chirurgien.
Le patient a été observé pendant la nuit et a reçu son congé le lendemain. L’imagerie TDM postopératoire immédiate (figures 4 à 6) a confirmé le bon positionnement orbitaire du matériel. Des précautions pour les sinus (éviter de se moucher, d’appuyer ou d’augmenter la pression intrathoracique) ont été recommandées pour prévenir une éventuelle atteinte vasculaire et visuelle due à de l’air orbitaire emprisonné involontairement, et Augmentin a été prescrit pendant 7 jours. En raison de la fistule nasale-orbitaire préexistante, les irrigations des sinus ont été reportées.
Lors du suivi de 8 mois, le patient a signalé une amélioration significative de la diplopie, avec des mouvements extraoculaires intacts et aucune récidive de fistule des paupières ou de sinusite. Les progrès cliniques seront surveillés à l’aide d’une imagerie des sinus par tomodensitométrie en série pour détecter une récidive potentielle de la sinusite maxillaire.
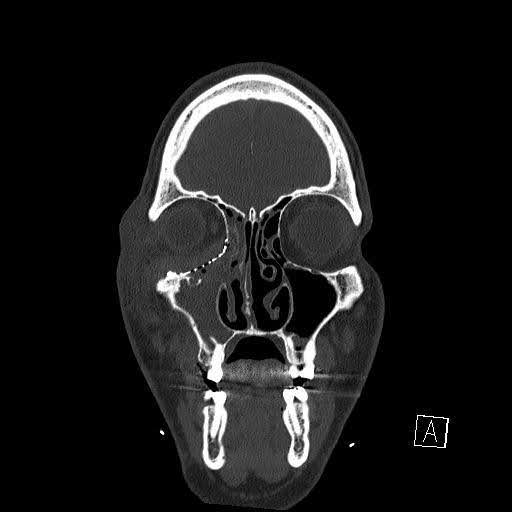
Graphique 4. Tomodensitométrie coronale sans contraste du jour 1 postopératoire immédiat. Image TDM montrant la présence d’une opacification persistante précoce dans le sinus maxillaire droit.
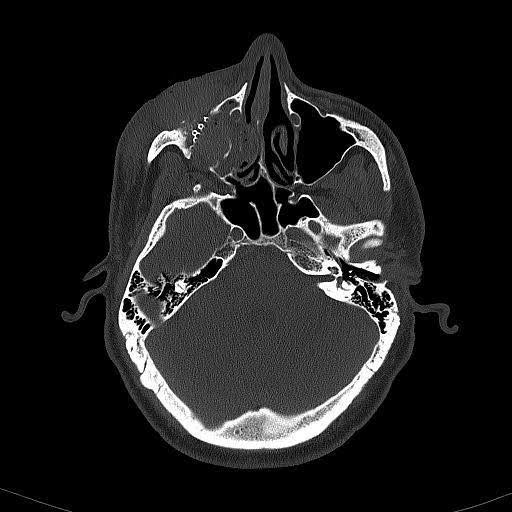
Graphique 5. Tomodensitométrie axiale sans contraste du jour 1 postopératoire immédiat. Image CT démontrant le nouvel implant du plancher orbital, qui ne s’étend pas au-delà du bord infraorbitaire.
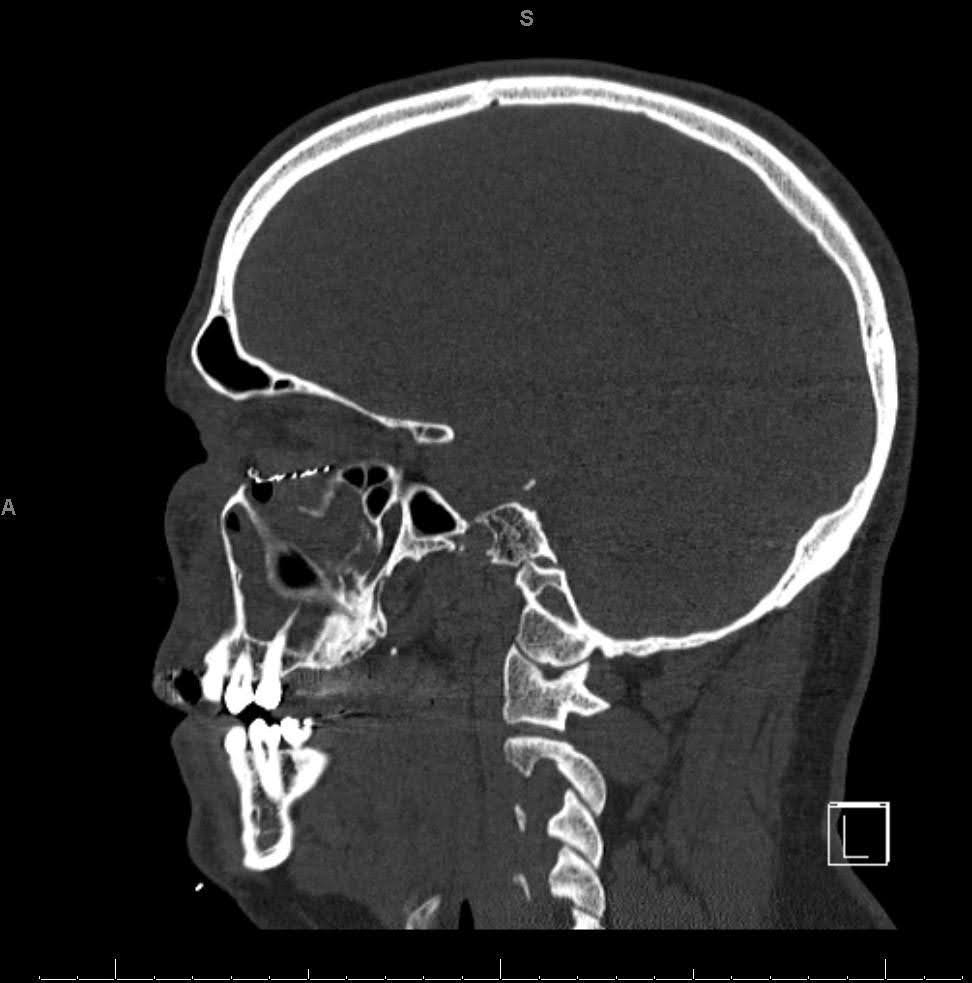
Graphique 6. Tomodensitométrie sagittale sans contraste postopératoire immédiate du jour 1. Image CT montrant le positionnement approprié de l’implant du plancher orbitaire avec la partie postérieure reposant au-dessus d’un rebord stable de l’os orbitaire postérieur.
Ce cas présentait un SOCF retardé résultant d’un mauvais positionnement du matériel, nécessitant le retrait du matériel infecté, la restauration de l’anatomie native et la correction de la diplopie.
Les indications chirurgicales de la réparation du plancher orbitaire comprennent : 1) un piégeage du muscle extraoculaire avec ou sans réflexe oculocardiaque, 2) un globe mal positionné avec diplopie persistante, 3) une diplopie avec un défaut orbitaire (plus grand que 2 à 3 cm2 avec un déplacement d’au moins 3 mm) et une énophtalmie qui en résulte ou une fracture impliquant plus de 50 % du plancher orbitaire, 4) du matériel orbitaire extrudé ou infecté, et 5) un SOCF persistant qui ne se résout pas avec une gestion conservatrice. 11 à 15
Les complications tardives de la chirurgie orbitaire, résultant d’un retard de cicatrisation des plaies, d’une fibrose et d’une contracture cicatricielle, englobent un éventail de problèmes nécessitant souvent une chirurgie de révision. Ces complications comprennent l’ectropion, l’entropion, la défaillance matérielle, les infections chroniques, la formation de fistules, les paresthésies persistantes et la lagophtalmie. La contracture cicatricielle et le raccourcissement lamellaire de diverses approches chirurgicales peuvent entraîner un ectropion et un entropion. 16 L’approche transconjonctivale, préservant le tarse, est privilégiée pour les patients présentant un vecteur négatif, réduisant ainsi le risque de formation d’ectropions.
La diplopie persistante, survenant dans 8 à 52 % des cas pendant des semaines après l’opération, est exacerbée par un œdème préopératoire, une fibrose intrinsèque, une ischémie musculaire, une inflammation et une mauvaise mise en place de l’implant provoquant un conflit musculaire extraoculaire. 5,7,17 L’imagerie aide à identifier les causes de la diplopie. Si le volume orbitaire postopératoire est normal, l’observation permet une compensation potentielle du système nerveux central. Dans ce cas, une diplopie persistante résultait d’un placement, d’une forme et d’une taille incorrects de l’implant, entraînant un volume orbitaire insuffisant. Distincte de la malpositionnement du globe, les lésions traumatiques des nerfs crâniens ou des muscles extraoculaires peuvent également provoquer une diplopie prolongée avec strabisme. Après avoir rétabli le volume orbital et la position du globe, un spécialiste du strabisme est essentiel pour évaluer et traiter la diplopie due à ces blessures.
Une autre complication tardive comprend une énophtalmie retardée (survenant dans 7 à 27 % des cas postopératoires) et un hypoglobus, qui peut apparaître progressivement en raison de déficits tissulaires dus à une dévascularisation et à une ischémie antérieures. Cependant , une cause plus fréquente, comme observé dans ce cas, est l’expansion aberrante de la cavité orbitaire avec le déplacement de l’implant ou un mauvais dimensionnement. Le traitement efficace de l’énophtalmie tardive pose des défis et peut nécessiter le remplacement ou l’augmentation de l’implant pour restaurer le volume orbitaire approprié. 5
Des études récentes soulignent les avantages des implants individualisés créés par l’impression 3D sélective avec de meilleurs résultats et des taux de révision plus faibles comparables à la neuronavigation peropératoire. 19,20 Les inconvénients comprennent une augmentation des coûts et des retards de fabrication de quelques semaines. 20 La décision entre les implants individualisés et non individualisés doit être adaptée. L’auteur principal (TL) réserve généralement des implants de plancher orbitaire personnalisés aux patients présentant des fractures zygomaticomaxillaires complexes et des fractures concomitantes du plancher orbitaire nécessitant une correction simultanée de l’aplatissement malaire.
Pour prévenir les complications orbitaires, il est crucial d’éviter les erreurs courantes lors de la chirurgie initiale. Nous décrirons brièvement les facteurs potentiels qui pourraient avoir contribué aux complications observées chez ce patient. Une exposition inadéquate peut avoir joué un rôle important pour ce patient. L’implant orbitaire doit idéalement reposer sur le plancher orbitaire postérieur et/ou latéral stable et une paroi orbitaire médiale stable. L’importante anomalie de la paroi orbitaire médiale de notre patient, qui s’étendait vers l’arrière, n’a probablement pas été correctement exposée. Dans de tels cas, une incision transcarunculaire postérieure au canal lacrymal, en plus d’une approche transconjonctivale, peut être nécessaire pour une bonne exposition de la paroi orbitaire médiale. Une dissection sous-périostée prudente minimise les lésions lors de la dissection supérieure le long de la paroi orbitaire médiale, où l’identification des artères comme l’ethmoïde antérieure et l’ethmoïde postérieure est cruciale. Rester dans le plan sous-périosté est également essentiel pour préserver des structures telles que le muscle oblique inférieur lors de la dissection intraorbitaire.
De même, la fracture s’étend assez largement vers l’arrière le long du plancher orbitaire, et cette région est probablement restée insuffisamment exposée. Cela est évident à partir du déplacement inférieur de l’implant dans le sinus maxillaire. Étant donné la présence de nerfs crâniens et de muscles extraoculaires cruciaux à l’apex orbitaire, il existe une hésitation et une anxiété naturelles associées à la dissection dans cette zone. L’utilisation de la neuronavigation, en particulier dans les cas de révision, ajoute une couche supplémentaire de réconfort et de certitude, en particulier lorsqu’il s’agit d’une anatomie considérablement modifiée. Une exposition insuffisante de la fracture entraîne une réduction incomplète et des complications potentielles, notamment le déplacement des implants dans le sinus, entraînant une malposition du globe ou le piégeage du tissu orbitaire. Ceci, à son tour, peut entraîner des limitations de la motilité extraoculaire en raison de l’attache des muscles extraoculaires.
Lors de la conception de la forme de l’implant, il est important de tenir compte de la douce courbe en S du plancher orbitaire naturel lorsqu’il est vu dans un plan sagittal. Le sol descend immédiatement en arrière du bord, puis monte doucement vers le haut plus près de l’apex orbital. Le long du plancher orbitaire médial, il y a une transition douce vers la paroi orbitaire médiale. Malheureusement, il semble que l’implant original du plancher orbitaire n’ait pas suivi ces contours, ce qui a entraîné la reconstruction d’une partie du défaut du plancher orbitaire sans le composant de la paroi orbitaire médiale. Cela a probablement contribué à la sinusite chronique et à la formation d’une fistule des paupières après que le composant médial de l’implant orbitaire a obstrué le complexe ostéoméal naturel qui permet un bon drainage du sinus maxillaire. Une fois que la sinusite chronique s’est développée, la colonisation bactérienne s’est développée le long de la face orbitaire de l’implant et a contribué à l’infection périorbitaire en cours.
En ce qui concerne la taille de l’implant, il est important de le façonner de manière à ce que l’implant se trouve à l’arrière du bord infra-orbitaire afin d’éviter l’érosion du matériel par la paupière inférieure. Il est préférable d’éviter un placement excessif de matériel le long de la surface antérieure du bord infraorbitaire pour éviter la palpabilité de l’implant, les cicatrices indésirables et/ou l’exposition au matériel, comme on l’observe chez ce patient particulier. En ce qui concerne les dimensions antérieures et postérieures de l’implant de plancher orbitaire, l’implant doit être suffisamment long pour atteindre un os stable situé à l’arrière tout en prenant soin d’éviter d’empiéter sur le contenu de l’apex orbitaire. Au cours du processus de dimensionnement et de mise en forme de l’implant, la neuronavigation peut aider à identifier l’os orbitaire médial, postérieur et latéral stable pour l’implantation. Après la pose d’un nouvel implant de plancher orbitaire, une sonde de neuronavigation peut être utilisée pour tracer le contour du nouveau matériel de plancher orbitaire afin d’assurer une forme, un positionnement et une stabilité appropriés en peropératoire. L’utilisation peropératoire de la neuronavigation peut être particulièrement bénéfique dans un cas complexe de révision orbitale comme celui-ci ou chez les patients présentant des problèmes concomitants de sinus ou de base du crâne.
Une option plus coûteuse est la tomodensitométrie peropératoire, où l’implant du plancher orbitaire est placé et scanné pour confirmer le positionnement de l’implant. Cela permet des ajustements immédiats sans avoir besoin de se rendre davantage au bloc opératoire. Il est important de noter que malgré de nombreuses études comparant les résultats chirurgicaux à l’œil controlatéral, il n’y a pas toujours une symétrie 3D exacte dans les deux orbites. 21
Pour éviter toute migration retardée du matériel, la fixation de l’implant de plancher orbital est cruciale. Idéalement, la vis de fixation doit passer à travers l’implant, le fixant à un segment stable du plancher orbitaire. Dans les cas où il y a un défaut presque total du plancher orbital, le matériel peut être fixé à un os stable le long du bord infraorbitaire. Le placement optimal de la vis se fait le long des extrémités médiales ou latérales de l’orbite, là où la peau sus-jacente est plus épaisse (peau nasale ou régions canthales latérales). Dans ce cas, l’excès de titane du matériel d’origine a été placé le long du segment central du bord infraorbitaire qui sous-tend la fine peau de la paupière inférieure, contribuant au problème de défaillance matérielle.
Les auteurs principaux (TL, DS) recommandent des implants en polyéthylène poreux (Medpor) ou hybrides Medpor-titane pour minimiser les cicatrices anormales, la croissance des tissus mous et la contracture cicatricielle. Les implants Medpor-titane sont dotés d’une radio-opacité pour une identification facile sur les tomodensitogrammes, contrairement à Medpor radiotransparent seul. Les études montrent systématiquement des taux plus faibles de syndrome d’adhérence orbitaire avec les implants Medpor par rapport aux plaques de titane nues. 22 à 25 Le revêtement en polyéthylène favorise la croissance fibrovasculaire sans attache cicatricielle, cruciale dans les cas de révision de la diplopie. 17,23
Après avoir retiré le matériel d’origine en cas d’infection persistante, la décision de placer un autre implant de plancher orbitaire dépend de la capacité à maintenir la position du globe. Chez ce patient, on s’attendait à ce qu’un hypoglobus et une énophtalmie sévères soient attendus en raison de l’augmentation du volume orbitaire et du manque de soutien le long du plancher orbitaire et de la paroi médiale. Étant donné qu’il n’y avait pas d’infection purulente grossière et qu’il y avait des tissus environnants sains, une reconstruction alloplasique immédiate du plancher orbitaire a été effectuée. En cas d’infection active, un débridement et l’utilisation d’un matériau de greffe autogène vascularisé peuvent être envisagés. L’une des options qui a été employée avec succès par l’auteur principal (TL) est une greffe d’os iliaque enveloppée dans un lambeau péricrânien vascularisé à partir de la voûte crânienne (Figure 7). S’il y a un risque de contamination sinonasale ou d’infection persistante, il est essentiel d’envelopper l’ensemble de la greffe osseuse avec un lambeau péricrânien pour éviter l’échec total de la greffe osseuse.
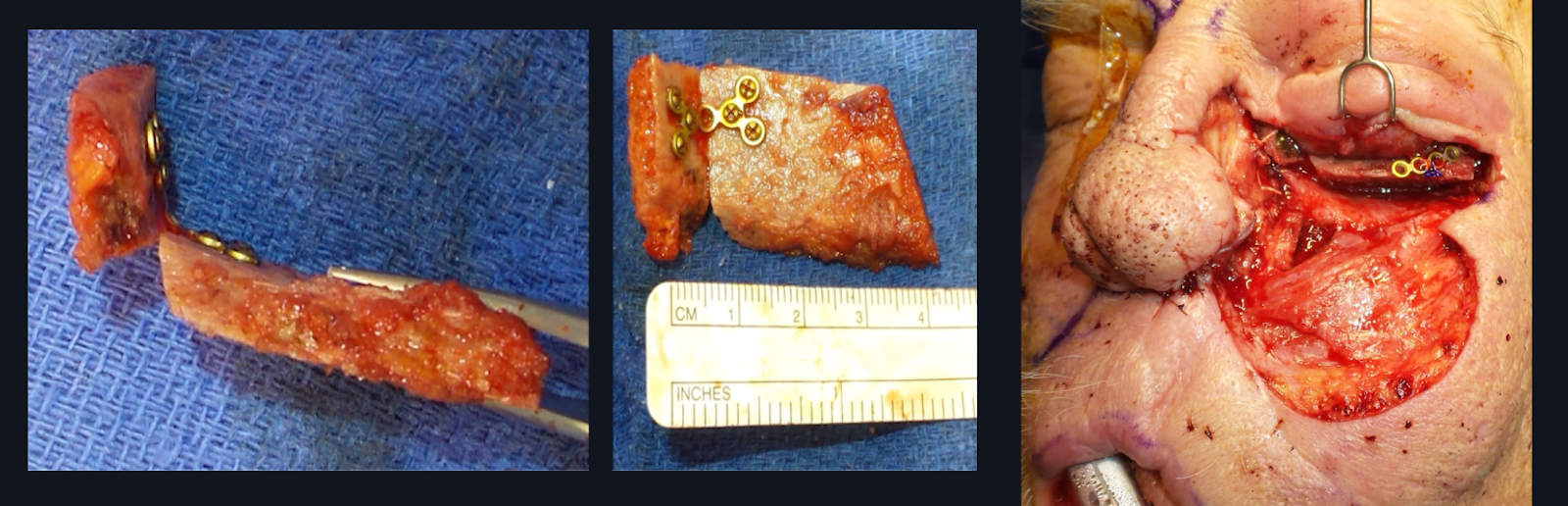
Graphique 7. Greffe osseuse iliaque utilisée pour reconstruire l’anomalie du plancher médial et orbitaire. Il s’agit d’une photographie peropératoire d’une greffe osseuse iliaque (à gauche et au centre) enveloppée dans un lambeau péricrânien vascularisé de la voûte crânienne ; elle peut être utilisée pour reconstruire le plancher orbitaire (à droite). Ce patient avait un implant de plancher orbitaire infecté avec des antécédents de radiation. En raison de préoccupations concernant la peau irradiée ne tolérant pas l’implant orbitaire Medpor, l’orbite du patient a été reconstruite par une greffe osseuse iliaque. Ce type de reconstruction osseuse non vascularisée doit être enveloppé dans un lambeau péricrânien vascularisé s’il existe un risque de communication sinonasale ou d’infection.
En conclusion, les cas de fracture du plancher orbitaire de révision peuvent présenter un ensemble unique de complications qui nécessitent plusieurs facteurs pour être pris en compte pour un traitement réussi. L’utilisation d’une combinaison d’outils d’appoint tels que la neuronavigation peropératoire et l’endoscopie nasale peut être utile dans la prise en charge d’un cas complexe de fracture orbitaire avec sinusite concomitante. Une attention particulière à l’approche chirurgicale et au matériel orbitaire peut également contribuer au succès à long terme de la chirurgie.
- Neuronavigation Medtronic StealthStation.
- Implant orbital Stryker Medpor-Titanium.
Rien à divulguer.
Le patient visé dans cet article vidéo a donné son consentement éclairé pour être filmé et est conscient que des informations et des images seront publiées en ligne.
References
- Anabtawi M, Tompkins H, Salvi SM, Lee NJ. Prise en charge de la pneumo-orbite récurrente secondaire à la fistule sino-orbitaire post-traumatique à l’aide d’un implant en titane imprimé en 3D personnalisé guidé par la navigation : un rapport de cas et une revue de la littérature. Chirurgie buccale. 2021; 14(3):285-294. doi :10.1111/ors.12577.
- Huelse R, Freuschle A, Hörmann K, Stuck BA. [Fistule orbito-cutanée après reconstruction orbitaire]. HNO. 2013; 61(4):344-346. doi :10.1007/s00106-012-2529-7.
- Kim JI, Cheon TU, Kim TK, Nam JG. Fistule sino-cutanée après utilisation de l’implant Medpor dans la fracture de l’éruption orbitaire. J Craniofac Surg. 2020; 31(6):1766-1767. doi :10.1097/SCS.000000000006549.
- Lee TS, Appelbaum EN, Sheen D, Han R, Wie B. Perforation œsophagienne due au placement du matériel de la colonne cervicale antérieure : série de cas. Int J Otolaryngol. 2019;2019:7682654. doi :10.1155/2019/7682654.
- Boyette JR, Pemberton JD, Bonilla-Velez J. Prise en charge des fractures orbitaires : défis et solutions. Clin Ophthalmol. 2015;9:2127-2137. doi :10.2147/OPTH. Réf. S80463.
- Ridgway EB, Chen C, Colakoglu S, Gautam S, Lee BT. L’incidence de la malposition de la paupière inférieure après la réparation d’une fracture faciale : une étude rétrospective et une méta-analyse comparant les incisions sous-tarsiennes, sous-ciliaires et transconjonctivales. Plast Reconstr Surg. 2009; 124(5):1578-1586. doi :10.1097/PRS.0b013e3181babb3d.
- Roth FS, Koshy JC, Goldberg JS, Soparkar CNS. Perles de la gestion des traumatismes orbitaires. Semin Plast Surg. 2010; 24(4):398-410. doi :10.1055/s-0030-1269769.
- Shin JW, Lim JS, Yoo G, Byeon JH. Une analyse des fractures pures et des symptômes oculaires associés. J Craniofac Surg. 2013; 24(3):703-707. doi :10.1097/SCS.0b013e31829026ca.
- Barcic S, Blumer M, Essig H, et al. Comparaison des approches transconjonctivales préseptales et rétroseptales chez les patients présentant des fractures isolées du plancher orbitaire. J Craniomaxillofac Surg. 2018; 46(3):388-390. doi :10.1016/j.jcms.2017.12.013.
- Korchia D, Braccini F, Paris J, Thomassin J. Approche transconjonctivale dans la blépharoplastie de la paupière inférieure. Can J Plast Surg. 2003; 11(3):166-170. doi :10.1177/229255030301100311.
- Bonsembiante A, Valente L, Ciorba A, Galiè M, Pelucchi S. Approche endoscopique transnasale pour le traitement des fractures de la paroi orbitaire médiale. Ann Maxillofac Surg. 2019; 9(2):411-414. doi :10.4103/ams.ams_173_19.
- Clauser L, Galiè M, Pagliaro F, Tieghi R. Énophtalmie posttraumatique : étiologie, principes de reconstruction et de correction. J Craniofac Surg. 2008; 19(2):351-359. doi :10.1097/SCS.0b013e3180534361.
- de Silva DJ, Rose GE. Éruption orbitale, fractures et course. Ophtalmologie. 2011; 118(8):1677-1680. doi :10.1016/j.ophtha.2011.05.001.
- Kunz C, Sigron GR, Jaquiéry C. Résultat fonctionnel après prise en charge non chirurgicale des fractures de l’orbite - le biais de la prise de décision en fonction de la taille du défaut : examen critique de 48 patients. Br J Oral Maxillofac Surg. 2013; 51(6):486-492. doi :10.1016/j.bjoms.2012.09.016.
- Sung YS, Chung CM, Hong IP. La corrélation entre le degré d’œnophtalmie et l’étendue de la fracture de la paroi orbitaire médiale laissée non traitée pendant plus de six mois : une analyse rétrospective de 81 cas dans un seul établissement. Arch Plast Surg. 2013; 40(4):335-340. doi :10.5999/aps.2013.40.4.335.
- Kesselring AG, Promes P, Strabbing EM, van der Wal KGH, Koudstaal MJ. Malposition de la paupière inférieure suite à une chirurgie de fracture orbitaire : une analyse rétrospective basée sur 198 chirurgies. Traumatisme cranio-maxillo-facial. 2016; 9(2):109-112. doi :10.1055/s-0035-1567813.
- Balaji SM. Diplopie résiduelle dans les fractures de l’os orbitaire traitées. Ann Maxillofac Surg. 2013; 3(1):40-45. doi :10.4103/2231-0746.110078.
- Chen CT, Huang F, Chen YR. Prise en charge de l’énophtalmie post-traumatique. Chang Gung Med J. 2006; 29(3):251-261.
- Tavassol F, Gellrich NC. [Compétence et communication dans la mise en œuvre de la planification chirurgicale assistée par ordinateur]. Chirurg. 2021; 92(3):194-199. doi :10.1007/s00104-020-01348-8.
- Zimmerer RM, Ellis E, Aniceto GS, et al. Une étude prospective multicentrique pour comparer la précision de la reconstruction orbitaire interne post-traumatique avec des implants orbitaires standard préformés et individualisés. J Craniomaxillofac Surg. 2016; 44(9):1485-1497. doi :10.1016/j.jcms.2016.07.014.
- Felding UNA. Fractures par éruption - clinique, imagerie et anatomie appliquée de l’orbite. Dan Med J. 2018; 65(3).
- Syndrome d’adhérence orbitale suite à l’utilisation d’un treillis orbitaire préprofilé en titane pour la reconstruction des défauts post-traumatiques du plancher orbitaire. Traumatisme cranio-maxillo-facial. 2017; 10(1):77-83. doi :10.1055/s-0036-1584398.
- Blessing NW, Rong AJ, Tse BC, Erickson BP, Lee BW, Johnson TE. Reconstruction osseuse orbitaire avec des implants poreux en polyéthylène-titane prédimensionnés et préprofilés. Chirurgie de reconnaissance de plastron ophtalmique 2021 mai-juin 01 ; 37(3):284-289. doi :10.1097/IOP.000000000001829.
- Lee HBH, Nunery WR. Syndrome d’adhérence orbitaire secondaire au matériau de l’implant en titane. Chirurgie de reconnaissance de plastron ophtalmique 2009; 25(1):33-36. doi :10.1097/IOP.0b013e3181929b6e.
- Sleem H, Wahdan W. Syndrome d’adhérence orbitale : caractérisation clinique et traçage des facteurs de risque (recherche clinique rétrospective). Égyptien J Chirurgie buccale et maxillo-faciale. 2018;9:17-21. doi :10.21608/OMX.2018.5622.
Cite this article
Sheen D, Yu C, Debs S, Yu KM, Calder AN, Quinn KJ, Sismanis D, Lee T. Neuronavigation et endoscopie comme outils d’appoint dans la révision des implants de plancher orbitaire : prise en charge chirurgicale d’un implant de plancher orbitaire infecté et mal placé avec fistule chronique des paupières et sinusite. J Med Insight. 2024; 2024(410). doi :10.24296/jomi/410.







