CDH1遺伝子変異に対する予防的全胃切除術
Main Text
Table of Contents
遺伝性びままん胃がん(HDGC)症候群は、CDH1遺伝子の変異により、患者が生涯にわたり胃がんを発症しやすい傾向にあります。そのため、この症候群の患者には一般的に全胃切除術が推奨されます。このケースでは、患者は早期発症性直腸がんと診断された後に遺伝子検査で偶然発見されたCDH1変異を呈呈しました。予防的に全胃切除術と後結腸性ルー・アン・Y食道空腸吻合術を受けました。術後の経過は特に異常なく、術後3日目に退院しました。彼女の病理検査では、粘膜に限定されたシグネットリング細胞癌の複数の焦点が示されました。このビデオでは、Roux-en-Y食道空腸吻合再建術を用いた予防的全胃切除術を行う経験豊富な外科医の技術を実演しています。
遺伝性びまん性胃がん(HDGC)症候群は、CDH1遺伝子の変異による常染色体優性遺伝疾患です。これはまれな疾患であり、胃がんの1〜3%しか発症しません。しかし、この疾患の患者は生涯にわたり胃がんを発症するリスクが56〜83%であり、40歳未満で診断されることが多いです。1,2 女性は乳腺小葉癌を発症するリスクも高いです。生涯で胃がんを発症する重大なリスクがあるため、遺伝子検査でCDH1変異が判明した患者には予防的な全胃切除術が推奨されます。
患者は39歳の女性で、何年も前に直腸がんの既往があり、治療に成功し、その後の遺伝子検査でCDH1遺伝子に生殖細胞変異が見つかりました。
腹部検査は、前回手術でよく治癒した切開部(低位前方切除および迂回回腸造瘻)のみが重要である。
患者は上部内視鏡検査を受け、胃は正常に見えました。組織学的検査のために冷鉗子を用いた生検の結果、頭頂細胞肥大が認められ、悪性腫瘍の証拠はありませんでした。
HDGC患者は、粘膜下の性質を持つびまん性(または凝集性の低いタイプの)胃がんを発症します。これは、病気の進行のかなり後期に粘膜を侵害したときに初めて粘膜表面に見えることを意味します。したがって、HDGC患者における致命的な胃がん予防の唯一の確実な方法として、予防的な全胃切除術が推奨されています。
20歳未満の患者や手術治療を控える場合は、連続的な上部内視鏡検査を伴う内視鏡的監視が代替手段となります。正確な監視頻度は不明ですが、ほとんどのガイドラインでは内視鏡検査を6〜12か月ごとに実施し、最低30回の生検を推奨しています。各解剖部位から5回ずつ、すなわち幽門前、前乳門、転換帯、体、眼底、心臓です。3–5 患者には、慎重な内視鏡検査を行っても、がんの浸潤が小さく広範囲に分布しているため、早期の胃がんを見逃す可能性があることを明確に伝えるべきです。しかし 、研究によれば、胃切除を延期した患者は、初期胃切除術を受けた患者と同様の生存結果を得ており、多くの患者は縦断的カウンセリングの後に予防的全胃切除を選択することが理解されています。7
この動画では従来の開放式による予防的な全胃切除術が示されていますが、現在では多くの外科医がこの手術を低侵襲方式、例えば腹腔鏡下またはロボット手術で行っています。重篤な罹患率や死亡率に差はありませんが、低侵襲アプローチは術後の痛みが少なく、開放的アプローチよりも入院期間が短くなります。
予防的全胃切除術の主な目的は、すべての胃粘膜を除去し、胃がんのリスクを排除することです。そのため、凍結切片の病理評価は術中に行われ、胃切除標本の近位縁が食道扁平上皮粘膜を100%示し、遠位縁に十二指腸にのみ見られるブルナー腺が示されていることを確認します。
全胃切除術を受ける患者は仰向けになり、上部正中切開から腹部に入ります。腹膜表面と肝臓は転移性疾患がないか慎重に検査されます。その後、ファルシフォーム靭帯を外し、トンプソンリトラクターを装着します。
リトラクターを設置したら、まず胃結腸靭帯を通じて小嚢に入ります。その後、左側の胃消化血管とすべての短胃血管を血管封閉装置(LigaSure)で分割します。その後、解離はより大きな曲率に沿って右へ進み、胃結腸幹に向かいます。ここで、右胃消化静脈と動脈がLigaSureで分離・結紮されます。これが完了すると、十二指腸の最初の部分はEndo-GIA 60mmタン荷重ステープラーの単発焼成で分割されます。
注意はより小さい曲率に向けられます。LigaSureでは小網膜を開けて、右の胃静脈と動脈を取ります。次に、横隔食道靭帯を分割し、腹部内の下部4〜5cmの食道を切り離し、両方の迷走神経を分割します。これにより近位胃と遠位食道への可動性が提供され、十二指腸の分裂と相まって胃を頭方向に動員し、左胃静脈と動脈の解離を容易にします。これらはEndo-GIAタン式ロードホチキスで分割されます(図1)。

次に、胃食道接合部の1〜2cm上で分岐部位が選ばれます。これを焼灼術で行い、食道が分割される4つの象限に3-0シルク牽引縫合を挿入します。食道が分割された後、胃標本は現場から送られ、近位および遠位縁に残留胃粘膜がないかを確認するために凍結切片検査に送られます。
HDGCのために行われる全胃摘出術は予防的であるため、D1+またはD2リンパ節摘出術は必要ありません。しかし、胃切除標本とともに、直接の腹周リンパ節(D1リンパ節摘出術に該当します)は一括で摘出されます。
食道空腸吻合術は、25mmのCovidien EEAホチキスで端から側に合わせてホチキスで行われます。まず、食道の切断面に3-0 PDSのパースストリング縫合を挿入し、EEAステープラーのアンビルを固定します。その後、空腸をトライツ靭帯から遠位~30cmの位置に分けて、約60cmの後結腸状ルー肢を作ります。2層の手縫いの左右に空腸吻合術は、内側にランニング用の全層PDS縫合糸と、外側に間断した3-0シルクレンバート縫合糸を用いて行われます。腸系膜の陰湿筋は3-0シルク縫合糸で閉じます。
ルーの枝は、中央結腸管の左側にある横中結腸の切開を後尾部のように通過します。食道に進む際にルーの枝をねじらないように注意してください。次に、ステープルで食道空腸吻合術を行い、ルーの枝からホチキスラインを切り取り、ホチキスを腸切開内に挿入します。その後、スパイクはルーの枝の無腸状縁から突き出し、食道の金床と結合します。その後、ホチキスを発射し、食道ドーナツを最終マージン評価のために送ります。麻酔科の同僚はその後、鼻胃管を吻合部からルーの肢へと挿入します。ルーの四肢の張り出しは、Endo-GIAタン製ロードホチキスの単発焼成で切除されます(図2)。最後に、食道裂孔を数本の中断2-0シルク縫合で再接近し、ルー肢を3-0シルク縫合で横隔膜腹膜に固定します。横中結腸の腸間膜閉鎖も、中断された3-0シルク縫合糸で閉じられています。
経験豊富な紹介センターでは、全胃切除術が最小限の罹患率と死亡率で実施可能です。当機関で全胃切除術を受けた148人の患者を対象とした最近の回顧的レビューでは、90日間の主要罹患率と死亡率はそれぞれ14%と3%でした。中央値入院期間は8日で、再入院率は22%で、主に脱水や栄養障害が原因でした。8 この場合、患者は単純に病院で治療を受けました。術後2日目に上部消化管嚥下検査を受け、吻合漏は陰性でした。3日目には全液食で自宅退院しました。
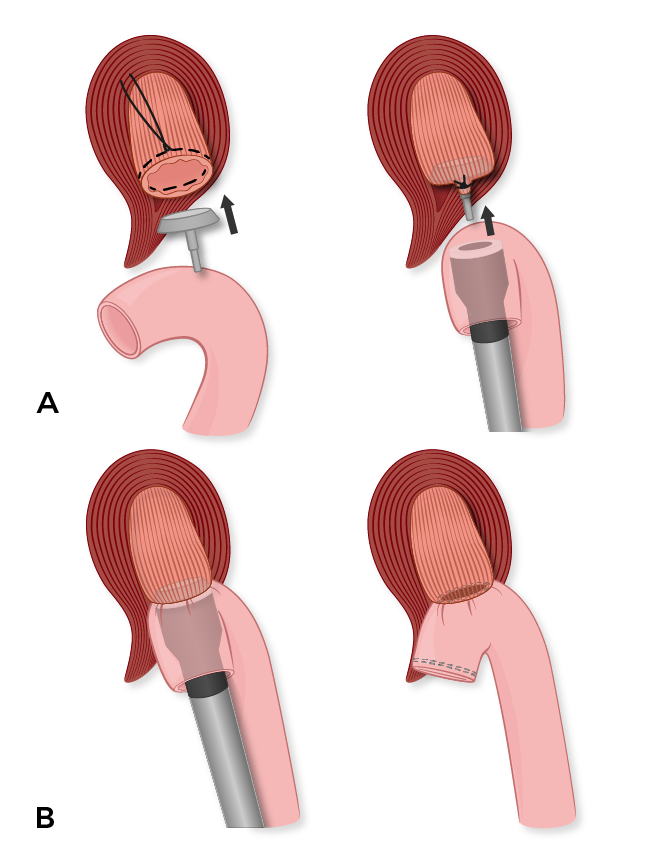
ある。金床は近位端、すなわち食道切断線に縫い付けられ、受け取り端として機能します。EEAホチキスは空腸ルー肢のホチキス線の開口部から導入され、無腸結界の縁に突き出して挿入端として機能します。
B.金床とEEAホチキスは結合してから焼成され、両側の食道空腸吻合が形成されます。その後、空腸性ルー肢の切断端をエンドGIAホチキスで切除します。
全胃切除術:
多焦点性腺癌、凝集性の低いタイプで、固有椎板に限定されています(総観報告参照)。9つのリンパ節に悪性腫瘍の証拠はありません(0/9)。
最終食道切縁:
食道の一部で診断異常は認められません。悪性腫瘍の証拠はありません。
腫瘍病期概要:m p T1a N0。
腫瘍の大きさ(最大寸法):最大0.1cm(コメント参照)。
WHO分類:凝集性の低い癌(シグネットリング細胞癌および変異を含む)。
組織学的評価:G3(分化が不十分)。
浸潤の程度:腫瘍は固有椎板のみに侵入します。
原発腫瘍:pT1a(腫瘍が固有椎板または粘膜筋に侵襲)。
小血管(血液/リンパ)浸潤:欠如。
大血管(静脈)浸潤:欠如。
ペリニューラル侵入:欠席。
近位食道縁:扁平状の粘膜食道で、浸潤性癌(パートB)は関与していません。
遠位十二指腸縁:浸潤性癌は関与していません。
局所リンパ節:pN0(局所リンパ節転移なし):検査したリンパ節の数:9個。
Bookwalter、Thompson、またはOmni手術用リトラクターのような自己引き込みシステムは、手術中の曝露を大幅に促進します。LigaSureデバイスは効率的な止血解離を促進し、結び目やホチキスを必要とせずに右胃骨頂などの主要な血管柄の分割を可能にします。十二指腸と空腸の両方は、トリステープル技術付きのEndo-GIAタンロードホチキス(0.95-1.12mm高)で分割され、食道空腸吻合術は25mmのCovidien EEAステープラー(4.8mmのステープル高さ)で行われます。
特に開示することはない。
この動画記事で言及されている患者は、撮影に同意しており、情報や画像がオンラインで公開されることを認識しています。
References
- アメリカ臨床腫瘍学会。遺伝性びまん性胃がん。2012年6月25日公開。2021年12月11日アクセス。 https://www.cancer.net/cancer-types/hereditary-diffuse-gastric-cancer
- ハンスフォードS、カウラP、李昌 H他。遺伝性びまん性胃がん症候群:CDH1変異およびそれ以降。 JAMAオンコール。2015;1(1):23-32. doi:10.1001/jamaoncol.2014.168。
- ブレア・V、マクラウド・M、カルネイロ・ Fら。遺伝性びまん性胃がん:最新の臨床実践ガイドライン。 ランセット・オンコール。2020;21巻8号:e386-e397。 doi:10.1016/S1470-2045(20)30219-9。
- リムYC、ディ・ピエトロM、オドノバン Mら。遺伝性びまん性胃がんの基準を満たす家族の患者が内視鏡的監視を受けている場合、評価する前向きコホート研究。 消化管内分泌科。2014;80(1):78-87. doi:10.1016/j.gie.2013.11.040.
- フィッツジェラルド・RC、ハードウィック・R、ハンツマン Dら。遺伝性びまん性胃がん:臨床管理のための最新コンセンサスガイドラインと今後の研究方向。 ジェネル医学雑誌。2010;47(7):436-444. doi:10.1136/JMG.2009.074237。
- シスコRM、フォードJM、ノートンJA。遺伝性びまん性胃がん:スクリーニングおよび予防的手術における遺伝子検査の示唆。 がん。2008;113巻(7号補遺):1850-1856年。 DOI:10.1002/CNCR.23650。
- フリードマンM、アダーT、パテルD、ラウワーズGY、ユンSS、マレンJT、チョンDC。遺伝性びまん性胃がん症候群の管理における監視内視鏡。 クリン・ガストロエンターロール・ヘパトール。2021;19(1):189-191. DOI:10.1016/J.CGH.2019.10.033.
- Li SS、Costantino CL、Mullen JT。全胃切除術の罹患率と死亡率:90日間アウトカムの包括的解析。 J Gastrointest Surg。2019;23(7):1340-1348. DOI:10.1007/s11605-019-04228-7。


.jpg&w=3840&q=75&dpl=dpl_3yD9ySFXbUa5mvXabuURncQ2mg38)