Bonebridge Implant
Main Text
Table of Contents
Les implants à conduction osseuse peuvent améliorer l’audition chez les patients atteints de surdité de transmission ou mixte ainsi que dans les cas de surdité unilatérale (SSD). L’implant Bonebridge est composé de trois composants : un aimant, un transducteur interne et un audio processeur externe. Dans ce cas, le patient avait déjà subi une résection d’un schwannome vestibulaire via une craniotomie de la fosse moyenne dans le but de préserver l’audition. Malheureusement, le patient a finalement perdu l’audition de l’oreille droite, ce qui a entraîné un SSD. Ici, nous démontrons la technique chirurgicale étape par étape de l’implant Bonebridge pour permettre la transmission du son de l’oreille sourde du patient à la cochlée controlatérale via la conduction osseuse.
Les implants à conduction osseuse sont utilisés chez les patients atteints de surdité de transmission ou mixte, ainsi que dans les cas de surdité unilatérale. Le dispositif Bonebridge est un implant à conduction osseuse transcutanée actif qui comporte à la fois des composants internes et externes. 1 La partie implantée se compose à la fois d’un aimant et d’un transducteur de masse flottant à conduction osseuse (BC-FMT), tandis que le composant externe est un audio processeur. Les composants internes et externes sont reliés par voie transcutanée par un aimant, et une pile d’appareil auditif alimente l’audio processeur à l’extérieur. 1 Cette connexion transcutanée est unique en ce sens qu’il n’y a aucun défaut dans la peau ou les tissus mous qui est présent avec les versions antérieures des implants à conduction osseuse. L’audio processeur détecte le son et le transmet à l’implant via l’aimant, qui à son tour vibre à l’intérieur de l’os, ce qui entraîne une conduction osseuse « active » du son. 1 Le Bonebridge peut être réalisé chez des patients âgés de plus de cinq ans (> 12 ans aux États-Unis) qui présentent une surdité unilatérale de transmission ou mixte qui répond à des exigences spécifiques de seuil de moyenne des tons purs. 1, 2 La perte auditive du côté affecté peut être sévère, mais l’oreille controlatérale doit avoir une audition relativement normale (seuil de conduction osseuse supérieur à 20 dB de 500 Hz à 3 kHz). Il est également indiqué chez les patients qui présentent une perte auditive de transmission ou mixte et dont la moyenne des sons purs est inférieure ou égale à 45 dB à 500 Hz et à 1, 2 et 3 kHz. deux
Ce patient a développé une surdité unilatérale après une craniotomie de la fosse moyenne pour la résection d’un schwannome vestibulaire.
La perte auditive est évaluée grossièrement à l’aide des tests de Weber et de Rinne. Ces tests utilisent un diapason pour différencier la perte auditive conductive et neurosensorielle.
Le test de Weber est effectué en plaçant un diapason vibrant sur le front ou l’incisive sur la ligne médiane. On demande au patient d’identifier de quel côté les vibrations sont entendues le plus fort. Si le patient souffre d’une perte auditive de transmission, le son se localisera à l’oreille altérée. Si le patient souffre d’une perte auditive neurosensorielle, le son se localisera dans l’oreille la mieux entendante, indiquant une perte auditive neurosensorielle dans l’oreille opposée. 3, 4
Le test de Rinne est utilisé pour différencier la perte auditive neurosensorielle et la perte auditive de transmission. Le test est effectué en plaçant le diapason vibrant sur l’os mastoïdien derrière l’oreille (conduction osseuse) jusqu’à ce que le patient ne puisse plus entendre, puis en déplaçant rapidement le diapason juste latéralement au conduit auditif externe (conduction aérienne). Chez les patients présentant une audition normale ou une perte auditive neurosensorielle, la conduction aérienne sera perçue comme plus forte que la conduction osseuse. Chez les patients atteints de surdité de transmission, la conduction osseuse sera supérieure à la conduction aérienne. 3, 4 Le test de Rinne peut également être effectué en plaçant le diapason sur la mastoïde et latéralement à l’EAC à des moments séparés et en demandant à quel endroit le patient perçoit le son comme étant plus fort. 3, 4 Cependant, ces tests ne sont pas sans limites, et leur précision varie considérablement. 5 De plus, une seule fréquence (généralement 512 Hz) est testée.
L’étalon-or pour le diagnostic de la perte auditive est un audiogramme à tons purs avec des techniques de masquage appropriées et des scores de reconnaissance des mots. Il fait la distinction entre la perte auditive de transmission et la perte auditive neurosensorielle et fournit également des seuils auditifs qui aident à définir la gravité de la perte auditive et les fréquences auditives les plus affectées. 6
Imagerie
Une tomodensitométrie (TDM) doit être effectuée avant l’implantation de Bonebridge afin d’évaluer l’aptitude de l’os temporal à l’implantation du BC-FMT et d’exclure une pathologie rétrocochléaire. 1 Certains chirurgiens choisissent d’utiliser l’analyse CT 3D pour créer un modèle de puits d’os temporal. D’autres ont même créé des modèles imprimés en 3D de l’os temporal pour la planification dans des cas complexes. 7
La perte auditive unilatérale peut être conductive, neurosensorielle ou mixte, et est différenciée par des tests de Weber et de Rinne ainsi que par un audiogramme. Les étiologies de la surdité de transmission sont nombreuses et comprennent l’otosclérose, la luxation ossiculaire, la déhiscence du canal semi-circulaire supérieur, la malformation congénitale et l’épanchement de l’oreille moyenne. Les étiologies de la perte auditive neurosensorielle comprennent la presbyacousie, la maladie de Ménière, les causes infectieuses et une pathologie rétrocochléaire telle qu’un schwannome vestibulaire. Tout patient présentant une surdité neurosensorielle unilatérale ou asymétrique nécessite une évaluation plus approfondie pour détecter toute pathologie rétrocochléaire. Dans le cadre de ces résultats, une IRM est nécessaire pour évaluer et confirmer le diagnostic. 8 La résection chirurgicale d’un schwannome vestibulaire peut entraîner une perte auditive réduite ou complète. Le risque de cette perte varie en fonction de l’approche chirurgicale. La craniotomie de la fosse moyenne et les approches rétrosigmoïdes permettent de préserver l’audition, mais ces taux varient considérablement et dépendent à la fois du chirurgien et des facteurs du patient/tumoral.
Les patients atteints de SSD peuvent être traités avec une variété d’appareils. Il s’agit d’appareils auditifs, d’implants à conduction osseuse ou même d’implants cochléaires. Une option pour les patients atteints de surdité unilatérale est les appareils auditifs CROS (Air Conduction Conlateral Routing of Signal). Ces appareils acheminent le son de l’oreille non fonctionnelle vers l’oreille fonctionnelle. Cependant, ces dispositifs ne sont acceptés que par 10 à 20 % des patients, 80 à 90 % des patients souffrant de perte auditive unilatérale optant pour un implant à conduction osseuse. 2 La SSD est également de plus en plus traitée par implant cochléaire, avec de plus en plus de preuves de son efficacité et de l’amélioration des scores de qualité de vie des patients.
Le type traditionnel d’implant à conduction osseuse est l’appareil auditif percutané à ancrage osseux (BAHA). Ces dispositifs se composent d’une vis en titane ostéointégrée et d’un pilier, qui fait saillie à travers les tissus mous et la peau. Bien que ces appareils soient efficaces dans le traitement de la perte conductive/auditive et de la surdité unilatérale, ils sont associés à des complications telles que l’infection autour de la vis en titane, la prolifération cutanée et la déhiscence de la plaie. 9
Ces complications sont plus susceptibles de survenir avec les dispositifs percutanés qu’avec les dispositifs transcutanés qui ne communiquent pas avec un environnement extérieur. Les avantages du Bonebridge comprennent une meilleure esthétique et un temps d’activation plus précoce (2 à 4 semaines) car l’appareil ne nécessite pas d’ostéointégration. 1 Il n’y a pas de différences significatives entre les deux appareils en ce qui concerne le gain fonctionnel et les scores de reconnaissance de mots. 9, 10
Les appareils passifs à conduction osseuse reposent sur les vibrations de la peau et des tissus mous et ne font pas vibrer l’os directement. Comme le Bonebridge, ils sont transcutanés, mais le son est capté de l’environnement et transformé en un signal électrique qui stimule ensuite l’aimant et ne stimule pas directement l’os du crâne. 11 Une étude a comparé les dispositifs passifs et actifs et a révélé qu’il y avait des complications cutanées similaires avec le transcutané que le BAHA.
Ce patient était atteint de SSD, l’une des trois principales indications de la pose de Bonebridge.
Le résultat idéal de sa chirurgie serait une amélioration notable de sa capacité à entendre. Une étude de synthèse a révélé que les patients, avec une perte auditive de transmission ou mixte et traités avec l’implant Bonebridge, avaient un gain fonctionnel de 24 à 37 dB, qui était stable dans le temps. 1, 2
La surdité unilatérale est la nouvelle indication de l’implantation de Bonebridge, et il y a moins d’études qui évaluent les résultats chez ces patients. Cependant, les petites études qui ont été réalisées démontrent une amélioration de la reconnaissance vocale dans les environnements calmes et bruyants. 12
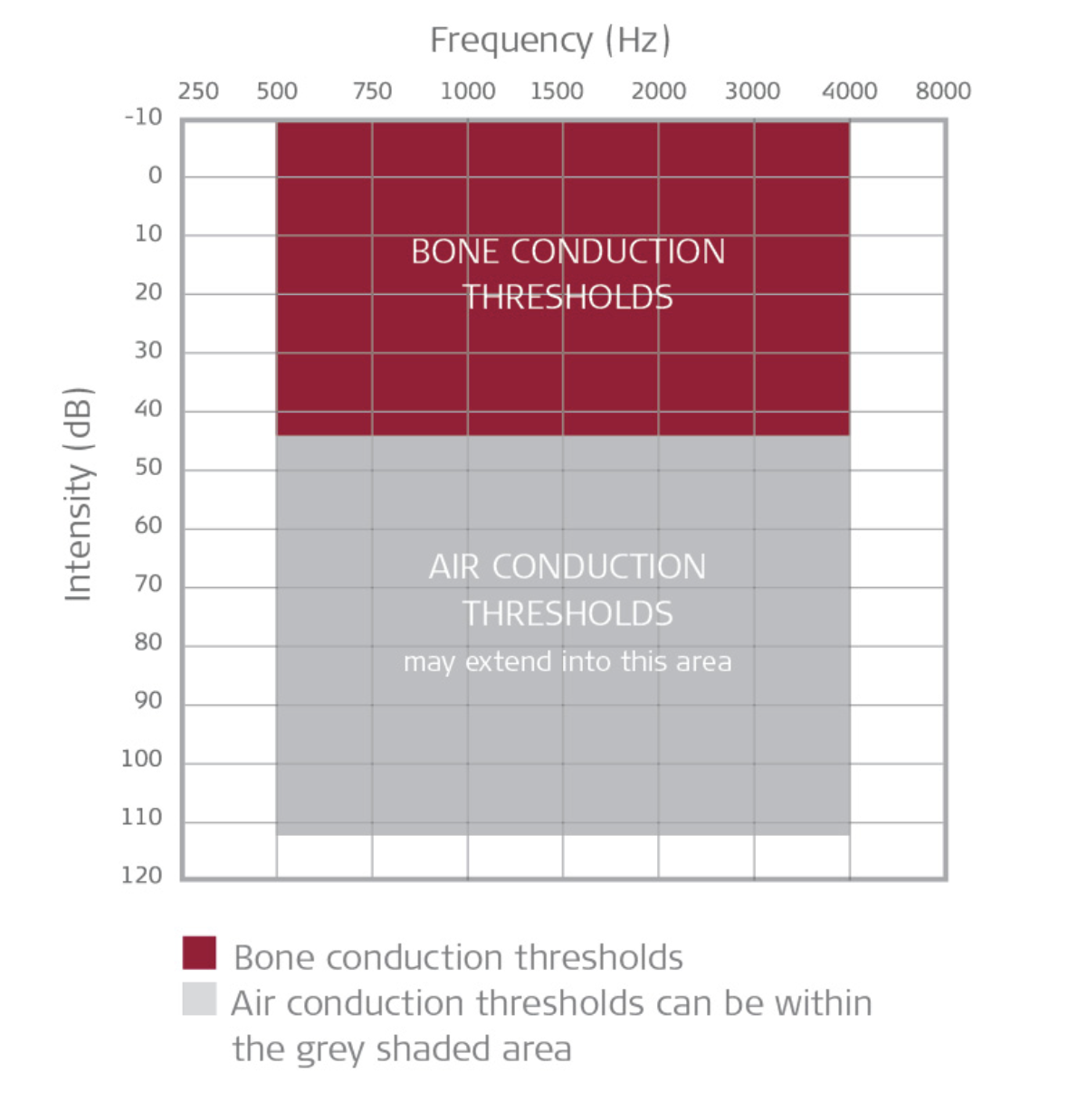
Figure 1 : Critères audiologiques pour Bonebridge.
En plus d’une exigence d’âge, les patients doivent avoir une perte auditive de transmission, mixte ou unilatérale qui répond aux exigences de seuil de moyenne des tons purs précédemment définies. 1, 2 Il a été démontré que les patients atteints d’atrésie du conduit auditif en bénéficient considérablement car ils ont un grand espace air-os avec un mécanisme d’oreille interne préservé. De même, les patients atteints d’otosclérose, de sténose du conduit auditif ou d’une oreille drainante chronique qui empêche l’utilisation d’appareils auditifs traditionnels en bénéficieront également. 1, 2
Après l’implantation de Bonebridge, les patients auront un gros artefact à l’IRM qui affecte considérablement la capacité d’évaluer à la fois les voûtes crâniennes ipsilatérales et controlatérales. 13
La surdité unilatérale a été ajoutée à la liste des indications des implants à conduction osseuse dans les années 2000.2 Le développement d’implants transcutanés à conduction osseuse tels que l’implant Bonebridge a permis de réduire considérablement les complications associées aux modèles percutanés plus traditionnellement utilisés, qui sont utilisés depuis les années 1970.2, 9 Le dispositif Bonebridge a été implanté pour la première fois en 2011. deux
La procédure peut être effectuée sous anesthésie locale ou générale. 1 Les approches comprennent le placement d’une fosse mastoïdienne, rétrosigmoïde ou moyenne. Pour l’approche mastoïdienne, une incision postauriculaire standard est pratiquée. L’exposition du canal postérieur et du cortex mastoïdien doit être réalisée. Ces repères, ainsi que la ligne temporale, aideront à identifier l’angle sinodural, qui est le site idéal pour l’implantation de la BC-FMT. 2 On prend ensuite soin de mesurer l’emplacement de l’appareil dans la mastoïde. L’évaluation préopératoire avec TDM peut aider à assurer une planification appropriée de l’emplacement. Le site est ensuite préparé pour l’implant à l’aide d’une perceuse. La profondeur du foret est déterminée par l’anatomie du patient. Dans les cas où le patient a une mastoïde fine (c’est-à-dire une dure-mère ou une sigmoïde à proximité), un lifting peut être nécessaire afin d’éviter la compression de ces structures. Une nacelle est une rondelle mince dont l’épaisseur peut être fixée aux ailes du BC-FMT, d’une épaisseur de 1 à 4 mm. 2 Une poche sous-périostée est créée à côté du site percé dans la mastoïde pour accueillir la partie bobine du dispositif, similaire à la préparation du site pour un récepteur/stimulateur d’implant cochléaire. Deux avant-trous sont ensuite créés avec le foret inclus dans le kit Bonebridge. Le BC-FMT est fixé à l’aide de deux vis, et la plaie est ensuite fermée en couches.
L’intervention chirurgicale dure moins d’une heure, avec une perte de sang minimale, et est réalisée en ambulatoire. Le résultat esthétique est excellent car l’incision est cachée derrière l’oreille. Il n’y a pas de composants externes permanents par rapport aux modèles percutanés.1 Un dispositif externe est connecté par un aimant pour permettre la conduction des signaux de l’environnement extérieur.
Le Bonebridge offre des avantages substantiels aux patients, avec de meilleurs résultats auditifs et relativement peu de complications. 2 Les effets indésirables après l’implantation sont rares, mais comprennent des douleurs, des étourdissements, des acouphènes ou des infections cutanées mineures. Ces complications disparaissent généralement en quelques jours avec une prise en charge médicale. 2 Les patients atteints de SSD notent généralement des améliorations de la reconnaissance vocale dans des environnements calmes et bruyants, à la fois objectivement et subjectivement. Les patients sont également généralement satisfaits de leurs appareils. deux
L’implant Bonebridge continue d’être une option bien tolérée, sûre et efficace pour le traitement des patients atteints de perte auditive unilatérale, mixte ou de transmission.
Foret diamanté Stryker 5
Kit d’implant Bonebridge
Rien à divulguer.
Le patient visé dans cet article vidéo a donné son consentement éclairé pour être filmé et est conscient que des informations et des images seront publiées en ligne.
References
- Miller ME. Dispositifs auditifs ostéointégrés : Bonebridge. Otolaryngol Clin Amérique du Nord. 2019; 52(2):265-272. doi :10.1016/j.otc.2018.11.006.
- Sprinzl GM, Wolf-Magele A. L’implant auditif à conduction osseuse Bonebridge : critères d’indication, chirurgie et revue systématique de la littérature. Clin Otolaryngol. 2016; 41(2):131-143. doi :10.1111/coa.12484.
- Procédure recommandée pour les essais au diapason de Rinne et Weber. Société britannique d’audiologie. F. J. Audiol. 1987; 21(3):229-230. doi :10.3109/03005368709076410.
- Sheehy JL, Gardner G, Hambley WM. Tests de diapason en otologie moderne. Arc oto-laryngol. 1971; 94(2):132-138. doi :10.1001/archotol.1971.00770070368009.
- Kelly EA, Li B, Adams ME. Précision diagnostique des tests au diapason pour la perte auditive : une revue systématique. Otolaryngol Chirurgie du cou de la tête 2018; 159(2):220-230. doi :10.1177/0194599818770405.
- Davies RA. Audiométrie et autres tests auditifs. Handb Clin Neurol. 2016;137:157-176. doi :10.1016/B978-0-444-63437-5.00011-X.
- Mukherjee P, Cheng K, Flanagan S, Greenberg S. Utilité des os temporaux imprimés en 3D dans la planification préopératoire pour les cas complexes de BoneBridge. Eur Arch Otorhinolaryngol. 2017;274:3021-3028. doi :10.1007/s00405-017-4618-4.
- Reiss M, Reiss G. Zur differentialdiagnose der einseitigen schwerhörigkeit [Diagnostic différentiel de la perte auditive unilatérale]. Praxis (Berne 1994). 2000; 89(6):241-247.
- Gerdes T, Salcher RB, Schwab B, Lenarz T, Maier H. Comparaison des résultats audiologiques entre un instrument à conduction osseuse transcutanée et percutanée dans la perte auditive de transmission. Otol Neurotol. 2016; 37(6):685-691. doi :10.1097/MAO.000000000001010.
- Ihler F, Blum J, Berger MU, Weiss BG, Welz C, Canis M. La prédiction de la reconnaissance vocale dans le bruit avec un système auditif à conduction osseuse semi-implantable par stimulation externe par conduction osseuse externe avec bandeau : une étude prospective. Les tendances entendent. 3 octobre 2016;20:2331216516669330. doi :10.1177/2331216516669330.
- Zernotti ME, Di Gregorio MF, Galeazzi P, Tabernero P. Résultats comparatifs des appareils auditifs actifs et passifs par conduction osseuse transcutanée. Acta Otolaryngol. 2016; 136(6):556-558. doi :10.3109/00016489.2016.1143119.
- Salcher R, Zimmermann D, Giere T, Lenarz T, Maier H. Résultats audiologiques en SSD avec un implant à conduction osseuse transcutanée active en position rétrosigmoïdale. Otol Neurotol. 2017; 38(5):642-647. doi :10.1097/MAO.000000000001394.
- Steinmetz C, Mader I, Arndt S, Aschendorff A, Laszig R, Hassepass F. Artefacts IRM après l’implantation de Bonebridge. Eur arch oto-rhino-laryngol. 2014; 271(7):2079-2082. doi :10.1007/s00405-014-3001-y.
Cite this article
Kaylie DM, Freeman CG, Brown CS. Implant Bonebridge. J Med Insight. 2022; 2022(273). doi :10.24296/jomi/273.


