Bonebridge-Implantat
Main Text
Table of Contents
Knochenleitungsimplantate können das Gehör bei Patienten mit Schallleitungs- oder Mischschwerhörigkeit sowie bei einseitiger Taubheit (SSD) verbessern. Das Bonebridge-Implantat besteht aus drei Komponenten: einem Magneten, einem internen Schallkopf und einem externen Audioprozessor. Der Patient wurde in diesem Fall zuvor einer Resektion eines vestibulären Schwannoms über eine Kraniotomie der mittleren Fossa unterzogen, um das Gehör zu erhalten. Leider verlor der Patient letztendlich das Gehör auf dem rechten Ohr, was zu SSD führte. Hier demonstrieren wir die Schritt-für-Schritt-Operationstechnik für das Bonebridge-Implantat, um eine Schallübertragung vom tauben Ohr des Patienten zur kontralateralen Cochlea über die Knochenleitung zu ermöglichen.
Knochenleitungsimplantate werden bei Patienten mit Schallleitungs- oder Mischschwerhörigkeit sowie bei einseitiger Taubheit eingesetzt. Das Bonebridge-Gerät ist ein aktives transkutanes Knochenleitungsimplantat, das sowohl interne als auch externe Komponenten aufweist. 1 Der implantierte Teil besteht sowohl aus einem Magneten als auch aus einem Knochenleitungs-Floating-Masse-Wandler (BC-FMT), während die externe Komponente ein Audioprozessor ist. Die internen und externen Komponenten sind transkutan über einen Magneten verbunden, und eine Hörgerätebatterie versorgt den Audioprozessor extern. 1 Diese transkutane Verbindung ist insofern einzigartig, als es keinen Defekt in der Haut oder im Weichgewebe gibt, der bei früheren Versionen von Knochenleitungsimplantaten vorhanden ist. Der Audioprozessor erkennt Schall und überträgt ihn über den Magneten an das Implantat, der wiederum im Knochen vibriert, was zu einer "aktiven" Knochenschallleitung führt. 1 Die Bonebridge kann bei Patienten über fünf Jahren (> 12 in den Vereinigten Staaten) durchgeführt werden, die einen Schallleitungs- oder gemischten einseitigen Hörverlust haben, der bestimmte Anforderungen an die durchschnittliche Reintonschwelle erfüllt. 1, 2 Der Hörverlust auf der betroffenen Seite kann schwerwiegend sein, aber das kontralaterale Ohr sollte ein relativ normales Gehör haben (Knochenleitungsschwelle über 20 dB von 500 Hz bis 3 kHz). Es ist auch indiziert bei Patienten mit Schallleitungs- oder Mischschwerhörigkeit und einem Knochenreintondurchschnitt von höchstens 45 dB bei 500 Hz und 1, 2 und 3 kHz. arabische Ziffer
Dieser Patient entwickelte eine einseitige Taubheit nach einer mittleren Fossa-Kraniotomie zur Resektion eines vestibulären Schwannoms.
Hörverlust wird grob mit den Weber- und Rinne-Tests bewertet. Diese Tests verwenden eine Stimmgabel, um zwischen Schallleitungs- und Schallempfindungsschwerhörigkeit zu unterscheiden.
Der Weber-Test wird durchgeführt, indem eine vibrierende Stimmgabel über die Stirn oder den Schneidezahn an der Mittellinie gelegt wird. Der Patient wird gebeten zu erkennen, auf welcher Seite die Vibrationen lauter zu hören sind. Wenn der Patient einen Schallleitungsschwerhörigkeit hat, lokalisiert sich der Schall für das beeinträchtigte Ohr. Wenn der Patient einen sensorineuralen Hörverlust hat, lokalisiert sich der Klang auf das besser hörende Ohr, was auf einen sensorineuralen Hörverlust im gegenüberliegenden Ohr hinweist. 3, 4
Der Rinne-Test dient zur Unterscheidung zwischen sensorineuraler und Schallleitungsschwerhörigkeit. Der Test wird durchgeführt, indem die vibrierende Stimmgabel über den Warzenknochen hinter dem Ohr gelegt wird (Knochenleitung), bis der Patient nicht mehr hören kann, und dann die Stimmgabel schnell seitlich zum äußeren Gehörgang bewegt wird (Luftleitung). Bei Patienten mit normalem Gehör oder sensorineuralem Hörverlust wird die Luftleitung als lauter empfunden als die Knochenleitung. Bei Patienten mit Schallleitungsschwerhörigkeit ist die Knochenleitung größer als die Luftleitung. 3, 4 Der Rinne-Test kann auch durchgeführt werden, indem die Stimmgabel zu getrennten Zeiten auf dem Mastoid und seitlich zum EAC platziert wird und gefragt wird, an welcher Stelle der Patient das Geräusch lauter wahrnimmt. 3, 4 Diese Tests sind jedoch nicht ohne Einschränkungen, und es gibt erhebliche Unterschiede in ihrer Genauigkeit. 5 Zusätzlich wird nur eine einzige Frequenz (typischerweise 512 Hz) getestet.
Der Goldstandard für die Diagnose von Hörverlust ist ein Reinton-Audiogramm mit geeigneten Maskierungstechniken und Worterkennungswerten. Es unterscheidet zwischen Schallleitungs- und Schallempfindungsschwerhörigkeit und bietet auch Hörschwellengrenzwerte, die helfen, den Schweregrad des Hörverlusts und die am stärksten betroffenen Hörfrequenzen zu definieren. 6
Bildgebung
Die Computertomographie (CT) muss vor der Bonebridge-Implantation durchgeführt werden, um die Eignung des Schläfenbeins für die Implantation des BC-FMT zu beurteilen und eine retrocochleare Pathologie auszuschließen. 1 Einige Chirurgen entscheiden sich für die 3D-CT-Analyse, um eine Vorlage für den Schläfenknochenwell zu erstellen. Andere haben sogar 3D-gedruckte Modelle des Schläfenbeins für die Planung in komplexen Fällen erstellt. 7
Einseitiger Hörverlust kann konduktiv, sensorineural oder gemischt sein und wird durch Weber- und Rinne-Tests sowie ein Audiogramm unterschieden. Die Ätiologien des Schallleitungsschwerhörs sind zahlreich und umfassen Otosklerose, Gehörknöchelchendislokation, Dehiszenz des oberen halbkreisförmigen Kanals, angeborene Fehlbildungen und Mittelohrerguss. Zu den Ätiologien des sensorineuralen Hörverlusts gehören Presbyakusis, Morbus Menière, infektiöse Ursachen und eine retrocochleäre Pathologie wie ein vestibuläres Schwannom. Jeder Patient mit einseitigem oder asymmetrischem sensorineuralem Hörverlust muss weiter untersucht werden, um eine retrocochleäre Pathologie zu erkennen. Im Rahmen dieser Befunde ist ein MRT erforderlich, um die Diagnose weiter zu bewerten und zu bestätigen. 8 Die chirurgische Resektion eines vestibulären Schwannoms kann zu einem verminderten oder vollständigen Hörverlust führen. Das Risiko dieses Verlustes variiert je nach chirurgischem Ansatz. Sowohl die Granulotomie der mittleren Fossa als auch die retrosiggoiden Ansätze ermöglichen die Erhaltung des Gehörs, aber diese Raten variieren stark und hängen sowohl von Chirurgen- als auch von Patienten- / Tumorfaktoren ab.
Patienten mit SSD können mit einer Vielzahl von Geräten behandelt werden. Diese reichen von Hörgeräten, Knochenleitungsimplantaten bis hin zu Cochlea-Implantaten. Eine Option für Patienten mit einseitiger Taubheit ist das konlaterale Routing von Signalhörgeräten (CROS). Diese Geräte leiten Schall vom nicht funktionierenden Ohr zum funktionellen Ohr. Diese Geräte werden jedoch nur von 10-20% der Patienten akzeptiert, wobei 80-90% der Patienten mit einseitigem Hörverlust sich für ein Knochenleitungsimplantat entscheiden. 2 SSD wird auch zunehmend mit Cochlea-Implantaten behandelt, wobei die Wirksamkeit und die Verbesserung der Lebensqualität der Patienten zunehmen.
Die traditionelle Art des Knochenleitungsimplantats ist das perkutane, knochenverankerte Hörgerät (BAHA). Diese Geräte bestehen aus einer osseointegrierten Titanschraube und einem Abutment, das durch das Weichgewebe und die Haut ragt. Während diese Geräte bei der Behandlung von Schallleitungs- / Hörverlust und einseitiger Taubheit wirksam sind, sind sie mit Komplikationen wie Infektionen um die Titanschraube, Hautüberwucherung und Wunddehiszenz verbunden. 9
Diese Komplikationen treten bei perkutanen Geräten häufiger auf als bei transkutanen Geräten, die nicht mit einer äußeren Umgebung kommunizieren. Zu den Vorteilen der Bonebridge gehören eine verbesserte Kosmetik und eine frühere Aktivierungszeit (2-4 Wochen), da das Gerät keine Osseointegration erfordert. 1 Es gibt keine signifikanten Unterschiede zwischen den beiden Geräten in Bezug auf Funktionsverstärkung und Worterkennungswerte. 9, 10
Passive Knochenleitungsgeräte sind auf die Vibration der Haut und des Weichgewebes angewiesen und vibrieren den Knochen nicht direkt. Wie die Bonebridge sind sie transkutan, aber der Schall wird aus der Umgebung eingefangen und in ein elektrisches Signal umgewandelt, das dann den Magneten stimuliert und den Schädelknochen nicht direkt stimuliert. 11 Eine Studie verglich die passiven und aktiven Geräte und stellte fest, dass es ähnliche kutane Komplikationen mit transkutan wie die BAHA gab.
Dieser Patient hatte SSD, eine der drei primären Indikationen für die Bonebridge-Platzierung.
Das ideale Ergebnis ihrer Operation wäre eine spürbare Verbesserung ihrer Hörfähigkeit. Eine Übersichtsstudie ergab, dass die Patienten mit Schallleitungs- oder Mischverlustgehör, die mit dem Bonebridge-Implantat behandelt wurden, einen funktionellen Gewinn von 24 bis 37 dB aufwiesen, der im Laufe der Zeit stabil war. 1, 2
Einseitige Taubheit ist die neueste Indikation für die Bonebridge-Implantation, und es gibt weniger Studien, die die Ergebnisse bei diesen Patienten bewerten. Die kleineren Studien, die abgeschlossen wurden, zeigen jedoch eine verbesserte Spracherkennung sowohl in ruhigen als auch in lauten Umgebungen. 12
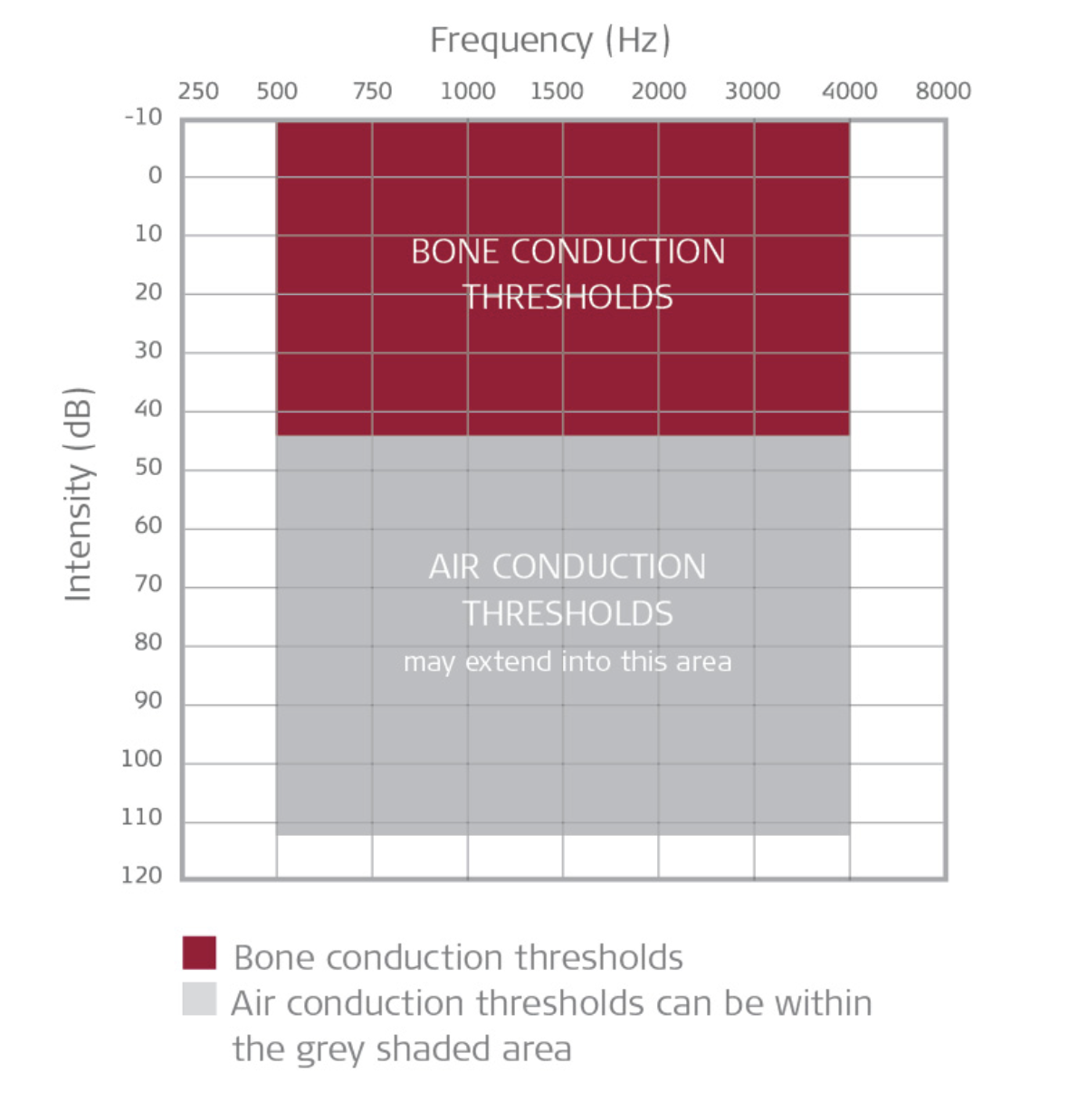
Abbildung 1: Audiologische Kriterien für Bonebridge.
Zusätzlich zu einer Altersanforderung sollten Patienten einen Schallleitungs-, Misch- oder einseitigen Hörverlust haben, der die zuvor definierten Anforderungen an den Reintondurchschnittsschwellenwert erfüllt. 1, 2 Patienten mit Gehörgangsatresie haben nachweislich erhebliche Vorteile, da sie eine große Luft-Knochen-Lücke mit einem erhaltenen Innenohrmechanismus aufweisen. Ebenso profitieren Patienten mit Otosklerose, Gehörgangstenose oder einem chronisch entleerenden Ohr, das die Verwendung herkömmlicher Hörgeräte verhindert. 1, 2
Nach der Bonebridge-Implantation haben die Patienten ein großes Artefakt im MRT, das die Fähigkeit, sowohl die ipsilateralen als auch die kontralateralen Schädelgewölbe zu beurteilen, signifikant beeinflusst. 13
Einseitige Taubheit wurde in den 2000er Jahren in die Liste der Indikationen für Knochenleitungsimplantate aufgenommen.2 Die Entwicklung transkutaner Knochenleitungsimplantate wie des Bonebridge-Implantats ermöglichte eine erhebliche Reduzierung der Komplikationen im Zusammenhang mit den traditionell verwendeten perkutanen Modellen, die seit den 1970er Jahren verwendet werden.2, 9 Das Bonebridge-Gerät wurde erstmals 2011 implantiert. arabische Ziffer
Das Verfahren kann entweder unter örtlicher Betäubung oder Vollnarkose durchgeführt werden. 1 Ansätze umfassen eine Mastoid-, Retrosigmoid- oder mittlere Fossa-Platzierung. Für den Warzenzugang wird ein postaurikulärer Standardschnitt durchgeführt. Die Exposition sowohl des hinteren Kanals als auch des mastoiden Kortex sollte durchgeführt werden. Diese Orientierungspunkte werden zusammen mit der zeitlichen Linie helfen, den sinoduralen Winkel zu identifizieren, der der ideale Ort für die Implantation des BC-FMT ist. 2 Es wird dann darauf geachtet, zu messen, wo sich das Gerät im Mastoid befindet. Die präoperative Beurteilung mit CT kann dazu beitragen, eine angemessene Standortplanung sicherzustellen. Anschließend wird die Stelle mit einem Bohrer für das Implantat vorbereitet. Die Bohrtiefe wird durch die Anatomie des Patienten bestimmt. In Fällen, in denen der Patient einen dünnen Mastoid hat (d. H. Dura oder Sigmoid in unmittelbarer Nähe), kann ein Lift erforderlich sein, um eine Kompression dieser Strukturen zu vermeiden. Ein Lift ist eine dünne Unterlegscheibe, die an den Flügeln des BC-FMT mit einer Dicke von 1 bis 4 mm befestigt werden kann. 2 Eine subperiostale Tasche wird neben der gebohrten Stelle im Mastoid geschaffen, um den Spulenteil des Geräts aufzunehmen, ähnlich der Standortvorbereitung für einen Cochlea-Implantat-Empfänger/-Stimulator. Mit dem Bohrer, der im Bonebridge-Kit enthalten ist, werden dann zwei Pilotlöcher erstellt. Der BC-FMT wird mit zwei Schrauben gesichert und die Wunde anschließend schichtweise verschlossen.
Die Operation dauert weniger als eine Stunde, mit minimalem Blutverlust und wird ambulant durchgeführt. Das kosmetische Ergebnis ist hervorragend, da der Schnitt hinter dem Ohr verborgen ist. Im Vergleich zu perkutanen Modellen gibt es keine permanenten externen Komponenten.1 Ein externes Gerät ist über einen Magneten angeschlossen, um die Leitung von Signalen aus der äußeren Umgebung zu ermöglichen.
Die Bonebridge bietet den Patienten erhebliche Vorteile mit verbesserten Hörergebnissen und relativ wenigen Komplikationen. 2 Nebenwirkungen nach der Implantation sind selten, umfassen jedoch Schmerzen, Schwindel, Tinnitus oder kleinere Hautinfektionen. Diese Komplikationen klingen in der Regel innerhalb weniger Tage mit medizinischer Behandlung ab. 2 Patienten mit SSD bemerken typischerweise Verbesserungen der Spracherkennung in ruhigen und lauten Umgebungen, sowohl objektiv als auch subjektiv. Es wird auch festgestellt, dass die Patienten im Allgemeinen mit ihren Geräten zufrieden sind. arabische Ziffer
Das Bonebridge-Implantat ist nach wie vor eine gut verträgliche, sichere und wirksame Option für die Behandlung von Patienten mit einseitigem, gemischtem oder Schallleitungsschwerhörigkeit.
Stryker 5 Diamantbohrer
Bonebridge Implantat-Kit
Nichts zu enthüllen.
Der in diesem Videoartikel erwähnte Patient hat seine informierte Zustimmung zum Filmen gegeben und ist sich bewusst, dass Informationen und Bilder online veröffentlicht werden.
References
- Miller ME. Osseointegrierte Hörgeräte: Bonebridge. Otolaryngol Clin North Am. 2019;52(2):265-272. doi:10.1016/j.otc.2018.11.006.
- Sprinzl GM, Wolf-Magele A. Das Knochenleitungs-Hörimplantat Bonebridge: Indikationskriterien, Operation und systematische Literaturübersicht. Clin Otolaryngol. 2016;41(2):131-143. doi:10.1111/coa.12484.
- Empfohlene Vorgehensweise für Rinne und Weber Stimmgabeltests. British Society of Audiology. Br J Audiol. 1987;21(3):229-230. doi:10.3109/03005368709076410.
- Sheehy JL, Gardner G, Hambley WM. Stimmgabeltests in der modernen Otologie. Arch Otolaryngol. 1971;94(2):132-138. doi:10.1001/archotol.1971.00770070368009.
- Kelly EA, Li B, Adams ME. Diagnostische Genauigkeit von Stimmgabeltests für Hörverlust: eine systematische Überprüfung. Otolaryngol Kopf Hals Surg. 2018;159(2):220-230. doi:10.1177/0194599818770405.
- Davies RA. Audiometrie und andere Hörtests. Handb Clin Neurol. 2016;137:157-176. doi:10.1016/B978-0-444-63437-5.00011-X.
- Mukherjee P, Cheng K, Flanagan S, Greenberg S. Nutzen von 3D-gedruckten Schläfenknochen in der präoperativen Planung für komplexe BoneBridge-Fälle. Eur Arch Otorhinolaryngol. 2017;274:3021-3028. doi:10.1007/s00405-017-4618-4.
- Reiss M, Reiss G. Zur Differentialdiagnose der einseitigen Schwerhörigkeit. Praxis (Bern 1994). 2000;89(6):241-247.
- Gerdes T, Salcher RB, Schwab B, Lenarz T, Maier H. Vergleich audiologischer Ergebnisse zwischen einem transkutanen und einem perkutanen Knochenleitungsinstrument bei Schallleitungsschwerhörigkeit. Otol Neurotol. 2016;37(6):685-691. doi:10.1097/MAO.0000000000001010.
- Ihler F, Blum J, Berger MU, Weiss BG, Welz C, Canis M. Die Vorhersage der Spracherkennung bei Lärm mit einem semiimplantierbaren Knochenleitungshörsystem durch externe Knochenleitungsstimulation mit Stirnband: eine prospektive Studie. Trends hören. 2016 Okt 3;20:2331216516669330. doi:10.1177/2331216516669330.
- Zernotti ME, Di Gregorio MF, Galeazzi P, Tabernero P. Comparative outcomes of active and passive hearing devices by transcutaneous bone conduction. Acta Otolaryngol. 2016;136(6):556-558. doi:10.3109/00016489.2016.1143119.
- Salcher R, Zimmermann D, Giere T, Lenarz T, Maier H. Audiologische Ergebnisse in SSD mit einem aktiven transkutanen Knochenleitungsimplantat in retrosigmoidaler Position. Otol Neurotol. 2017;38(5):642-647. doi:10.1097/MAO.0000000000001394.
- Steinmetz C, Mader I, Arndt S, Aschendorff A, Laszig R, Hassepass F. MRT-Artefakte nach Bonebridge-Implantation. Eur Arch Otorhinolaryngol. 2014;271(7):2079-2082. doi:10.1007/s00405-014-3001-y.
Cite this article
Kaylie DM, Freeman CG, Brown CS. Bonebridge Implantat. J Med Einblick. 2022;2022(273). doi:10.24296/jomi/273.


