Rectopexia de sutura laparoscópica conculdoplastia, reparación de la pared vaginal y perineorrafia para el prolapso rectal
1,2; 1,2*; 1,3*
1Pelvic Floor Disorders Center, Massachusetts General Hospital, Boston, MA
2Department of Obstetrics, Gynecology and Reproductive Biology, Massachusetts General Hospital, Boston, MA
3Section of Colorectal Surgery, Department of Surgery, Massachusetts General Hospital, Boston, MA
*Operating Surgeons
Main Text
Table of Contents
La paciente es una mujer de 87 años que presentaba antecedentes de estreñimiento y prolapso rectal molesto que requería reducción manual del prolapso rectal. En el examen, se encontró que tenía prolapso rectal de espesor completo y prolapso de órganos pélvicos de la pared vaginal posterior en estadio II. Deseaba un manejo quirúrgico definitivo de su prolapso y optó por una rectopexia de sutura laparoscópica y reparación de la pared vaginal posterior y perineorrafia. Se le realizó pruebas de fisiología anorrectal y urodinámicas, así como una defecografía antes de la cirugía para ayudar con la planificación quirúrgica. La cirugía no fue complicada. Fue dada de alta el primer día postoperatorio y su recuperación postoperatoria no fue notable.
La paciente es una mujer de 87 años con antecedentes médicos significativos para el síndrome del intestino irritable con estreñimiento que presentó síntomas de estreñimiento refractarios a los cambios en la dieta y abultamiento rectal molesto que requirió reducción manual. Ella negó la incontinencia urinaria. Ella es nulípara y no sexualmente activa.
En el examen, su abdomen estaba blando, no distraído y sin ningún tipo de evidencia de hernias. Tenía una incisión vertical en la línea media de la piel bien curada. En el examen pélvico, con Valsalva, la pared vaginal posterior descendió 1 cm más allá del himen. En el examen rectovaginal, tenía un bolsillo rectovaginal. Finalmente, mientras estaba sentada en el inodoro, se descubrió que tenía prolapso rectal de espesor completo con esfuerzo, así como un ano patuloso en reposo.
El paciente se sometió a una defecografía, y los resultados se pueden ver en la Figura 1.
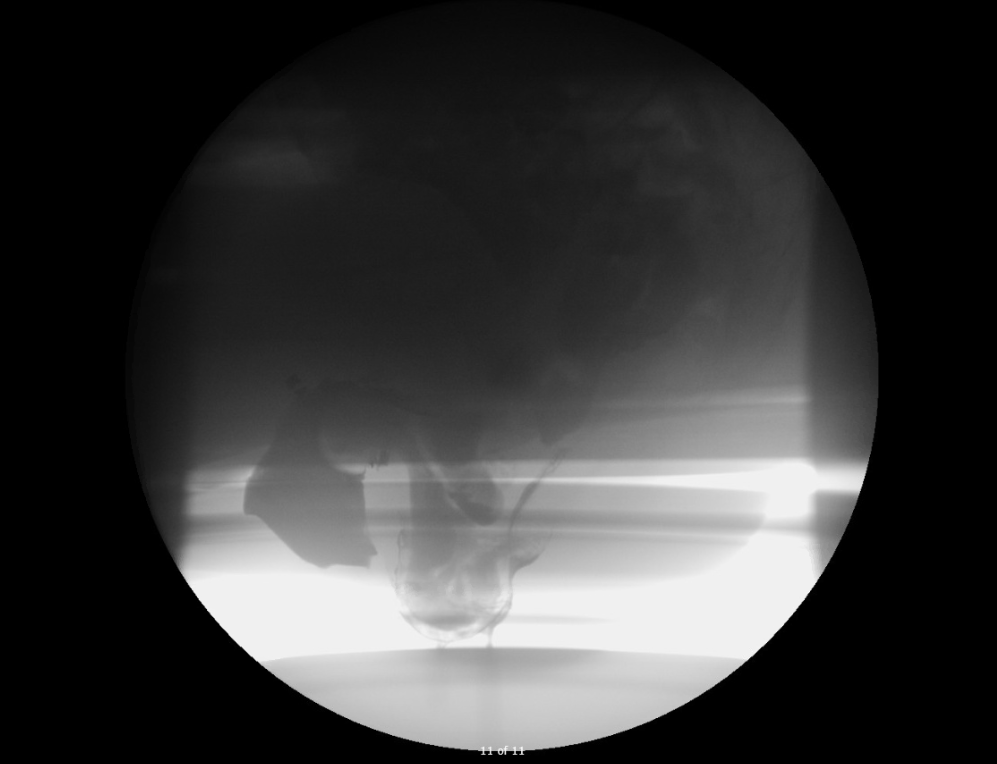
Figura 1. Resultados de la defecografía
Invaginación rectorrectal de espesor completo con prolapso rectal.
Invaginación intestinal posterior de un enterocele en el recto y la vagina.
En la manometría anorrectal, se encontró que tenía un tono muy bajo tanto en reposo como con compresión. Se realizaron pruebas urodinámicas (UDT) para descartar la incontinencia urinaria de esfuerzo oculta. En la UDT, no hubo incontinencia urinaria de esfuerzo con reducción del prolapso, no hubo hiperactividad del detrusor y capacidad normal de la vejiga. La recomendación fue que no se realizara ningún procedimiento contra la incontinencia en el momento de la reparación del prolapso.
En la defecografía, hubo un prolapso rectal con un enterocele prolapsado en el recto y la vagina.
Sus estudios de laboratorio preoperatorios incluyeron hemograma completo, panel metabólico básico y un electrocardiograma (ECG). Todos los valores estaban dentro de los límites normales. El ECG mostró un ritmo sinusal normal. Fue autorizada médicamente para la cirugía.
Si no se trata, el prolapso rectal puede provocar incontinencia anal secundaria al estiramiento crónico del esfínter anal y la neuropatía posterior. También se puede ver estreñimiento o defecación obstruida. En raras ocasiones, el prolapso rectal puede causar encarcelamiento o estrangulamiento del recto prolapsado. 1 Hay informes raros de isquemia2 por prolapso rectal y gangrena. 3
El tratamiento del prolapso rectal depende de los síntomas, los objetivos y los antecedentes médicos y quirúrgicos anteriores del paciente. Desafortunadamente, esta afección no tiene opciones de tratamiento no quirúrgico y, en general, se desaconseja el manejo expectante porque el prolapso rectal tiende a empeorar con el tiempo; si no se trata, puede provocar incontinencia anal.
Las opciones quirúrgicas para el tratamiento del prolapso rectal incluyen:
- Rectopexia de sutura posterior abierta o mínimamente invasiva (laparoscópica o robótica):
- Sin resección sigmoide: esto está particularmente indicado para pacientes con incontinencia o que tienen un alto riesgo de incontinencia (es decir, con presiones anales muy bajas en las pruebas de fisiología anorrectal).
- Con resección sigmoide – para pacientes con estreñimiento concomitante.
- La decisión de proceder con una técnica abierta o mínimamente invasiva se guía por la experiencia del proveedor y la idoneidad del paciente.
- Rectopexia de malla ventral abierta o mínimamente invasiva (laparoscópica o robótica): Este enfoque omite la disección del recto posteriormente y, por lo tanto, se cree que ahorra nervios. Se describió para pacientes con invaginación intestinal interna y prolapso de espesor completo. Es una buena opción para pacientes con hernias sin salida concomitantes (enteroceles, sigmoidoceles) o pacientes con síntomas de incontinencia fecal y estreñimiento. Es importante mencionar que a las pacientes con rectocele asociado se les podría ofrecer una sacrocolpopexia combinada cuando el ápice de la vagina está mal suspendido. En los casos en que es necesario abordar un enterocele, a los pacientes que buscan reparación de tejido nativo a menudo se les ofrece una culdoplastia.
- Perineal: Este enfoque se asocia con una menor morbilidad; sin embargo, muchos creen que conduce a un riesgo mucho mayor de recurrencia. También hay mucho debate sobre el resultado funcional, y algunos expertos sugieren un aumento en la incontinencia fecal postoperatoria en comparación con los pacientes tratados con enfoques abdominales no reseccionales. Dadas estas preocupaciones, en general, este enfoque se reserva para pacientes con comorbilidades significativas.
La Sociedad Americana de Cirujanos de Colon y Recto recomienda procedimientos abdominales como la fijación rectal en pacientes sanos. 4 Los abordajes perineales deben reservarse para pacientes con comorbilidades preexistentes y donde se desee minimizar la morbilidad del procedimiento.
A pesar de la reparación quirúrgica, los problemas funcionales como el estreñimiento pueden persistir. 1, 3 La elección del procedimiento también puede empeorar la función en algunos pacientes al precipitar la incontinencia fecal (después de una resección intestinal) o el estreñimiento (después de la denervación del suelo pélvico).
Hasta el 3% de las mujeres en los Estados Unidos informan tener algún tipo de prolapso de órganos pélvicos,1 y el prolapso rectal afecta al 1% de los adultos mayores de 65 años de edad. 5
Los factores de riesgo para el prolapso rectal incluyen el sexo femenino,1, 5 años mayores de 40,1, 5 multiparidades,1, 6 partos vaginales de bebés que son grandes para la edad gestacional,1 y estreñimiento crónico. 1 Otros factores de riesgo incluyen anomalías anatómicas pélvicas como la bolsa profunda de Douglas, afecciones atónicas del suelo pélvico o del canal anal y falta de fijación normal del recto. 1 Los trastornos del tejido conectivo como los síndromes de Marfan y Ehlers-Danlos y algunas afecciones neurológicas como accidente cerebrovascular, demencia y lesiones de la médula espinal también se han asociado con el prolapso rectal. 1
La causa del prolapso rectal es multifactorial. Generalmente, comienza como una invaginación intestinal del recto que progresa hasta la evisceración final del recto a través de un ano patuloso. 1, 5, 6
Hay características anatómicas que se han descrito asociadas con el prolapso rectal, como un colon sigmoide redundante, diástasis del elevador ano, callejón sin salida profundo y falta de fijación normal del recto, dando lugar a un mesorrecto excepcionalmente hipermóvil y laxitud de los ligamentos laterales. El objetivo de la cirugía es restaurar la anatomía y abordar estas características.
Para esta paciente, debido a que la manometría anorrectal mostró un tono de esfínter bajo en reposo y con compresión, se sintió que estas bajas presiones la ponían en riesgo de desarrollar incontinencia fecal con cualquier cirugía que requiriera resección intestinal. Esto llevó a la decisión de ofrecer una rectopexia sin resección en lugar de una rectopexia de resección.
Dados los hallazgos del enterocele en su defecografía, discutimos las mejores maneras de abordarlo en el momento de la cirugía. Se discutió la opción de la cultoplastia versus una rectopexia de malla ventral. En última instancia, se determinó que, dado el hecho de que la pared posterior de la vagina estaba bien suspendida, probablemente le iría muy bien con una reparación nativa como una culdoplastia, y que la malla podría realizarse en caso de que hubiera una recurrencia futura.
Después de la evaluación y el asesoramiento, este paciente optó por someterse a un procedimiento quirúrgico.
El paciente fue llevado al quirófano donde se obtuvo anestesia general con un tubo endotraqueal. Se colocó una sonda gástrica oral. Recibió heparina subcutánea para profilaxis de tromboembolismo venoso y cefazolina intravenosa y metronidazol para profilaxis antibiótica. Fue colocada en la posición de litotomía dorsal en estribos de aleta amarilla. Se colocó un catéter Foley permanente en la vejiga y se drenó la vejiga.
La entrada en el abdomen se realizó bajo visión directa mediante la técnica de Hasson. Una vez confirmada la entrada abdominal, el abdomen fue insuflado con CO2. Se realizó una encuesta abdominal, y se observó que había una bolsa profunda de Douglas, intestino delgado y grueso normal, así como útero y anexos normales. Se colocaron tres puertos laparoscópicos adicionales bajo visualización directa: un puerto de 10 mm en el cuadrante inferior derecho, un puerto de 5 mm en el cuadrante superior derecho y un puerto de 5 mm en el cuadrante inferior izquierdo. El prolapso rectal se redujo. Una vez que se identificó la anatomía presacral a nivel de S1, el promontorio sacro se limpió con el dispositivo armónico. Usando el armónico, el recto se liberó de sus uniones sacras y laterales hasta los elevadores, con una cuidadosa atención para transectar el tallo lateral derecho del recto mientras se preservaba el izquierdo para mantener parte de la inervación al recto. La bolsa profunda de Douglas se abrió en el extremo más distal, y el recto anterior se separó de la vagina al cuerpo perineal.
El recto se aseguró entonces en tensión al promontorio sacro con tres suturas de 0 Gore-Tex. El recto se elevó hacia el abdomen, y el borde cortado de la bolsa de Douglas se elevó al nivel del promontorio sacro. Todas las suturas fueron atadas extracorpóreamente.
Una vez que se completó la rectopexia de sutura, la atención se dirigió a laculdoplastia laparoscópica. Utilizando los puertos laparoscópicos colocados previamente, se colocaron suturas de púas V-Loc 3-0. Se aproximó el peritoneo que recubre el recto anterior y la pared lateral pélvica, borrando así el callejón sin salida posterior.
Luego se realizó cistoscopia, notable por fuertes chorros ureterales bilaterales y mucosa vesical normal sin evidencia de cálculos, lesiones u objetos extraños.
La fascia del puerto del cuadrante inferior derecho de 12 mm se cerró con un Vicryl 0 (Polyglactin 910) utilizando un dispositivo de cierre de fascia laparoscópica. La fascia umbilical se cerró con 0 Vicryl (Poliglactina 910) bajo visualización directa. Las incisiones en la piel se reapromiguularon utilizando 4-0 Monocryl (Poliglecaprone 25) seguido de Steri-Strips.
Una vez que se completó el procedimiento laparoscópico, la atención se centró en la reparación posterior y la perineorrafia extendida para abordar el prolapso de la pared vaginal posterior. La fourchette posterior se agarró a ambos lados con abrazaderas Allis. El área de disección anticipada se inyectó con Marcaine al 0,25% con epinefrina. Luego se realizó una incisión en forma de diamante sobre la piel del cuerpo perineal y el epitelio vaginal posterior. Se extirpó la piel que recubre el cuerpo perineal y el epitelio vaginal posterior. El cuerpo perineal fue diseccionado bruscamente del tabique rectovaginal. La incisión vaginal de la línea media se realizó desde el perineo hasta el borde proximal del rectocele. El epitelio vaginal se diseccionó del tejido conectivo rectovaginal subyacente. Usando un dedo colocado en el recto como guía, la capa fibromuscular rectovaginal se imbricó usando 2-0 PDS II (Polidioxanona) de manera corriente. Se colocó una capa adicional para el refuerzo. De este modo, se logró un excelente soporte de la pared vaginal posterior y se recortó el exceso de epitelio vaginal. El cuerpo perineal se volvió a unir a la fascia rectovaginal y se recreó utilizando una serie de puntos de corona de 0 Vicryl (Poliglactina 910). La incisión de la línea media se cerró de manera corriente usando 2-0 Vicryl (Polyglactin 910). El perineo se cerró con suturas submucosas y subcutáneas. La lesión rectal se excluyó con un examen rectal digital después de la reparación.
El paciente se sometió a un ensayo de anulación de relleno en el primer día postoperatorio. La vejiga se llenó a través del catéter Foley con 300 ml de agua estéril. Se retiró el catéter de Foley y el paciente pudo anular más de 200 ml, pasando así el ensayo de micción. Posteriormente, cumplió con todos los criterios de alta y fue dada de alta en casa el primer día postoperatorio después de una estancia hospitalaria poco notable.
El paciente fue atendido a las dos y siete semanas del postoperatorio. En estas visitas, informó que estaba bien y negó cualquier síntoma de prolapso, incontinencia anal o urinaria, o disfunción miccional.
- Bisturí armónico (Johnson & Johnson USA)
- Cistoscopio de 70 grados
Nada que revelar.
El paciente al que se hace referencia en este video artículo ha dado su consentimiento informado para ser filmado y es consciente de que la información y las imágenes se publicarán en línea.
Citations
- Bordeianou L, Hicks CW, Kaiser AM, Alavi K, Sudan R, Wise PE. Prolapso rectal: una visión general de las características clínicas, el diagnóstico y las estrategias de manejo específicas del paciente. J Gastrointest Surg Off J Soc Surg Aliment Tract. 2014;18(5):1059-1069. doi:10.1007/s11605-013-2427-7.
- La Torre F, La Torre V, Mazzi M, Giuliani A, Pontone S, La Gioia G. Tratamiento quirúrgico de la isquemia del prolapso rectal. Coloproctología Tecnológica. 2005;9(2):170.
- Borgaonkar VD, Deshpande SS, Borgaonkar VV, Rathod MD. Rectosigmoidectomía perineal de emergencia para el prolapso rectal gangrenoso: una experiencia de un solo centro con revisión de la literatura. Indio J Surg. 2017;79(1):45-50. doi:10.1007/s12262-016-1562-2.
- Bordeianou L, Paquette I, Johnson E, et al. Clinical Practice Guidelines for the Treatment of Rectal Prolapse . Recto dis colon. 2017;60(11):1121-1131. doi:10.1097/DCR.00000000000000889.
- Hatch Q, Steele SR. Prolapso rectal e invaginación intestinal. Gastroenterol Clin North Am. 2013;42(4):837-861. doi:10.1016/j.gtc.2013.08.002.
- Fox A, Tietze PH, Ramakrishnan K. Condiciones anorrectales: prolapso rectal. FP Essent. 2014;419:28-34.
Cite this article
Ortega MV, Von Bargen EC, Bordeianou LG. Rectopexia de sutura laparoscópica con culdoplastia, reparación de la pared vaginal y perineorrafia para el prolapso rectal. J Med Insight. 2022;2022(272). doi:10.24296/jomi/272.


