Laparoskopische Nahtrektopexie mit Culdoplastik, Vaginalwandreparatur und Perineorrhaphie bei Rektumprolaps
1,2; 1,2*; 1,3*
1Pelvic Floor Disorders Center, Massachusetts General Hospital, Boston, MA
2Department of Obstetrics, Gynecology and Reproductive Biology, Massachusetts General Hospital, Boston, MA
3Section of Colorectal Surgery, Department of Surgery, Massachusetts General Hospital, Boston, MA
*Operating Surgeons
Main Text
Table of Contents
Die Patientin ist eine 87-jährige Frau, die sich mit einer Vorgeschichte von Verstopfung und lästigem Rektumprolaps präsentierte, der eine manuelle Rektumprolapsreduktion erforderte. Bei der Untersuchung wurde festgestellt, dass sie einen rektalen Prolaps in voller Dicke und einen hinteren Beckenorganprolaps im Stadium II der Vaginalwand hatte. Sie wünschte sich eine definitive chirurgische Behandlung ihres Prolapses und entschied sich für eine laparoskopische Nahtrektopexie und eine hintere Vaginalwandreparatur und Perineorrhaphy. Sie hatte anorektale Physiologie und urodynamische Tests sowie eine Defäkographie vor der Operation, um die chirurgische Planung zu unterstützen. Die Operation war unkompliziert. Sie wurde am ersten postoperativen Tag entlassen und ihre postoperative Genesung war unauffällig.
Die Patientin ist eine 87-jährige Frau mit einer Vorgeschichte, die für das Reizdarmsyndrom mit Verstopfung von Bedeutung ist, die Symptome von Verstopfung aufwies, die auf Ernährungsänderungen und lästige rektale Vorwölbungen reagierten, die eine manuelle Reduzierung erforderten. Sie leugnete Harninkontinenz. Sie ist nullipar und nicht sexuell aktiv.
Bei der Untersuchung war ihr Bauch weich, ungedehnt und nicht zart, ohne Anzeichen von Hernien. Sie hatte einen gut verheilten vertikalen Mittellinien-Hautschnitt. Bei der Beckenuntersuchung mit Valsalva stieg die hintere Vaginalwand 1 cm über das Jungfernhäutchen hinaus. Bei der rektovaginalen Untersuchung hatte sie eine rektovaginale Tasche. Schließlich, während sie auf der Kommode saß, wurde festgestellt, dass sie einen rektalen Prolaps in voller Dicke mit Anstrengung sowie einen patulösen Anus in Ruhe hatte.
Der Patient wurde einer Defäkographie unterzogen, und die Ergebnisse sind in Abbildung 1 zu sehen.
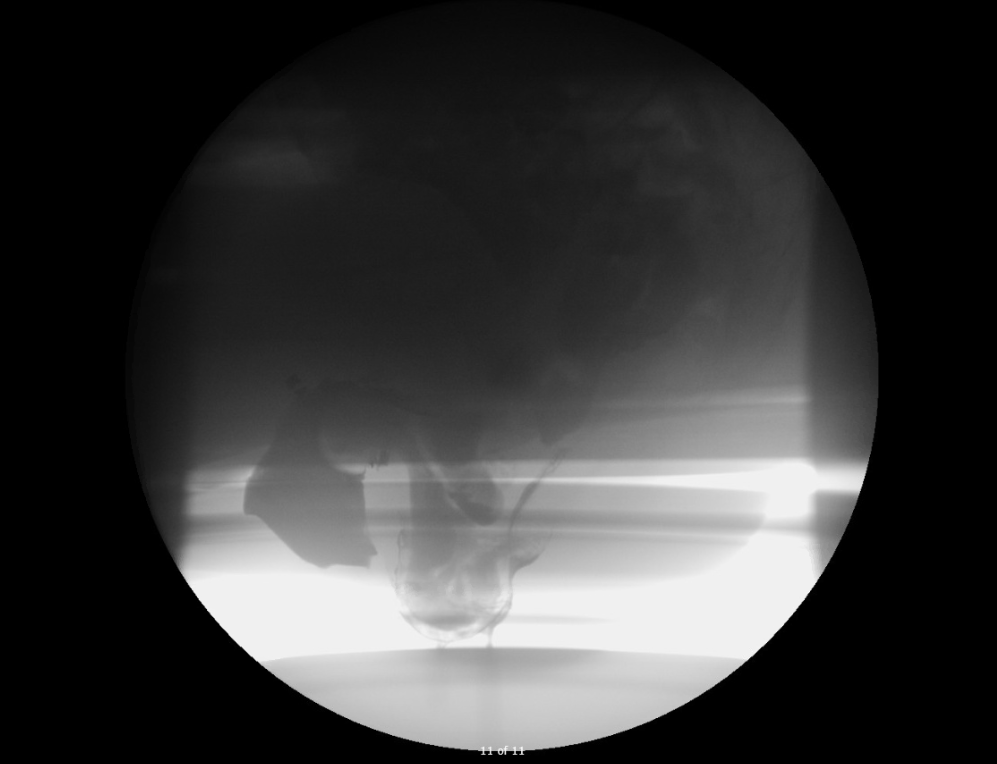
Abbildung 1. Ergebnisse der Defäkographie
Rektorektale Intusszeption in voller Dicke mit Rektumprolaps.
Anschließende Invagination einer Enterozele in das Rektum und die Vagina.
Bei der anorektalen Manometrie wurde festgestellt, dass sie sowohl in Ruhe als auch mit Druck einen sehr tiefen Ton hatte. Urodynamische Tests (UDT) wurden durchgeführt, um okkulte Belastungsinkontinenz auszuschließen. Bei UDT gab es keine Belastungsinkontinenz mit Prolapsreduktion, keine Detrusorüberaktivität und normale Blasenkapazität. Es wurde empfohlen, zum Zeitpunkt der Prolapsreparatur kein Anti-Inkontinenzverfahren durchzuführen.
Bei der Defäkographie gab es einen Rektumprolaps mit einer Enterozele, die in das Rektum und die Vagina prolabierte.
Ihre präoperativen Laborstudien umfassten ein komplettes Blutbild, ein grundlegendes metabolisches Panel und ein Elektrokardiogramm (EKG). Alle Werte lagen innerhalb normaler Grenzen. Das EKG zeigte einen normalen Sinusrhythmus. Sie wurde medizinisch zur Operation freigegeben.
Unbehandelt kann ein rektaler Prolaps zu Analinkontinenz führen, die auf eine chronische Dehnung des Analschließmuskels und eine anschließende Neuropathie zurückzuführen ist. Verstopfung oder behinderte Defäkation können ebenfalls gesehen werden. In seltenen Fällen kann ein Rektumprolaps zu einer Inhaftierung oder Strangulation des vorgefallenen Rektums führen. 1 Es gibt seltene Berichte über rektale Prolapsischämie 2 und Gangrän. 3
Die Behandlung des Rektumprolapses hängt von den Symptomen, Zielen und der bisherigen medizinischen und chirurgischen Vorgeschichte des Patienten ab. Leider hat dieser Zustand keine nicht-chirurgischen Behandlungsmöglichkeiten, und im Allgemeinen wird von einer erwartungsvollen Behandlung abgeraten, da sich der Rektumprolaps mit der Zeit tendenziell verschlechtert. Wenn es unbehandelt bleibt, kann es zu Analinkontinenz führen.
Chirurgische Optionen zur Behandlung von Rektumprolaps umfassen:
- Offene oder minimal-invasive (laparoskopische oder robotische) hintere Nahtrektopexie:
- Ohne Sigmoidresektion – dies ist besonders indiziert für Patienten mit Inkontinenz oder mit hohem Inkontinenzrisiko (d.h. mit sehr niedrigen Analdrücken bei anorektalen physiologischen Tests).
- Mit Sigmoidresektion – für Patienten mit begleitender Verstopfung.
- Die Entscheidung, mit einer offenen oder minimal-invasiven Technik fortzufahren, wird von der Erfahrung des Anbieters und der Patienteneignung geleitet.
- Offene oder minimalinvasive (laparoskopische oder robotische) ventrale Netzrektopexie: Dieser Ansatz verzichtet auf die Sezierung des Rektums posterior und gilt daher als nervenschonend. Es wurde für Patienten mit interner Invagination und Prolaps in voller Dicke beschrieben. Es ist eine gute Option für Patienten mit begleitenden Sackgassenhernien (Enteroceles, Sigmoidoceles) oder Patienten mit Symptomen von Stuhlinkontinenz und Verstopfung. Es ist wichtig zu erwähnen, dass Patienten mit assoziierter Rektozele eine kombinierte Sakrokolpopexie angeboten werden könnte, wenn die Spitze der Vagina schlecht suspendiert ist. In Fällen, in denen eine Enterozele behandelt werden muss, wird Patienten, die eine native Gewebereparatur suchen, oft eine Kuldoplastik angeboten.
- Perineal: Dieser Ansatz ist mit einer geringeren Morbidität verbunden; Es wird jedoch von vielen angenommen, dass es zu einem viel höheren Risiko eines erneuten Auftretens führt. Es gibt auch viele Debatten über das funktionelle Ergebnis, wobei einige Experten eine Zunahme der postoperativen Stuhlinkontinenz im Vergleich zu Patienten vorschlagen, die mit nichtresektionalen abdominalen Ansätzen behandelt werden. Angesichts dieser Bedenken ist dieser Ansatz im Allgemeinen Patienten mit signifikanten Komorbiditäten vorbehalten.
Die American Society of Colon and Rectal Surgeons empfiehlt abdominale Verfahren wie die rektale Fixierung bei ansonsten gesunden Patienten. 4 Perineale Ansätze sollten Patienten mit bereits bestehenden Komorbiditäten vorbehalten sein, bei denen eine Minimierung der Eingriffsmorbidität gewünscht ist.
Trotz chirurgischer Reparatur können funktionelle Probleme wie Verstopfung bestehen bleiben. 1, 3 Die Wahl des Verfahrens kann auch die Funktion bei einigen Patienten verschlechtern, indem sie Stuhlinkontinenz (nach einer Darmresektion) oder Verstopfung (nach Denervierung des Beckenbodens) auslöst.
Bis zu 3% der Frauen in den USA berichten, dass sie irgendeine Form von Beckenorganprolaps haben,1 und Rektumprolaps betrifft 1% der Erwachsenen über 65 Jahre. 5
Zu den Risikofaktoren für einen Rektumprolaps gehören das weibliche Geschlecht, 1, 5 Jahre größer als 40,1, 5 Multiparitäten, 1, 6 vaginale Entbindungen von Säuglingen, die für das Gestationsalter1 groß sind, und chronische Verstopfung. 1 Andere Risikofaktoren sind anatomische Anomalien des Beckens wie ein tiefer Douglas-Beutel, atonische Bedingungen des Beckenbodens oder des Analkanals und das Fehlen einer normalen Fixierung des Rektums. 1 Bindegewebserkrankungen wie das Marfan- und das Ehlers-Danlos-Syndrom und einige neurologische Erkrankungen wie Schlaganfall, Demenz und Rückenmarksläsionen wurden ebenfalls mit einem Rektumprolaps in Verbindung gebracht. 1
Die Ursache des Rektumprolapses ist multifaktoriell. Im Allgemeinen beginnt es als eine Invagination des Rektums, die über einen patulösen Anus zur endgültigen Ausweidung des Rektums fortschreitet. 1, 5, 6
Es gibt anatomische Merkmale, die beschrieben wurden, um mit Rektumprolaps in Verbindung gebracht zu werden, wie ein redundanter Sigma, Diastasis des Levator ani, tiefe Sackgasse und das Fehlen einer normalen Fixierung des Rektums, was zu einem außergewöhnlich hypermobilen Mesorektum und einer Laxheit der Seitenbänder führt. Das Ziel der Operation ist es, die Anatomie wiederherzustellen und diese Merkmale anzugehen.
Für diese Patientin, weil die anorektale Manometrie einen niedrigen Schließmuskeltonus in Ruhe und mit Druck zeigte, wurde festgestellt, dass diese niedrigen Drücke sie dem Risiko aussetzten, bei jeder Operation, die eine Darmresektion erforderte, eine Stuhlinkontinenz zu entwickeln. Dies führte zu der Entscheidung, anstelle der Resektionsrektopexie eine Rektopexie ohne Resektion anzubieten.
Angesichts der Befunde der Enterozele in ihrer Defäkographie diskutierten wir die besten Möglichkeiten, sie zum Zeitpunkt der Operation anzugehen. Die Option der Kuldoplastik gegenüber einer ventralen Netzrektopexie wurde diskutiert. Letztendlich wurde festgestellt, dass sie angesichts der Tatsache, dass die hintere Wand der Vagina gut suspendiert war, wahrscheinlich sehr gut mit einer nativen Reparatur wie einer Culdoplastik zurechtkommen würde und dass ein Netz durchgeführt werden könnte, sollte es zu einem zukünftigen Wiederauftreten kommen.
Nach der Beurteilung und Beratung entschied sich dieser Patient für einen chirurgischen Eingriff.
Der Patient wurde in den Operationssaal gebracht, wo eine Vollnarkose mit einem Endotrachealtubus erhalten wurde. Eine orale Magensonde wurde platziert. Sie erhielt subkutanes Heparin zur Prophylaxe venöser Thromboembolien und intravenöses Cefazolin und Metronidazol zur Antibiotikaprophylaxe. Sie wurde in der Position der dorsalen Lithotomie in Gelbflossensteigbügeln platziert. Ein Verweil-Foley-Katheter wurde in die Blase gelegt und die Blase wurde entleert.
Der Eintritt in den Bauch wurde unter direkter Sicht mit der Hasson-Technik durchgeführt. Sobald der Baucheintritt bestätigt war, wurde der Bauch mit CO2 inuffliert. Eine Bauchuntersuchung wurde durchgeführt, und es wurde festgestellt, dass es einen tiefen Beutel von Douglas, normalen Dünn- und Dickdarm sowie normale Gebärmutter und Adnexa gab. Drei weitere laparoskopische Ports wurden unter direkter Visualisierung platziert: ein 10-mm-Port im rechten unteren Quadranten, ein 5-mm-Port im rechten oberen Quadranten und ein 5-mm-Port im linken unteren Quadranten. Der Rektumprolaps wurde reduziert. Sobald die präsakrale Anatomie auf der Ebene von S1 identifiziert wurde, wurde das sakrale Vorgebirge mit dem Harmonic-Gerät geräumt. Mit der Harmonischen wurde das Rektum von seinen sakralen und lateralen Anhaftungen bis zu den Levatoren befreit, wobei sorgfältig darauf geachtet wurde, den rechten lateralen Stiel des Rektums zu durchqueren, während der linke erhalten blieb, um einen Teil der Innervation zum Rektum aufrechtzuerhalten. Der tiefe Beutel von Douglas wurde am distalsten Ende geöffnet, und das vordere Rektum wurde von der Vagina zum perinealen Körper getrennt.
Das Rektum wurde dann auf Spannung zum Sakralvorgebirge mit drei Nähten von 0 Gore-Tex gesichert. Das Rektum wurde in den Bauch gehoben, und die Schnittkante des Beutels von Douglas wurde auf die Ebene des Sakralvorsprungs angehoben. Alle Nähte wurden extrakorporal gebunden.
Nachdem die Nahtrektopexie abgeschlossen war, richtete sich die Aufmerksamkeit auf die laparoskopische Kuldoplastik. Mit den zuvor platzierten laparoskopischen Ports wurden 3-0 V-Loc Stachelnähte platziert. Das Peritoneum, das über dem vorderen Rektum und der Beckenseitenwand lag, wurde angenähert, wodurch die hintere Sackgasse ausgelöscht wurde.
Anschließend wurde eine Zystoskopie durchgeführt, die sich durch starke bilaterale Harnleiterdüsen und normale Blasenschleimhaut ohne Anzeichen von Steinen, Läsionen oder Fremdkörpern auszeichnete.
Die Faszie des 12-mm-Anschlusses des rechten unteren Quadranten wurde mit einem 0 Vicryl (Polyglactin 910) mit einer laparoskopischen Faszienverschlussvorrichtung verschlossen. Die Nabelschnurfaszie wurde mit 0 Vicryl (Polyglactin 910) unter direkter Visualisierung verschlossen. Die Hautschnitte wurden dann mit 4-0 Monocryl (Poliglecaprone 25) reapproximiert, gefolgt von Steri-Strips.
Sobald der laparoskopische Eingriff abgeschlossen war, richtete sich die Aufmerksamkeit auf die posteriore Reparatur und verlängerte die Perineorhaare, um den hinteren Vaginalwandprolaps zu behandeln. Die hintere Fourchette wurde beidseitig mit Allis-Klemmen gegriffen. Die Fläche der erwarteten Dissektion wurde dann mit 0,25% Marcain mit Epinephrin injiziert. Ein rautenförmiger Schnitt wurde dann über die perineale Körperhaut und das hintere Vaginalepithel gemacht. Die Haut, die über dem perinealen Körper und dem hinteren Vaginalepithel lag, wurde herausgeschnitten. Der perineale Körper wurde scharf aus dem rektovaginalen Septum seziert. Der vaginale Mittellinienschnitt wurde dann vom Perineum bis zur proximalen Grenze der Rektozele durchgeführt. Das Vaginalepithel wurde dann vom darunter liegenden rektovaginalen Bindegewebe abgeseziert. Mit einem Finger, der zur Orientierung in das Rektum gelegt wurde, wurde die rektovaginale fibromuskuläre Schicht mit 2-0 PDS II (Polydioxanon) laufend imgraviert. Zur Verstärkung wurde eine zusätzliche Schicht angebracht. So wurde eine hervorragende Unterstützung der hinteren Vaginalwand erreicht und das überschüssige Vaginalepithel wurde beschnitten. Der perineale Körper wurde wieder an die rektovaginale Faszie angeschlossen und mit einer Reihe von Kronenstichen von 0 Vicryl (Polyglactin 910) nachgebildet. Der Mittellinienschnitt wurde dann laufend mit 2-0 Vicryl (Polyglactin 910) geschlossen. Das Perineum wurde mit submukösen und subkutanen Nähten verschlossen. Eine rektale Verletzung wurde mit einer digitalen rektalen Untersuchung nach der Reparatur ausgeschlossen.
Der Patient wurde am ersten postoperativen Tag einer Verfüllentleerungsstudie unterzogen. Die Blase wurde über den Foley-Katheter mit 300 ml sterilem Wasser gefüllt. Der Foley-Katheter wurde entfernt, und der Patient konnte mehr als 200 ml entleeren und damit die Entleerungsstudie bestehen. Anschließend erfüllte sie alle Entlassungskriterien und wurde nach einem unauffälligen Krankenhausaufenthalt am ersten postoperativen Tag nach Hause entlassen.
Der Patient wurde nach zwei und sieben Wochen postoperativ gesehen. Bei diesen Besuchen berichtete sie, dass es ihr gut ging und leugnete jegliche Symptome von Prolaps, Anal- oder Harninkontinenz oder Voiding-Dysfunktion.
- Harmonisches Skalpell (Johnson & Johnson USA)
- 70-Grad-Zystoskop
Nichts zu offenbaren.
Der Patient, auf den in diesem Videoartikel Bezug genommen wird, hat seine Einverständniserklärung gegeben, gefilmt zu werden, und ist sich bewusst, dass Informationen und Bilder online veröffentlicht werden.
Citations
- Bordeianou L, Hicks CW, Kaiser AM, Alavi K, Sudan R, Wise PE. Rektumprolaps: ein Überblick über klinische Merkmale, Diagnosen und patientenspezifische Managementstrategien. J Gastrointest Surg Off J Soc Surg Aliment Tract. 2014;18(5):1059-1069. doi:10.1007/s11605-013-2427-7
- La Torre F, La Torre V, Mazzi M, Giuliani A, Pontone S, La Gioia G. Chirurgische Behandlung der Rektumprolapsischämie. Technische Koloproktologie. 2005;9(2):170.
- Borgaonkar VD, Deshpande SS, Borgaonkar VV, Rathod MD. Notfall perineale Rektosigmoidektomie für gangränösen Rektumprolaps: eine einzentrische Erfahrung mit Literaturübersicht. Indischer J Surg. 2017;79(1):45-50. doi:10.1007/s12262-016-1562-2
- Bordeianou L, Paquette I, Johnson E, et al. Clinical Practice Guidelines for the Treatment of Rectal Prolapse. Dis colon rectum. 2017;60(11):1121-1131. doi:10.1097/DCR.0000000000000889
- Luke Q, Steele SR. Rektumprolaps und Invagination. Gastroenterol Clin Nord Am. 2013;42(4):837-861. doi:10.1016/j.gtc.2013.08.002
- Fuchs A, Tietze PH, Ramakrishnan K. Anorektale Zustände: Rektumprolaps. FP Essent. 2014;419:28-34.
Cite this article
Ortega MV, Von Bargen EC, Bordeianou LG. Laparoskopische Nahtrektopexie mit Kuldoplastik, Vaginalwandreparatur und Perineorrhaphie bei Rektumprolaps. J Med Einblick. 2022;2022(272). doi:10.24296/jomi/272.


