Paratiroidectomía mínimamente invasiva bajo anestesia local de bloqueo cervical para el hiperparatiroidismo primario y el adenoma paratiroideo
Main Text
Table of Contents
Con una mejoría tanto en la identificación preoperatoria del tumor paratiroideo como en el uso del ensayo intraoperatorio de hormona paratiroidea (PTH), la paratiroidectomía mínimamente invasiva (MIP) ahora se realiza con mayor frecuencia en pacientes con hiperparatiroidismo primario (pHPT) en comparación con la exploración cervical tanto históricamente como con la exploración cervical. Aún así, muchas instituciones no están familiarizadas con la realización de MIP bajo anestesia regional o local. Presentamos dicha operación bajo anestesia local de bloqueo cervical.
Alrededor del 85% de los pacientes con hiperparatiroidismo primario (pHPT) albergan un solo adenoma y se curan mediante la resección de la lesión única. Los pacientes restantes presentan adenomas dobles (3-5%) o hiperplasia de cuatro glándulas (10-15%). 1 La paratiroidectomía mínimamente invasiva focalizada (MIP) ahora es factible bajo anestesia regional o local. La MIP se realiza después de la localización paratiroidea preoperatoria, generalmente con exploraciones sestamibi de alta calidad, ecografía o tomografía computarizada paratiroidea de cuatro dimensiones (4DCT). Se emplea un ensayo rápido de hormona paratiroidea (PTH) intraoperatoria para confirmar una resección adecuada.
La paciente es una mujer de 60 años con hiperparatiroidismo primario bioquímicamente inequívoco. Estaba siendo evaluada para un nódulo tiroideo y en el trabajo para eso se encontró que tenía niveles elevados de calcio en la sangre y la orina. Los síntomas del paciente incluyen osteoporosis franca con una puntuación T de -2,6 en el cuello femoral y -2,3 en la columna lumbar. No tiene antecedentes de nefrolitiasis ni síntomas neurocognitivos manifiestos. No hay quejas de ronquera, dificultad para tragar o dificultad para respirar. No tiene antecedentes de radiación en el cuello o la cara.
La evaluación bioquímica demuestra un calcio sérico total de 10,7 mg/dl (rango de referencia 8,8–10,2 mg/dl), niveles elevados de PTH de 76–81 pg/ml (rango de referencia 10–65 pg/ml) e hipercalciuria con un calcio urinario de 24h de 438 mg/24h. Las imágenes preoperatorias con ultrasonido y sestamibi con tomografía computarizada por emisión de fotón único (SPECT) sugirieron una lesión paratiroidea inferior izquierda.
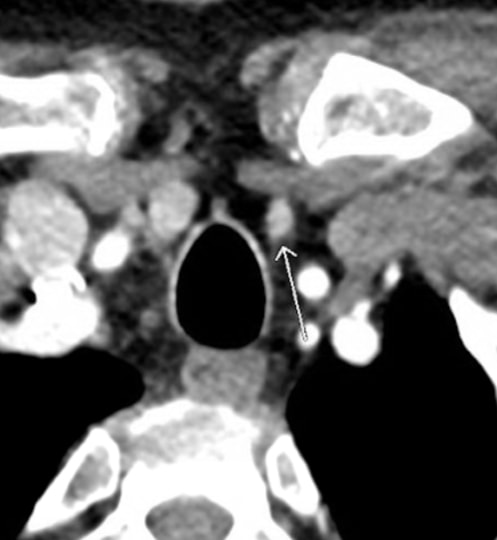
La modalidad de imagen más precisa para la planificación preoperatoria en pacientes con pHPT es la paratiroides 4DCT. La paratiroides 4DCT es similar a la angiografía por TC. 2 El término se deriva de la tomografía computarizada tridimensional con una dimensión añadida que se refiere a los cambios en la perfusión del contraste a lo largo del tiempo. Se obtienen imágenes multiplanares exquisitamente detalladas que acentúan las diferencias en las características de perfusión de las glándulas paratiroides hiperfuncionales (por ejemplo, captación y lavado rápidos) con las de las glándulas paratiroides normales y otras estructuras en el cuello. En comparación con sestamibi con SPECT, 4DCT es significativamente menos costoso pero se asocia con una mayor exposición a la radiación ionizante y, por lo tanto, debe usarse con precaución en niños y adultos jóvenes. 3 Además, debido al uso de contraste intravenoso, debe evitarse en pacientes con insuficiencia renal, así como en pacientes con un carcinoma de tiroides concomitante y bien diferenciado.
La modalidad más utilizada sigue siendo sestamibi con SPECT, que genera localización tridimensional. Una limitación importante de las exploraciones de sestamibi es la coexistencia de nódulos tiroideos u otros tejidos metabólicamente activos (por ejemplo, ganglios linfáticos, nódulos tiroideos y cáncer de tiroides metastásico) que pueden imitar los adenomas paratiroideos, causando así resultados falsos positivos. Sestamibi con SPECT no proporciona una representación anatómica detallada y solo puede detectar adenomas dobles e hiperplasia multiglandular en el 25-45% de los casos. número arábigo
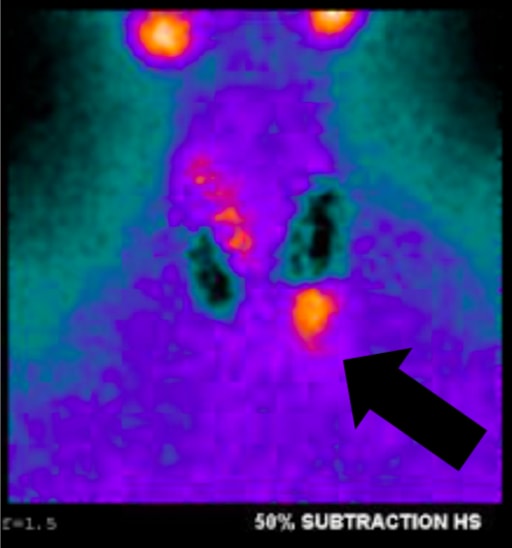 Fig. 1a, Sestamibi con SPECT del paciente de este artículo. La flecha indica el adenoma paratiroideo en la posición inferior izquierda.
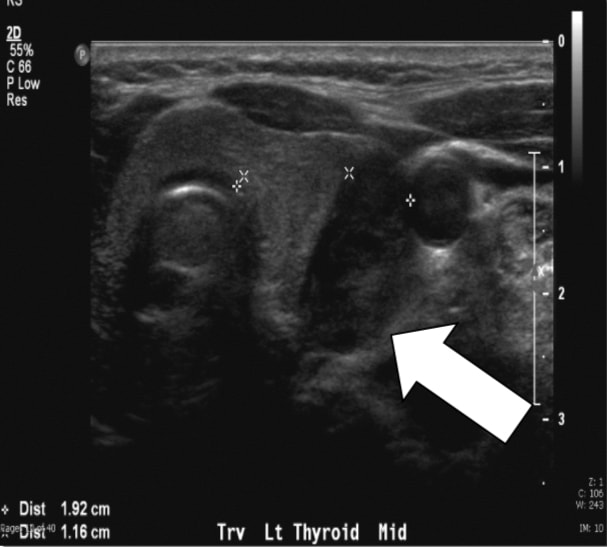
Fig. 1a, Sestamibi con SPECT del paciente de este artículo. La flecha indica el adenoma paratiroideo en la posición inferior izquierda.Realizamos ultrasonidos de forma rutinaria porque son efectivos, no invasivos y económicos. Las limitaciones incluyen tanto la dependencia del operador como la incapacidad para obtener imágenes de adenomas mediastínicos porque se limita al cuello. La glándula paratiroides normal es generalmente demasiado pequeña para ser visualizada ecográficamente, mientras que el agrandamiento paratiroideo observado en pHPT a menudo se identifica como una masa ovoide extratiroidea homogéneamente hipoecoica. Los adenomas paratiroideos son típicamente vasculares, y una rama arterial a menudo se puede seguir hasta el polo superior o inferior de la lesión. Por sí mismo, el ultrasonido tiene aproximadamente una tasa de verdadero positivo del 50-75% con tasas generalmente mejores para las glándulas más grandes. número arábigo
Este paciente fue remitido después de una imagen positiva por parte del endocrinólogo (tanto la ecografía como el sestamibi con SPECT sugirieron una lesión paratiroidea inferior izquierda). En tal escenario, no sometería al paciente a una exploración 4DCT.
La historia natural de la pHPT no tratada se ha estudiado en detalle e implica el deterioro de las funciones óseas y renales, neurocognitivas y cardiovasculares, que están más allá del alcance del artículo. 4
No hay otro tratamiento curativo para la pHPT excepto la cirugía. Sin embargo, la reducción temporal del calcio sérico se puede hacer farmacológicamente. 4
Las indicaciones para miP son las mismas que para la exploración cervical tradicional: pacientes sintomáticas o con pHPT asintomática que cumplen con los criterios establecidos por la reunión de consenso más reciente de los Institutos Nacionales de Salud (NIH). 4 Además, ahora hay datos significativos para apoyar un uso más liberal de la cirugía porque la enfermedad se ha asociado con varias morbilidades "no clásicas", algunas de las cuales parecen mejorar después de la operación. 4 Estos incluyen deficiencias neurocognitivas y anomalías cardiovasculares.
La cirugía unilateral para la pHPT se defendió por primera vez en 1975, y el lado a explorar se eligió en función de la palpación, las imágenes esofágicas, la venografía o la arteriografía. 5 El éxito del PDM ha sido confirmado por la evidencia de tasas de curación y complicación que son al menos tan buenas como las logradas por la exploración bilateral convencional. 6 La tasa de complicaciones de la MIP es similar o menor en comparación con el enfoque cervical estándar. 7 La lesión recurrente del nervio laríngeo puede ocurrir en 0.5-1.0% de los casos. 6 El riesgo de hipoparatiroidismo permanente está ausente si se explora y extirpa una sola glándula, pero siempre existe una preocupación en los pacientes sometidos a paratiroidectomía subtotal por enfermedad multiglandular.
La paciente actual demostró una cura bioquímica de su pHPT y no tuvo complicaciones.
Prefiero la anestesia de bloqueo local y regional con atención de anestesia monitoreada (MAC) en lugar de la anestesia general que usa un tubo endotraqueal (ETT) o una máscara laríngea de las vías respiratorias (LMA). El bloqueo regional es realizado por el cirujano en el quirófano, y la suplementación intravenosa es dirigida por el anestesiólogo. En la mayoría de los pacientes, se usa lidocaína al 1% que contiene 1:100,000 epinefrina y se agrega durante la operación según sea necesario. Se tiene cuidado de aspirar antes de administrar el anestésico para evitar la administración intravascular. El volumen total acumulado de lidocaína administrada es típicamente de 18 a 25 ml. La sedación intravenosa se usa para minimizar la ansiedad del paciente mientras mantiene a un paciente despierto y consciente que puede fonear. 1
La anestesia regional evita las complicaciones asociadas con la anestesia general, como náuseas y vómitos. Evitar la intubación endotraqueal es beneficioso porque se ha informado que causa cambios en las cuerdas vocales en hasta el 5% de los pacientes. 6, 8 Además, explorar a un paciente consciente permite la evaluación intraoperatoria de las funciones del nervio laríngeo superior y recurrente porque el paciente puede vocalizar durante el procedimiento.
Ninguna modalidad de imágenes preoperatorias reemplazará la necesidad de un cirujano paratiroideo bien entrenado y reflexivo. 9 Los cirujanos que realizan MIP deben comprender la embriología y la anatomía de las glándulas paratiroides. El desarrollo embrionario y el descenso al cuello cervical de las glándulas paratiroides conducen a una anatomía altamente variable. El tejido paratiroideo ectópico se encuentra comúnmente dentro de la tiroides, el timo, el mediastino, la vaina carotídea y el surco traqueoesofágico. Las glándulas no descendidas pueden ubicarse a lo largo de la bifurcación carotídea o a lo largo de la laringe.
La técnica MIP se individualiza después de que se ha localizado el adenoma paratiroideo. Típicamente, se realiza una incisión de Kocher abreviada de 2.5 a 3.5 cm, seguida de la creación de colgajos subplatísticos limitados y la apertura del rafe mediano. La glándula tiroides se moviliza entonces anteromedialmente. Luego se identifica el adenoma paratiroideo, ayudado por la imagen preoperatoria. Es importante manipular el adenoma paratiroideo suavemente para evitar la ruptura de su cápsula, que puede derramar células tumorales paratiroideas. Si se agarra la glándula paratiroides, es preferible manejar la paratiroides por la almohadilla de grasa que a menudo se extiende alrededor de la glándula o su suministro de sangre arterial final. El suministro de sangre arterial final se liga con clips o lazos de seda. Antes de la escisión del adenoma paratiroideo, el nervio laríngeo recurrente está protegido. La cirugía paratiroidea es un procedimiento meticuloso y la experiencia operatoria se correlaciona con las tasas de recurrencia y persistencia, así como con las complicaciones. 1 El procedimiento se guía por mediciones intraoperatorias de PTH.
La medición intraoperatoria de la PTH se emplea de forma rutinaria. La vida media circulante de la PTH es de 3.5 a 4.0 minutos, y por lo tanto los niveles de PTH se obtienen antes de la cirugía y a los 5 y 10 minutos después de la extracción del tumor. Los niveles de PTH deben disminuir (>50%) dentro de los 5 o 10 minutos posteriores a la extirpación del adenoma paratiroideo hiperfuncional, ya que las glándulas paratiroides normales restantes son la única fuente de PTH. Si este es el caso, el paciente no requiere exploración adicional. El fracaso del nivel de PTH venosa periférica para disminuir adecuadamente sugiere que el tejido paratiroideo hiperfuncional restante, y la cirugía adicional está indicada bajo anestesia regional o general. Además de ser un complemento valioso para confirmar la integridad de la resección paratiroidea, el ensayo rápido de PTH es un complemento útil para otros aspectos en el tratamiento de la pHPT. Realizamos rutinariamente aspiraciones con aguja fina ex vivo de tejido extirpado durante la cirugía paratiroidea para medir la PTH. Un aspirado positivo demostrará niveles de PTH superiores a 1.000 pg/ml. Esto ha eliminado la necesidad de análisis de secciones congeladas en la mayoría de los casos. Aunque dependemos en gran medida del ensayo de PTH intraoperatorio, no reemplaza el juicio clínico, y el ensayo debe interpretarse en este contexto. 1
La patología reveló una glándula paratiroides agrandada (1,8 cm) y celular con un peso de 507 mg (normal alrededor de 30-40 mg). En la visita postoperatoria ocho días después de la cirugía, el calcio sérico total de la paciente era normal a 9,5 mg/dl (rango de referencia 8,8–10,2 mg/dl), y tenía un nivel normal de PTH de 32 pg/ml (rango de referencia 10–65 pg/ml). Su función de las cuerdas vocales también era normal.
No se utilizó ningún equipo especial.
Nada que revelar.
El paciente al que se hace referencia en este video artículo ha dado su consentimiento informado para ser filmado y es consciente de que la información y las imágenes se publicarán en línea.
References
- Carling T, Udelsman R. Enfoque centrado en la paratiroidectomía. Mundo J Surg. 2008;32(7):1512-1517. doi:10.1007/s00268-008-9567-z.
- Starker LF, Mahajan A, Björklund P, Sze G, Udelsman R, Carling T. 4D parathyroid CT como el estudio de localización inicial para pacientes con hiperparatiroidismo primario de novo. Ann Surg Oncol. 2011;18(6):1723-1728. doi:10.1245/s10434-010-1507-0.
- Mahajan A, Starker LF, Ghita M, Udelsman R, Brink JA, Carling T. Tomografía computarizada paratiroidea de cuatro dimensiones: evaluación de la exposición a la dosis de radiación durante la localización preoperatoria de tumores paratiroideos en el hiperparatiroidismo primario. Mundo J Surg. 2012;36(6):1335-1339. doi:10.1007/s00268-011-1365-3.
- Bilezikian JP, Brandi ML, Eastell R, et al. Directrices para el tratamiento del hiperparatiroidismo primario asintomático: resumen del Cuarto Taller Internacional. J Clin Endocrinol Metab. 2014;99(10):3561-3569. doi:10.1210/jc.2014-1413.
- Roth SI, Wang CA, Potts JT Jr. El enfoque en equipo para el hiperparatiroidismo primario. Hum Pathol. 1975;6(6):645-648. doi:10.1016/S0046-8177(75)80073-6.
- Udelsman R, Lin Z, Donovan P. La superioridad de la paratiroidectomía mínimamente invasiva basada en 1650 pacientes consecutivos con hiperparatiroidismo primario. Ana Surg. 2011;253(3):585-591. doi:10.1097/SLA.0b013e318208fed9.
- Bergenfelz A, Lindblom P, Tibblin S, Westerdahl J. Exploración unilateral versus bilateral del cuello para el hiperparatiroidismo primario: un ensayo controlado aleatorio prospectivo. Ana Surg. 2002;236(5):543-551. doi:10.1097/01.SLA.0000032949.36504.C3.
- Kark AE, Kissin MW, Auerbach R, Meikle M. Cambios en la voz después de la tiroidectomía: papel del nervio laríngeo externo. Br J Med (Clin Res Ed). 1984;289(6456):1412-1415. doi:10.1136/bmj.289.6456.1412.
- Stålberg P, Carling T. Tumores paratiroideos familiares: diagnóstico y tratamiento. Mundo J Surg. 2009;33(11):2234-2243. doi:10.1007/s00268-009-9924-6.
Cite this article
Carling T. Paratiroidectomía mínimamente invasiva bajo anestesia de bloqueo cervical local para el hiperparatiroidismo primario y el adenoma paratiroideo. J Med Insight. 2022;2022(225). doi:10.24296/jomi/225.