Nefrectomía laparoscópica izquierda del donante
Main Text
Table of Contents
Durante la última década, la nefrectomía laparoscópica de donante ha reemplazado gradualmente el enfoque abierto convencional y se ha convertido en el estándar de atención en los trasplantes de riñón de donante vivo. En comparación con la nefrectomía abierta, la nefrectomía laparoscópica reduce el dolor postoperatorio, acorta la duración de la estancia hospitalaria y mejora el resultado estético. A continuación se ilustra nuestra técnica estándar de nefrectomía laparoscópica pura del donante.
Trasplante de riñón, laparoscopia, nefrectomía del donante, donante vivo, procedimiento quirúrgico mínimamente invasivo
Se trata de una mujer de 61 años sin antecedentes médicos significativos más allá de una cesárea previa. No tener antecedentes médicos que la excluyeran de donar un riñón.
En la figura 1 se muestran los hallazgos de una TC abdominal con contraste intravenoso que autoriza al paciente a realizar nefrectomía del donante izquierdo.
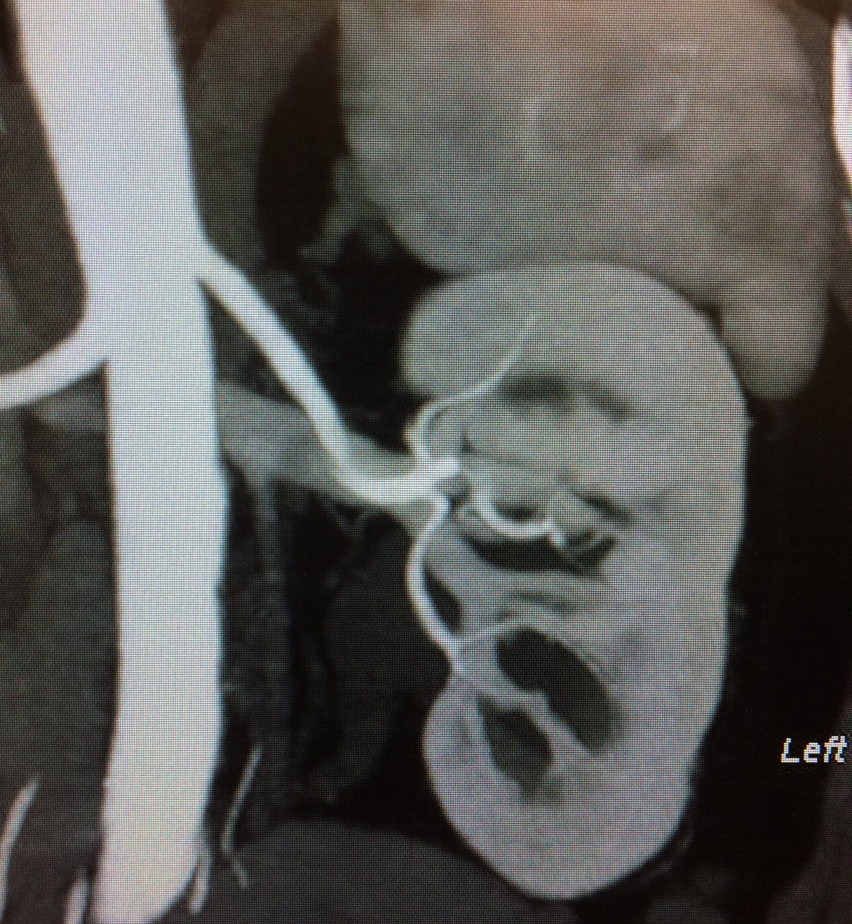 Figura 1. IV Computarizada abdominal con contraste. Hallazgos: posición renal normal dentro de las fosas renales. Los cálices renales son normales en morfología y distribución. Hay que tener en cuenta los numerosos quistes parapélvicos izquierdos. La pelvis renal única y los uréteres se observan bilateralmente. No hay pielocaliectasias ni hidrouréter. No se identifican masas renales o ureterales ni cálculos. RIÑÓN DERECHO: 1 arteria y 2 venas. RIÑÓN IZQUIERDO: 1 arteria y 1 vena.
Figura 1. IV Computarizada abdominal con contraste. Hallazgos: posición renal normal dentro de las fosas renales. Los cálices renales son normales en morfología y distribución. Hay que tener en cuenta los numerosos quistes parapélvicos izquierdos. La pelvis renal única y los uréteres se observan bilateralmente. No hay pielocaliectasias ni hidrouréter. No se identifican masas renales o ureterales ni cálculos. RIÑÓN DERECHO: 1 arteria y 2 venas. RIÑÓN IZQUIERDO: 1 arteria y 1 vena.
El paciente fue colocado en la mesa de quirófano en la posición de decúbito derecho. Las incisiones y la colocación de los puertos se pueden ver en la Figura 2. Se realizó una incisión de Pfannenstiel de 6 cm de longitud para introducir en la cavidad abdominal. Se instaló un puerto de mano (Gelport, Applied Medical) en esta incisión y se creó un neumoperitoneo con una presión de 10-15 mmHg. Se le insertaron dos puertos de 12 mm en el ombligo y en el cuadrante superior izquierdo. También se le insertó un puerto de 5 mm en la parte superior del abdomen en la línea media.
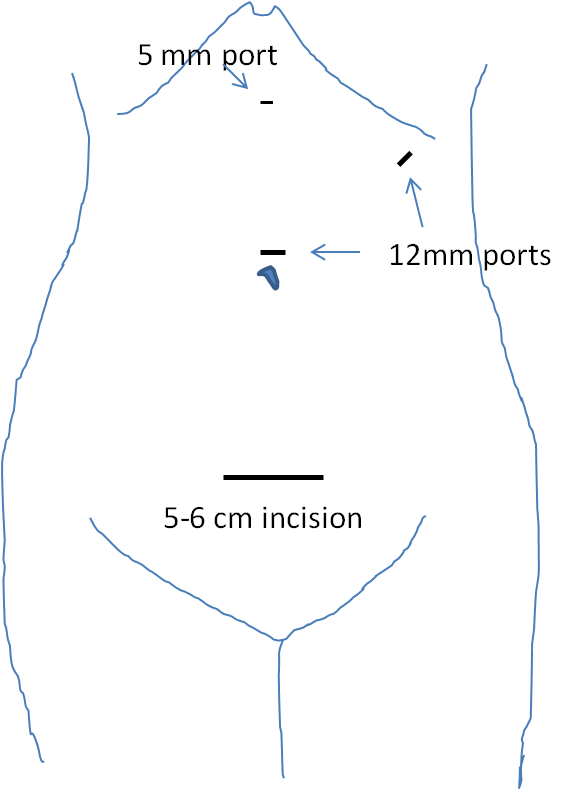 Figura 2. Incisiones y colocación de puertos. Se realizó una incisión de Pfannenstiel de 6 cm de largo y se insertó allí un puerto de mano (Gelport, Applied Medical). Se le colocaron dos puertos de 12 mm en el ombligo y en el cuadrante superior izquierdo. Se insertó un puerto de 5 mm en la línea media de la parte superior del abdomen.
Figura 2. Incisiones y colocación de puertos. Se realizó una incisión de Pfannenstiel de 6 cm de largo y se insertó allí un puerto de mano (Gelport, Applied Medical). Se le colocaron dos puertos de 12 mm en el ombligo y en el cuadrante superior izquierdo. Se insertó un puerto de 5 mm en la línea media de la parte superior del abdomen.
El procedimiento se inició movilizando el colon izquierdo medialmente para exponer el espacio retroperitoneal izquierdo. El riñón izquierdo se identificó mediante la disección de la fascia de la Gerota y luego se movilizó desde el polo superior hasta el polo inferior. A continuación, se identificó el uréter izquierdo y se liberó hacia el espacio pélvico. Para obtener una mejor exposición del hilio renal, se insertó un retractor hepático a través del Gelport. Se identificaron la vena renal izquierda y la vena gonadal, y se seccionó la vena gonadal con el LigaSure. A continuación, se identificó la vena suprarrenal, que también fue seccionada por el LigaSure. A continuación, se identificó la arteria renal y se expuso hacia la aorta. Se diseccionaron cuidadosamente todos los tejidos conectivos o linfáticos entre la arteria renal y la glándula suprarrenal o la vena renal. Ahora, se movilizó el polo superior del riñón y luego se inspeccionó la estructura detrás de la vena renal tirando hacia arriba de la pelvis renal. Había dos venas lumbares. Una vena más pequeña fue seccionada por el LigaSure, y la vena lumbar principal, con un diámetro de aproximadamente 5 mm, fue recortada con un clip de Hem-o-lok (Weck) y luego seccionada por el LigaSure.
El riñón estaba completamente libre de las estructuras circundantes y listo para ser extirpado. Después de notificar al equipo receptor, se configuró la mesa trasera. El uréter se recortó con una pinza de Hem-o-lok lo más distalmente posible, y se seccionó el uréter. En este punto, se insertó un Endo Catch (Covidien-Medtronic) de 15 cm en la cavidad abdominal a través del Gelport. El riñón izquierdo se colocó cuidadosamente en la bolsa y la bolsa se cerró a la mitad. A continuación, se extrajo el riñón lateralmente para estirar la arteria. A continuación, se grapó la arteria renal cerca de la aorta con ENDO TA-30 (Covidien-Medtronic) y se aplicó una pinza Hem-o-lok sobre la grapa. A continuación, se seccionó la arteria renal. A continuación, se grapó la vena renal distal a la vena suprarrenal y se seccionó. Luego, el riñón se extrajo inmediatamente del cuerpo y se perfundió con una solución fría de UW en la mesa trasera. A continuación, el riñón fue transportado a la sala receptora.
Los dos puntos descendentes se colocaron de nuevo en el lugar original. Las dos incisiones de puerto de 12 mm se cerraron con Endo Close con sutura 0 Vicryl, y la piel de esas incisiones se cerró en una capa con sutura Vicryl 3-0. La incisión de Pfannenstiel se cerró en cuatro capas con sutura 0 Vicryl, sutura #1 PDS, sutura Vicryl 3-0 y sutura Monocryl 4-0. El paciente toleró bien el procedimiento. Los bloqueos de TAP fueron realizados por el anestesiólogo y el paciente fue transportado a la sala de recuperación en condición estable.
Más de 100,000 pacientes están actualmente en la lista de espera de trasplante de riñón en los Estados Unidos, pero cada año hay menos de 20,000 donantes disponibles (United Network for Organ Sharing, https://www.unos.org). Para aumentar el número de donantes potenciales, se ha desarrollado una cirugía laparoscópica mínimamente invasiva de donante, que ha aumentado significativamente el número de trasplantes renales de donante vivo. 1 Durante la última década, la nefrectomía laparoscópica del donante ha reemplazado gradualmente a la nefrectomía abierta en la mayoría de los centros de trasplante en los Estados Unidos. No existen diferencias significativas entre las nefrectomías laparoscópicas y abiertas con respecto a la supervivencia del injerto a 1 año, a pesar del aumento de la WIT y el mayor tiempo quirúrgico asociado a la cirugía laparoscópica. De 2 a 4 años Las ventajas de la nefrectomía laparoscópica del donante incluyen una incisión más pequeña, un mejor resultado estético, una menor incidencia de hernia incisional y adherencia, menos dolor postoperatorio, una hospitalización más corta y un regreso más temprano al trabajo. 5 Nuestro centro informó previamente una revisión retrospectiva de un solo centro para comparar la nefrectomía laparoscópica y la nefrectomía abierta de donante vivo. 6 No hubo diferencias estadísticamente significativas entre los dos grupos en cuanto al tiempo quirúrgico, la función renal postoperatoria del donante y del receptor, y la incidencia de complicaciones mayores. Sin embargo, la duración de la estancia hospitalaria fue significativamente menor (p < 0,0001) en la nefrectomía laparoscópica (2,87 días) que en la nefrectomía abierta (3,6 días). Cuando se compararon los primeros 100 casos laparoscópicos con los últimos 100 casos, hubo una diferencia estadísticamente significativa en el tiempo quirúrgico a favor de la nefrectomía laparoscópica posterior, lo que indica que la cirugía laparoscópica tarda más en ser competente.
En este artículo, hemos presentado nuestro método para realizar una nefrectomía laparoscópica pura del donante. Sin embargo, existen otros dos métodos de cirugías laparoscópicas: las nefrectomías laparoscópicas asistidas por la mano y las asistidas por robot. La nefrectomía laparoscópica manual del donante ha demostrado ser ventajosa en cuanto a la duración de la operación y el sangrado intraoperatorio, en comparación con la nefrectomía laparoscópica pura del donante. Lo más probable es que estas ventajas se atribuyan a una identificación más fácil de la anatomía y a un manejo más rápido de cualquier sangrado con el método asistido por la mano. De 7 a 9 años La experiencia con la nefrectomía de donante asistida por robot es aún limitada; sin embargo, se ha realizado de forma segura con resultados favorables. 9-12 Algunos centros informaron que la nefrectomía robótica es superior a la nefrectomía laparoscópica del donante en las puntuaciones de dolor postoperatorio, el requerimiento analgésico y la duración de la estancia hospitalaria, a pesar de la mayor duración de la operación. Sin embargo, la nefrectomía robótica requiere mucho tiempo y es costosa, lo que justifica más análisis médicos y financieros.
En conclusión, la nefrectomía laparoscópica del donante se ha convertido en el estándar de atención, lo que tiene el impacto potencial de aumentar el número de donantes vivos al ofrecer menos dolor postoperatorio, menor duración de la estancia hospitalaria y mejores resultados estéticos.
- Gelport (Medicina Aplicada)
- LigaSure, Maryland Mandíbula (Covidien)
- Clip Hem-o-lok (Weck)
- Grapadoras Multifire Endo TA 30 (2,5 mm) (Covidien AutoSuture)
Nada que revelar.
El paciente al que se hace referencia en este videoartículo ha dado su consentimiento informado para ser filmado y es consciente de que la información y las imágenes se publicarán en línea.
References
- Ratner LE, Ciseck LJ, Moore RG, Cigarroa FG, Kaufman HS, Kavoussi LR. Nefrectomía laparoscópica de donante vivo. Trasplante. 1995; 60:1047–1049.
- Dols LF, Ijzermans JN, Wentink N, et al. Seguimiento a largo plazo de un ensayo aleatorizado que comparó la nefrectomía laparoscópica y la nefrectomía abierta de donante vivo con miniincisión. Am J Trasplante. Noviembre de 2010; 10(11):2481-7. doi:10.1111/j.1600-6143.2010.03281.x.
- Wolf JS Jr, Merion RM, Leichtman AB, et al. Ensayo controlado aleatorizado de nefrectomía de donante vivo asistida por mano versus nefrectomía quirúrgica abierta de donante vivo. Trasplante. 27 de julio de 2001; 72(2):284-90. doi:10.1097/00007890-200107270-00021.
- Wilson CH, Sanni A, Rix DA, Soomro NA. Nefrectomía laparoscópica versus nefrectomía abierta para donantes vivos de riñón. Sistema de la Base de Datos Cochrane Rev. 9 de noviembre de 2011; (11):CD006124. doi:10.1002/14651858.CD006124.pub2.
- Fonouni H, Mehrabi A, Golriz M, et al. Comparación de la nefrectomía laparoscópica versus la nefrectomía abierta de donante vivo: una visión general de las complicaciones quirúrgicas y el resultado. Langenbecks Arch Surg. Junio de 2014; 399(5):543-51. doi:10.1007/s00423-014-1196-4.
- Tsoulfas G, Agorastou P, Ko DS, Hertl M, Elias N, Cosimi AB, Kawai T. Nefrectomía laparoscópica vs nefrectomía abierta del donante: lecciones aprendidas de la experiencia de un solo centro académico. Mundo J Nefrol. 6 de enero de 2017; 6(1):45-52. doi:10.5527/wjn.v6.i1.45.
- Kokkinos C, Nanidis T, Antcliffe D, Darzi AW, Tekkis P, Papalois V. Comparación de la nefrectomía laparoscópica versus la nefrectomía manual de donante vivo. Trasplante. 2007; 83:41–47. doi:10.1097/01.tp.0000248761.56724.9c.
- Halgrimson WR, Campsen J, Mandell MS, Kelly MA, Kam I, Zimmerman MA. Complicaciones del donante después de la nefrectomía laparoscópica en comparación con la nefrectomía de donante vivo asistida por la mano: un análisis de la literatura. J Trasplante. 2010; 2010: 825689. doi:10.1155/2010/825689.
- Serrano OK, Kirchner V, Bangdiwala A, et al. Evolución de la nefrectomía de donante vivo en un solo centro: resultados a largo plazo con 4 técnicas diferentes en más de 4000 donantes a lo largo de 50 años. Trasplante. junio de 2016; 100(6):1299-305. doi:10.3390/jcm10061195.
- Giacomoni A, Di Sandro S, Lauterio A, et al. Nefrectomía robótica para donación en vida: técnica quirúrgica y revisión sistemática de la literatura. Am J Surg. 2016 Jun; 211(6):1135-42. doi:10.1016/j.amjsurg.2015.08.019.
- Hubert J, Renoult E, Mourey E, Frimat L, Cormier L, Kessler M. Asistencia robótica completa durante las nefrectomías laparoscópicas de donantes vivos: una evaluación de 38 procedimientos en un solo sitio. Int J Urol. 2007; 14:986–989. doi:10.1111/j.1442-2042.2007.01876.x.
- Bhattu AS, Ganpule A, Sabnis RB, Murali V, Mishra S, Desai M. Nefrectomía laparoscópica asistida por robot frente a nefrectomía laparoscópica estándar del donante: un estudio prospectivo comparativo aleatorizado. J Endourol. 2015; 29: 1334–1340. doi:10.1089/end.2015.0213.
Cite this article
Kimura S, Kawai T. Nefrectomía laparoscópica izquierda del donante. J Med Insight. 2024; 2024(170). doi:10.24296/jomi/170.


