Partielle Mastektomie (Lumpektomie) mit Savi Scout bei einem nicht tastbaren Papillom
Main Text
Table of Contents
Die partielle Mastektomie der Brust, auch Lumpektomie genannt, ist ein brusterhaltendes Verfahren, bei dem viele verschiedene Arten von Massen und Unregelmäßigkeiten im Brustgewebe entfernt werden. Dabei handelt es sich um einen kleinen Schnitt, der an den Brustwarzenrändern oder entlang der natürlichen Brustkonturen verborgen wird, gefolgt von einer Dissektion des betroffenen Bereichs. Das exzidierte Gewebe wird dann zur endgültigen Gewebediagnose in die Pathologie geschickt und gegebenenfalls um festzustellen, ob geeignete Ränder erreicht wurden. Darüber hinaus kann der Einsatz von Savi Scout helfen, die Masse zu lokalisieren, wenn sie sonst schwer zu identifizieren oder zu lokalisieren wäre. Viele verschiedene Brustpathologien können auf diese Weise entfernt werden, sowohl gutartige als auch bösartige, abhängig von biologischen und patientenspezifischen Details. Im vorliegenden Fall wird ein nicht tastbares Papillom – typischerweise eine gutartige Brustläsion mit erhöhtem Risiko für ein okkultes prämalignes duktales Carcinoma in situ (DCIS) – aufgrund des Vorhandenseins von damit verbundenen besorgniserregenden Symptomen bei der Patientin operativ exzidiert.
Gutartige Brustpathologie; brusterhaltende Operationen; Brustkrebs; Brustchirurgie; drahtlose Lokalisierungstechniken.
Intraduktale Papillome sind häufige Brustmassen, die aus der Proliferation von Papillenzellen in den Gängen des Brustgewebes bestehen. 1 Diese Läsionen können tastbare Massen, Brustschmerzen und Brustwarzenausfluss verursachen, der für die Patientinnen von Belang ist. Wenn intraduktale Papillome besorgniserregende Merkmale in der Bildgebung, der körperlichen Untersuchung oder der Pathologie aufweisen, wird eine chirurgische Exzision durch partielle Brustmastektomie empfohlen, wobei sich einige für die Verwendung der Radarlokalisierung von Savi Scout entscheiden. Diese Nachweismethode kann helfen, die Masse während der chirurgischen Exzision abzugrenzen, indem eine Sonde über den bildgeführten, präoperativ platzierten Scout innerhalb des betreffenden Bereichs gelegt wird. Das Ziel des Verfahrens im zugehörigen Video ist es, die Läsion vollständig zu entfernen, so dass sie von der Pathologie vollständig auf eine zugrunde liegende prämaligne DCIS untersucht werden kann, um festzustellen, ob eine weitere medizinische oder chirurgische Behandlung erforderlich ist.
Die Patientin ist eine 46-jährige prämenopausale Frau ohne andere medizinische oder chirurgische Vorgeschichte, die sich zunächst in der Klinik für Brustchirurgie vorstellte, nachdem ihre jährliche Screening-Mammographie eine nicht tastbare rechte Brustmasse von 0,6 x 0,8 x 0,7 cm bei 11 Uhr (oc) und 1 cm von der Brustwarze (FTN) entfernt entdeckte (Abbildung 1). Sie hatte zuvor drei Screening-Mammographien ohne nennenswerte Befunde. Die Screening-Mammographie wurde für nicht schlüssig erklärt (BI-RADS 0), und ein Brustultraschall wurde mit ähnlichen Befunden abgeschlossen. Weitere Gespräche mit der Patientin ergaben, dass in den letzten Monaten ein blutiger Ausfluss auf der rechten Seite ihres BHs zu sehen war, aber keine anderen Bedenken oder Symptome. Aufgrund der nicht schlüssigen bildgebenden Befunde wurde entschieden, eine diagnostische Mammographie durchzuführen, um eine spezifischere Beurteilung (Abbildungen 2a und 2b) im Anschluss an eine ultraschallgesteuerte Kern-Nadel-Biopsie durchzuführen und den Clip für eine Gewebediagnostik zu lokalisieren (Abbildung 3). Die Pathologie zeigte ein intraduktales Papillom mit duktaler Hyperplasie und apokrine Metaplasie ohne Atypie. Angesichts ihres anhaltenden blutigen Brustwarzenausflusses gab es Bedenken hinsichtlich möglicher zugrunde liegender prämaligner Zellen (auf die später mehr eingegangen wird); Daher wurde empfohlen, dass sich die Patientin einer partiellen Mastektomie unterzieht. Die Masse blieb ungreifbar; Daher wurde kurz vor dem operativen Eingriff ein Savi Scout platziert, um den Problembereich zu lokalisieren.
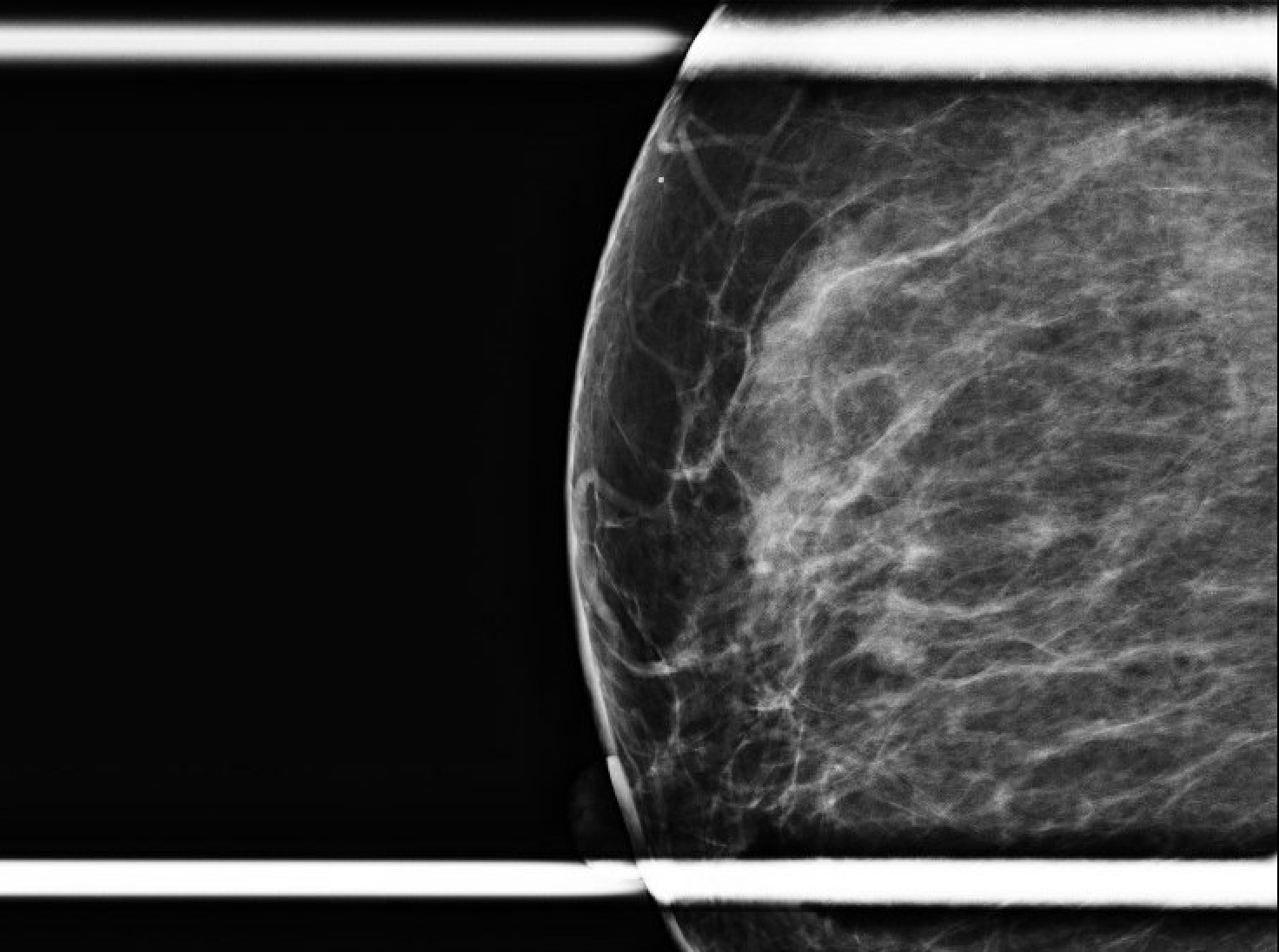
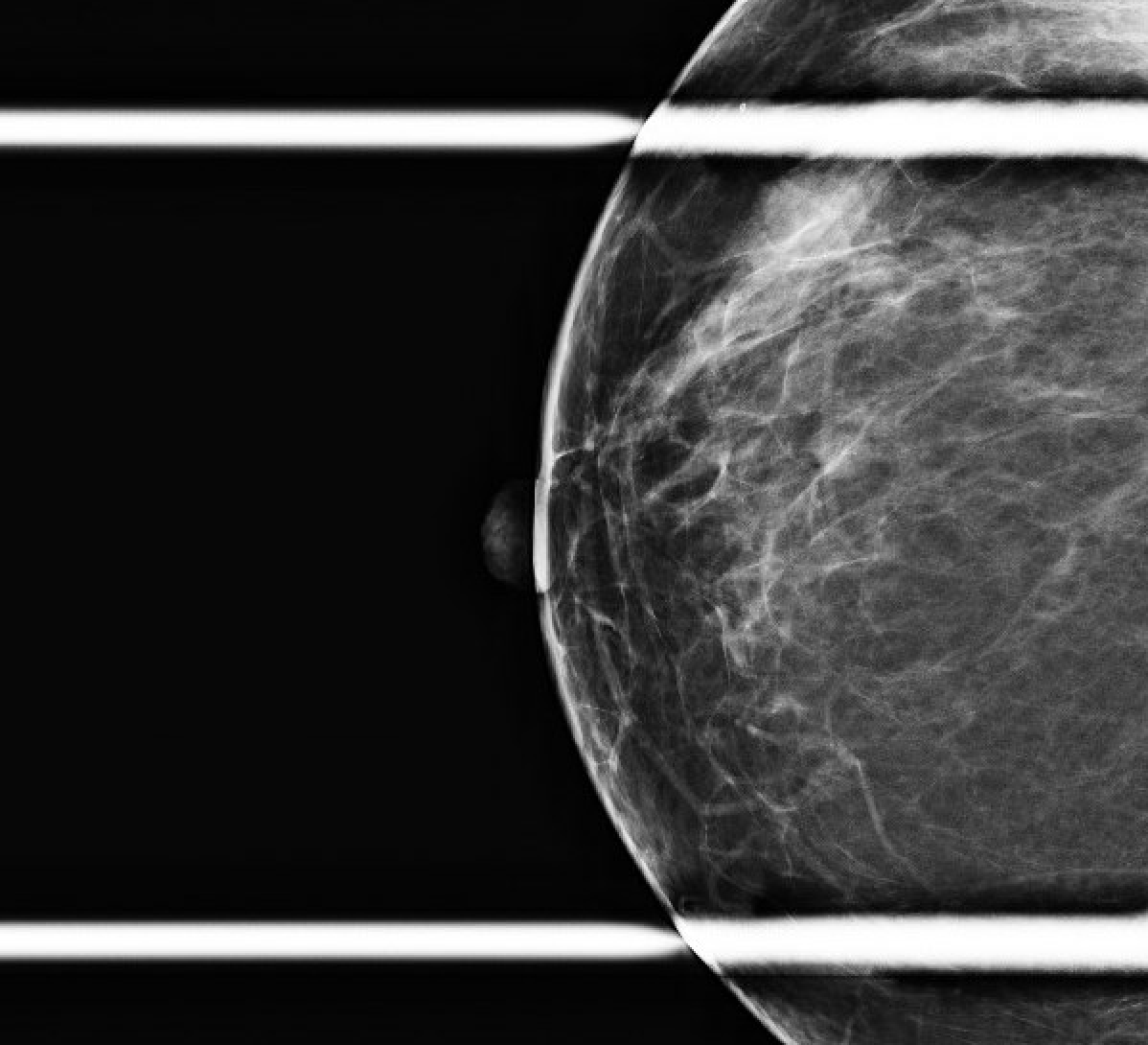
Abbildung 1. Initiale Screening-Mammographie (R mediolaterale Orientierung, gefolgt von kraniokaudaler Orientierung). Es stellte sich heraus, dass der fragliche Bereich etwa 0,6 x 0,8 x 0,7 cm groß war und sich bei 11 oc und 1 cm FTN befand.
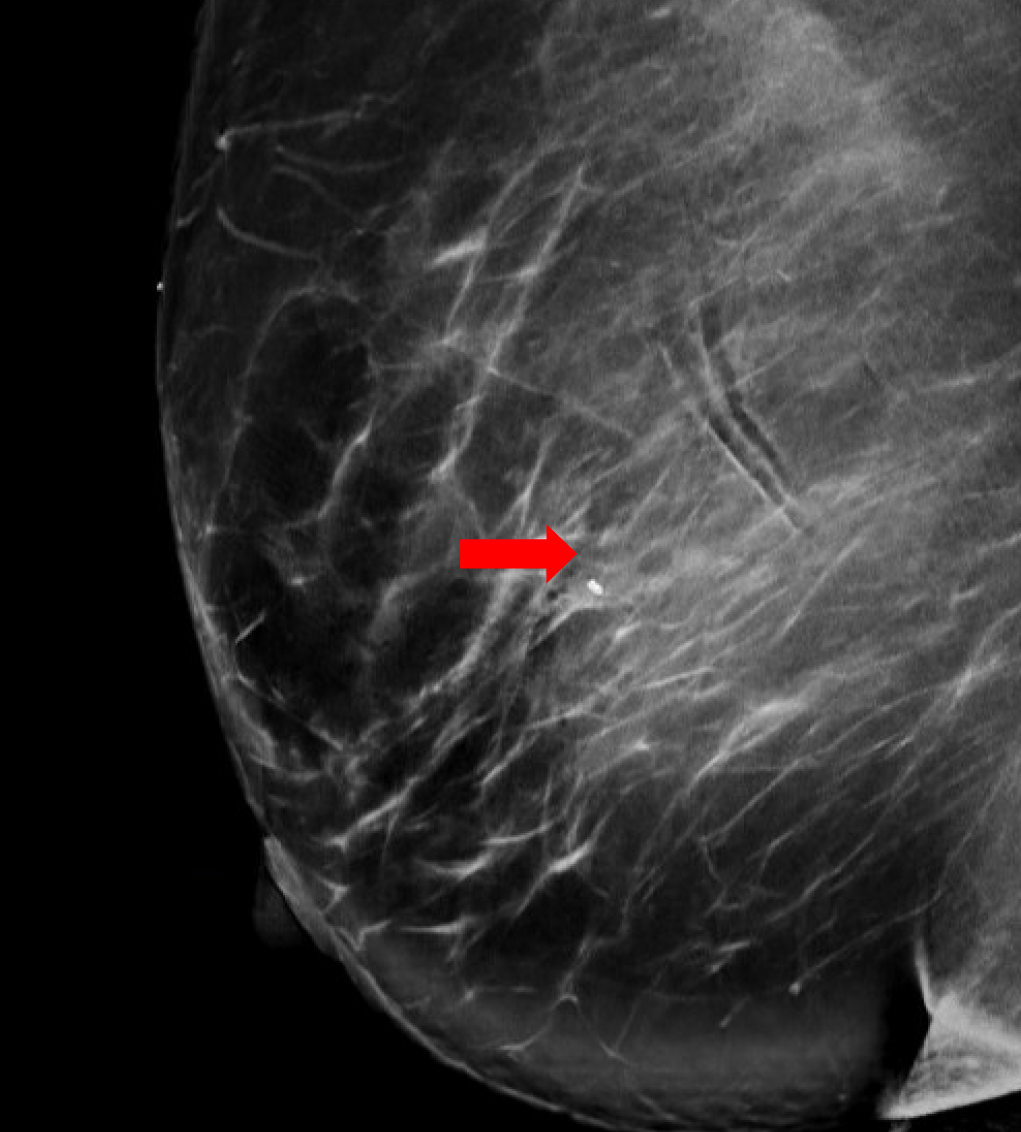
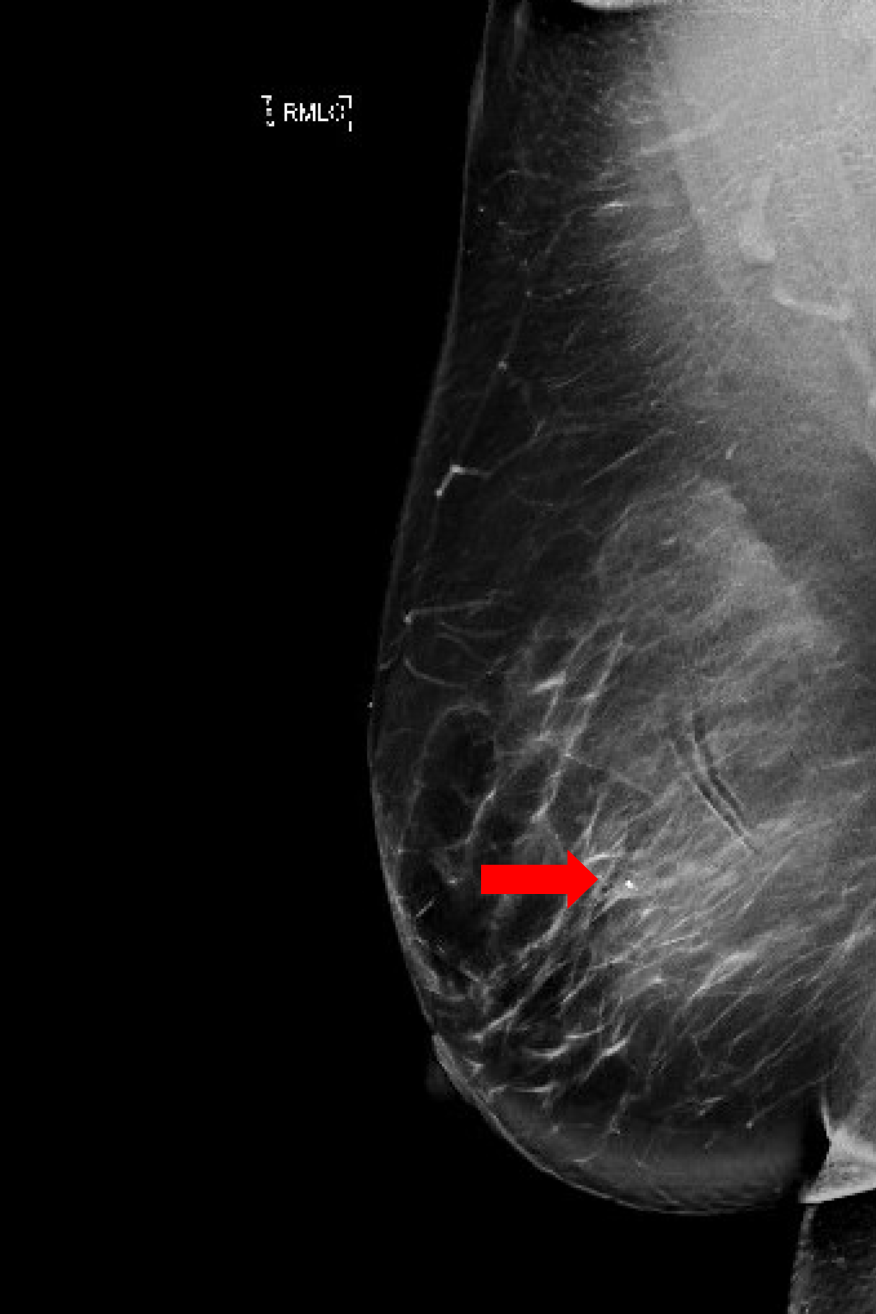
Abbildung 2a. Diagnostische Mammographie nach der Biopsie. Rechte mediolaterale schräge Ansicht, einschließlich eines vergrößerten Bereichs zur besseren Detailgenauigkeit des gewundenen Biopsieclips im Problembereich (Pfeil).
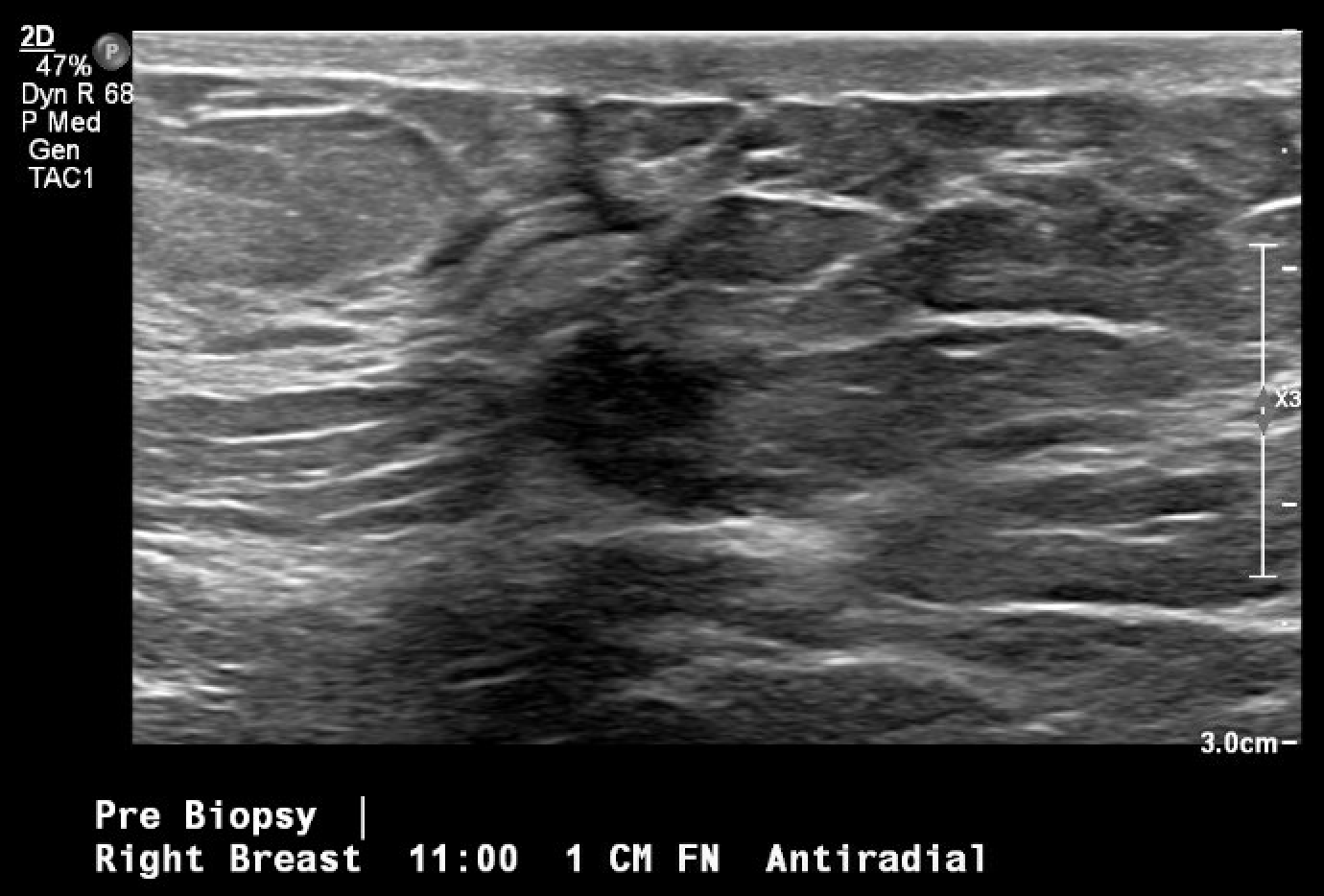
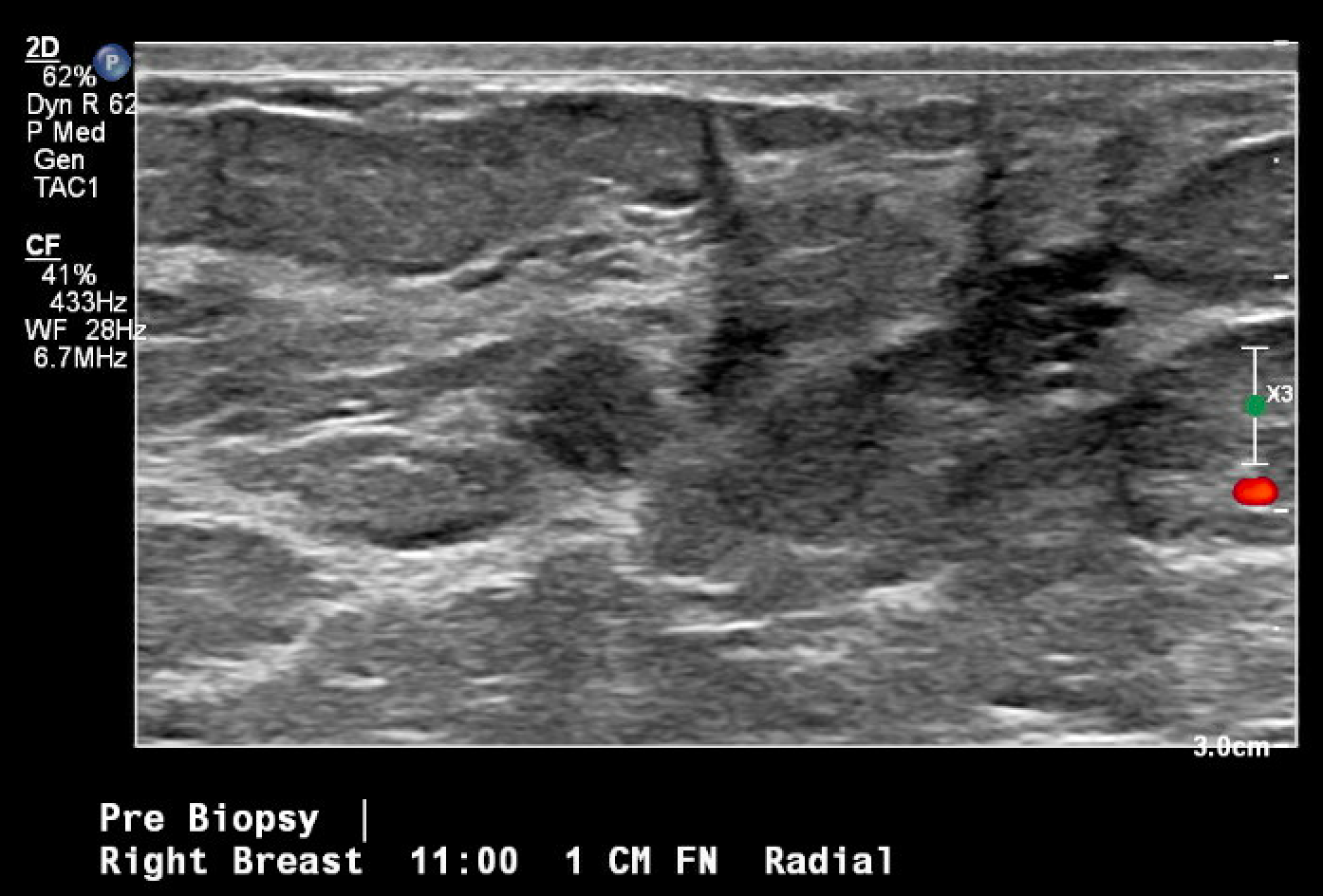
Abbildung 2b. Kraniokaudale Ansicht der diagnostischen Mammographie nach der Biopsie. Einschließlich eines genaueren Bildes des Bereichs mit dem gewickelten Biopsieclip (Pfeil).
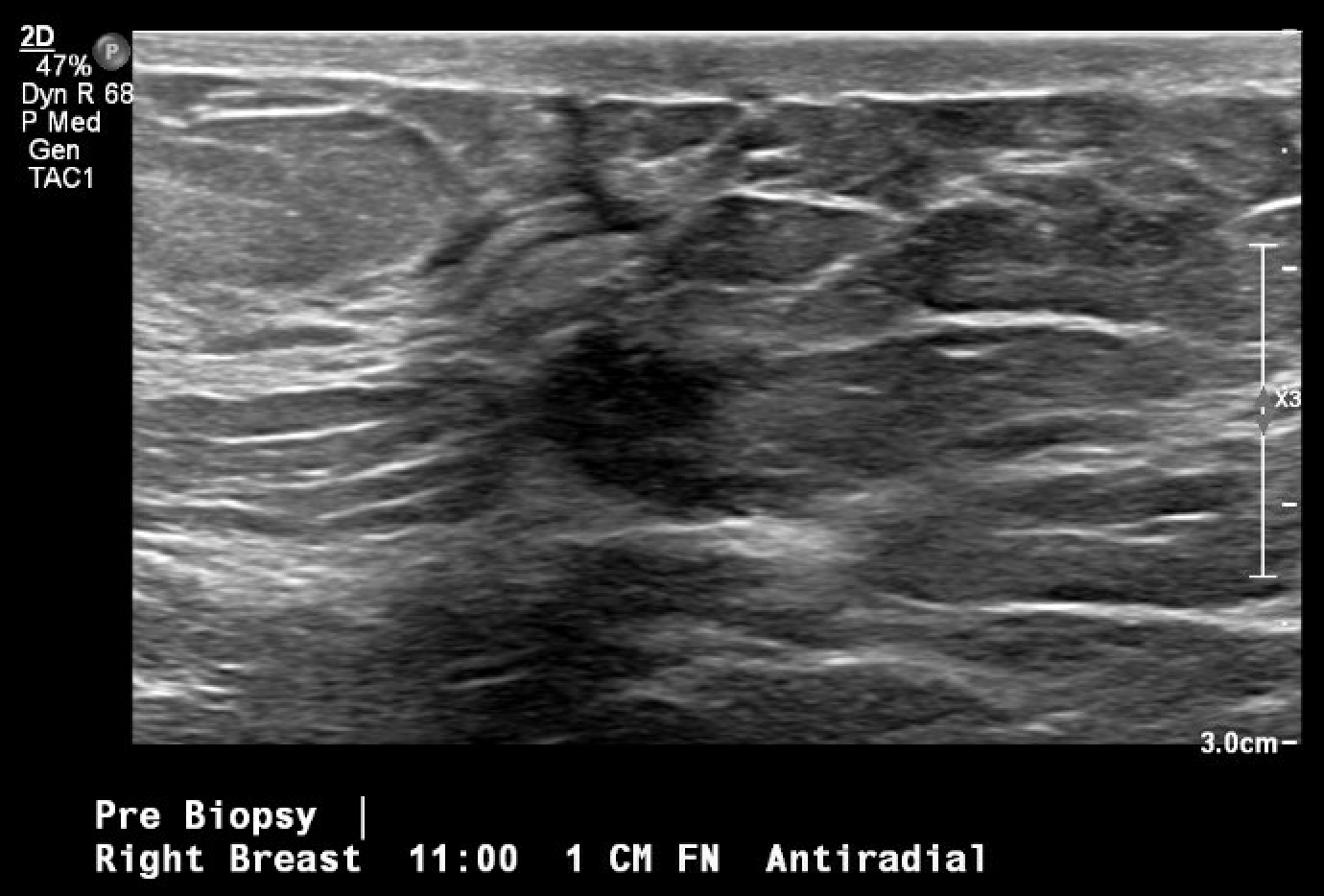
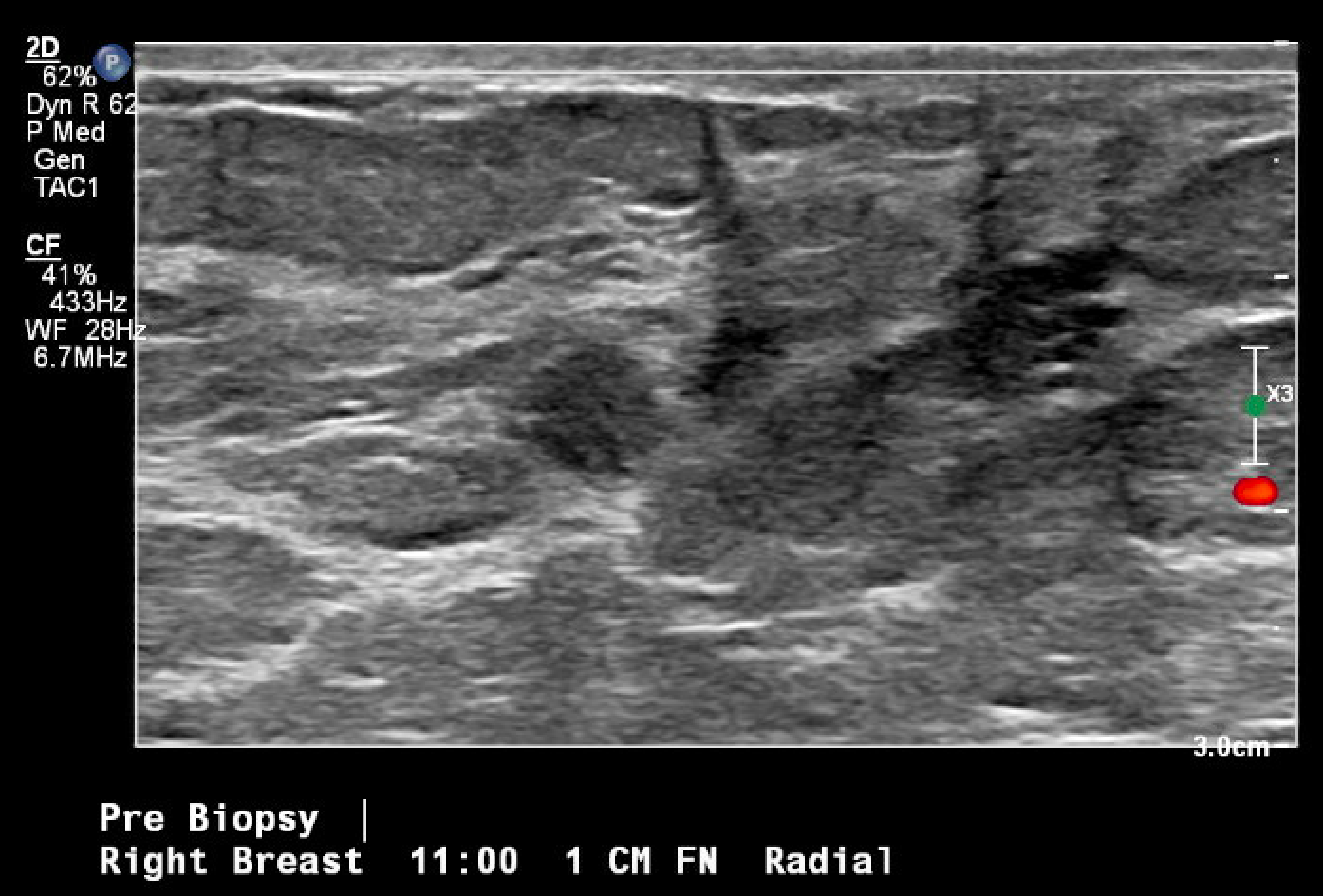
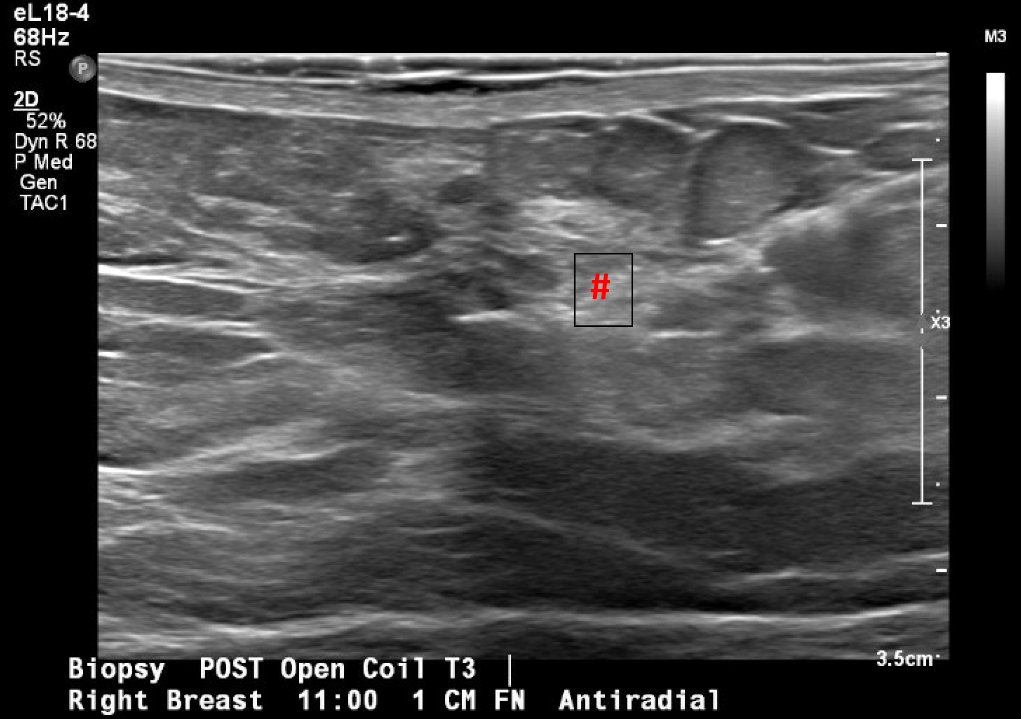
Abbildung 3. Ultraschallgesteuerte Lokalisation und Biopsie der betreffenden Brustmasse, die erstmals in der Screening-Mammographie zu sehen war. Das Bild nach der Biopsie enthält typische Gewebeveränderungen, die nach einer Kern-Nadel-Biopsie zu sehen sind (Raute).
Papillome können bei der Untersuchung nicht immer als tastbare Masse erscheinen. Oft zeigen sie sich zunächst als blutiger Brustwarzenausfluss aus den betroffenen Kanälen, ähnlich wie bei der oben genannten Patientin. Eine vollständige Brustuntersuchung sollte bei allen Patientinnen mit einer Hauptbeschwerde über eine Brustmasse durchgeführt werden. Dies sollte eine Untersuchung der Lymphknoten, einschließlich der Achselhöhle, beinhalten, um mögliche vergrößerte Lymphknoten zu ertasten. Sollten diese vorhanden sein, sollte der Anbieter auf mögliche zugrunde liegende Malignität achten, und möglicherweise sind weitere Untersuchungen erforderlich, um sie auszuschließen. Beim Versuch, den Brustwarzenausfluss auszudrücken, sollte der Anbieter nach Möglichkeit auch versuchen zu bestimmen, aus welchen Kanälen der Ausfluss stammt, insbesondere wenn mehrere beteiligt zu sein scheinen.
Eine diagnostische Mammographie ist in der Regel die erste Wahl für die Bildgebung von Brustmassen, einschließlich Papillomen. Ein Brustultraschall kann auch durchgeführt werden, wenn eine weitere Untersuchung erforderlich ist, ähnlich wie bei der oben genannten Patientin. Wenn die Ergebnisse nicht schlüssig sind oder eine empfindlichere Bildgebung erforderlich ist, kann eine Brust-MRT durchgeführt werden, aber dies ist in der Regel die letzte Wahl und nicht immer erforderlich. Die Verfügbarkeit der Bildgebung im OP kann bei der Lokalisierung der Masse hilfreich sein, wenn sie nicht tastbar ist und der Savi Scout nicht präoperativ platziert werden kann.
Naturgeschichte
Papillome der Brust beginnen als gutartige Polypen der Gänge in der Brust und können bis zu 4 bis 5 cm groß werden, wobei die meisten kleiner als 1 cm bleiben.2 Wenn sich Papillome in der Nähe der Brustwarze befinden, können sie blutigen Ausfluss aus der Brustwarze verursachen. Sie sind auch mit einem erhöhten Risiko für die Entwicklung eines duktalen Carcinoma in situ (DCIS) der Brust verbunden, mit einem Risiko von etwa 5–20 % für Papillome ohne Atypien, die zum Zeitpunkt ihrer Exzision krebsartiges oder präkanzeröses Gewebe enthalten. Das Risiko steigt bei Menschen mit Atypien auf etwa 30–40 %. 2 Es sollten weitere Gespräche mit Patientinnen geführt werden, bei denen Atypien in ihrer Papillomabiopsie festgestellt wurden, einschließlich der Möglichkeit einer postoperativen endokrinen Therapie zur präventiven Behandlung von Brustkrebs. 1 Personen mit aufgewerteten Massen können nach der Entfernung der ursprünglichen Masse eine weitere medizinische Behandlung oder einen chirurgischen Eingriff benötigen; Die Behandlung von malignem und prämalignem Brustkrebs geht jedoch über den Rahmen dieser Übersichtsarbeit hinaus.
Nach der Kernnadelbiopsie der Masse für eine Gewebediagnose hängt die Behandlung vom Vorhandensein von Atypien im Papillom ab. Eine chirurgische Exzision mittels Lumpektomie wird für Patienten mit Atypien empfohlen, da das Risiko eines Upstaging und einer zugrunde liegenden DCIS innerhalb des Papilloms erhöht ist, die später in dieser Übersichtsarbeit ausführlich erörtert wird. Wenn das Papillom bei der Biopsie keine Atypien aufweist, sind die Patientenmerkmale der entscheidende Faktor zwischen der chirurgischen Exzision und der engmaschigen Überwachung mit jährlicher Bildgebung. Zu den besorgniserregenden Merkmalen gehören blutiger Ausfluss der Brustwarze, eine Masse > einer Größe von 1,5 cm oder > 3 cm von der Brustwarze entfernt oder eine Diskrepanz zwischen Bildgebung und Biopsie. 1 Liegen diese besorgniserregenden Befunde vor, folgt in der Regel die Empfehlung zur chirurgischen Exzision, um die Abklärung der zugrundeliegenden Hochrisikoläsionen oder Malignität abzuschließen. Patienten, die asymptomatisch sind und diese Merkmale nicht aufweisen, können mit jährlichen Mammographien auf Veränderungen überwacht werden. 1,3 kg
Ziel der Behandlung mit chirurgischer Exzision und partieller Mastektomie (Lumpektomie) ist es, mögliches krebsartiges Brustgewebe zu entfernen und die weitere Entwicklung oder das Wiederauftreten dieses Krebses zu verhindern. Der Patient im obigen Fall hatte möglicherweise ein kleines Papillom; Ihr gleichzeitiger blutiger Brustwarzenausfluss gab jedoch Anlass zur Sorge über mögliche zugrunde liegende Prämalignität oder Atypien, so dass sie sich einer Exzisionsbiopsie mittels Lumpektomie unterzog. 4
Das intraduktale Papillom der Brust muss von der Papillomatose unterschieden werden – einem hyperplastischen Epithel in mehreren Kanälen, das am häufigsten bei jüngeren Patientinnen auftritt. Ein Rezidiv ist häufig und betrifft die beidseitigen Brüste. Die Papillomatose ist auch mit einem 1,5- bis 2-fach erhöhten Risiko für die Entwicklung von DCIS im Vergleich zu Patienten ohne Diagnose verbunden und wird mit chirurgischer Exzision behandelt. 5
Wie bei jedem chirurgischen Eingriff sollten jeder Patient und seine Begleiterkrankungen vollständig untersucht werden, bevor sie sich einer Lumpektomie unterziehen. Im Gegensatz zu einer standardmäßigen, einfachen Mastektomie kann eine partielle Mastektomie unter MAC und örtlicher Betäubung durchgeführt werden. Diese Optionen können einen sichereren Operationsplan für Patienten mit schweren Komorbiditäten bieten. Nichtsdestotrotz sollten alle notwendigen präoperativen Herz-, Lungen- und anderen Systeme mit Verdacht auf oder bekannte Komorbiditäten untersucht werden, damit der Patient ordnungsgemäß für den Operationssaal freigegeben wird.
Dieser Fall zeigt das typische Verfahren und die wichtigsten Schritte bei der Durchführung einer partiellen Mastektomie (Lumpektomie) mit Savi Scout Lokalisation. Durch einen kleinen Schnitt wurde alles notwendige Gewebe komplikationslos entfernt. Die Bildgebung nach der Biopsie und der Savi Scout-Platzierung wurde während des gesamten Falls gezeigt, um den Gesamtverlauf der Exzision zu bestimmen. Der Savi Scout war jedoch von entscheidender Bedeutung, um sicherzustellen, dass wir nur den Problembereich entfernt haben. Der Problembereich wurde erfolgreich in einem Bereich mit der stärksten Radarreaktion lokalisiert, und die Dissektion in Richtung dieser Region begann durch den kleinen Hautschnitt. Nachdem die Sonde den erforderlichen Abstand zum Savi-Marker gemessen hatte, um anzuzeigen, dass unser biopsierter Bereich angemessen lokalisiert war, wurde die Region akribisch als kleiner "Würfel" aus dem verbleibenden Brustgewebe herauspräpariert. Während der Dissektion jeder Seite wurde der Savi Scout mit Hilfe der Sonde wiederholt im isolierten Brustgewebe identifiziert. Es kam zu einem minimalen Blutverlust, und nach Abschluss der Operation war nur eine sehr geringe Blutstillung erforderlich. Insgesamt hatte der Patient eine Gesamtoperationszeit von ca. 1 Stunde. Die Orientierung wurde während der gesamten Lumpektomie beibehalten, und jede Seite des "Würfels" wurde mit den für die Pathologie standardisierten Tintenfarben markiert. Die Probe wurde intraoperativ in einem tragbaren Röntgenschrank geröntgt, in dem sich sowohl der Biopsieclip als auch der Savi Scout-Marker befanden (Abbildung 4). Das exzidierte Gewebe wurde in die Pathologie geschickt, wo die endgültige Diagnose als intraduktales Papillom ohne Atypie bestätigt wurde.

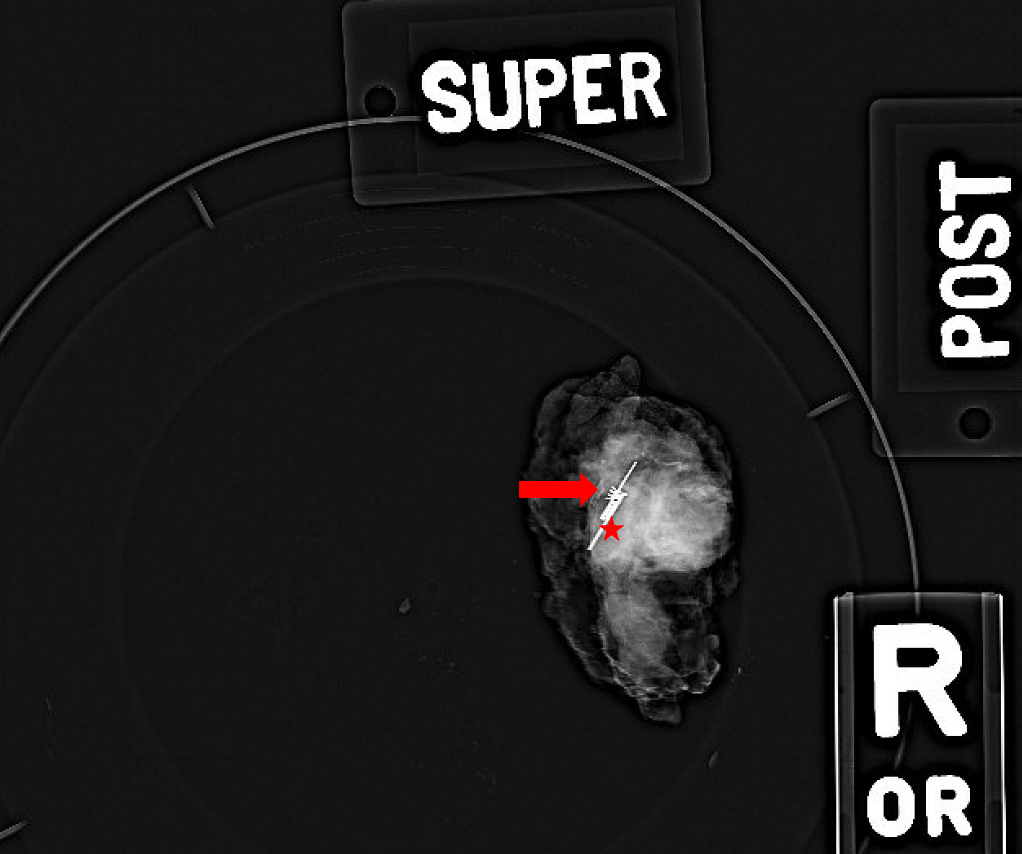
Abbildung 4. Das intraoperative Röntgen der exzidierten Masse. Wird verwendet, um den biopsierten Bereich mit dem gewickelten Clip (Pfeil) zu bestätigen, und der zuvor platzierte Savi Scout, der wie eine Langhantel (Stern) geformt ist, wird entfernt. Falls erforderlich, können Röntgenaufnahmen nach der Exzision auch zeigen, ob an den Rändern der exzidierten Masse noch besorgniserregendes Gewebe vorhanden ist.
Nach dem Eingriff erholte sich die Patientin in der PACU für die erforderliche Zeit in unserer Einrichtung. Sie wurde entlassen, nachdem sie alle Kriterien erfüllt hatte, und erholte sich zu Hause gut. Bei ihrem Nachsorgetermin heilte ihr Schnitt gut ab, ohne nennenswerte Narbe und ohne kosmetische Bedenken. Auch ihr blutiger Brustwarzenausfluss war zu diesem Zeitpunkt bereits verschwunden.
Im Vergleich zu einer totalen Mastektomie ist die Operationszeit für eine Lumpektomie in der Regel stark verkürzt und erfordert keine so umfangreiche Dissektion. Darüber hinaus ist bei einer Lumpektomie, wie bei dem oben beschriebenen Patienten, in der Regel keine Übernachtung erforderlich. Die Lumpektomie bietet daher nicht nur eine schnellere Genesung der Patientinnen, sondern kann gegebenenfalls auch zu einer viel kostengünstigeren Option für die chirurgische Behandlung der Brustpathologie führen.
Brusterhaltende chirurgische Optionen können für Patientinnen die bevorzugte Wahl sein, wenn es um die Entfernung von typischerweise gutartigen Läsionen geht. Die Zufriedenheit der Patientin mit dem postoperativen Erscheinungsbild und der Kosmesis korreliert mit der Menge des herausgeschnittenen Brustvolumens; 6 Daher ist die Lokalisation der Masse von entscheidender Bedeutung, um sicherzustellen, dass nur das benötigte, betreffende Brustgewebe entfernt wird und jede mögliche gesunde Brust zurückbleibt. Die Lokalisierungsoptionen haben sich im Laufe der Jahre weiterentwickelt. Der anfängliche Einsatz der Drahtlokalisierung wurde als akzeptable Option erachtet und wird heute in einigen Einrichtungen fortgesetzt; 7,8 Patientenbeschwerden, Drahtverschiebungen und -migration sowie schlechte kosmetische und chirurgische Ergebnisse führten jedoch zur Entwicklung effektiverer Lokalisationsoptionen. 8,9,10,11 In einer Metaanalyse wurde ein Trend zu weniger positiven Rändern und weniger Re-Exzision bei der Nicht-Draht-Lokalisation im Vergleich zur drahtgeführten Lokalisierung festgestellt; 8 Dies war jedoch statistisch nicht signifikant. Eine bessere Lebensqualität und Kosmesis wurden gegenüber den nicht drahtgebundenen Lokalisationsgruppen, einschließlich Savi Scout, begünstigt, was wahrscheinlich mit der erhöhten Menge an gesundem Gewebe zusammenhängt, das wahrscheinlich an Ort und Stelle bleibt, und der Vermeidung einer erneuten Operation. 8 Da der Radiologe den drahtlosen Lokalisierer an jedem Eintrittspunkt in das Gewebe einführen kann, ohne einen großen Schnitt zu hinterlassen, kann der chirurgische Schnitt auf die kosmetisch ansprechendste Option für den Patienten vorgenommen werden. 8 Bei der Behandlung einer wahrscheinlich gutartigen Läsion, wie z. B. eines Papilloms ohne Atypie, trägt die Verwendung von nicht drahtgesteuerten Lokalisierungsoptionen dazu bei, sicherzustellen, dass der Zielbereich entfernt wird, und die Patientenergebnisse postoperativ zu verbessern.
Die chirurgische Behandlung von Papillomen im Vergleich zum wachsamen Abwarten wurde mehreren verschiedenen Vergleichen und eingehenden Untersuchungen unterzogen. Es ist zunächst wichtig festzustellen, ob das Papillom bei der Biopsie Atypien aufweist oder nicht. Wenn ein biopsiebestätigtes Papillom mit Atypie diagnostiziert wird, wird aufgrund des erhöhten Risikos eines Upgrades zum Zeitpunkt der Exzision immer eine chirurgische Exzision empfohlen. 12,13 Es gab jedoch mehrere Untersuchungen darüber, ob Papillome ohne Atypie überhaupt einer chirurgischen Exzision bedürfen oder ob es sicherer wäre, wachsam zu warten, da das Risiko einer Operation vermieden würde. Eine kleine retrospektive Studie an einer einzigen Einrichtung überprüfte 138 Fälle von Papillom ohne Atypie und stellte fest, dass 2,4 % der chirurgisch herausgeschnittenen Pathologien und weitere 11,67 % zu Hochrisikoläsionen hochgestuft wurden. 14 Die konservative Managementgruppe hatte eine große Anzahl von Patienten, die für die Nachsorge verloren gingen, und konnte daher nicht zu dem Schluss kommen, dass wachsames Abwarten bei Papillomen ohne Atypie ratsam war. 14 Die Ergebnisse dieser Studie waren ähnlich wie bei mehreren anderen, mit einer relativ hohen Rate an Papillomen, die zu Hochrisiko- oder In-situ-Läsionen hochgestuft wurden. 15–17 Uhr Dennoch wurde in diesen Studien nicht zwischen denjenigen unterschieden, die Hochrisikosymptome oder -befunde enthalten, und solchen, die ansonsten gutartig erscheinen. Da keine Störfaktoren berücksichtigt wurden, wurde in zusätzlichen Studien versucht zu bestimmen, welche Anzeichen oder Symptome auf ein höheres Risiko für ein Upgrade bei Papillomen ohne Atypie hinweisen. Bestimmte Studien kategorisierten Papillome nach Größe, bildgebender Konkordanz und anderen besorgniserregenden Symptomen, einschließlich blutigem Brustwarzenausfluss. Eine solche Studie ergab, dass nur 2,1 % der Patienten zum Zeitpunkt der chirurgischen Exzision ein Upgrade auf Malignität hatten; 18 Es wurde jedoch empfohlen, größere Massen von mehr als 1,5 cm zu exzidieren, da sie mit einem höheren Upgrade-Risiko verbunden sind (p = 0,02). 18 Eine Metaanalyse, die auch die Daten von zwei anderen Einrichtungen umfasste, wurde durchgeführt, um das Risiko eines Läsionsupgrades nach der Exzision zu bestimmen, und ergab, dass nur 0,6 % der exzidierten Läsionen postoperativ ein Upstaging erforderten. 19 Diese Ergebnisse umfassten keine Papillome, die nicht mit ihrer Bildgebung übereinstimmten oder anderweitig als Hochrisikoläsionen galten. Sie kamen zu dem Schluss, dass risikoarme, konkordante Papillome ohne Atypien wachsam abgewartet werden können und chirurgische Eingriffe vermieden werden können, vorausgesetzt, es treten keine besorgniserregenden Entwicklungen auf. 19 Die klinische Beurteilung und die Besorgnis sollten das medizinische Management leiten, wenn es entscheidet, ob eine chirurgische Exzision erforderlich ist, wie dies im oben diskutierten Fall der Fall war.
Für die Durchführung der partiellen Mastektomie mit Savi Scout Lokalisierung wurden verschiedene Geräte eingesetzt. Der Savi Scout und seine Lokalisationssonde waren in diesem Fall unerlässlich, um Gewebe zu lokalisieren, das nicht leicht zu identifizieren war. Das von Merit Medical Systems hergestellte SCOUT Radar-Lokalisierungssystem hilft dabei, die richtige Richtung zum im Gewebe platzierten Chip und seinen Abstand zur Sonde zu identifizieren. Darüber hinaus wurde bei dem Verfahren ein tragbarer Röntgenschrank verwendet, um das exzidierte Gewebe abzubilden, um eine sofortige, intraoperative Bestätigung zu erhalten, dass der biopsierte Bereich vollständig entfernt wurde. Das Trident HD Specimen Radiography System wurde während des Eingriffs in dem zugehörigen Video verwendet; Es gibt jedoch zahlreiche andere Optionen, die in verschiedenen Institutionen verfügbar sein können.
Wir erklären, dass dieser Artikel ohne jegliches Sponsoring oder finanzielle Unterstützung durch Dritte erstellt wurde.
Die Autoren danken Dr. Lauren Kwasny, DO, für die Organisation und Bereitstellung der Möglichkeit, an dieser Bildungsmöglichkeit teilzunehmen.
Der Patient, auf den sich dieser Videoartikel bezieht, hat seine Einverständniserklärung gegeben, gefilmt zu werden, und ist sich bewusst, dass Informationen und Bilder online veröffentlicht werden.
References
- Sabel MS. Proliferative Läsionen ohne Atypien: Intraduktale Papillome. In: UpToDate. Chagpar AB, Whitman GJ, Hrsg. Wolters Kluwer, 2025. Abgerufen am 29. März 2025.
- Calvillo KZ, Portnow LH. Intraduktale Papillome der Brust. Ann Brustchirurgie. 2021;5:18-24. doi:10.21037/abs-20-113.
- Amerikanische Gesellschaft der Brustchirurgen. Brusterhaltende Operation/partielle Mastektomie. Amerikanische Gesellschaft der Brustchirurgen; 2020. Verfügbar ab: https://www.breastsurgeons.org/docs/statements/asbrs-rg-breast-conserving-surgery-partial-mastectomy.pdf.
- Al Sarakbi W, Worku D, Escobar PF, Mokbel K. Brustpapillome: derzeitige Behandlung mit Schwerpunkt auf einer neuen diagnostischen und therapeutischen Modalität. Int Semin Surg Oncol. 2006; 3(1). doi:10.1186/1477-7800-3-1.
- Debnath D, Al-Okati D, Ismail W. Multiple Papillomatose der Brust und Behandlungswahl der Patientin. Pathologische Abteilung Int. 2010;2010:540590. doi:10.4061/2010/540590.
- Cochrane RA, Valasiadou P, Wilson ARM, et al. Die Kosmesis und Zufriedenheit nach einer brusterhaltenden Operation korreliert mit dem Prozentsatz des herausgeschnittenen Brustvolumens. Br J Surg. 2003; 90(12):1505-1509. doi:10.1002/bjs.4344.
- Hall F, Frank H. Präoperative Lokalisation von nicht tastbaren Brustläsionen. Am J Roentgenol. 1979;132:101-105. doi:10.2214/ajr.132.1.101.
- Garzotto F, Comoretto RI, Michieletto S, et al. Präoperative Lokalisation von nicht tastbaren Brustläsionen, innovative Techniken und klinische Ergebnisse in der chirurgischen Praxis: eine systematische Übersichtsarbeit und Metaanalyse. J Brust. 2021;58:93-105. doi:10.1016/j.breast.2021.04.007.
-
Ahmed M, van Hemelrijck M, Douek M. Systematische Überprüfung der radiogesteuerten versus drahtgesteuerten Lokalisation bei der Behandlung von nicht tastbaren Brustkrebsarten. Brustkrebs erneut behandeln. Juli 2013; 140(2):241-52. doi:10.1007/s10549-013-2547-5.
-
Dua SM, Gray RJ, Keshtgar M. Strategien zur Lokalisation von untastbaren Brustläsionen. J Brust. 2011;20:246-253. doi:10.1016/j.breast.2011.01.007.
-
Pouw B, de Wit-van der Veen LJ, Stokkel MPM, Loo CE, Vrancken Peeters MJ, Valdés Olmos RA. Auf dem Weg zur Lokalisierung von radioaktiven Keimen bei nicht tastbaren Brustkrebsoperationen? Eine Meta-Analyse. J Surg Oncol. 2015; 111:185-191. doi:10.1002/jso.23785.
-
Catanzariti F, Avendano D, Cicero G, et al. Hochrisikoläsionen der Brust: gleichzeitige Diagnoseinstrumente und Behandlungsempfehlungen. Einblicke Bildgebung. 2021; 12(1):63. doi:10.1186/s13244-021-01005-6.
-
Lamb LR, Bahl M. Evidenzbasierter pragmatischer Ansatz für die Behandlung von Borderline- oder Hochrisiko-Brustläsionen. AJR Am J Roentgenol. 2022; 218(1):186-187. doi:10.2214/AJR.21.26340.
-
Moynihan A, Quinn EM, Smith CS et al. Gutartiges Brustpapillom: Ist eine chirurgische Exzision notwendig? J Brust. 2019; 26(4):705-710. doi:10.1111/tbj.13642.
-
Tatarian T, Sokas C, Rufail M, et al. Intraduktales Papillom mit gutartiger Pathologie bei der Brustkernbiopsie: Exzidieren oder nicht? Ann SurgOncol. 2016; 23(8):2501‐2507.8. doi:10.1245/s10434-016-5182-7.
-
Jaffer S, Nagi C, Bleiweiss IJ. Die Exzision ist indiziert für intraduktale Papillom der Brust, das bei der Kernnadelbiopsie diagnostiziert wird. Krebs. 2009; 115(13):2837‐2843.9. doi:10.1002/cncr.24321.
-
Rizzo M, Linebarger J, Lowe MC et al. Management von papillären Brustläsionen, die bei der Kernnadelbiopsie diagnostiziert wurden: klinische pathologische und radiologische Analyse von 276 Fällen mit chirurgischer Nachsorge. J AmColl Surg. 2012; 214(3):280‐287. doi:10.1016/j.jamcollsurg.2011.12.005.
-
Polat DS, Knippa EE, Ganti R, Seiler SJ, Goudreau SH. Gutartige Brustpapillome ohne Atypie, die mit einer Kernnadelbiopsie diagnostiziert wurden: Ergebnis der chirurgischen Exzision und der bildgebenden Nachsorge. Eur J Radiol. 2020;131:109237. doi:10.1016/j.ejrad.2020.109237.
-
Grimm, LJ, Bookhout, CE, et al. Konkordante, nicht-atypische Brustpapillome erfordern keine chirurgische Exzision: eine 10-jährige Studie an mehreren Institutionen und Überprüfung der Literatur. Clin Imag. 51:180-185. doi:10.1016/j.clinimag.2018.04.021.
Cite this article
Flessland OD, Moberg LA, Fortes TA. Partielle Mastektomie (Lumpektomie) mit Savi Scout bei einem nicht tastbaren Papillom. J Med Insight. 2025; 2025(492). doi:10.24296/jomi/492.



