Implante de fibra de carbono para fixação de uma fratura subtrocantérica patológica
Massachusetts General Hospital
Main Text
Table of Contents
Aqui, apresentamos um paciente com fratura patológica subtrocantérica do fêmur, secundária a um adenocarcinoma pulmonar primário não diagnosticado. A fratura, ocorrendo no contexto de dor persistente e não traumática nas coxas e joelhos, levou à rápida identificação de sua natureza patológica no Pronto-Socorro. O plano de tratamento envolveu redução aberta e fixação interna utilizando uma unha de fibra de carbono, considerando a necessidade imediata de estabilização e fatores oncológicos subjacentes.
O foco principal era alcançar a fixação de fraturas, tradicionalmente realizada com dispositivos intramedulares. No entanto, a decisão de usar um prego de fibra de carbono foi tomada devido à natureza patológica da fratura e à necessidade subsequente de intervenção oncológica pós-cirúrgica. A radiolucidez única da fibra de carbono auxilia no planejamento pós-operatório da radiação, garantindo visualização ótima e precisão no direcionamento de lesões ósseas. Essa abordagem contribui para a redução de fraturas enquanto minimiza a interferência com a radioterapia.
O procedimento cirúrgico envolveu a inserção de hastes intramedulares com unha de fibra de carbono, alcançando redução bem-sucedida de fraturas e posicionamento ideal do hardware. Avaliação histopatológica confirmou adenocarcinoma pulmonar metastático. Após a operação, o paciente recebeu radioterapia paliativa e terapia direcionada, demonstrando melhora substancial no acompanhamento de dois meses (Figura 6).
O caso destaca o uso estratégico de implantes de fibra de carbono no manejo de fraturas patológicas, oferecendo vantagens em imagens pós-operatórias, monitoramento de doenças e precisão no planejamento da radioterapia. A abordagem multidisciplinar ressalta a importância de considerar as nuances da seleção do implante, especialmente na doença óssea metastática, para otimizar os resultados.
Implantes de fibra de carbono; fratura patológica; Doença óssea metastática.
Um paciente apresentou uma fratura patológica subtrocantérica do fêmur no lado direito, ocorrendo no contexto de um adenocarcinoma pulmonar primário inicialmente não diagnosticado. Seu histórico médico incluiu dor persistente e não traumática nas coxas e joelhos, que piorou progressivamente, culminando em aumento repentino da dor, fraqueza nas pernas e uma queda subsequente após a perna ceder na escada. Ao ser apresentado ao Pronto-Socorro, a natureza patológica da fratura foi prontamente identificada. Após uma avaliação oncológica, o plano de tratamento envolveu uma redução aberta e fixação interna, optando por unha de fibra de carbono devido à necessidade imediata de estabilização da fratura e às considerações oncológicas subjacentes.
Neste caso, o foco principal era alcançar a fixação da fratura, uma tarefa tradicionalmente realizada com um dispositivo intramedular. No entanto, considerando a natureza patológica da fratura e a necessidade subsequente de intervenção oncológica após a cirurgia, decidiu-se utilizar um prego de fibra de carbono. Fraturas patológicas, comuns em condições metastáticas, frequentemente exigem radioterapia pós-operatória para tratar células cancerígenas residuais e facilitar a cicatrização óssea nativa. A implementação do planejamento de tratamento de radioterapia, envolvendo simulação de tomografia computadorizada, é significativamente auxiliada por implantes de fibra de carbono, aprimorando a visualização e a precisão no direcionamento da lesão óssea. Essa abordagem visa alcançar o objetivo de redução de fraturas, minimizando a interferência causada pelos implantes metálicos tradicionais durante o planejamento da radiação.
Uma mulher branca geriátrica foi encontrada com fratura patológica subtrocantérica. Curiosamente, em exames adicionais, foi diagnosticado que o paciente apresentava um carcinoma pulmonar primário. O uso de um prego de fibra de carbono durante a redução aberta e a fixação interna não apenas estabilizou a fratura, mas também otimizou a precisão no planejamento pós-operatório de radiação.
O paciente negou qualquer golpe na cabeça ou perda de consciência e não apresentou sinais de delírio ou confusão. O exame físico do membro inferior direito foi limitado devido à dor. Sua perna direita estava visivelmente encurtada. O exame revelou dor e resistência limitada no extensor halucis longus (EHL), flexor hallucis longus (FHL), tibial anterior (TA) e gastrocnêmio (GS). Pulsos distas, incluindo dorsal pedis (DP) e tíbia posterior (PT), estavam intactos, e o pé direito demonstrou calor e perfusão adequada. A avaliação subsequente da lesão dos tecidos moles revelou interrupções no nervo peroneal superficial (SPN), nervo peroneal profundo (DPN), nervo tibial (TN), nervo safeno e nervo sural.
A imagem radiográfica do quadril direito e do fêmur em sua apresentação inicial após a queda revelou uma fratura subtrocantérica deslocada com deslocamento medial do fragmento distal. A cabeça femoral permaneceu bem assente no acetábulo, e o restante do fêmur permaneceu intacto (Figura 1). O estreitamento degenerativo do espaço articular com osteófitos marginais foi evidente. Uma tomografia computorizada (TC) com contraste do tórax mostrou uma grande massa do lobo superior direito envolvendo o brônquio principal direito, resultando em atelectasia completa do lobo superior direito (Figura 2). A missa suspeitava de malignidade. Múltiplos linfonodos mediastinais e bilaterais hilares aumentados são preocupantes para doenças metastáticas. Uma tomografia computadorizada não ampliada do fêmur direito revelou lucências intracorticais inespecíficas do eixo médio do fêmur na margem inferior da fratura. Esse achado levantou preocupações sobre lesões permeativas subjacentes e uma fratura patológica (Figura 3). Embora a ressonância magnética (RM) de acompanhamento possa ter ajudado a determinar a presença de lesões ósseas subjacentes, a avaliação em ambiente agudo é limitada por edema e hemorragia, o que levou à decisão de não realizar esse exame.
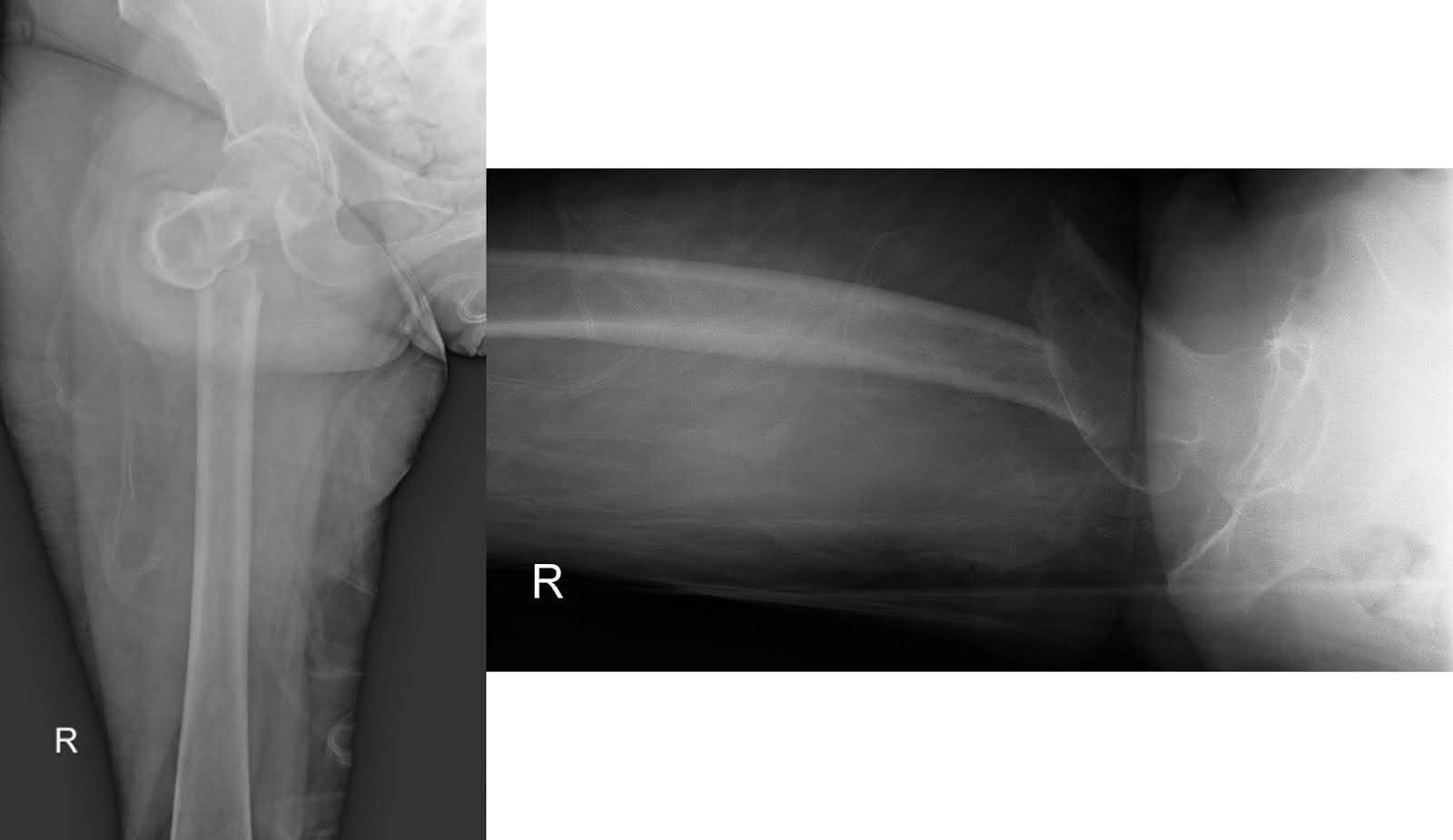
Figura 1. Radiografias AP e laterais do quadril direito ilustrando uma fratura subtrocantérica deslocada. A cabeça femoral mantém a redução dentro do acetábulo, enquanto o restante do fêmur permanece estruturalmente intacto.
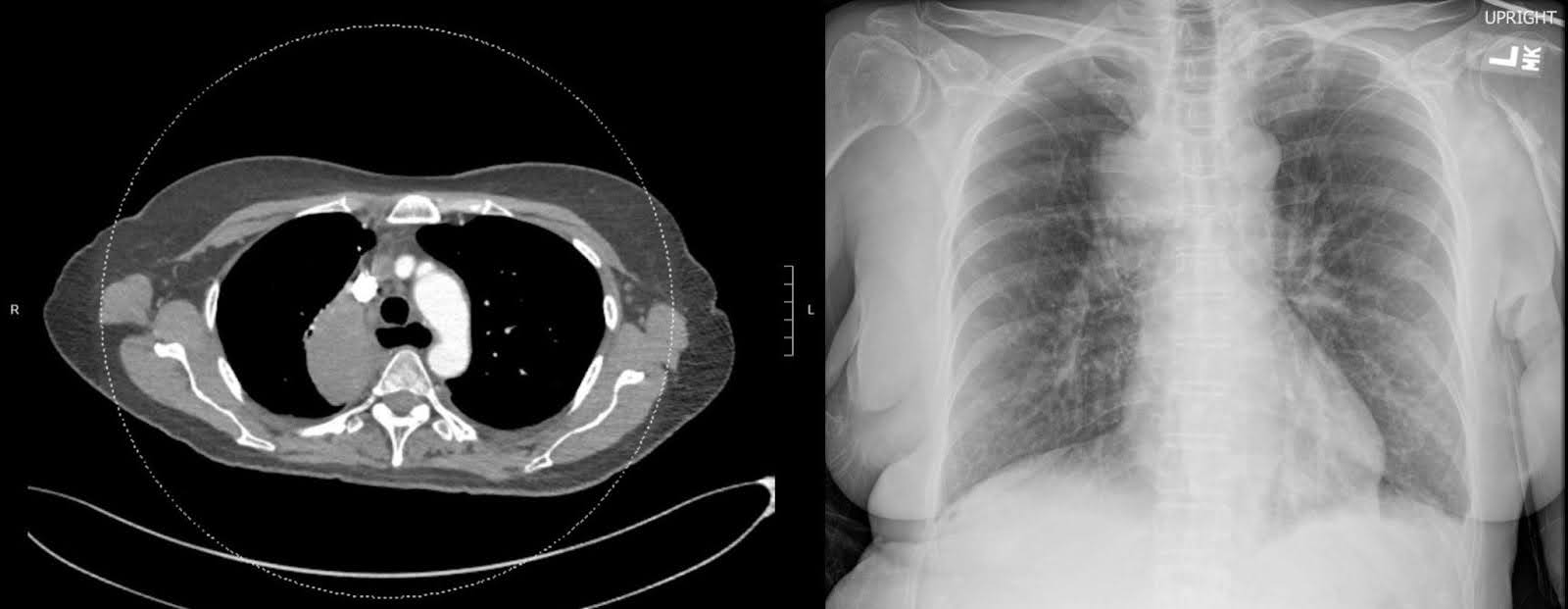
Figura 2. Uma massa heterogeneamente aprimorada, localizada na região paramediastinal direita do lobo superior direito, foi encontrada durante uma tomografia computorizada do tórax com contraste. A presença desse achado sugere um diagnóstico de câncer primário de pulmão.
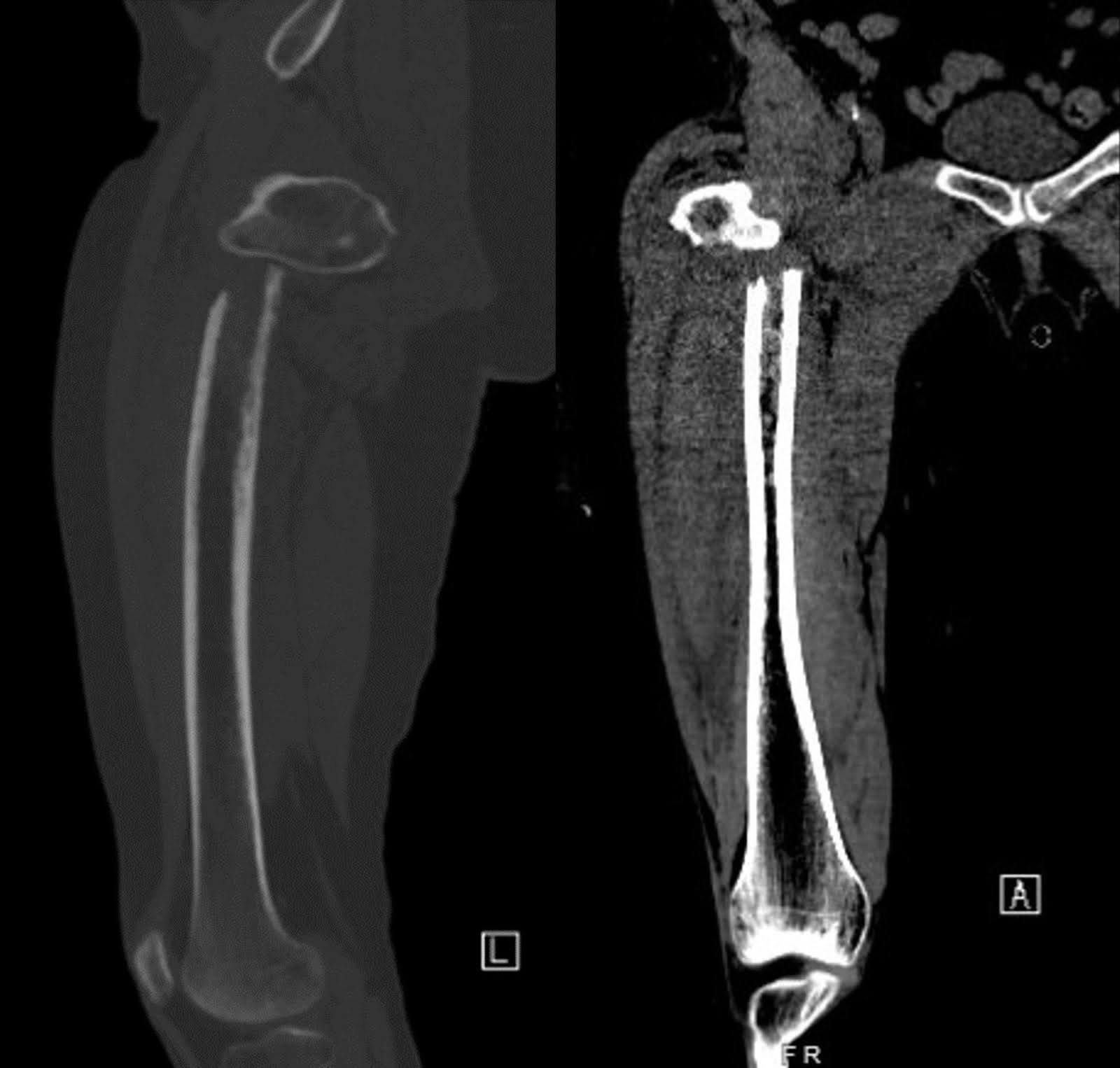 Figura 3. Imagens de tomografia computorizada lateral e AP sem contraste do fêmur direito mostram lucências intracorticais no meio do fêmur do fêmur, sugerindo uma possível fratura patológica.
Figura 3. Imagens de tomografia computorizada lateral e AP sem contraste do fêmur direito mostram lucências intracorticais no meio do fêmur do fêmur, sugerindo uma possível fratura patológica.
Fraturas patológicas, distintas das traumáticas, surgem como resultado de uma condição subjacente, incluindo, mas não se limitando a, osteoporose, câncer, infecção ou distúrbios metabólicos. Essa categoria distinta de fraturas é caracterizada pela influência de processos patológicos que comprometem a integridade estrutural do osso.1 Fraturas patológicas podem levar a morbidade significativa e declínio na qualidade de vida geral.2 O sistema esquelético é o terceiro local mais comum para metástases, atrás apenas do pulmão e do fígado.Cerca de 70% de todas as metástases ósseas ocorrem devido a cânceres de mama e próstata metastáticos, sendo tumores de pulmão, rim e tireoide as próximas causas mais comuns em termos de prevalência.4
Pacientes com fraturas patológicas podem apresentar dor e inchaço no local da fratura, além de dificuldade para andar, redução da amplitude de movimento, equimose, edema local e encurtamento perceptível das extremidades.5 Um indicador clínico de fraturas patológicas está em sua causa subjacente, frequentemente apresentando trauma mínimo — consideravelmente menos força do que a necessária para fraturar um osso saudável.6 Embora raras, fraturas patológicas podem ser o sinal apresentado de uma malignidade subjacente.7 Isso ressalta a necessidade de investigação meticulosa e escrutínio diagnóstico, especialmente em casos onde há histórico de trauma limitado ou ausente.
Uma fratura patológica do fêmur apresenta desafios semelhantes a uma fratura traumática do fêmur, mas introduz considerações pós-operatórias adicionais que impactam a seleção do implante. Semelhante ao manejo de fraturas de fêmur em ossos saudáveis, é fundamental alcançar a redução e estabilização das fraturas. Isso não apenas alivia a dor e proporciona estabilidade para a caminhada, mas também estabelece um ambiente biomecânico propício à cicatrização ideal de fraturas.
O manejo das fraturas subtrocantéricas apresenta desafios para alcançar a redução e a fixação, sendo que a redução frequentemente exige técnicas percutâneas ou abertas.8 A fixação cirúrgica, uma intervenção bem tolerada, demonstra resultados funcionais comparáveis à fixação não patológica.9 Do ponto de vista oncológico do tratamento, tratar as células malignas no osso é fundamental para uma cicatrização óssea eficaz. No regime de tratamento pós-fratura, a quimioterapia e a radioterapia desempenham papéis cruciais para alcançar esse objetivo. A radioterapia, normalmente planejada com terapia por feixe externo, exige uma tomografia computadorizada pré-tratamento para um planejamento preciso. No entanto, a presença de implantes metálicos pode causar dispersão do feixe, reduzindo a resolução de imagem e impactando os planos de radioterapia. Implantes de fibra de carbono, desprovidos das propriedades radiográficas dos metais, podem cumprir efetivamente os objetivos de redução e cicatrização de fraturas, ao mesmo tempo em que afetam minimamente as terapias adjuvantes essenciais para a radioterapia.10
O objetivo da fixação do osso longo após uma fratura é facilitar a cicatrização adequada, restaurar a estabilidade e promover a recuperação funcional. Ao considerar opções de tratamento para fraturas subtrocantéricas do fêmur, as principais modalidades de fixação incluem fixação por unha ou placa, com a literatura ortopédica atual favorecendo a fixação de unhas.8 Na seleção dos materiais para implantes, é fundamental considerar a etiologia subjacente da fratura e a proficiência do cirurgião em ambas as técnicas.
Para pacientes com fraturas patológicas secundárias a doença óssea metastática, os pregos de fibra de carbono podem ser uma alternativa preferível aos de titânio, devido à sua radiolucidez e propriedades mecânicas favoráveis.Implantes de fibra de carbono diminuem significativamente o espalhamento na tomografia computorizada e reduzem artefatos de suscetibilidade na ressonância magnética, o que permite visualização melhor da cicatrização óssea, vigilância pós-operatória para recorrência ou progressão local da doença e precisão no planejamento da radiação.10,13,14
Embora existam várias vantagens na fixação de fibra de carbono, não há diferenças nos resultados funcionais e nos perfis de complicações da fixação de fibra de carbono e metálica.11,12 Ambas as técnicas alcançam o objetivo de estabilização da fratura e manutenção da redução com baixo risco de complicações e cicatrização bem documentada e biocompatibilidade. Consequentemente, o cirurgião cirúrgico deve ponderar cuidadosamente sua proficiência e nível de conforto com cada método de fixação e tipo de implante no processo de tomada de decisão.12,15
Ao formular a estratégia de tratamento para uma fratura subtrocantérica patológica, é fundamental levar em conta tanto os objetivos de curto quanto de longo prazo. A curto prazo, utilizar um implante de fibra de carbono para fixação visa estabelecer estabilidade óssea após a redução da fratura. A redução da fratura restaura o comprimento dos membros, a tensão muscular e as relações anatômicas normais. Manter essa redução diminui a dor ao estabilizar adequadamente os fragmentos ósseos.16 Como dispositivo de compartilhamento de carga, o implante pode permitir que o paciente se mobilize imediatamente, reduzindo o risco de tromboembolismo venoso, úlceras e descondicionamento rápido.17
No período intermediário pós-operatório, a estabilidade proporcionada pelo implante desempenha um papel crucial na promoção da cicatrização das fraturas, especialmente quando combinada com terapia adjuvante para o tratamento do câncer.18 Optar por um implante de fibra de carbono não só simplifica o monitoramento radiográfico pós-operatório da doença, mas também aprimora a precisão do planejamento da radioterapia. Essa escolha estratégica contribui para a maior precisão e eficácia na abordagem geral do tratamento.19
Implantes de fibra de carbono podem ser contraindicados para tumores ósseos diáfisos humerais, que exigem ressecção segmentar grande com um segmento ósseo residual curto (5 cm) e um espaçador de cimento substancial. Tais implantes podem falhar por tensão devido a forças de flexão na porção distal da unha intramedular, onde há um descompasso de módulo de elasticidade entre o espaçador de cimento e o osso residual. Nesses cenários, as unhas intramedulares de titânio surgem como uma escolha preferível, oferecendo uma solução potencial para enfrentar os desafios associados aos implantes de fibra de carbono nesse contexto específico.20
Os cirurgiões precisam levar em conta sua familiaridade e nível de conforto com implantes de fibra de carbono, considerando a curva de aprendizado associada a esses implantes. Implantes de fibra de carbono têm sido associados a tempos cirúrgicos e de fluoroscopia mais longos, além de aumento da perda de sangue, especialmente em oncologia ortopédica e da coluna.12,21 Equilibrar considerações clínicas e proficiência do cirurgião é essencial ao decidir sobre a adequação dos implantes de fibra de carbono nessa área especializada.
A utilização de implantes de fibra de carbono em ortopedia exige uma consideração minuciosa de vários fatores clínicos cruciais. Apesar das complicações e taxas de falha comparáveis aos implantes de titânio, os implantes de fibra de carbono carecem de flexibilidade intraoperatória para flexão ou contorno. Os cirurgiões devem realizar um planejamento pré-operatório meticuloso para garantir um ajuste ideal.22 Embora a radiolucidez da fibra de carbono seja vantajosa para estudos de imagem pós-operatórios, confirmar a posição do implante durante a operação pode apresentar desafios. Pelo contrário, implantes metálicos, embora sem flexibilidade intraoperatória, frequentemente interrompem o planejamento da radiação e dificultam o cálculo e a entrega precisos da dose.23,24 Além disso, em situações em que a doença se estende à articulação e exige substituição, os implantes de fibra de carbono podem não ser a opção mais adequada. Portanto, a decisão de empregar implantes de fibra de carbono envolve uma avaliação detalhada de seus benefícios e limitações em contextos clínicos específicos.
Foi realizada uma haste intramedular do fêmur direito para fixação operatória da lesão, além de uma biópsia aberta para determinar a etiologia da doença óssea metastática. Segundo estudos de imagem, isso parecia ser um câncer primário de pulmão com metástase no osso. O paciente foi colocado em um decúbito lateral com a ajuda de um puff. Todas as proeminências ósseas eram adequadamente acolchoadas. Ocorreram a colocação de uma rolagem subaxilar e a liberação do nervo peroneal esquerdo.
Foi feita uma incisão lateral na coxa proximal e, posteriormente, foi realizada uma abordagem subvasto para expor o local da fratura. Um retrator Cobra facilitou a exposição após a identificação do local da fratura. Amostras permanentes e congeladas de patologia foram obtidas usando curettes. A patologia congelada confirmou adenocarcinoma pulmonar metastático. Foi realizado desbridamento agressivo da lesão tumoral, tanto dentro quanto externa do osso. Foi realizada uma irrigação abundante do campo cirúrgico com solução de peróxido.
Utilizando luvas novas e um novo conjunto de instrumentos, foi feita uma incisão subsequente próxima ao local inicial para acessar o fêmur proximal. A fáscia do glúteo médio foi incisa longitudinalmente para identificar a ponta da maior tuberosidade. Um fio-guia de 3,2 mm marcava o ponto de partida, garantindo uma excelente posição tanto na visão anteroposterior (AP) quanto lateral. Manter o fêmur em posição neutra era facilitado por um pino de Shantz, auxiliando na rotação interna e na aducção do fragmento femoral proximal.
O fragmento significativamente flexível passou por posicionamento adicional para garantir a extensão. Uma ferramenta de redução de dedos, apoiada por dois pinos Shantz no fêmur proximal e no eixo femoral, foi usada para alcançar a redução anatômica da fratura. Com a fratura reduzida, o aafetor de abertura foi usado para abrir a trajetória no fêmur proximal. Avançando um fio-guia com ponta esférica, mantivemos a redução e confirmamos a excelente posição do fio no fêmur distal. Foi medida uma prego de fibra de carbono de 360 mm com 11 mm de diâmetro. Alargamos sequencialmente até o tamanho 12,5 mm e inserimos suavemente usando um trocador de tubos para remover o fio guia da ponta da bola e inserir o liso. O prego femoral de fibra de carbono era inserido sobre o fio liso da forma tradicional, com o braço de mira posicionado anteriormente, girando externamente o braço de mira conforme o prego avançava. A haste é batida até sua posição final até que a parte superior da haste seja coberta pelo fêmur proximal.
Manipulando os tecidos moles, utilizamos a incisão da biópsia para inserir o triplo trochar pelo braço de mira. Depois, inserimos pelo fio-guia do fémur a trajetória no pescoço do fémur para o parafuso do quadril. Na fluoroscopia, a posição correta foi confirmada. Foi alcançado o reaming para um comprimento de 95 mm. O instrumento para o parafuso do quadril era fixado sem dificuldade, inicialmente batendo no caminho e depois inserindo o parafuso seguindo a trajetória marcada no pescoço do fémoral, e então fixando-o com o parafuso de ajuste.
Mantendo uma PA perfeita do quadril e joelho direitos, a porção distal do prego era fixada com dois parafusos de titânio de 5,0 mm medindo 40 e 40,5 mm de comprimento (Figura 4). As imagens finais confirmaram a redução bem-sucedida da fratura e o posicionamento ideal do hardware (Figura 5). Foi realizada uma irrigação abundante, seguida de fechamento camada por camada. Não houve complicações durante o caso. A duração do caso foi de 121 minutos, com uma perda de sangue estimada de 250 mL.
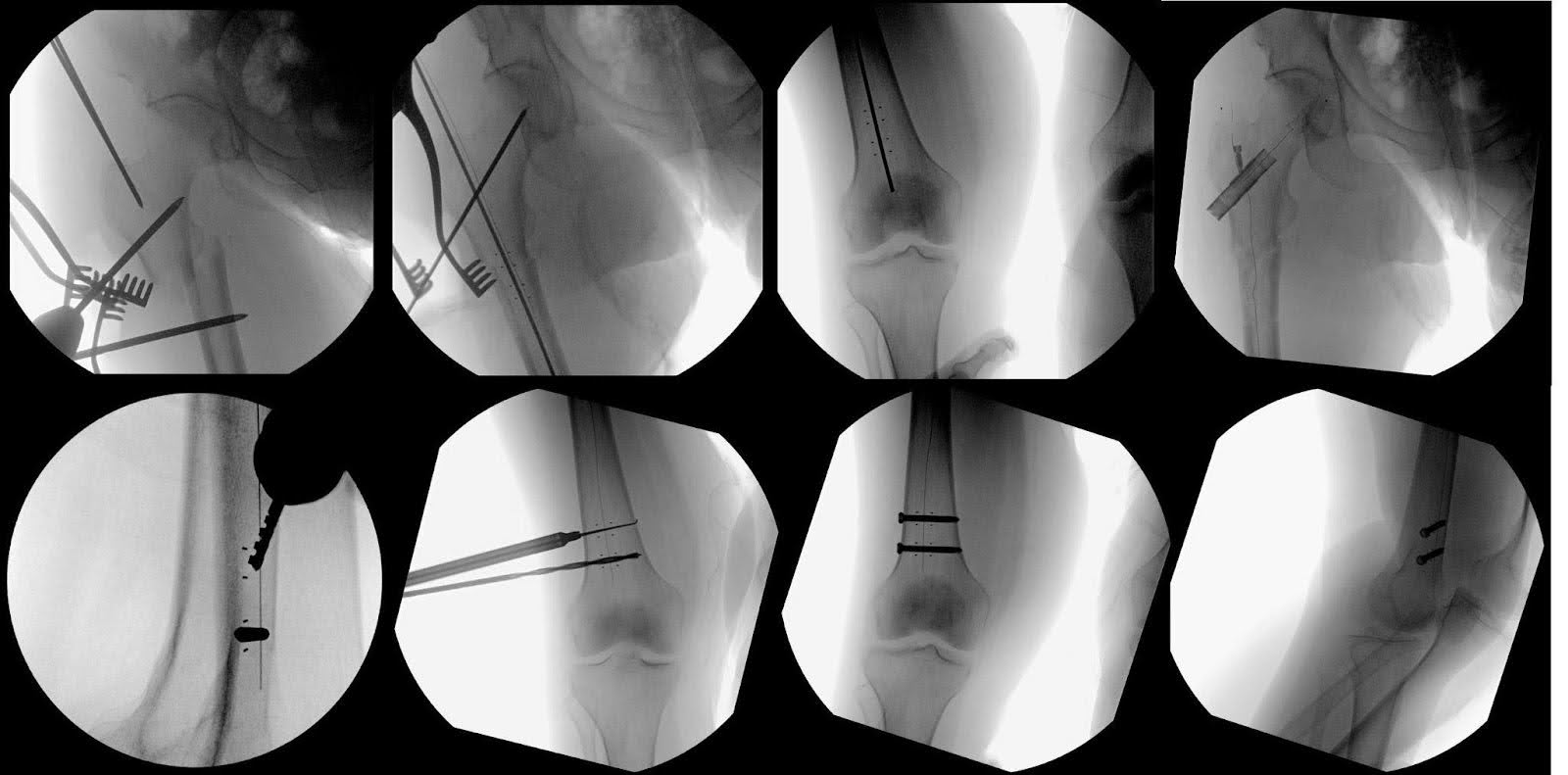
Figura 4. A fluoroscopia foi usada para demonstrar as diferentes etapas cirúrgicas envolvidas no tratamento da fratura do fêmur. Isso incluiu mostrar o ponto de partida e a redução da fratura usando pinos de Shandz. Imagens adicionais foram usadas para mostrar o prego de fibra de carbono, o parafuso de quadril de fibra de carbono e dois parafusos de encaixe de titânio usados para garantir a estabilidade do prego. Marcadores radioopacos auxiliavam na visualização dessas aberturas, observáveis tanto a partir de vistas AP quanto laterais. Vale destacar que as guias para esses furos de entrada diferem das circulares padrão normalmente visíveis em fluoroscopia para pregos de titânio.
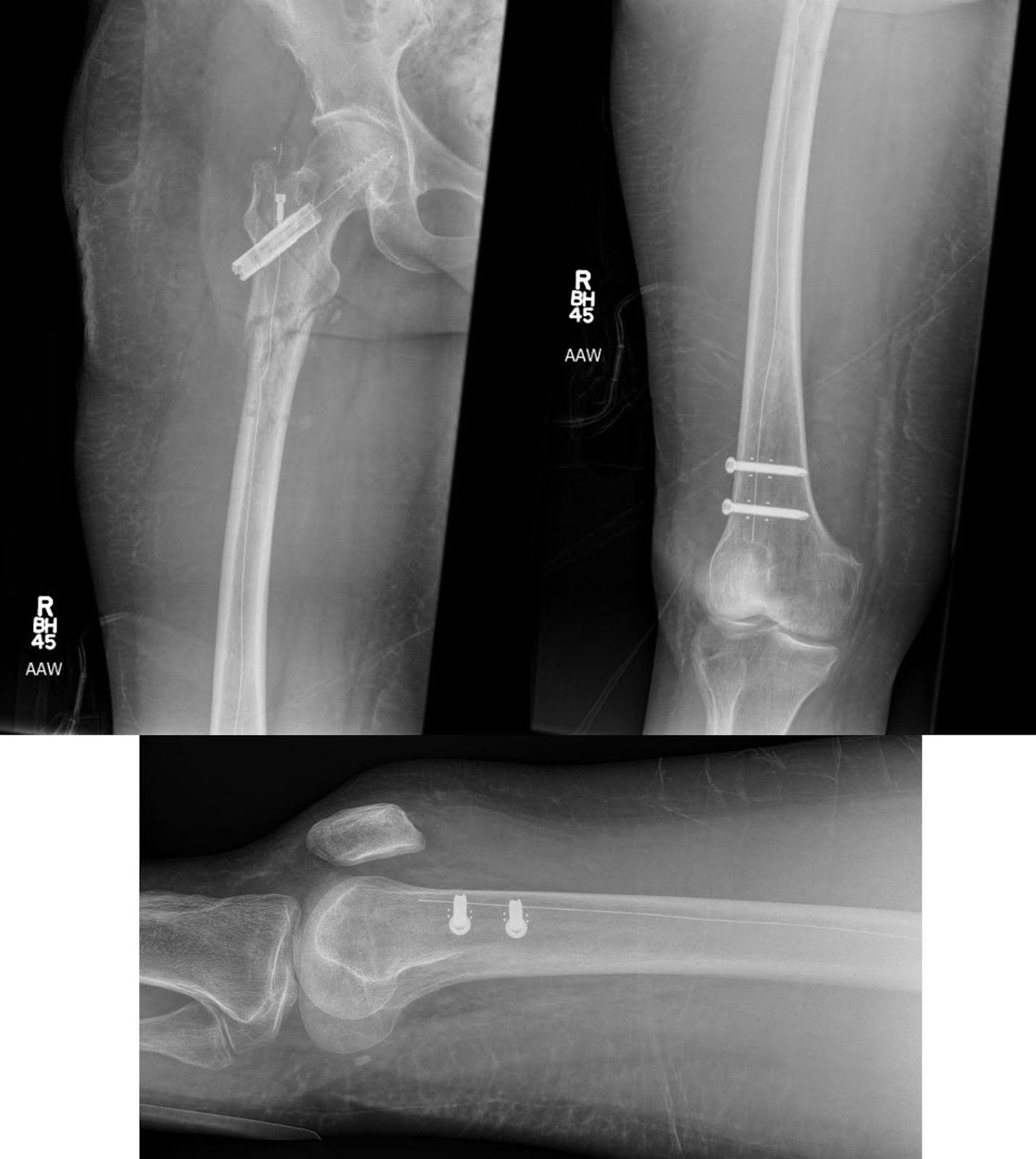
Figura 5. Um raio-x PA do fêmur e um raio-x lateral do joelho após a fixação intramedular da haste de fibra de carbono para fratura patológica subtrocantérica do fêmur direito mostram melhora do alinhamento sem sinais de complicações do hardware. A parte inferior da perna não revela lesões líticas suspeitas adicionais, e não há indicação de novas fraturas.
Foi realizada uma biópsia aberta do fêmur proximal direito além da fixação operária, e um espécime de 5,5x5,5x2,5 cm, composto por fragmentos de tecido mole rosa e avermelhado e empoeirados, foi enviado para avaliação histopatológica por um patologista ósseo e de tecidos moles treinado em fellowship. Uma imunocoloração para PD-L1 foi realizada em um bloqueio tecidular representativo e revelou >100 células tumorais disponíveis para pontuação. PD-L1 apresentou coloração membranosa de forte intensidade em >95% das células tumorais (escore de proporção tumoral, ou TPS, >95%).25 A imunohistoquímica mostrou células tumorais positivas para TTF-1 e Napsin-A e negativas para p40. Diante desses achados, o diagnóstico patológico final da lesão proximal do fêmur direito é carcinoma metastático compatível com carcinoma primário pulmonar.26–28
Um mês após a cirurgia, o paciente recebeu 20 Gy de radiação paliativa em cinco frações no quadril direito. No contexto da doença óssea metastática, a radioterapia mitiga a ativação dos osteoclastos, mata células tumorais e alivia a dor óssea ao produzir ossificação.29 Simultaneamente, a oncologia médica iniciou o tratamento do paciente com Capmatinib, uma terapia direcionada usada para tratar câncer de pulmão metastático não de pequenas células. No acompanhamento de dois meses, o paciente demonstrou melhora substancial, podendo andar sem andador. Seus joelhos estavam estáveis sob estresse valgo e varo em extensão total e flexão de 30°. Flexão do quadril, extensão, rotação interna e rotação externa estavam dentro dos limites normais. Seis semanas após iniciar o Capmatinib, o paciente estava respondendo bem ao tratamento. Uma tomografia do tórax mostrou diminuição da massa no lobo superior direito e diminuição da linfadenopatia mediastinal bilateral e hilar. Na consulta de acompanhamento mais recente, seu estado funcional não mostrou mudanças significativas nem alterações aparentes no hardware, e ela continua recebendo Capmatinib, passando por monitoramento radiográfico frequente (Figura 7).
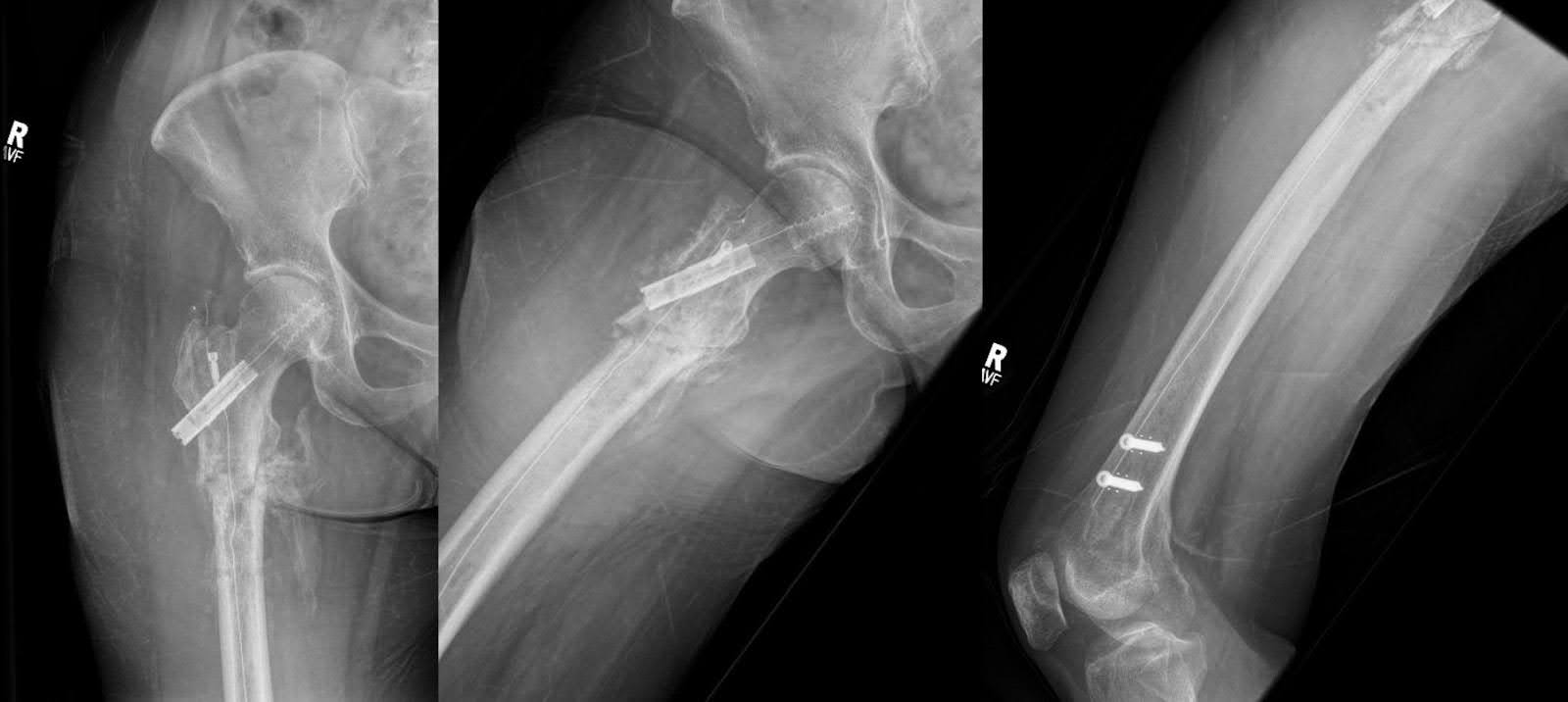
Figura 6. As radiografias AP e laterais do fêmur e uma radiografia lateral do joelho, dois meses após a fixação, mostram a formação de novos calos e pontes ósseas, mantendo o alinhamento original. Não há novas fraturas presentes, mas mudanças degenerativas leves foram observadas no quadril direito.
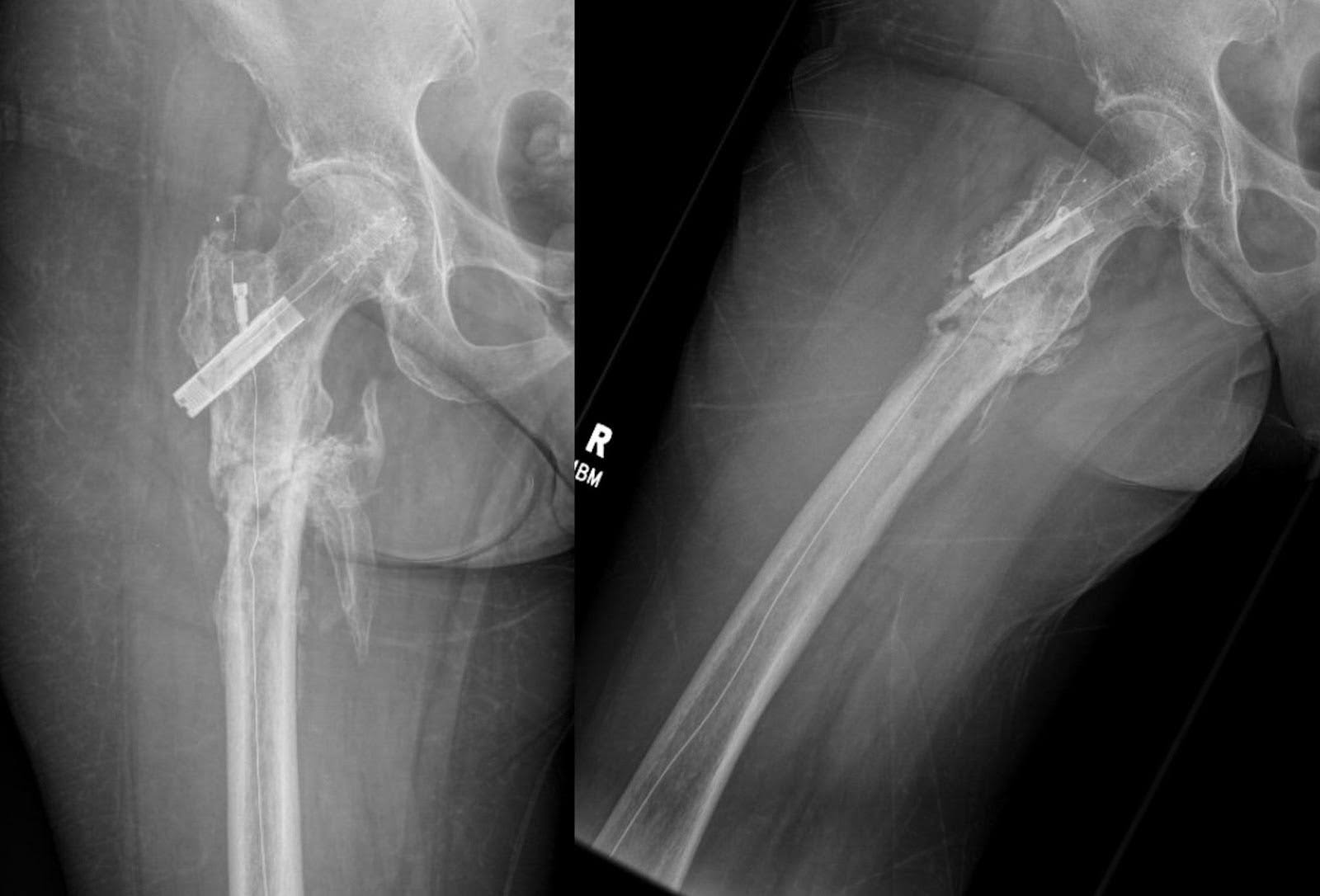
Figura 7. Seis meses após a fixação, os raios-x da AP e do fêmur lateral revelam formação contínua de calos e abundante ponte óssea, mantendo o alinhamento inicial. A fratura apresenta sinais de cicatrização incompleta, juntamente com a presença de formação óssea heterotópica. Não há complicações aparentemente no hardware ou indicações de novas fraturas. Além disso, alterações degenerativas análogas persistem no quadril direito.
A metástase desempenha um papel significativo na morbidade e mortalidade associadas ao câncer.30 O câncer de pulmão, o segundo carcinoma mais comum em homens e mulheres, respectivamente, apresenta preferência por metástase no cérebro, ossos e glândulas adrenais.31,32 A doença óssea metastática não apenas causa dor debilitante aos pacientes, mas também impõe um ônus financeiro substancial. A estimativa atual de 250.000 pacientes nos Estados Unidos lidando com essa condição se traduz em um custo anual de saúde de 12 bilhões de dólares.33,34 Avanços nos tratamentos, embora tenham melhorado as taxas de sobrevivência ao câncer, levaram consequentemente a uma maior incidência de doença óssea metastática. Fraturas patológicas decorrentes dessa condição decorrem de inúmeras lesões que atingem um tamanho que compromete a integridade estrutural do osso, culminando em fraturas.35 Para melhorar a sobrevivência e qualidade de vida do paciente a longo prazo, é fundamental priorizar estrategicamente modalidades de tratamento adequadas no manejo da doença.36
Como esse paciente não possuía diagnóstico oncológico antes da fratura do fêmur, é importante destacar os pontos-chave que podem ajudar a identificar lesões ósseas de risco antes da fratura. O paciente relatou vários meses de dor no quadril antes da fratura, que muitas vezes pode ser o primeiro achado clínico de qualquer carcinoma visceral. A análise de antecedentes e achados de exames físicos que revelam dor sem explicação, especialmente a dor funcional, devem ser investigados. O método mais adequado de avaliação é com radiografias simples de todo o osso na extremidade afetada, para garantir que a dor referida não seja um fator clínico que mascara.
Após o tratamento adequado da fratura e a sobrevivência imediata da fase pós-operatória, a atenção deve se voltar para o tratamento da doença subjacente, o que exige uma abordagem multidisciplinar envolvendo oncologia médica e radioterápia. A oncologia médica oferece tratamento sistêmico tanto para o câncer primário quanto para suas lesões metastáticas. A oncologia radioterápica desempenha um papel crítico no tratamento local durante o período pós-operatório subagudo, direcionando agressivamente as células cancerígenas disseminadas para facilitar o processo essencial de cicatrização óssea. Embora as séries de casos relatem uma menor taxa de progressão da doença após a estabilização da unha medular, o risco de falha do hardware aumenta com a sobrevivência do paciente.Implantes de fibra de carbono podem melhorar o monitoramento de doenças e a cicatrização óssea quando usados com técnicas avançadas de imagem.12 Estudos que investigam desfechos relatados pelos pacientes e a relação custo-benefício dos implantes de fibra de carbono em comparação com o titânio podem potencializar a adoção clínica.
Não é usado nenhum equipamento especial além do implante de fibra de carbono.
O autor correspondente é palestrante remunerado e consultor da CarboFix Orthopaedics Ltd.
O paciente referido neste artigo em vídeo deu seu consentimento informado para ser filmado e está ciente de que informações e imagens serão publicadas online.
Animação adicionada após a publicação em 03/10/2025. Nenhuma alteração foi feita no conteúdo do artigo.
References
- Haase SC. Tratamento de fraturas patológicas. Clino de mão. 2013; 29(4):579-584. DOI:10.1016/j.hcl.2013.08.010.
- Coleman RE. Características clínicas da doença óssea metastática e risco de morbidade esquelética. Clin Cancer Res. 2006; 12(20 Pt 2):6243s-6249s. DOI:10.1158/1078-0432.CCR-06-0931.
- Hage WD, Aboulafia AJ, Aboulafia DM. Incidência, localização e avaliação diagnóstica da doença óssea metastática. Orthop Clin Norte Am. 2000; 31(4):515-528, vii. DOI:10.1016/S0030-5898(05)70171-1.
- Christ AB, Piple AS, Gettleman BS, et al. Prevalência de tumores malignos primários, taxas de fratura patológica e mortalidade no contexto de doença óssea metastática. Osso Jt Aberto. 2023; 4(6):424-431. DOI:10.1302/2633-1462.46.BJO-2023-0042. R1.
- Johnson SK, Knobf MT. Intervenções cirúrgicas para pacientes com câncer com fraturas patológicas iminentes ou reais. Enfermagem Ortopédica. 2008; 27(3):160-171; questionário 172-173. DOI:10.1097/01.NOR.0000320543.90115.d5.
- De Mattos CBR, Binitie O, Dormans JP. Fraturas patológicas em crianças. Res. Articulação Óssea 2012; 1(10):272-280. DOI:10.1302/2046-3758.110.2000120.
- Kim LD, Bueno FT, Yonamine ES, Próspero JD de, Pozzan G. Metástase óssea como primeiro sintoma de tumores: papel de um estudo imuno-histoquímico no estabelecimento do tumor primário. Rev Bras Ortop (São Paulo). 2018; 53(4):467-471. DOI:10.1016/j.rboe.2018.05.015.
- Yoon RS, Donegan DJ, Liporace FA. Redução de fraturas subtrocantéricas do fêmur: dicas e truques, o que fazer e o que não fazer. J Trauma ortopédico. 2015; 29 Suppl 4:S28-33. DOI:10.1097/BOT.00000000000000287.
- Weiss RJ, Ekström W, Hansen BH, et al. Fraturas subtrocantéricas patológicas em 194 pacientes: uma comparação do resultado após o tratamento cirúrgico de fraturas patológicas e não patológicas. J Surg Oncol. 2013; 107(5):498-504. DOI:10.1002/jso.23277.
- Depauw N, Pursley J, Lozano-Calderon SA, Patel CG. Avaliação de implantes cirúrgicos de fibra de carbono e titânio para terapia de prótons e fótons. Pract Radiat Oncol. 2023; 13(3):256-262. DOI:10.1016/j.prro.2023.01.009.
- Lozano-Calderon SA, Rijs Z, Groot OQ, et al. Resultados de ossos longos tratados com hastes de fibra de carbono para indicações oncológicas: estudo multi-institucional internacional. J Am Acad Orthop Surg. 2024; 32(3):e134-e145. DOI:10.5435/JAAOS-D-22-01159.
- Yeung CM, Bhashyam AR, Groot OQ, et al. Comparação de hastes intramedulares de fibra de carbono e titânio em oncologia ortopédica. Osso Jt Aberto. 2022; 3(8):648-655. DOI:10.1302/2633-1462.38.BJO-2022-0092. R1.
- Ernstberger T, Heidrich G, Bruening T, Krefft S, Buchhorn G, Klinger HM. A relevância validada interobservador dos materiais espaçadores intervertebrais nos artefatos de ressonância magnética. Coluna Vertebral Eur, J., 2007; 16(2):179-185. DOI:10.1007/S00586-006-0064-5.
- Alvarez-Breckenridge C, de Almeida R, Haider A, et al. Implantes espinhais de polieteretercetona reforçados com fibra de carbono para tratamento de tumores espinhais: vantagens e limitações percebidas. Neuroespinha. 2023; 20(1):317-326. DOI:10.14245/ns.2244920.460.
- Clunk MJ, Gonzalez MR, Denwood HM, et al. Um PEEK em fibra de carbono: um guia prático para implantes poliméricos compósitos de alto desempenho para oncologia ortopédica. J Orthop. 2023;45:13-18. DOI:10.1016/j.jor.2023.09.011.
- Manglani HH, Marco RA, Picciolo A, Healey JH. Emergências ortopédicas em pacientes com câncer. Semin Oncol. 2000; 27(3):299-310.
- Booth K, Rivet J, Flici R, et al. Protocolo de mobilidade progressiva reduz a taxa de tromboembolismo venoso em pacientes de terapia intensiva com trauma: um projeto de melhoria da qualidade. J Enfermagem de Trauma. 2016; 23(5):284-289. DOI:10.1097/JTN.00000000000000234.
- Colyer RA. Estabilização cirúrgica de fraturas neoplásicas patológicas. Curr Probl Câncer. 1986; 10(3):117-168. DOI:10.1016/S0147-0272(86)80005-8.
- Xin-ye N, Xiao-bin T, Chang-ran G, Da C. A perspectiva de implantes de fibra de carbono na radioterapia. J Appl Clin Med Phys. 2012; 13(4):3821. DOI:10.1120/jacmp.v13i4.3821.
- Bhashyam AR, Yeung C, Sodhi A, et al. Haste intramedular reforçada com fibra de carbono vs. titânio para tumores ósseos do úmero. J Cirurgia de cotovelo de ombro. 2023; 32(11):2286-2295. DOI:10.1016/j.jse.2023.04.023.
- Cofano F, Di Perna G, Monticelli M, et al. Implantes reforçados com fibra de carbono vs implantes de titânio para fixação em metástases espinhais: um estudo clínico comparativo sobre segurança e eficácia da nova "estratégia de carbono". J Clin Neurosci. 2020;75:106-111. DOI:10.1016/j.jocn.2020.03.013.
- Yeung CM, Bhashyam AR, Patel SS, Ortiz-Cruz E, Lozano-Calderón SA. Implantes de fibra de carbono em oncologia ortopédica. J Clin Med. 2022; 11(17). DOI:10.3390/jcm11174959.
- Tedesco G, Gasbarrini A, Bandiera S, Ghermandi R, Boriani S. Os implantes compostos de PEEK/fibra de carbono podem aumentar a eficácia da radioterapia no tratamento de tumores da coluna. J Cirurgia da Coluna. 2017; 3(3):323-329. DOI:10.21037/jss.2017.06.20.
- Nevelsky A, Borzov E, Daniel S, Bar-Deroma R. Efeitos de perturbação dos parafusos PEEK de fibra de carbono na distribuição da dose de radioterapia. J Appl Clin Med Phys. 2017; 18(2):62-68. DOI:10.1002/ACM2.12046.
- Keppens C, Dequeker EM, Pauwels P, Ryska A, 't Hart N, von der Thüsen JH. Imuno-histoquímica PD-L1 no câncer de pulmão de células não pequenas: desvendando diferenças na concordância e interpretação da coloração. Arco de Virchows 2021; 478(5):827-839. DOI:10.1007/S00428-020-02976-5.
- Yatabe Y, Mitsudomi T, Takahashi T. TTF-1 expressão em adenocarcinomas pulmonares. Am J Surg Pathol. 2002; 26(6):767-773. DOI:10.1097/00000478-200206000-00010.
- Zhang P, Han YP, Huang L, Li Q, Ma DL. Valor da napsina A e do fator de transcrição da tireoide-1 na identificação do adenocarcinoma primário de pulmão. Oncol Lett. 2010; 1(5):899-903. DOI:10.3892/ol_00000160.
- Affandi KA, Tizen NMS, Mustangin M, Zin RRMRM. A imuno-histoquímica p40 é um excelente marcador no carcinoma primário de células escamosas do pulmão. J Pathol Transl Med. 2018; 52(5):283-289. DOI:10.4132/jptm.2018.08.14.
- De Felice F, Piccioli A, Musio D, Tombolini V. O papel da radioterapia no tratamento de metástases ósseas. Oncotarget. 2017; 8(15):25691-25699. DOI:10.18632/oncotarget.14823.
- Nooh A, Goulding K, Isler MH, et al. Melhora precoce da dor e do resultado funcional, mas não da qualidade de vida após a cirurgia para doença metastática dos ossos longos. Clin Orthop Relat Res. 2018; 476(3):535-545. DOI:10.1007/S11999.00000000000000065.
- Siegel RL, Miller KD, Wagle NS, Jemal A. Estatísticas do câncer, 2023. CA Câncer J Clin. 2023; 73(1):17-48. DOI:10.3322/caac.21763.
- Popper HH. Progressão e metástase do câncer de pulmão. Metástase de Câncer Rev. 2016; 35(1):75-91. DOI:10.1007/s10555-016-9618-0.
- Guy GP, Ekwueme DU, Yabroff KR, et al. Carga econômica da sobrevivência ao câncer entre adultos nos Estados Unidos. J Clin Oncol. 2013; 31(30):3749-3757. DOI:10.1200/JCO.2013.49.1241.
- Li S, Peng Y, Weinhandl ED, et al. Número estimado de casos prevalentes de doença óssea metastática na população adulta dos EUA. Clin Epidemiol. 2012;4:87-93. DOI:10.2147/CLEP. S28339.
- Em branco AT, Lerman DM, Patel NM, Rapp TB. A intervenção profilática é mais custo-efetiva do que o tratamento de fraturas patológicas na doença óssea metastática? Clin Orthop Relat Res. 2016; 474(7):1563-1570. DOI:10.1007/s11999-016-4739-x.
- Gutowski CJ, Zmistowski B, Fabbri N, Boland PJ, Healey JH. O uso de agentes biológicos em pacientes com câncer renal e de pulmão deve afetar nosso manejo cirúrgico das metástases femorais? Clin Orthop Relat Res. 2019; 477(4):707-714. DOI:10.1097/CORR.00000000000000434.
- Miller BJ, Soni EEC, Gibbs CP, Scarborough MT. Ortopedia. 2011; 34(4). DOI:10.3928/01477447-20110228-12.
- Arpornsuksant P, Morris CD, Forsberg JA, Levin AS. Quais fatores estão associados à progressão da lesão metastática local após a estabilização da haste intramedular? Clin Orthop Relat Res. 2022; 480(5):932-945. DOI:10.1097/CORR.00000000000002104.
Cite this article
Rizk PA, Werenski JO, Lozano-Calderon SA. Implante de fibra de carbono para fixação de uma fratura subtrocantérica patológica. J Med Insight. 2024; 2024(443). DOI:10.24296/jomi/443.



