Timectomia robotica per miastenia grave
Main Text
Table of Contents
La miastenia grave è una malattia autoimmune che colpisce la trasmissione dell'acetilcolina coinvolta nella contrazione del muscolo scheletrico. L'approccio ai pazienti miastenici è complesso in quanto il trattamento ottimale prevede una tecnica multidisciplinare di terapie mediche e chirurgiche combinate. La terapia medica con acetilcolinesterasi e immunomodulatori può fornire sollievo dai sintomi ed eliminare la sensazione di affaticamento e debolezza. La timectomia chirurgica può aiutare a ridurre i sintomi, prevenire le recidive e ridurre il fabbisogno giornaliero di farmaci. La timectomia è stata tradizionalmente eseguita tramite un approccio transsternale, ma le tecniche minimamente invasive e robotiche sono diventate sempre più comuni. Qui, presentiamo il nostro approccio per la timectomia totale robotica attraverso un approccio sinistro.
La miastenia grave è una malattia autoimmune che colpisce i recettori nicotinici postsinaptici dell'acetilcolina che controllano la funzione volontaria del muscolo scheletrico. Questo è comunemente mediato dagli anticorpi anti-recettore dell'acetilcolina (anti-AChR). L'insorgenza e l'entità della malattia possono variare in modo significativo, ma di solito comportano un certo grado di debolezza progressiva degli occhi, delle estremità o dei muscoli orofaringei/respiratori. 1 In combinazione con la terapia medica, la chirurgia è diventata lo standard di cura poiché i pazienti post-timectomia hanno maggiori probabilità di avere un miglioramento e/o una risoluzione dei sintomi con meno dipendenza dalla terapia medica. 2, 3
La paziente è una donna di 23 anni a cui è stata diagnosticata la miastenia grave generalizzata anti-AChR positiva diversi anni fa. Il suo disturbo principale era affaticamento, debolezza facciale e visione doppia. È stata mantenuta con prednisone e piridostigmina al giorno, ma ha avuto un progressivo peggioramento dei sintomi. Ora ha bisogno di dosi crescenti di corticosteroidi e infusioni endovenose di immunoglobuline per il controllo dei sintomi. Per il resto è sana e non ha una storia medica o chirurgica passata pertinente. Non ha una storia familiare di miastenia grave o altre malattie autoimmuni.
L'esame fisico ha rivelato una giovane donna dall'aspetto sano con segni vitali normali. Non ha deficit sensoriali, i riflessi tendinei sono tutti normali e non c'è debolezza degli arti superiori o inferiori da sforzo. Ha una lieve ptosi che viene suscitata quando si tiene lo sguardo verso l'alto per circa un minuto.
Il paziente è stato sottoposto a tomografia computerizzata trasversale del torace che ha mostrato iperplasia timica senza timoma dominante. Non c'era linfoadenopatia associata o invasione delle strutture circostanti. Un'immagine rappresentativa è mostrata nella Figura 1.
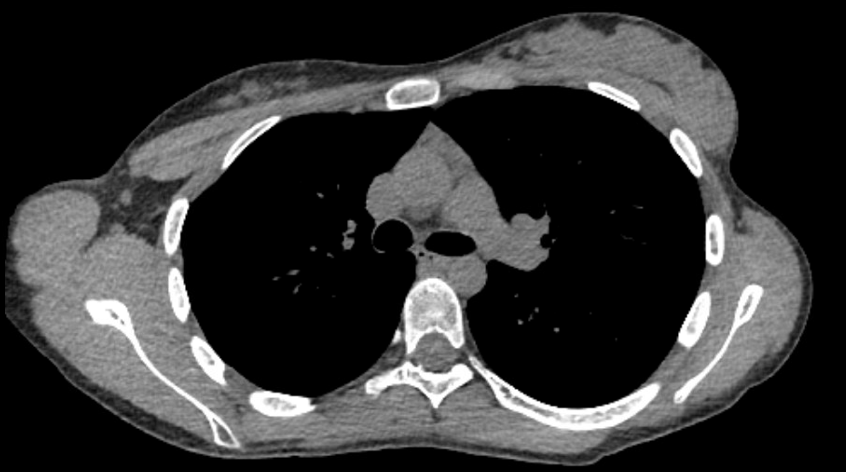 Figura 1. Sezione trasversale rappresentativa della tomografia computerizzata assiale che mostra iperplasia timica senza timoma dominante.
Figura 1. Sezione trasversale rappresentativa della tomografia computerizzata assiale che mostra iperplasia timica senza timoma dominante.
Il trattamento della miastenia grave è tipicamente multidisciplinare e richiede la cooperazione tra neurologi e chirurghi toracici. Dopo la diagnosi, i pazienti di solito vengono sottoposti a una combinazione di terapie mediche, tra cui acetilcolinesterasi come la piridostigmina, muscarinici come la propantelina e immunomodulatori come corticosteroidi, metotrexato o ciclofosfamide. L'infusione di immunoglobuline per via endovenosa (IVIG) può essere necessaria per la malattia refrattaria. 1
Una volta controllata con un regime stabile, la maggior parte dei pazienti viene indirizzata alla timectomia chirurgica, che ha dimostrato di ridurre la dipendenza dalle terapie mediche e di ridurre i sintomi riportati.
Il nostro video mostra una timectomia totale robotica tramite un approccio toracico sinistro. Utilizzando tecniche toracoscopiche o robotiche, le timectomie minimamente invasive vengono sempre più eseguite utilizzando approcci subxifoideo, sinistro, destro o bilaterale. Raramente, un approccio transsternale può essere necessario per i tumori di grandi dimensioni o quelli con una componente invasiva. 4-6
Il nostro paziente aveva precedentemente controllato la miastenia che ora ha richiesto un'escalation delle terapie mediche. Si pensava che la timectomia potesse permetterle di svezzarsi dal suo attuale farmaco senza recidiva dei sintomi.
I pazienti affetti da miastenia grave devono essere ottimizzati prima di sottoporsi a timectomia chirurgica. Dopo l'intervento chirurgico, i pazienti non ottimizzati possono manifestare una "crisi miastenica", che si presenta con profonda debolezza, insufficienza respiratoria e incapacità di svezzarsi dal ventilatore. Per evitare ciò, abbiamo pianificato il nostro intervento una settimana dopo la sua ultima infusione di IVIG e le abbiamo anche somministrato dosi intraoperatorie di steroidi. Inoltre, sono state utilizzate tecniche di anestesia specializzate, tra cui l'evitamento di paralitici e l'anestesia endovenosa totale, per evitare potenziali complicanze miasteniche postoperatorie.
Qui presentiamo una timectomia totale robotica tramite approccio toracico sinistro. Questa procedura prevede la rimozione dell'intero timo e del grasso pericardico associato. I bordi per questa resezione includono i nervi frenici sinistro e destro lateralmente, lo sterno anteriormente, il pericardio posteriormente, il diaframma inferiormente e le corna superiori del timo superiormente. Tutto il tessuto adiposo all'interno di questi confini viene resecato facendo attenzione a non danneggiare le importanti strutture vicine, tra cui la vena innominata, il cuore, l'aorta e i nervi frenici bilaterali.
Il paziente è posizionato supino con una protuberanza sotto il lato operatorio. Ciò consente l'esposizione completa del torace sinistro mentre si lascia cadere la spalla fuori dal campo per evitare collisioni robotiche. L'ingresso avviene nel torace in corrispondenza della linea ascellare anteriore nel 4° spazio intercostale con un trocar robotico da 8 mm. Due trocar robotici da 8 mm vengono quindi posizionati sotto visualizzazione diretta, uno nella linea medioclavicolare nella piega sottomammaria e un altro nella linea ascellare posteriore nel terzo spazio intercostale. Infine, una porta assistente da 12 mm è triangolata tra le due porte inferiori nel 5° o 6° spazio intercostale. Una volta posizionate tutte le porte di lavoro, il robot viene agganciato. La telecamera è posizionata nella porta robotica centrale tra le due porte di lavoro. Sebbene ci siano molte opzioni disponibili, i nostri strumenti preferiti includono una pinza Cadiere nella mano sinistra e una lunga pinza bipolare nella mano destra.
La dissezione viene iniziata il più inferiormente possibile appena medialmente al nervo frenico. Il tessuto adiposo del mediastino viene mobilizzato dal diaframma sottostante e dal pericardio in modo caudale-cefalico. Utilizzando una combinazione di dissezione smussa ed elettrocauterizzazione, la mobilizzazione continua medialmente e superiormente fino a quando non si incontra la vena innominata. Quest'area viene affrontata con meticolosa cautela e qualsiasi vena drenante verso l'innominato viene controllata con cauterio o clip chirurgiche. Le corna superiori destra e sinistra del timo sono retratte verso il basso e sezionate liberamente. Infine, la dissezione viene effettuata nel torace destro. La pleura mediastinica destra può essere aperta per consentire l'identificazione del nervo frenico destro.
Una volta che il timo e il grasso mediastinico sono completamente mobilizzati, il campione viene estratto utilizzando una sacca di recupero dalla porta dell'assistente. Un singolo drenaggio Blake viene utilizzato per il drenaggio toracico e posizionato attraverso una delle incisioni robotiche della porta. Il robot viene sganciato e il resto delle porte viene rimosso e chiuso con suture sottocuticolari.
Dopo l'intervento, il drenaggio pleurico è stato monitorato ed è stato entro i limiti normali. Il drenaggio di Blake è stato rimosso la mattina seguente e il paziente è stato dimesso il primo giorno postoperatorio. La patologia finale era coerente con l'iperplasia timica. Al follow-up di 9 mesi, il paziente è per lo più privo di sintomi, ad eccezione di una lieve diplopia presente solo con estrema stanchezza. È stata svezzata a basse dosi di prednisone e non necessita più di infusioni di IVIG.
- Constantine Poulos, MD: scrittura, revisione e editing
- Tong-Yan Chen, MD: produzione, scrittura, revisione e montaggio video
- Lana Schumacher, MD: produzione, scrittura, revisione e montaggio video
Tutti gli autori hanno dichiarato che non ci sono conflitti di interesse.
Il paziente a cui si fa riferimento in questo video articolo ha dato il proprio consenso informato ad essere filmato ed è consapevole che le informazioni e le immagini saranno pubblicate online.
Animazione aggiunta dopo la pubblicazione il 10/03/2025. Non sono state apportate modifiche al contenuto dell'articolo.
References
- Vincent A, Palace J, Hilton-Jones D. Miastenia gravis. Lancetta. 2001; 357(9274):2122-2128. DOI:10.1016/S0140-6736(00)05186-2.
- Gronseth GS, Barohn R, Narayanaswami P. Practice advisory: timectomia per miastenia gravis (aggiornamento dei parametri pratici): rapporto del sottocomitato per lo sviluppo, la diffusione e l'implementazione delle linee guida dell'American Academy of Neurology. Neurologia. 2020; 94(16):705-709. DOI:10.1212/WNL.00000000000009294.
- Wolfe GI, Kaminski HJ, Aban IB, et al. Studio randomizzato di timectomia nella miastenia grave. N Engl J Med. 2016; 375(6):511-522. DOI:10.1056/NEJMoa1602489.
- Marulli G, Comacchio GM, Rea F. Timoctomia robotica. J Vis Surg. 2017;3:68. DOI:10.21037/jovs.2017.05.01.
- Wei B, Cerfolio R. Timectomia robotica. J Vis Surg. 2016;2:136. DOI:10.21037/jovs.2016.07.17.
- Holleran TJ, Napolitano MA, Crowder HR, Sparks AD, Antevil JL, Trachiotis GD. Risultati clinici e approccio tecnico della timectomia nell'amministrazione sanitaria dei veterani. Ann Thorac Surg. 2022; 113(5):1648-1655. DOI:10.1016/j.athoracsur.2021.05.020.
Cite this article
Poulos CM, Chen TY, Schumacher L. Timectomia robotica per miastenia grave. J Med Insight. 2024; 2024(426). DOI:10.24296/jomi/426.



