Derivação toracofemoral: uma abordagem retroperitoneal
Main Text
Table of Contents
A intervenção cirúrgica para a doença oclusiva aortoilíaca (DAIA) continua sendo uma ferramenta vital no manejo da DAIA. A AIOD é causada pela oclusão das artérias infrarrenal e/ou ilíaca, frequentemente secundária à aterosclerose. Aqui, apresentamos o caso de um paciente jovem do sexo masculino com histórico de hiperlipidemia familiar e uso crônico de tabaco que passou por um procedimento de bypass tohoracofemoral (TFB) via abordagem retroperitoneal. Apresentou sintomas clássicos de dor bilateral nas pernas ao caminhar, dor noturna nos membros inferiores e pulsos correlacionados na diminuição dos membros. A TFB foi a abordagem preferida devido à carga agressiva e mole da placa que se estende até a aorta suprarrenal, o que impedia a reparação endovascular e teria maior risco de bypass padrão infrarrenal aortofemoral (AFB). Este vídeo e o relato do caso apresentam uma explicação detalhada de uma abordagem retroperitoneal para um procedimento TFB e as indicações sutis das intervenções cirúrgicas para AIOD. 1,2
A doença oclusiva aortoilíaca (DAIA) é uma manifestação complexa da doença arterial periférica (DAP), na qual o lúmen da aorta infrarrenal e/ou as artérias ilíacas são obliterados secundariamente devido à aterosclerose (frequentemente uma mistura de placas calcificadas e ricas em lipídios). A DAP sintomática pode ser causada por placas ateroscleróticas primárias estreitando o lúmen e limitando o fluxo, ou por obstrução secundária das complicações embolicas dessas placas. 1,2 A AIOD frequentemente apresenta sintomas que evoluem da claudicação nas nádegas/coxas, para dor em repouso nos membros inferiores e, na forma mais grave, para ulceração isquêmica. A descrição clássica para a apresentação da AIOD foi feita por Leriche, com sua síndrome homônima consistindo em claudicação nádega/coxa, ausência de pulsos femorais e disfunção erétil. 1,2 Ao apresentar embolização distal concomitante ou oclusão infrainguinal, a AIOD pode resultar em isquemia crônica ameaçadora de membros (CLTI), que apresenta um prognóstico ruim. 3
Os fatores de risco mais significativos para aterosclerose e, consequentemente, para a AIOD, são o consumo de tabaco e o diabetes mellitus. 1 A hiperlipidemia, que pode ser induzida pelo estilo de vida ou devido à hiperlipidemia familiar de início precoce, também contribui para o desenvolvimento da AIOD. Outros fatores de risco incluem aumento da idade, histórico familiar, sexo masculino e raça. 4,5
A prevalência de AIOD na população geral varia de 3,56% a mais de 14%. 4,6 Estudos mostraram uma prevalência maior na faixa etária de 70 a 80 anos, de 14% a 23%. 8,9 À medida que a população continua envelhecendo e as taxas de diabetes e doenças cardiovasculares aumentam, haverá potencial para uma maior carga de AIOD. Portanto, é importante identificar pacientes em risco único para obter intervenção precoce.
O exame deve ser iniciado com um Índice Tornozelo-Braquial (ABI). 10-12 Suspeita clínica para AIOD deve ser alta, com um ABI anormal e exame de pulso femoral ausente/anormal. No paciente sintomático, a avaliação deve prosseguir com uma arteriograma por tomografia computadorizada (CTA) para delimitar a natureza da doença e estabelecer a estratificação adequada do risco para a intervenção. No entanto, ainda existem alguns pacientes sintomáticos que podem ser tratados inicialmente por medidas conservadoras, como programas de caminhada e cilostazol. Esses pacientes não precisam passar por CTA, pois seria radiação indesejada e exposição a meios de contraste. 13,14
Independentemente da estratégia de intervenção, todos os pacientes precisam de um manejo médico ideal das doenças crônicas, incluindo avaliação para administração de estatinas e antiplaquetarias, adoção de um regime de exercícios e cessação do tabagismo. 11,15,16 Para aqueles em quem a intervenção é necessária, a terapia endovascular é frequentemente a primeira linha de tratamento, com bypass cirúrgico reservado para aqueles com aneurisma concomitante ou carga doença mais extensa.
O paciente é um homem de 52 anos com histórico médico de hiperlipidemia familiar de início precoce e uso anterior de tabaco (50 maços-ano) que inicialmente apresentou um enxerto de bypass da artéria coronariana (CABG) secundário a um infarto agudo do miocárdio. Durante a avaliação clínica para a CABG, foi constatado que ele apresentava uma oclusão aórtica infrarrenal. Após passar por uma CABG bem-sucedida e reabilitação cardíaca, ele foi avaliado em uma clínica vascular. O paciente relatou sucesso na cessação do tabagismo após o CABG, mas ainda endossa claudicação de curta distância com dor de cólica nas coxas/glúteos/panturrilhas bilaterais a 50 jardas. Além disso, ele tinha um histórico pessoal significativo de hiperlipidemia e histórico familiar de vários parentes de primeiro grau com eventos cardiovasculares índice abaixo dos 50 anos. Ele parecia saudável, sem feridas isquêmicas, mas ausente de pulsos femorais/poplíteos e pedal.
A CTA demonstrou uma oclusão aórtica completa no nível das artérias renais bilaterais a partir de uma combinação de placa aterosclerótica calcificada e mole. Significativamente, neste caso, o ateroma se estendeu proximalmente até o nível da artéria mesentérica superior (AME), como visto na Figura 1, o que teria complicado o clampamento suprarrenal e comprometido o fluxo apropriado para o bypass aortofemoral padrão (AFB). A aorta supracelíaca estava livre de doença arterial (Figura 2). A oclusão se estendeu às artérias femorais comuns bilaterais, onde o fluxo foi reconstituído a partir das arteriais colaterais ilíacas epigástricas e circunflexas. As artérias femurais comuns bilaterais (CFA) apresentavam placas ateromatosas com aproximadamente 60% de estenose, e o escoamento estava intacto abaixo da bifurcação da CFA.
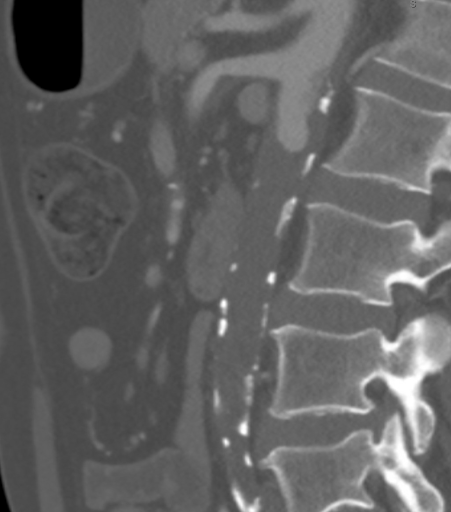
Figura 1. CTA mostrou que o ateroma se estendia proximalmente até o nível da artéria mesentérica superior (SMA), o que teria complicado o clampamento suprarrenal e comprometido o fluxo apropriado para a AFB padrão.
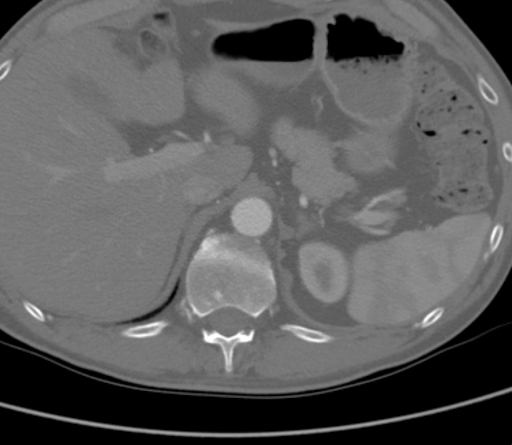
Figura 2. CTA mostrou que a aorta supracelíaca estava livre de doença arterial.
Como em qualquer paciente com claudicação, a primeira opção de tratamento é conservadora, com terapia médica ideal e cessação do tabagismo. No entanto, a durabilidade dos procedimentos de inflow, combinada com baixa morbidade e mortalidade em pacientes selecionados adequadamente, torna a intervenção adequada para pacientes como aqueles que permanecem sintomáticos apesar das medidas conservadoras. O Consenso Inter-Sociedade para o Manejo da Doença Arterial Periférica (TASC II)17 é um excelente guia para descrever as diversas opções de tratamento e a justificativa para a escolha adequada com base na anatomia do paciente e nas comorbidades. Em geral, para pacientes como este, com oclusão aórtica alimpa e oclusão ilíaca externa que exigirá endoarterectomia CFA, a abordagem cirúrgica aberta é o manejo preferido. O bypass cirúrgico aberto da aorta infrarrenal para a endoarterectomia bilateral CFA +/- CFA é a reconstrução mais comum para AOID grave, com uma permeabilidade de 10 anos relatada de até 90%. No entanto , certas restrições anatômicas, como a carga da doença no local de clampagem proximal ou a falha da AFB prévia, podem limitar a abordagem padrão, caso em que um bypass para a CFA bilateral usando a aorta torácica descendente como entrada é uma abordagem viável. A permeabilidade aos 5 anos é maior que 80% quando realizada por toracotomia ou abordagem retroperitoneal na aorta torácica distal descendente. 18 Em um paciente com comorbidades médicas graves que impedem a operação em nível aórtico, o bypass axilo-bifemoral com endarterectomia da CFA concomitante seria outra opção viável, embora com uma permeabilidade esperada de apenas ~50% aos 5 anos.
Esse paciente é jovem e em forma após cessar de fumar e uma revascularização coronariana bem-sucedida. Ele permaneceu sintomático e, dada sua idade, ainda desejava uma distância maior a pé para facilitar o emprego, o estilo de vida diário e a maior capacidade de exercícios para uma saúde a longo prazo.
A decisão de usar um sítio alternativo de entrada aórtica na aorta torácica descendente foi tomada principalmente como resultado secundário ao ateroma mole dentro de um local típico de clampagem justtarenal, o que teria comprometido a anastomose aórtica proximal padrão. Além disso, decidiu-se usar uma abordagem retroperitoneal em vez de toracotomia esquerda, pois isso permitiria uma avaliação dúplex intraoperatória dos vasos viscerais e renais para garantir um fluxo adequado e realizar bypass visceral concomitante, se necessário. Além disso, dado seu jovem, poderíamos deixar o local de entrada da cavidade torácica para futuras revascularizações, se necessário.
Os passos de um bypass tohoracofemoral (TFB) devem ser familiares para a maioria dos cirurgiões vasculares, pois imitam muitos dos mesmos sequenciamentos de uma AFB padrão, só que com um local alternativo de entrada. O paciente é posicionado em um decúbito lateral direito modificado, com os quadris o mais próximos possível de planos para permitir acesso femoral adequado para realizar a endarterectomia quando indicada, como neste paciente. A operação deve começar com as exposições da virilha através de incisões oblíquas para limitar o tempo total de abertura do retroperitônio (RP) e diminuir as perdas insensíveis. Quando se espera uma endarterectomia femoral concomitante, é crucial controlar a artéria femoral superficial (SFA) e a profunda femoral (PA) até as zonas livres de placas para garantir uma endarterectomia adequada. O principal local de falha na AFB são as anastomoses femorais, portanto, atenção meticulosa a essa etapa é necessária.
Após uma dissecação arterial adequada, o ligamento inguinal deve ser levemente dividido para evitar a compressão dos membros do enxerto ao passarem para a região femoral. Isso também permite a visualização direta da veia ilíaca circumflexa superficial enquanto ela passa sobre a artéria ilíaca externa distal (EIA) e a ligadura antes do tunelamento. As virilha devem ser preenchidas com gaze úmida e a atenção voltada para a exposição aórtica.
Uma incisão curvilínea é então feita começando no 8º ou 9º espaço intercostal na maioria dos pacientes, pois isso facilita a divisão do diafragma, se necessário, para garantir um controle proximal adequado, como visto neste caso. Isso deve ser feito com o entendimento de que pode levar a hérnia diafragmática ou derrame pleural posterior, evitado se não necessário. Em alguns pacientes, a cavidade torácica não precisa ser formalmente penetrada, mas não hesite em fazê-lo se necessário. A incisão é então transportada obliquamente pelo abdômen até a borda lateral do músculo reto abdominal e estendida para baixo alguns centímetros abaixo do nível do umbílico. Isso permite a divisão da musculatura abdominal sem sacrificar o músculo reto. Após dividir o transverso do abdome, o plano RP é criado retraindo de forma direta o peritônio medialmente para fora da parede abdominal. Achamos mais fácil desenvolver o plano no quadrante inferior esquerdo primeiro e identificar o ureter para garantir que ele não seja lesionado. Isso permite acesso rápido aos vasos ilíacos e, em seguida, o plano pode ser desenvolvido superiormente, levantando o rim e o baço para cima e medialmente. Neste ponto, deve ser realizada a ligadura da veia lombar-renal para prevenir sangramento e identificar a artéria renal esquerda.
Uma vez concluída a rotação visceral medial, um afastador Omni é colocado para auxiliar na visualização e o crus esquerdo do diafragma é dividido com cauter, expondo a aorta supracelíaca. O controle circunferencial da aorta nesse nível é obtido com fita umbilical para facilitar o clampamento cruzado completo caso surja uma complicação aórtica. Os túneis podem então ser feitos de forma contínua até a virilha. O túnel esquerdo deve ser bem fácil, já que o ureter e o cólon foram medializados. O túnel da virilha direita requer uma dissecação suave para identificar a bifurcação aórtica e, em seguida, a varredura superior do ureter usando dissecação com o dedo, facilitada pela sensação dos vasos ilíacos com a unha. Cateteres de borracha vermelha são colocados para segurar os túneis em ambos os lados e a heparina é administrada.
Antes da colocação da pinça proximal, preferimos usar o duplex estéril intraoperatório para garantir que a aorta esteja livre de ateroma. Em casos com placa posterior, pode ser preferível a pinça total proximal e distal padrão e uma dissecação mais superior na aorta, facilitada pela divisão do diafragma. Neste caso, a aorta supracelíaca era normal no duplex e, por isso, uma pinça Satinsky com mordida lateral foi usada para controle.
Uma vez que a pinça é fixada e verificada como oclusiva, a aortotomia é estendida com um punção aórtica para remover uma elipse de tecido, e o enxerto é chanfrado e costurado de ponta a ponta. O corpo principal do enxerto deve ser deixado longo o suficiente para que os membros alcancem ambas as artérias femorais.
Após a anastomose proximal, o enxerto deve ser lavado com soro fisiológico heparinizado, usar pinças macias e os membros escavados em túnel com pouquíssima redundância. A operação deve então se mover para a virilha direita, com clampagem do SFA, PA e EIA nessa ordem, seguida por arteriotomia longitudinal e endarterectomia, se indicado, como neste caso. O membro do enxerto é então chanfrado e anastomizado de ponta a ponta. A anastomose do femoral esquerdo é realizada de maneira semelhante, e depois é realizado o duplex completo de cada reparo, seguido por exame visual e pulsivo dos pés para garantir que não haja embolização e um bom resultado hemodinâmico.
Neste ponto, a heparina é revertida com protamina e um novo painel de coagulação é enviado para auxiliar na ressuscitação e hemostasia. As virilha devem ser deixadas abertas para fechar por último e cheias com gaze seca e agentes hemostáticos conforme necessário. O RP é então inspecionado meticulosamente quanto à hemostasia e ao soro salino quente usado para lavagem. Se o diafragma fosse aberto, como neste caso, um dreno torácico é colocado e então o diafragma fechado com uma sutura monofilamentosa de travamento e funcionamento 0-0. As costelas são reaproximadas com o ponto trançado #2 e o conteúdo abdominal retorna à posição normal. A incisão RP é fechada com sutura monofilamentosa absorvível #1 e as virilha fechadas em camadas.
Embora a divisão do diafragma não seja necessária para toda TFB via exposição RP, ela pode facilitar a visualização do baço enquanto ele é mobilizado e permite um controle aórtico mais próximo. Isso é especialmente útil em pacientes do sexo masculino com hábito corporal de 'barril' devido ao tabagismo crônico, como visto neste caso. O diafragma pode ser dividido com grampos roxos de carga em um grampeador endo-GIA para diminuir o sangramento nas bordas cortadas e facilitar o fechamento na extremidade do estojo. Preferimos usar a técnica de sutura de travamento ao fechar, pois ela evita que a linha de sutura fique frouxa enquanto as costelas são reaproximadas.
A visualização do local da pinça supra-celíaca deve ser excelente, pois a pinça lateral pode ser difícil de costurar. Ainda assim, os efeitos fisiológicos de uma pinça parcial com redução da isquemia visceral superam o incômodo do cirurgião. Ao usar um punção aórtica para remover uma elipse apropriada do tecido, a anastomose proximal pode ser facilitada. Mesmo assim, como visto neste caso, a linha de sutura proximal pode exigir suturas de reparo. O ideal é realizar isso antes da remoção da gramposa para evitar a necessidade de reprender várias vezes. Preferimos testar a anastomose injetando soro fisiológico heparinizado com uma seringa bulbosa antes da remoção da pinça para identificar defeitos evidentes na linha de sutura. Uma vez removida a grampeça, quaisquer pontos de reparo restantes são melhor realizados com pontos de suporte de pledget e atar de nós preciso.
A vantagem da avaliação dúplex intraoperatória não pode ser subestimada. Optamos por realizar isso após a conclusão da anastomose proximal em todos os casos para garantir que não haja complicações ao clampar uma perfusão visceral adequada. Exame de pulso e/ou Doppler de onda contínua sozinhos podem ser enganosos. Ao garantir um reparo adequado, a atenção pode ser desviada da incisão RP e toda a atenção é dada à realização das anastomoses femurais.
A estratégia de usar a exposição aórtica toracoretroperitoneal esquerda para a TFB, como visto em nosso paciente, oferece algumas vantagens em relação à técnica tradicional de toracotomia. A principal vantagem dessa exposição é a vantagem de evitar complicações pulmonares. 18 Um benefício secundário é o acesso direto às artérias celíaca, mesentérica superior e renal esquerda, que podem ser revascularizadas se indicado. 18 Além disso, isso facilita a escavação de túneis em áreas mais desafiadoras, pois os túneis podem ser acessados diretamente. As possíveis desvantagens em relação à abordagem tradicional de duas cavidades são o aumento da probabilidade de lesão esplênica e maior incidência de hérnia incisional.
Nossa paciente teve uma recuperação hospitalar sem incidentes e agora está há mais de um ano após o procedimento, com ABI normal e status funcional ilimitado.
Em conclusão, a TFB é uma alternativa de tratamento segura e eficaz ao bypass axilo-bifemoral quando a anatomia do paciente e a extensão da carga da doença aórtica a tornam menos favorável. O melhor julgamento clínico deve ser delegado ao cirurgião cirúrgico com base em sua experiência e na apresentação clínica individual do paciente. Como visto em nossos pacientes e em séries já relatadas, permanece um papel contínuo da TFB em populações selecionadas de pacientes.
- Omni-retrator.
Nada a revelar.
O paciente referido neste artigo em vídeo deu seu consentimento informado para ser filmado e está ciente de que informações e imagens serão publicadas online.
Animação adicionada após a publicação em 30/05/2025. Nenhuma alteração foi feita no conteúdo do artigo.
References
-
Síndrome de Frederick M, Newman J, Kohlwes J. Leriche. J Gen Estagiário Med. Outubro de 2010; 25(10):1102-4. DOI:10.1007/s11606-010-1412-z.
-
Rodríguez SP, Sandoval F. Doença oclusiva aorto-ilíaca, uma síndrome silenciosa. Representante de Caso BMJ. 15 de julho de 2019; 12(7):e230770. DOI:10.1136/bcr-2019-230770.
-
Narula N, Dannenberg AJ, Olin JW, et al. Patologia da doença arterial periférica em pacientes com isquemia crítica de membro. J Am Coll Cardiol. 30 de outubro de 2018; 72(18):2152-2163. DOI:10.1016/j.jacc.2018.08.002.
-
Allison MA, Cushman M, Solomon C, et al. Etnia e fatores de risco para mudança no índice tornozelo-braquial: o Estudo Multiétnico da Aterosclerose. J Vasc Surg. Novembro de 2009; 50(5):1049-56. DOI:10.1016/j.jvs.2009.05.061.
-
Criqui MH, Vargas V, Denenberg JO, et al. Etnia e doença arterial periférica: o Estudo de População de San Diego. Circulação. 25 de outubro de 2005; 112(17):2703-7. DOI:10.1161/CIRCULATIONAHA.105.546507.
-
Berger JS, Hochman J, Lobach I, Adelman MA, Riles TS, Rockman CB. Carga de fatores de risco modificáveis e a prevalência de doença arterial periférica em diferentes territórios vasculares. J Vasc Surg. Setembro de 2013; 58(3):673-81.e1. DOI:10.1016/j.jvs.2013.01.053.
-
Diehm C, Schuster A, Allenberg JR, et al. Alta prevalência de doença arterial periférica e comorbidade em 6880 pacientes da atenção primária: estudo transversal. Aterosclerose. Janeiro de 2004; 172(1):95-105. DOI:10.1016/S0021-9150(03)00204-1.
-
Olin JW, Sealove BA. Doença arterial periférica: visão atual sobre a doença e seu diagnóstico e tratamento. Mayo Clin Proc. Julho de 2010; 85(7):678-92. DOI:10.4065/MCP.2010.0133.
-
Prevalência e fatores de risco para doença arterial periférica nos Estados Unidos: resultados da Pesquisa Nacional de Saúde e Nutrição, 1999-2000. Circulação. 10 de agosto de 2004; 110(6):738-43. DOI:10.1161/01.CIR.0000137913.26087.F0.
-
Guirguis-Blake JM, Evans CV, Redmond N, Lin JS. Triagem para doença arterial periférica usando o índice tornozelo-braquial: relatório de evidências atualizado e revisão sistemática para a Força-Tarefa de Serviços Preventivos dos EUA. JAMA. 10 de julho de 2018; 320(2):184-196. DOI:10.1001/jama.2018.4250.
-
Grupo de Redação de Diretrizes de Extremidades Inferiores da Sociedade de Cirurgia Vascular; Conte MS, Pomposelli FB, Clair DG, et al; Sociedade de Cirurgia Vascular. Diretrizes práticas da Society for Vascular Surgery para doença oclusiva aterosclerótica das extremidades inferiores: manejo da doença assintomática e claudicação. J Vasc Surg. Março de 2015; 61(3 Suppl):2S-41S. DOI:10.1016/j.jvs.2014.12.009. Errata em: J Vasc Surg. Maio de 2015; 61(5):1382.
-
Gerhard-Herman MD, Gornik HL, Barrett C, et al. 2016 Diretriz AHA/ACC sobre o Manejo de Pacientes com Doença Arterial Periférica de Membros Inferiores: Resumo Executivo: Um Relatório da Força-Tarefa do American College of Cardiology/American Heart Association sobre Diretrizes de Prática Clínica. Circulação. 21 de março de 2017; 135(12):e686-e725. DOI:10.1161/CIR.00000000000000470. Errata em: Circulação. 21 de março de 2017; 135(12):e790. DOI:10.1161/CIR.00000000000000501.
-
Ahmed S, Raman SP, Fishman EK. Angiografia por TC e imagem 3D na doença oclusiva aortoilíaca: vias colaterais na síndrome de Leriche. Abdom Radiol (NY). Setembro de 2017; 42(9):2346-2357. DOI:10.1007/S00261-017-1137-0.
-
Koelemay MJ, den Hartog D, Prins MH, Kromhout JG, Legemate DA, Jacobs MJ. Diagnóstico de doença arterial dos membros inferiores com ultrassonografia duplex. Br J Surg. Março de 1996; 83(3):404-9. DOI:10.1002/bjs.1800830336.
-
Gardner AW, Poehlman ET. Programas de reabilitação de exercícios para o tratamento da dor de claudicação. Uma meta-análise. JAMA. 27 de setembro de 1995; 274(12):975-80.
-
Weitz JI, Byrne J, Clagett GP, et al. Diagnóstico e tratamento da insuficiência arterial crônica dos membros inferiores: uma revisão crítica. Circulação. 1º de dezembro de 1996; 94(11):3026-49. DOI:10.1161/01.cir.94.11.3026. Errata em: Circulação. 29 de agosto de 2000; 102(9):1074.
-
Norgren L, Hiatt WR, Dormandy JA, Nehler MR, Harris KA, Fowkes FG; Grupo de Trabalho TASC II. Consenso Inter-Sociedade para o Manejo da Doença Arterial Periférica (TASC II). J Vasc Surg. Janeiro de 2007; 45 Suppl S:S5-67. DOI:10.1016/j.jvs.2006.12.037.
-
Crawford JD, Scali ST, Giles KA, et al. Resultados contemporâneos do bypass toracofemoral. J Vasc Surg. Abril de 2019; 69(4):1150-1159.e1. DOI:10.1016/j.jvs.2018.07.053.
Cite this article
Allan JM, Aucoin V, Pearce BJ. Bypass toracofemoral: uma abordagem retroperitoneal. J Med Insight. 2024; 2024(353). DOI:10.24296/jomi/353.



