Bypass toracofemorale: un approccio retroperitoneale
Main Text
Table of Contents
L'intervento chirurgico per la malattia occlusiva aortoiliaca (AIOD) rimane uno strumento fondamentale nella gestione dell'AIOD. L'AIOD è causata dall'occlusione delle arterie infrarenali e/o iliache, spesso secondaria all'aterosclerosi. Qui presentiamo il caso di un giovane paziente maschio con una storia di iperlipidemia familiare e uso cronico di tabacco che ha subito una procedura di bypass toracemo-femorale (TFB) tramite un approccio retroperitoneale. Si presentò con sintomi classici di dolore bilaterale alle gambe durante la camminata, dolore notturno agli arti inferiori e correlati impulsi diminuiti agli arti inferiori. La TFB è stata l'approccio preferito a causa del carico aggressivo e morbido della placca che si estende nell'aorta suprarenale, il che impediva la riparazione endovascolare e avrebbe aumentato il rischio di bypass aortofemorale infrarenale standard (AFB). Questo video e il referto del caso presentano una spiegazione dettagliata di un approccio retroperitoneale a una procedura TFB e le indicazioni sfumate degli interventi chirurgici per l'AIOD. 1,2
La malattia occlusua aortoiliaca (AIOD) è una manifestazione complessa della malattia arteriosa periferica (PAD), in cui il lume dell'aorta infrarenale e/o le arterie iliache vengono annullati secondariamente a causa dell'aterosclerosi (spesso un mix di placca calcificata e ricca di lipidi). La PAD sintomatica può essere causata da placche aterosclerotiche primarie che restringono il lume e limitano il flusso, oppure da un'ostruzione secondaria dovuta alle complicazioni emboliche di queste placche. 1,2 AIOD presenta frequentemente sintomi che progrediscono dalla claudicazione glutei/coscia, a dolori di riposo negli arti inferiori e, nella forma più grave, a ulcera ischemica. La descrizione classica della presentazione dell'AIOD è stata fatta da Leriche, con la sua sindrome omonima costituita da claudicazione glutei/cosce, assenza di polsi femorali e disfunzione erettile. 1,2 Quando si presenta embolizzazione distale concomitante o occlusione infrainguinale, l'AIOD può portare a ischemia cronica che minaccia gli arti (CLTI), con una prognosi negativa. 3
I fattori di rischio più significativi per l'aterosclerosi, e di conseguenza per l'AIOD, sono l'uso di tabacco e il diabete mellito. 1 L'iperlipidemia, che può essere indotta dallo stile di vita o dovuta a un'iperlipidemia familiare precoce, contribuisce anch'essa allo sviluppo dell'AIOD. Altri fattori di rischio includono l'aumento dell'età, la storia familiare, il sesso maschile e la razza. 4,5
La prevalenza dell'AIOD nella popolazione generale varia dal 3,56% a oltre il 14%. 4,6 Gli studi hanno mostrato una prevalenza più elevata nella fascia d'età 70-80 anni, dal 14% al 23%. 8,9 Con l'invecchiamento della popolazione e l'aumento dei tassi di diabete e malattie cardiovascolari, ci sarà il potenziale per un carico maggiore di AIOD. Pertanto, è importante identificare i pazienti a rischio unico per ottenere un intervento precoce.
L'analisi dovrebbe essere avviata con un indice caviglia brachiale (ABI). 10-12 Il sospetto clinico per l'AIOD dovrebbe essere alto con un ABI anomalo e un esame del polso femorale assente/anomalo. Nel paziente sintomatico, l'analisi dovrebbe procedere con una tomografia computerizzata (TCA) per delineare la natura della malattia e stabilire la corretta stratificazione del rischio per l'intervento. Tuttavia, ci sono ancora alcuni pazienti sintomatici che possono essere inizialmente gestiti con misure conservative come programmi di camminata e cilostazolo. Questi pazienti non devono sottoporsi a CTA poiché si tratta di radiazioni indesiderate e esposizione a mezzi di contrasto. 13,14
Indipendentemente dalla strategia di intervento, tutti i pazienti necessitano di una gestione medica ottimale delle malattie croniche, inclusa la valutazione per la somministrazione di statine e antipiastrine, l'adozione di un regime di esercizio fisico e la cessazione del fumo. 11,15,16 Per coloro in cui è necessario intervento, la terapia endovascolare è spesso la prima linea di trattamento, con il bypass chirurgico riservato a chi presenta aneurisma concomitante o un carico di malattia più esteso.
Il paziente è un uomo di 52 anni con una storia medica passata di iperlipidemia familiare precoce e uso passato di tabacco (50 pacchetti per anno) che inizialmente si è presentato per un innesto di bypass coronarico (CABG) secondario a un infarto acuto di miocardio. Durante la valutazione clinica per la CABG, è stata riscontrata un'occlusione aortica infrarenale. Dopo aver subito con successo una CABG e una riabilitazione cardiaca, è stato valutato in una clinica vascolare. Il paziente ha riportato successo nell'arresto del fumo dopo il CABG, ma mantiene comunque una claudicazione a breve distanza con dolore crampico nelle cosce/glutei/polpacci bilaterali a 50 yard. Inoltre, aveva una storia personale significativa di iperlipidemia e una storia familiare di diversi parenti di primo grado con eventi cardiovascolari indici sotto i 50 anni. Sembrava sano senza ferite ischemiche ma presentava polsi femorali/poplitei e pedali assenti.
La CTA ha dimostrato un'occlusione aortica completa a livello delle arterie renali bilaterali da una combinazione di placca aterosclerotica calcificata e morbida. In modo significativo, in questo caso, l'ateroma si estendeva prossimalmente fino al livello dell'arteria mesenterica superiore (SMA), come visto nella Figura 1, il che avrebbe complicato il clamping suprarenale e compromesso l'afflusso appropriato per il bypass aortofemorale standard (AFB). L'aorta supraceliaca era priva di malattie arteriose (Figura 2). L'occlusione si estese alle arterie femorali comuni bilaterali, dove il flusso veniva ricostituito dalle arterie collaterali epigastriche e circonflesse iliache. Le arterie femorali comuni bilaterali (CFA) presentavano una placca ateromatosa di circa il 60% di stenosi, e poi il deflusso era intatto sotto la biforcazione della CFA.
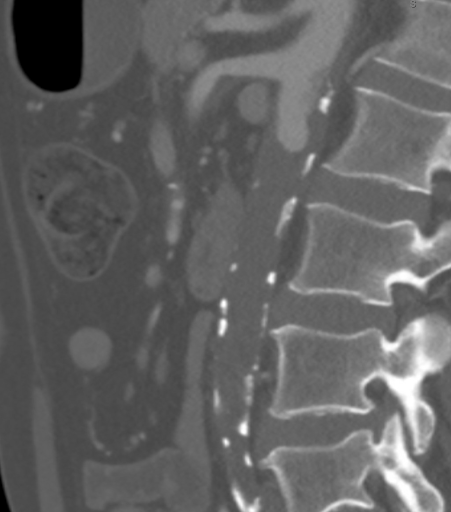
Figura 1. La CTA ha mostrato che l'ateroma si estendeva prossimalmente fino al livello dell'arteria mesenterica superiore (SMA), il che avrebbe complicato il clamping suprarenale e compromesso l'afflusso appropriato per la AFB standard.
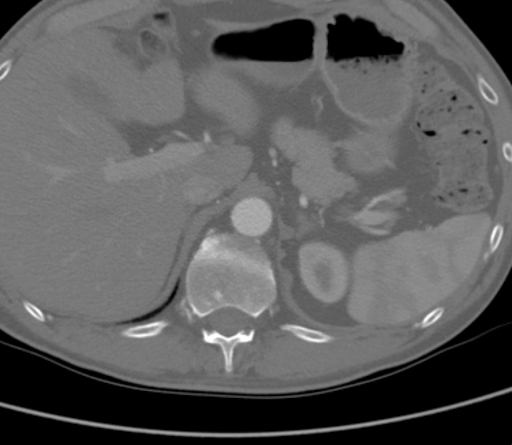
Figura 2. La CTA ha mostrato che l'aorta supraceliaca era priva di malattia arteriosa.
Come per ogni paziente con claudicazione, la prima opzione di trattamento è conservativa, con una terapia medica ottimale e la cessazione del fumo. Tuttavia, la durabilità delle procedure di aflusso, combinata con una bassa morbilità e mortalità nei pazienti selezionati in modo appropriato, rende l'intervento appropriato per pazienti come quelli che rimangono sintomatici nonostante le misure conservative. Il Consenso Inter-Società per la Gestione della Peripatia Arteriosa (TASC II)17 è un'eccellente guida per descrivere le varie opzioni di trattamento e la motivazione della scelta appropriata basata sull'anatomia del paziente e sulle comorbidità. In generale, per pazienti come questo, con occlusione aortica a flush e occlusione iliaca esterna che richiederà una CFA endarterectomia, la gestione preferita è un approccio chirurgico aperto. Il bypass chirurgico aperto dall'aorta infrarenale alla bilaterale CFA +/- CFA endarterectomia è la ricostruzione più comune per AOID grave, con una pernocenza a 10 anni riportata fino al 90%. 17 Tuttavia, alcuni vincoli anatomici come il carico di malattia nel sito di clamp prossimale o la precedente AFB fallita possono limitare l'approccio standard, nel qual caso un bypass verso la CFA bilaterale utilizzando l'aorta toracica discendente come afflusso è un approccio praticabile. La permeabilità a 5 anni è superiore all'80% se eseguita tramite toracotomia o approccio retroperitoneale dell'aorta toracica discendente distale. 18 In un paziente con gravi comorbidità mediche che impediscono l'operazione a livello aortico, il bypass ascello-bifemorale con concomitante endarterectomia CFA sarebbe un'altra opzione valida, sebbene con una patenza prevista di solo ~50% a 5 anni.
Questo paziente è giovane e in forma dopo aver smesso di fumare e aver avuto successo nella rivascolarizzazione coronarica. Rimase sintomatico e, data la sua età, desiderava ancora una maggiore distanza a piedi per facilitare l'impiego, lo stile di vita quotidiano e una maggiore capacità di esercizio fisico per una salute più duratura.
La decisione di utilizzare un sito alternativo di afflusso aortico nell'aorta toracica discendente è stata presa principalmente come secondaria rispetto all'ateroma molle all'interno di un tipico sito di pinza giustarinale, che avrebbe compromesso l'anastomosi aortica prossimale standard. Inoltre, si è deciso di utilizzare un approccio retroperitoneale invece di una toracotomia sinistra, poiché ciò avrebbe permesso una valutazione duplex intraoperatoria dei vasi viscerali e renali per garantire un flusso adeguato e eseguire il bypass viscerale concomitante se necessario. Inoltre, data la sua giovinezza, potremmo lasciare il sito di ingresso della cavità toracica per una futura rivascolarizzazione se necessario.
I passaggi di un bypass toracemorale (TFB) dovrebbero essere familiari alla maggior parte dei chirurghi vascolari, poiché imitano molte delle stesse sequenziazioni di una base aerea standard, solo con un sito di afflusso alternativo. Il paziente è posizionato in un decubio laterale destro modificato con le anche il più possibile piatte per consentire un adeguato accesso femorale per eseguire l'endarterectomia quando necessario, come in questo paziente. L'operazione dovrebbe iniziare con le esposizioni inguinali attraverso incisioni obliche per limitare il tempo totale di apertura del retroperitoneo (RP) e ridurre le perdite insensibili. Quando si prevede una concomitante endarterectomia femorale, è fondamentale controllare l'arteria femorale superficiale (SFA) e la profonda femorale (PA) fino alle zone libere di placca per garantire un'adeguata endarterectomia. Il principale luogo di guasto nell'AFB sono le anastomosi femorali, quindi si richiede un'attenzione meticolosa a questo passaggio.
Dopo un'adeguata dissezione arteriosa, il legamento inguinale deve essere leggermente diviso per evitare la compressione degli arti innesto mentre passano nella regione femorale. Questo permette anche la visualizzazione diretta della vena iliaca circonflessa superficiale mentre scorre sull'arteria iliaca esterna distale (EIA) e la legatura prima della tunneling. L'inguine dovrebbe essere riempita con garze umide e concentrarsi sull'esposizione aortica.
Nella maggior parte dei pazienti viene quindi effettuata un'incisione curvilinea a partire dall'ottavo o nono spazio intercostale, poiché ciò facilita la divisione del diaframma se necessario per garantire un adeguato controllo prossimale, come si vede in questo caso. Questo dovrebbe essere fatto con la consapevolezza che può portare a ernia diaframmatica successiva o versamento pleurale e da evitare se non necessario. In alcuni pazienti, la cavità toracica non deve essere formalmente penetrata, ma non esitare a farlo se necessario. L'incisione viene quindi portata in modo obliquo attraverso l'addome fino al bordo laterale del muscolo retto dell'addome e poi estesa verso il basso di pochi centimetri sotto il livello dell'ombelico. Questo permette la divisione della muscolatura addominale senza sacrificare il muscolo retto. Dopo aver diviso il transverso dell'addome, il piano RP si crea retraendo in modo obvio il peritoneo medialmente dalla parete addominale. Troviamo più semplice sviluppare prima il piano nel quadrante inferiore sinistro e identificare l'uretere per assicurarci che non venga danneggiato. Questo permette un rapido accesso ai vasi iliaci e poi il piano può essere sviluppato superiormente, sollevando rene e milza verso l'alto e medialmente. A questo punto, dovrebbe essere eseguita una legatura della vena lombare-renale per prevenire il sanguinamento e identificare l'arteria renale sinistra.
Una volta completata la rotazione viscerale mediale, viene posizionato un retrattore Omni per facilitare la visualizzazione e il crus sinistro del diaframma viene diviso con cauterio, esponendo l'aorta supraceliaca. Il controllo circonferenziale dell'aorta a questo livello si ottiene con un nastro ombelicale per facilitare il clamping incrociato completo in caso di complicazione aortica. I tunnel possono quindi essere realizzati in modo brusco nelle parti inguinali. Il tunnel sinistro dovrebbe essere abbastanza facile dato che uretere e colon sono stati medializzati. Il tunnel dell'inguine destro richiede una dissezione delicata per identificare la biforcazione aortica e poi una spazzatura superiore dell'uretere tramite la dissezione del dito, facilitata dal tocco dei vasi iliaci con l'unghia. Vengono posizionati cateteri di gomma rossa per sostenere i tunnel su entrambi i lati e viene somministrata l'eparina.
Prima della posa della pinza prossimale, preferiamo utilizzare il duplex sterile durante l'intervento per garantire che l'aorta sia libera da ateroma. Nei casi con placca posteriore, può essere preferibile la pinza totale prossimale e distale standard e una dissezione più superiore sull'aorta, facilitata dalla divisione del diaframma. In questo caso, l'aorta supraceliaca era normale sul duplex e quindi fu utilizzata una pinza Satinsky a morso laterale per il controllo.
Una volta fissata la pinza e controllata come occlusiva, l'aortotomia viene estesa con un pugno aortico per rimuovere un'ellisse di tessuto, e l'innesto viene smussato e cucito da un lato all'altro. Il corpo principale dell'innesto dovrebbe essere lasciato abbastanza lungo da avere una lunghezza adeguata affinché gli arti raggiungano entrambe le arterie femorali.
Dopo l'anastomosi prossimale, l'innesto dovrebbe essere lavato con soluzione salina eparinizzata, usare pinze morbide e gli arti scavati con pochissima ridondanza. L'operazione dovrebbe quindi spostarsi all'inguine destro con clampaggio di SFA, PA e EIA in quest'ordine, seguita da arteriotomia longitudinale e endarterectomia se necessario, come in questo caso. Il ramo innesto viene quindi smussato e anastomizzato da un lato all'altro. L'anastomosi del femore sinistro viene eseguita in modo simile, e successivamente viene completato il duplex di ogni riparazione, seguito da un esame visivo e polsario dei piedi per garantire l'assenza di embolizzazione e un buon risultato emodinamico.
A questo punto, l'eparina viene invertita con protamina e inviato un nuovo pannello di coagulazione per assistere la rianimazione e l'emostasi. L'inguine dovrebbe essere lasciata aperta per chiudere per ultima e riempita con garze secche e agenti emostatici secondo necessità. Il RP viene poi ispezionato meticolosamente per l'emostasia e la soluzione salina calda utilizzata per il lavaggio. Se il diaframma fosse aperto, come in questo caso, si inserisce un drenaggio toracico e poi il diaframma si chiude con una sutura monofilament 0-0 che si blocca e funziona. Le costole vengono riapprossimate con la sutura intrecciata #2 e il contenuto addominale è tornato alla posizione normale. L'incisione RP è chiusa con una sutura monofilament assorbibile #1 e le parti inguinali chiuse a strati.
Sebbene la divisione del diaframma non sia necessaria per tutte le TFB tramite esposizione RP, può facilitare la visualizzazione della milza durante la mobilizzazione e consente un controllo aortico prossimale. Questo è particolarmente utile nei pazienti maschi con un habitus corporeo a 'petto a barile' dovuto al fumo cronico, come si vede in questo caso. Il diaframma può essere diviso con graffette a carico viola in una cucitrice endo-GIA per ridurre lo spurgamento dai bordi tagliati e facilitare la chiusura alla fine del bossolo. Preferiamo utilizzare la tecnica di sutura a chiusura al momento della chiusura, poiché impedisce che la linea del punto si lasci mentre le costole vengono riapprossimative.
La visualizzazione del sito della pinza supra-celiaca dovrebbe essere eccellente, poiché la pinza laterale può essere ingombrante da cucire. Tuttavia, gli effetti fisiologici di una pinza parziale con ridotta ischemia viscerale superano il disagio del chirurgo. Utilizzando un punzone aortico per rimuovere un'ellisse appropriata del tessuto, si può facilitare l'anastomosi prossimale. Tuttavia, come si vede in questo caso, la linea di sutura prossimale può richiedere suture di riparazione. È ideale eseguire questo procedimento prima che la pinza venga rimossa per evitare la necessità di ri-clampare più volte. Preferiamo testare l'anastomosi iniettando soluzione salina eparinizzata con una siringa a bulbo prima della rimozione della pinza per identificare difetti evidenti nella linea di sutura. Una volta rimossa la pinza, eventuali suture di riparazione rimanenti sono meglio eseguite con suture di supporto a garnito e nodi precisi.
Il vantaggio della valutazione duplex intraoperatoria non può essere sottovalutato. Scegliamo di eseguire questa procedura dopo il completamento dell'anastomosi prossimale in ogni caso, per garantire che non ci siano complicazioni dovute al clampaggio di una perfusione viscerale adeguata. L'esame del polso e/o il Doppler a onda continua da soli possono essere ingannanti. Garantendo una riparazione adeguata, si può distogliere l'attenzione dall'incisione RP e dedicare piena attenzione all'esecuzione delle anastomosi femorali.
La strategia di utilizzare un'esposizione aortica toracoretroperitoneale sinistra per la TFB, come osservato nel nostro paziente, offre alcuni vantaggi rispetto alla tradizionale toracotomia. Il principale vantaggio di questa esposizione è quello di evitare complicazioni polmonari. 18 Un beneficio secondario è l'accesso diretto alle arterie celiache, mesenteriche superiori e renali sinistre, che possono essere rivascolarizzate se necessario. Inoltre , questo facilita il tunneling in campi più impegnativi, poiché i tunnel possono essere accessibili direttamente. I potenziali svantaggi rispetto all'approccio tradizionale a due carie sono la maggiore probabilità di lesioni spleniche e l'incidenza più elevata di ernia incisionale.
Il nostro paziente ha avuto un recupero ospedaliero senza incidenti e ora è passato più di un anno dalla procedura con ABI normale e uno stato funzionale illimitato.
In conclusione, la TFB è un'alternativa terapeutica sicura ed efficace al bypass ascello-bifemorale quando l'anatomia del paziente e l'entità del carico di malattia aortica la rendono meno favorevole. Il miglior giudizio clinico dovrebbe essere affidato al chirurgo operatorio in base alla sua esperienza e alla presentazione clinica individuale del paziente. Come visto con i nostri pazienti e nelle serie precedentemente riportate, il ruolo della TFB rimane in alcune popolazioni di pazienti selezionate.
- Omni-retractante.
Niente da rivelare.
Il paziente citato in questo video ha dato il suo consenso informato per essere filmato ed è consapevole che informazioni e immagini saranno pubblicate online.
Animazione aggiunta dopo la pubblicazione il 30/05/2025. Non sono state apportate modifiche al contenuto dell'articolo.
References
-
Frederick M, Newman J, Kohlwes J. Sindrome di Leriche. Stagista J Gen in Medicina. Ottobre 2010; 25(10):1102-4. doi:10.1007/s11606-010-1412-z.
-
Rodríguez SP, Sandoval F. Malattia oclusiva aortoiliaca e sindrome del silenzio. Rappresentante di caso BMJ. 15 luglio 2019; 12(7):e230770. doi:10.1136/BCR-2019-230770.
-
Narula N, Dannenberg AJ, Olin JW, e altri. Patologia della malattia delle arterie periferiche in pazienti con ischemia critica dell'arto. J Am Coll Cardiol. 30 ottobre 2018; 72(18):2152-2163. doi:10.1016/j.jacc.2018.08.002.
-
Allison MA, Cushman M, Solomon C, e altri. Etnia e fattori di rischio per il cambiamento nell'indice cavigliera-brachiale: lo studio multietnico sull'aterosclerosi. J Vasc Surg. Novembre 2009; 50(5):1049-56. doi:10.1016/j.jvs.2009.05.061.
-
Criqui MH, Vargas V, Denenberg JO, et al. Etnia e malattie arteriose periferiche: lo Studio della Popolazione di San Diego. Circolazione. 25 ottobre 2005; 112(17):2703-7. doi:10.1161/CIRCULATIONAHA.105.546507.
-
Berger JS, Hochman J, Lobach I, Adelman MA, Riles TS, Rockman CB. Carico modificabile dei fattori di rischio e prevalenza della malattia delle arterie periferiche in diversi territori vascolari. J Vasc Surg. settembre 2013; 58(3):673-81.e1. doi:10.1016/j.jvs.2013.01.053.
-
Diehm C, Schuster A, Allenberg JR, e altri. Alta prevalenza di malattia arteriosa periferica e comorbidità in 6880 pazienti di cure primarie: studio trasversale. Aterosclerosi. Gennaio 2004; 172(1):95-105. doi:10.1016/s0021-9150(03)00204-1.
-
Olin JW, Sealove BA. Malattie delle arterie periferiche: approfondimenti attuali sulla malattia, sulla sua diagnosi e gestione. Mayo Clin Proc. luglio 2010; 85(7):678-92. doi:10.4065/mcp.2010.0133.
-
Selvin E, Erlinger TP. Prevalenza e fattori di rischio per la malattia arteriolosa periferica negli Stati Uniti: risultati del National Health and Nutrition Examination Survey, 1999-2000. Circolazione. 10 agosto 2004; 110(6):738-43. doi:10.1161/01.CIR.0000137913.26087.F0.
-
Guirguis-Blake JM, Evans CV, Redmond N, Lin JS. Screening per la malattia delle arterie periferiche utilizzando l'indice cavigliera-brachiale: rapporto aggiornato sulle evidenze e revisione sistematica per la US Preventive Services Task Force. JAMA. 10 luglio 2018; 320(2):184-196. doi:10.1001/jama.2018.4250.
-
Gruppo di scrittura delle linee guida per gli arti inferiori della Society for Vascular Surgery; Conte MS, Pomposelli FB, Clair DG, ecc.; Società per la Chirurgia Vascolare. Linee guida di pratica della Society for Vascular Surgery per la malattia occlusiva aterosclerotica degli arti inferiori: gestione della malattia asintomatica e della claudicazione. J Vasc Surg. Marzo 2015; 61(3 Supporto): 2S-41S. doi:10.1016/j.jvs.2014.12.009. Errata in: J Vasc Surg. maggio 2015; 61(5):1382.
-
Gerhard-Herman MD, Gornik HL, Barrett C, et al. 2016 Linea guida AHA/ACC sulla gestione dei pazienti con malattia delle arterie periferiche degli arti inferiori: Riassunto esecutivo: Rapporto del gruppo di lavoro sull'American College of Cardiology/American Heart Association sulle linee guida di pratica clinica. Circolazione. 21 marzo 2017; 135(12):e686-e725. doi:10.1161/CIR.00000000000000470. Errata in: Circolazione. 21 marzo 2017; 135(12):e790. doi:10.1161/CIR.00000000000000501.
-
Ahmed S, Raman SP, Fishman EK. Angiografia TC e imaging 3D nella malattia occlusiva aortoiliaca: vie collaterali nella sindrome di Leriche. Abdom Radiol (NY). settembre 2017; 42(9):2346-2357. doi:10.1007/s00261-017-1137-0.
-
Koelemay MJ, den Hartog D, Prins MH, Kromhout JG, Legemate DA, Jacobs MJ. Diagnosi di malattia arteriosa degli arti inferiori con ecografia duplex. Br J Surg. Marzo 1996; 83(3):404-9. doi:10.1002/bjs.1800830336.
-
Gardner AW, Poehlman ET. Programmi di riabilitazione per il trattamento del dolore da claudicazione. Una meta-analisi. JAMA. 27 settembre 1995; 274(12):975-80.
-
Weitz JI, Byrne J, Clagett GP, e altri. Diagnosi e trattamento dell'insufficienza arteriale cronica degli arti inferiori: una revisione critica. Circolazione. 1 dicembre 1996; 94(11):3026-49. doi:10.1161/01.cir.94.11.3026. Errata in: Circolazione. 29 agosto 2000; 102(9):1074.
-
Norgren L, Hiatt WR, Dormandy JA, Nehler MR, Harris KA, Fowkes FG; Gruppo di lavoro TASC II. Consenso Inter-Società per la Gestione delle Malattie Arterie Periferiche (TASC II). J Vasc Surg. Gennaio 2007; 45 Supplemento S:S5-67. doi:10.1016/j.jvs.2006.12.037.
-
Crawford JD, Scali ST, Giles KA, e altri. Esiti contemporanei del bypass toracemorale. J Vasc Surg. aprile 2019; 69(4):1150-1159.e1. doi:10.1016/j.jvs.2018.07.053.
Cite this article
Allan JM, Aucoin V, Pearce BJ. Bypass toracofemorale: un approccio retroperitoneale. J Med Insight. 2024; 2024(353). doi:10.24296/jomi/353.



