अग्नाशय के कैंसर के लिए ओपन डिस्टल अग्नाशयेक्टोमी
Main Text
Table of Contents
डिस्टल अग्नाशयशोथ अग्नाशयशोथ के लिए सबसे अधिक बार की जाने वाली प्रक्रिया है- सौम्य और घातक दोनों- लेकिन अग्नाशयशोथ के उपचार में भी संकेत दिया जा सकता है। ऑपरेशन तिल्ली के एन-ब्लॉक रिसेक्शन के साथ किया जा सकता है, या स्प्लेनिक संरक्षण के साथ- स्प्लेनेक्टोमी को ऑन्कोलॉजिकल रिसेक्शन के लिए इंगित किया जाता है। ऑपरेटिव दृष्टिकोण- लैप्रोस्कोपिक, रोबोटिक, या ओपन- रोगी और नैदानिक परिदृश्य द्वारा निर्धारित किया जाता है। इस मामले में, हम एक रोगी में स्प्लेनेक्टोमी के साथ एक ओपन डिस्टल पैन्क्रियाटेक्टोमी करते हैं जो अग्नाशयी एडेनोकार्सिनोमा के लिए नियोएडजुवेंट उपचार से गुजरा है। यह मेटास्टैटिक बीमारी के प्रारंभिक निदान के बाद सर्जिकल रिसेक्शन से गुजरने वाले रोगी का एक अनूठा मामला है। रोगी एक 69 वर्षीय महिला है, जिसे शुरू में पेट दर्द और सूजन के साथ प्रस्तुत किया गया था, और उसके अग्न्याशय और बायोप्सी-सिद्ध एकल यकृत मेटास्टेसिस के शरीर में 2 सेमी संदिग्ध ट्यूमर पाया गया था। उसे नियोएडजुवेंट कीमोथेरेपी के एक विस्तारित पाठ्यक्रम के साथ इलाज किया गया था, और फिर से स्टेजिंग स्कैन ने महत्वपूर्ण प्रतिक्रिया दिखाई। केमोरेडिएशन पूरा हो गया था और यकृत मेटास्टेसिस अब इमेजिंग पर दिखाई नहीं दे रहा था। निदान के सत्ताईस महीने बाद उसे डिस्टल पैन्क्रियाटेक्टोमी और स्प्लेनेक्टोमी के लिए ऑपरेटिंग रूम में ले जाया गया; कोई यकृत या पेरिटोनियल मेटास्टेस नहीं देखा गया था। उसका पोस्टऑपरेटिव कोर्स समग्र रूप से घटनारहित था, और वह अच्छी तरह से ठीक हो गई। अंतिम सर्जिकल पैथोलॉजी ने पूर्ण रोग प्रतिक्रिया का प्रदर्शन किया, जिसमें बीमारी का कोई सबूत नहीं देखा गया और 0/11 लिम्फ नोड्स घातकता के लिए सकारात्मक थे। वर्तमान में उनकी मेडिकल ऑन्कोलॉजी टीम द्वारा हर तीन महीने में सीटी स्कैन और ट्यूमर मार्करों का पालन किया जा रहा है, और अब तक, फरवरी 2022 तक, पुनरावृत्ति का कोई सबूत नहीं है।
इसकी अपेक्षाकृत कम घटनाओं के बावजूद, अग्नाशय का कैंसर अमेरिका में कैंसर से मृत्यु का चौथा प्रमुख कारण है। अग्नाशयी डक्टल एडेनोकार्सिनोमा (पीडीएसी) अग्नाशय के कैंसर का सबसे आम प्रकार है, जिसमें रोगियों का एक छोटा अनुपात धीमी गति से बढ़ने वाले घातक अंतःस्रावी ट्यूमर को परेशान करता है। जोखिम कारकों में उन्नत आयु, पुरुष लिंग, मधुमेह, धूम्रपान का इतिहास, अग्नाशयशोथ और कुछ आनुवंशिक संवेदनशीलता लोकी शामिल हैं। इन ट्यूमर के आर 0 सर्जिकल रिसेक्शन उपचारात्मक उपचार का एकमात्र मौका प्रदान करता है। निदान में, अग्नाशय के कैंसर को अनियंत्रित / प्रसारित, स्थानीय रूप से उन्नत, सीमावर्ती बचाव योग्य या अग्रिम बचाव योग्य के रूप में वर्गीकृत किया जाता है (तालिका 1 देखें), जो काफी हद तक स्थानीय वाहिका की ट्यूमर भागीदारी और दूर के मेटास्टेस की उपस्थिति पर निर्भर करता है। 2 अग्नाशय के कैंसर का बहुमत (60-70%) ग्रंथि के सिर में उत्पन्न होता है, शेष शरीर और पूंछ में होता है। 1 डिस्टल पैन्क्रियाक्टॉमी में प्रासंगिक, स्प्लेनिक वाहिका की भागीदारी सर्जिकल रिसेक्शन के लिए एक निषेध नहीं है। दुर्भाग्य से, अधिकांश अग्नाशय के कैंसर रोगियों को निदान के समय बीमारी का दूर प्रसार होगा; यह अग्नाशय के शरीर और पूंछ के ट्यूमर वाले लोगों में और भी अधिक दर पर देखा जाता है क्योंकि अग्न्याशय के इस हिस्से में छोटे द्रव्यमान आमतौर पर स्पर्शोन्मुख होते हैं। अंत में अग्न्याशय के शरीर / पूंछ में पीडीएसी वाले केवल 5-7% व्यक्ति सर्जरी से गुजरेंगे। 3
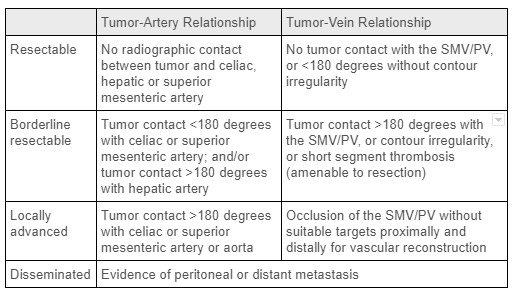
तालिका 1: अग्नाशय के कैंसर में ट्यूमर स्टेजिंग के लिए मानदंड। स्रोत: अग्नाशय के कैंसर के लिए वर्तमान सर्जिकल थेरेपी, नियोएडजुवेंट और एडजुवेंट थेरेपी2
उच्च जोखिम वाली विशेषताओं के बिना अग्रिम बचाव योग्य बीमारी वाले रोगियों के लिए, 2019 एनसीसीएन दिशानिर्देशों के अनुसार, सर्जरी अनुशंसित प्रथम-पंक्ति उपचार विकल्प है, और हाल के नैदानिक परीक्षणों द्वारा समर्थित है। 4">4 अग्नाशयी एडेनोकार्सिनोमा के सर्जिकल प्रबंधन के विकल्पों में सिर में घावों के लिए अग्नाशयी डुओडेनेक्टोमी (व्हिपल प्रक्रिया) और शरीर और पूंछ के घावों के लिए स्प्लेनेक्टोमी के साथ डिस्टल अग्नाशयोच्छेदन शामिल हैं। सीमावर्ती बचाव योग्य और स्थानीय रूप से उन्नत बीमारी के लिए पहली पंक्ति की चिकित्सा नियोएडजुवेंट उपचार (एनएटी) के साथ है, जिसमें फोल्फिरिनोक्स या जेमसिटाबाइन-नैब-पैक्लिटैक्सेल शामिल हैं।3 साहित्य का एक बढ़ता हुआ निकाय पीडीएसी में एनएटी का समर्थन करता है, जैसे कि कई नैदानिक परीक्षण अग्रिम बचाव योग्य बीमारी में शल्य चिकित्सा शोधन से पहले एनएटी की जांच कर रहे हैं। 5, 6 इस तरह के दृष्टिकोण के पेशेवरों और विपक्षों पर नीचे अधिक विस्तार से चर्चा की गई है।
उपचार के परिणाम रोगी प्रस्तुति में ट्यूमर के चरण और शल्य चिकित्सा शोधन की सीमा के आधार पर भिन्न होते हैं। अग्नाशय के कैंसर वाले सभी रोगियों के लिए समग्र 5 साल की जीवित रहने की दर लगभग 10% है। यह सफल आर 0 रिसेक्शन वाले रोगियों से भिन्न होता है, जो नोड-नकारात्मक बीमारी में लगभग 30% 5 साल की जीवित रहने की दर और नोड-पॉजिटिव बीमारी में 10% 5 साल की जीवित रहने की दर को दर्शाता है, निदान के समय प्रसारित बीमारी वाले रोगियों को, व्यावहारिक रूप से दीर्घकालिक अस्तित्व की कोई संभावना नहीं है। 1
रोगी एक 69 वर्षीय महिला है, जिसके पास एक महत्वपूर्ण धूम्रपान इतिहास, एचएलडी, एचटीएन और जीईआरडी है, जो शुरू में पेट दर्द, वजन घटाने और सूजन के साथ प्रस्तुत किया गया था। वर्कअप में एक सीटी स्कैन शामिल था जिसमें 2.1 सेमी मापने वाले अग्नाशयी शरीर द्रव्यमान और यकृत के घाव का पता चला था। ट्यूमर मार्कर सीए 19-9 को 69 यू / एमएल पर ऊंचा किया गया था। स्टेजिंग को पूरा करने के लिए सीटी चेस्ट मेटास्टैटिक बीमारी के लिए नकारात्मक था। यूएस-निर्देशित यकृत बायोप्सी से एडेनोकार्सिनोमा का पता चला। रोगी को फिर फोल्फिरिनोक्स के 4 चक्रों से गुजरना पड़ा। री-स्टेजिंग स्कैन ने यकृत के घावों के आकार में वृद्धि और अग्नाशय के द्रव्यमान में कमी का प्रदर्शन किया, और उसे चार चक्रों के लिए जेमसिटाबाइन / एब्राक्सेन में बदल दिया गया। सीटी दोहराने से यकृत और अग्नाशय ी द्रव्यमान दोनों में कमी देखी गई। एब्राक्सेन के कुल 17 चक्र प्रशासित किए गए, जिसमें सीटी स्थिर बीमारी दिखा रहा था और सीए 19-9 का 5 यू / एमएल था। फिर उसे जेमसिटाबाइन मोनोथेरेपी में ले जाया गया। उसने कम से कम दुष्प्रभावों के साथ कीमोथेरेपी को उल्लेखनीय रूप से सहन किया- अनिद्रा और न्यूरोपैथी का अनुभव करना।
केमोरेडिएशन के एक लंबे कोर्स (5 सप्ताह) को तब चल रही स्थिर बीमारी दी गई थी। रेडियोथेरेपी (आरटी) के साथ समवर्ती कैपेसिटाबिन प्रशासित किया गया था। एमआरआई के साथ यकृत इमेजिंग ने उपचार के पूरा होने पर बीमारी का कोई सबूत नहीं दिया। प्राथमिक ट्यूमर आकार में भी उल्लेखनीय रूप से कम हो गया था। बहु-विषयक चर्चा की आम सहमति यह थी कि डिस्टल पैन्क्रियाटेक्टोमी और स्प्लेनेक्टोमी के साथ सर्जिकल प्रबंधन एक उपयुक्त अगला कदम था, हालांकि अपरंपरागत, एक रोगी में शुरू में स्टेज IV अग्नाशय के कैंसर का निदान किया गया था, उसकी टिकाऊ प्रतिक्रिया और दोहराए जाने वाले इमेजिंग पर मेटास्टैटिक बीमारी के सबूत की कमी और कम ट्यूमर-मार्कर स्तर को देखते हुए।
प्रस्तुति में, रोगी ने पीलिया, पेट के द्रव्यमान, या पेट की सर्जिकल निशान का कोई सबूत नहीं दिखाया।
निदान में सीटी स्कैन ने अग्न्याशय के शरीर में एक विषम, अनियमित कम-क्षीणन अग्नाशय द्रव्यमान का प्रदर्शन किया, जो अग्नाशयी डक्टल फैलाव और अग्न्याशय के पैरेन्काइमा के शोष के साथ 2.1 सेमी x 2.1 सेमी मापता है, जो अग्नाशय ी घातकता के लिए संदिग्ध है। दाहिने हेपेटिक लोब में 9-मिमी हेटेरोजेनस कम-क्षीणन यकृत घाव को यकृत एमआरआई के साथ आगे की विशेषता थी, और अंततः यूएस-निर्देशित बायोप्सी ने मेटास्टैटिक एडेनोकार्सिनोमा की पुष्टि की।
एसएमए और एसएमवी द्रव्यमान से शामिल नहीं थे, लेकिन स्प्लेनिक नस का प्रभाव था।
प्रारंभिक निदान के बाद दो साल में सर्जिकल रिसेक्शन से पहले नियोएडजुवेंट उपचार पूरा होने के बाद सीटी स्कैन ने अग्न्याशय के शरीर में 1.2-सेमी x 0.5-सेमी हाइपोडेंस फोकस का प्रदर्शन किया, जो पूर्व इमेजिंग अध्ययनों से अपरिवर्तित था, जिसमें कोई डक्टल फैलाव नहीं था, लेकिन अग्नाशय की पूंछ का लगातार शोष था। लिवर एमआरआई ने अब कल्पना नहीं की कि दाहिने लोब में एक सबसेंटीमीटर यकृत घाव क्या बन गया था।
डिस्टल अग्नाशयोच्छेदन में ऑपरेटिव तकनीक आम तौर पर दो मॉडलों का अनुसरण करती है। कोई भी विच्छेदन को एक औसत-से-पार्श्व तरीके से कर सकता है, पहले अग्न्याशय के नीचे एक सुरंग बना सकता है और ग्रंथि को सही कर सकता है, विच्छेदन को अग्नाशयी पूंछ और स्प्लेनिक हिलम की ओर बढ़ा सकता है। वैकल्पिक रूप से, विच्छेदन ग्रंथि के पार्श्व पहलू पर शुरू किया जा सकता है और उपचारात्मक रूप से किया जा सकता है। हमारा पसंदीदा दृष्टिकोण औसत दर्जे का विच्छेदन है, हालांकि दोनों को शामिल करने वाली एक समझ और कौशल सर्जन को वैकल्पिक रास्ते प्रदान करता है जब एक कठिन विच्छेदन एक या दूसरे दृष्टिकोण को रोक सकता है।
डिस्टल अग्नाशयोच्छेदन स्प्लेनेक्टोमी के साथ या बिना किया जा सकता है। स्प्लेनिक संरक्षण के लिए सर्जिकल तकनीकों में अग्न्याशय के पीछे से स्प्लेनिक वाहिकाओं का सावधानीपूर्वक विच्छेदन, या छोटी गैस्ट्रिक वाहिकाओं का संरक्षण शामिल है, जो स्प्लेनिक वाहिकाओं के बंधाव की स्थापना में प्लीहा को रक्त की आपूर्ति प्रदान करते हैं, जिसे पहली बार वारशॉ एट अल द्वारा वर्णित किया गया था। 1988 में। 7 इस मामले में, हमने रोगी की ऑन्कोलॉजिकल प्रस्तुति की प्रकृति को देखते हुए स्प्लेनेक्टोमी करने के लिए चुना, हालांकि तिल्ली का संरक्षण कुछ नैदानिक लाभों को इंगित करता है, जैसे कि भारी पोस्टप्लेनेक्टोमी संक्रमण (ओपीएसआई) के जोखिम से बचना। डिस्टल पैन्क्रियाक्टॉमी के साथ संयोजन में स्प्लेनेक्टोमी से गुजरने वाले रोगियों में, ओपीएसआई के जोखिम को कम करने के लिए एनकैप्सुलेटेड जीवों के खिलाफ टीके लगाए जाने चाहिए। इसमें नीसेरिया मेनिन्जाइटिस, स्ट्रेप्टोकोकस निमोनिया और हेमोफिलस इन्फ्लूएंजा के खिलाफ टीकाकरण शामिल है। संक्रमण के मामले में रोगियों को नियमित रूप से एंटीबायोटिक दवाओं की आपातकालीन आपूर्ति भी दी जाती है।
डिस्टल अग्नाशयेक्टोमी और स्प्लेनेक्टोमी के साथ अग्नाशय के शरीर और पूंछ के घावों के सर्जिकल उपचार का लक्ष्य सभी बीमारियों को हटाने के साथ आर 0 रिसेक्शन है। यह रोगी को उपचारात्मक उपचार के लिए एकमात्र विकल्प प्रदान करता है। हालांकि पेरीओपरेटिव मृत्यु दर उच्च मात्रा वाले केंद्रों (1-2%) में कम है, रुग्णता उच्च (20-30%) बनी हुई है। इसमें अग्नाशयी फिस्टुला सहित ऑपरेशन से संबंधित जटिलताएं शामिल हैं, जो सबसे आम है, लेकिन परिणाम भी हैं, जैसे कि मधुमेह का विकास, जो लगभग 15-30% रोगियों में होता है। 9 इस प्रकार, अपेक्षाकृत रुग्ण ऑपरेशन के जोखिम को संभावित लाभों और आर 0 रिसेक्शन को प्राप्त करने की संभावना के खिलाफ भी तौला जाना चाहिए, जो कि बहु-विषयक सम्मेलनों में और रोगी और सर्जन के बीच समान रूप से होने वाली एक व्यक्तिगत चर्चा है।
इस मामले में एक अद्वितीय रोगी है, जो शुरू में मेटास्टैटिक बीमारी के साथ प्रस्तुत होता है, जिसने शल्य चिकित्सा शोधन से गुजरने से पहले दो साल से अधिक समय तक एनएटी के लिए टिकाऊ प्रतिक्रिया का प्रदर्शन किया, जिसमें एक पैथोलॉजिकल पूर्ण प्रतिक्रिया थी। यह उल्लेखनीय पाठ्यक्रम एक आउटलायर है, लेकिन पीडीएसी में उपचार के भविष्य के लिए महत्वपूर्ण आशा प्रदान करता है, और संभावित रूप से डाउन-स्टेजिंग बीमारी में एनएटी की शक्ति पर प्रकाश डालता है (रेक्टल कैंसर सहित अन्य पाचन तंत्र के कैंसर में देखा जाने वाला प्रतिमान, जिसमें एनएटी10 के बाद पूर्ण पैथोलॉजिकल प्रतिक्रिया अक्सर देखी जाती है)। साहित्य में कुछ केस रिपोर्ट समान रोगी प्रतिक्रियाओं का वर्णन करती हैं। 11
इस मामले की तकनीकी हाइलाइट्स में व्यापक फाइब्रोसिस के साथ एक कठिन रेट्रोपरिटोनियल विच्छेदन शामिल है, जैसा कि अक्सर एनएटी के बाद रोगियों में देखा जाता है। ट्यूमर को नरम और पतला होने के लिए नोट किया गया था, जो अक्सर नियोएडजुवेंट उपचार के लिए अच्छी प्रतिक्रिया वाले रोगियों में देखी जाने वाली विशेषता है। पीवी और एसएमवी, यकृत धमनी, गुर्दे की नस और अधिवृक्क नस सहित अग्न्याशय के शरीर और पूंछ के आसपास प्रमुख संवहनी संरचनाओं का विच्छेदन सभी बिना किसी घटना के आगे बढ़े। अग्न्याशय को एक स्टेपलर के साथ सही किया गया था, जिसमें सीम-गार्ड स्टेपल लोड का उपयोग किया गया था। एक नाली को अग्नाशयी ट्रांससेक्शन मार्जिन पर छोड़ दिया गया था, जैसा कि हमारा प्रोटोकॉल है। अनुमानित रक्त हानि 100 सीसी < थी और रोगी महत्वपूर्ण पोस्टऑपरेटिव जटिलताओं के बिना ठीक हो गया। विशेष रूप से, अंतिम सर्जिकल पैथोलॉजी ने एक पूर्ण पैथोलॉजिकल प्रतिक्रिया के साथ बीमारी का कोई सबूत नहीं दिखाया।
अग्नाशय के कैंसर का आधुनिक उपचार उस चरण पर निर्भर करता है जिस पर रोगी प्रस्तुत होता है, और रोगियों को कीमोथेरेपी और विकिरण चिकित्सा सहित मल्टीमोडिटी थेरेपी के साथ इलाज किया जाता है। आर 0 रिसेक्शन प्राप्त करने के उद्देश्य से, अग्रिम बचाव योग्य अग्नाशय के कैंसर का इलाज पहले सर्जरी के साथ किया जा सकता है; हालांकि, सर्जरी से पहले एनएटी की पेशकश करने में रुचि बढ़ रही है, यहां तक कि अग्रिम बचाव योग्य बीमारी में भी। जैसा कि ऊपर उल्लेख किया गया है, स्थानीय रूप से उन्नत और सीमावर्ती बचाव योग्य बीमारी में, पहली पंक्ति का उपचार एनएटी है; यदि रोगी एनएटी पर कोई बीमारी की प्रगति नहीं दिखाते हैं, तो सर्जिकल अन्वेषण आमतौर पर पेश किया जाता है, क्योंकि रेडियोग्राफिक निष्कर्ष अक्सर एनएटी के बाद बचाव की भविष्यवाणी नहीं करते हैं।
बचाव योग्य बीमारी में एनएटी के लाभों में सूक्ष्म रोग के पहले और तेजी से उपचार की अनुमति देना, रोगी चयन में सुधार, साथ ही उपचार के पूर्ण आहार को पूरा करने की उच्च संभावना शामिल है। सर्जरी के समय मेटास्टैटिक बीमारी पाए जाने वाले रोगियों (25% तक) की उच्च दर को देखते हुए, नियोएडजुवेंट उपचार की डिलीवरी ट्यूमर जीव विज्ञान को विकसित करने और संभावित रूप से उन रोगियों के लिए आत्म-चयन करने की अनुमति देती है जो एक शल्य चिकित्सा प्रक्रिया से लाभान्वित होने की संभावना रखते हैं जो रोगी को महत्वपूर्ण रुग्णता के लिए जोखिम में डालता है। एक अतिरिक्त लाभ यह है कि एनएटी.12 के बाद अग्नाशयी फिस्टुला का जोखिम स्पष्ट रूप से कम हो जाता है।
हालांकि, इस दृष्टिकोण के कुछ पतन हैं। एनएटी को छोड़ना किसी भी प्रगति से पहले ट्यूमर को हटाने का अवसर प्रदान करता है, क्योंकि सर्जिकल निष्कासन पीडीएसी में दीर्घकालिक इलाज का एकमात्र मौका है। एनएटी से गुजरने वाले पित्त अवरोध वाले रोगियों के लिए, पित्त स्टेंटिंग करने की आवश्यकता होती है, जो अपने स्वयं के स्वीकार्य जोखिमों को वहन करता है जिन्हें कई अध्ययनों में क्रॉनिकल किया गया है। 13
डिस्टल अग्नाशयोच्छेदन में प्रगति में न्यूनतम इनवेसिव तकनीकों का उपयोग शामिल है; लैप्रोस्कोपिक और रोबोटिक दोनों प्रक्रियाओं को देश भर में किया जा रहा है। हाल ही में, न्यूनतम इनवेसिव बनाम ओपन डिस्टल पैन्क्रियाटेक्टोमी के पहले यादृच्छिक नियंत्रित नैदानिक परीक्षण प्रकाशित किए गए थे। तेंदुए का परीक्षण संवहनी भागीदारी के बिना बाएं तरफा अग्नाशय के ट्यूमर वाले रोगियों के लिए एक बहु-रोगी-अंधा आरसीटी है। इस परीक्षण में, न्यूनतम इनवेसिव डिस्टल पैन्क्रियाटेक्टोमी कार्यात्मक वसूली के लिए कम समय से जुड़ा हुआ था; हालांकि, समग्र जटिलता दर प्रभावित नहीं हुई थी। एलएपीओपी परीक्षण एक संभावित आरसीटी है जो गैर-अंधा था, जो पोस्टऑपरेटिव अस्पताल में रहने की लंबाई के प्राथमिक समापन बिंदु का मूल्यांकन करता है। इस परीक्षण ने अस्पताल में रहने की लंबाई (5 दिन बनाम 6 दिन) में महत्वपूर्ण कमी का प्रदर्शन किया और कुल मिलाकर जटिलता दर में कोई बदलाव नहीं हुआ। इन आंकड़ों से पता चलता है कि न्यूनतम इनवेसिव डिस्टल पैन्क्रियाटेक्टोमी रोगियों को अधिक समीचीन वसूली की पेशकश कर सकती है। हालांकि, न्यूनतम इनवेसिव प्रक्रियाओं की तुलना करते समय ऑन्कोलॉजिक परिणामों के संबंध में डेटा की कमी है, और इस क्षेत्र में अधिक काम की आवश्यकता है। एनएटी वाले रोगियों में, विशेष रूप से यदि विकिरण एक घटक था, तो विच्छेदन को बनाने वाले प्रमुख वाहिकाओं के आसपास चिह्नित फाइब्रोसिस हो सकता है, हालांकि न्यूनतम इनवेसिव, अधिक कठिन।
फॉलोअप में, यह रोगी दैनिक जीवन की अपनी सामान्य गतिविधियों में लौटने में सक्षम था। उसने 25 पाउंड > वजन घटाने और चल रहे ढीले मल की सूचना दी। उसे अग्नाशयी एक्सोक्राइन अपर्याप्तता के लिए क्रेओन पर शुरू किया गया था। फरवरी 2022 में इस लेख के लेखन में सबसे हालिया इमेजिंग ने आवर्तक बीमारी का कोई सबूत नहीं दिखाया। रोगी को क्यू 3 महीने के सीटी स्कैन और ट्यूमर मार्कर माप के साथ उसकी मेडिकल ऑन्कोलॉजी टीम द्वारा पालन किया जाना जारी रहेगा।
खुलासा करने के लिए कुछ भी नहीं।
इस वीडियो लेख में संदर्भित रोगी ने फिल्माने के लिए अपनी सूचित सहमति दी है और वह जानता है कि जानकारी और छवियां ऑनलाइन प्रकाशित की जाएंगी।
References
- मैकगुइगन ए, केली पी, तुर्किंगटन आरसी, जोन्स सी, कोलमैन एचजी, मैककेन आरएस। अग्नाशय के कैंसर: नैदानिक निदान, महामारी विज्ञान, उपचार और परिणामों की समीक्षा। वर्ल्ड जे गैस्ट्रोएंटेरिओल। 2018;24(43):4846-4861. doi:10.3748/wjg.v24.i43.4846.
- कैमरन जेके, कैमरन एएम। वर्तमान सर्जिकल थेरेपी। फिलाडेल्फिया: एल्सेवियर मोस्बी; 2011.
- ओबा ए, हो एफ, बाओ क्यूआर, अल-मुसावी एमएच, शूलिक आरडी, डेल चियारो एम। ऑन्कोलॉजी में फ्रंटियर्स। 2020;10(245). दोई: 10.3389/
- घानेह पी, पामर डीएच, सिकोनी एस, et.al। ईएसपीएसी -5 एफ: सीमावर्ती बचाव योग्य अग्नाशय के कैंसर वाले रोगियों में नियोएडजुवेंट जेमसिटाबाइन प्लस कैपेसिटाबाइन (जीईएमकैप) या फोल्फिरिनोक्स या केमोरेडियोथेरेपी (सीआरटी) की तुलना में तत्काल सर्जरी के चार-हाथ, संभावित, बहुआयामी, अंतर्राष्ट्रीय यादृच्छिक चरण द्वितीय परीक्षण। जे क्लिन ओनकोल। 2020;38(15)4505. दोई: 10.1200/ JCO.2020.38.15_suppl.4505।
- मुलर पीसी, फ्रे एमसी, रुज़ा सीएम, एट अल। अग्नाशय के कैंसर में नियोएडजुवेंट कीमोथेरेपी: वर्तमान उच्च-स्तरीय साक्ष्य का मूल्यांकन। फार्माकोलॉजी। 2021;106:143-153. दोई: 10.1159 000510343/
- वर्स्टीजेन ई, सुकर एम, ग्रोटहुइस के, एट अल। प्रीऑपरेटिव केमोरेडियोथेरेपी बनाम तत्काल सर्जरी के लिए बचाव योग्य और सीमावर्ती बचाव योग्य अग्नाशय के कैंसर: डच यादृच्छिक चरण III प्रीओपन्क परीक्षण के परिणाम। जे क्लिन ओनकोल। 2020;38(16):1763-1773. दोई: 10.1200 / JCO.19.02274.
- प्लीहा के संरक्षण के साथ डिस्टल अग्नाशयोच्छेदन। जे हेपेटोबिलरी पैन्क्रियाट साइंस। 2010;17:818-812. दोई: 10.1007/s00534-009-0226-z.
- लिलेमो केडी, कौशल एस, कैमरून जेएल, सोहन टीए, पिट एचए, यो सीजे। डिस्टल अग्नाशयोच्छेदन: 235 रोगियों में संकेत और परिणाम। एन सुर्ग। 1999;229(5):693. दोई: 10.1097/00000658-199905000-00012।
- ब्रूजिन केएमजे, वैन ईजक सीएचजे। डिस्टल अग्नाशयोच्छेदन के बाद नई शुरुआत मधुमेह: एक व्यवस्थित समीक्षा। एन सुर्ग। 2015;216(5):854-61. doi:10.1097/ SLA.0000000000000000819.
- स्थानीय रूप से उन्नत रेक्टल कैंसर के लिए प्रीऑपरेटिव समवर्ती केमोरेडियोथेरेपी: उपचार के परिणाम और रोगसूचक कारकों का विश्लेषण। कैंसर का इलाज। 2012;44(2):104-112. दोई: 10.4143 / crt.2012.44.2.104.
- रियोस पेरेज़ एमवी, दाई बी, कोए ईजे, वोल्फ आरए, फ्लेमिंग जेबी। चरण IV अग्नाशय के कैंसर का उपचारात्मक सर्जरी के लिए प्रतिगमन और एक नवीन पूर्व-विवो केमोसेंसिटिव परख का परिचय। इलाज. 2015; 7 (12): e423. दोई: 10.7759 /
- हांक टी, सैंडिनी एम, फेरोन सीआर, एट अल। नियोएडजुवेंट कीमोथेरेपी के युग में अग्नाशयी फिस्टुला और दीर्घकालिक अस्तित्व के बीच संबंध। जामा सुर्ग। 2019;154(10):943-951. दोई: 10.1001 / jamasurg.2019.2272.
- कुवाटानी एम, नाकामुरा टी, हयाशी टी, एट अल। अग्नाशय के कैंसर के लिए एक नियोएडजुवेंट थेरेपी के दौरान पित्त जल निकासी के नैदानिक परिणाम: धातु बनाम प्लास्टिक स्टेंट। आंत यकृत। 2020;14(2):269-273. दोई: 10.5009/
- रिविएरे डी, गुरुसामी केएस, कूबी डीए, वोल्मर सीएम, बेसेलिंक एमजीएच, डेविडसन बीआर, वैन लारहोवन सीजेएचएम। अग्नाशय के कैंसर के लिए लैप्रोस्कोपिक बनाम ओपन डिस्टल अग्नाशयोच्छेदन। व्यवस्थित समीक्षाओं का कोचरन डेटाबेस। 2016;4 (CD011391). दोई: 10.1002/14651858.CD011391.pub2.
- - डी रूइज टी, वैन हिलस्ट जे, वैन सेंटवूर्ट एच, et.al। मिनिमली इनवेसिव बनाम ओपन डिस्टल पैन्क्रियाटेक्टोमी (लेपर्ड): एक बहुआयामी रोगी-अंधा यादृच्छिक नियंत्रित परीक्षण। एन सुर्ग। 2019;269(1):2-9. दोई: 10.1097/ SLA.00000000000002979.
- ब्योर्नसन बी, सैंडस्ट्रॉम पी, लार्सन एएल, हजलमारसन सी, गैसलैंडर टी लैप्रोस्कोपिक बनाम ओपन डिस्टल पैन्क्रियाक्टॉमी (एलएपीओपी): एकल केंद्र, गैर-अंधा, यादृच्छिक नियंत्रित परीक्षण के लिए अध्ययन प्रोटोकॉल। परीक्षण। 2019;20(356). दोई: 10.1186/s13063-019-3460-y.
Cite this article
हेनेसी एमएल, फर्नांडीज-डेल कैस्टिलो सी. अग्नाशय के कैंसर के लिए ओपन डिस्टल पैन्क्रियाटेक्टोमी। जे मेड इनसाइट। 2022;2022(339). दोई: 10.24296/

