外傷患者における迅速配列挿管(RSI)気道管理の薬理学
Main Text
すべての外傷患者に対する一次調査は、気道、呼吸、循環のABCから始まります。患者が気道管理が必要と判断された場合、気管挿管は迅速シーケンス挿管(RSI)を用いて行われることがあります。RSIでは、誘導剤と即効性神経筋遮断薬(NMBAまたは麻痺剤)を投与し、意識喪失と麻痺が達成された直後に挿管が行われます。1 外傷患者は、低酸素症、低換気、臨床状態の悪化の可能性、または精神状態の変化や頭部・頸部の損傷による気道の維持・保護の失敗など、さまざまな理由で挿管が必要となることがあります(表1)。歴史 的にRSIは「7つのp」の連続として説明されてきました:(1) 準備、(2) 前酸素供給、(3) 前治療、(4) 誘導を伴う麻痺、(5) 保護と位置、(6) 気管内チューブの挿入、(7) 挿管後の管理。3 本レビューでは、外傷患者における前治療、麻痺による誘導、挿管後の管理における一般的な薬剤の使用における薬理学、用量、その他の考慮事項に焦点を当てます。
気管挿管中は、気道内の交感神経と副交感神経の両方が刺激されることがあります。交感神経刺激は心拍数を1分間最大30回増加させ、平均動脈圧(MAP)を約25〜50 mmHg上昇させることがあり、これが頭蓋内圧(ICP)の増加に寄与する可能性があります。逆 に、小児患者は低酸素による副交感神経刺激や挿管中の喉頭操作による迷走神経刺激による徐脈を発症することがあります。5 さらに、気管内チューブの挿入は上気道反射を刺激し、咳、喉頭痙攣、下気道気管支攣縮を引き起こし、これらもICPの増加に寄与する可能性があります。3 前治療の目的はこれらの生理的反応を緩和することです。
フェンタニルは挿管に対する交感神経反応を鈍らせるために使用されることがあります。心拍数、血圧、またはICPの上昇による害のリスクが最も高い患者には、フェンタニルの事前治療を検討してください。これらの患者には、ICPが増加している(頭蓋内出血の有無にかかわらず)、既知または疑われる脳または大動脈瘤、または主要血管解離を含む場合があります。3 交感神経の駆動に依存して心拍出量を維持する患者、例えば非償正ショック状態にある患者や血行動態が不安定な患者にはフェンタニル前治療を避けてください。フェンタニルの作用の開始はほぼ瞬時で、作用時間は約30〜60分です。6 フェンタニルは、誘導剤の約3分前に、1〜3 mcg/kgの静脈投与で投与すべきです。急激な呼吸抑制を避けるため、前治療用量は30〜60秒間投与してください。高用量(5〜10 mcg/kg)のフェンタニルは、過度の低血圧、無呼吸、胸壁の硬直を引き起こすことが示されています。4
「血行動態不安定性」という用語は、文献では完全な一般的な合意なしに使われています。著者によって血行動態不安定性の定義基準は異なります。これらの基準には、心拍数、収縮期血圧、呼吸数の乱れが最も多く含まれます。カットオフポイントも異なり、平均値は>103 bpm、<96 mmHg、<34回/分の呼吸です。47
アトロピンは、挿管前に徐脈があった患者や、迷走神経刺激やスクシニルコリン使用により挿管中に徐脈になるリスクのある患者に対して、前薬として使用されることがあります。スクシニルコリンはムスカリン受容体への作用により徐脈を引き起こすか悪化させる可能性があります。この徐脈の発生率と重症度は、大人よりも子どもに多く見られます。7 2020年のPALSガイドラインでは、1歳未満の患者やスクシニルコリン投与中の高リスク患者において徐脈予防のために挿管前薬としてアトロピンを使用することが「合理的である可能性がある」とされています。8 成人および思春期の患者に対して、2回目のスクシニルコリン投与を検討します。徐脈予防のためのアトロピンの用量は0.02 mg/kg(最大用量0.5 mg)です。8、9 アトロピンの心拍数への影響は静脈内投与でほぼ即座に現れ、最大4分間持続します。10
リドカインは挿管時の咳反応を鈍らせ、血行動態や内側内膜圧(ICP)に与える影響を抑えるために用いられてきました。3、4 この効果の意義は不明であり、リドカインと挿管がICPや患者中心のアウトカムに与える影響を評価する研究は発表されていません。11 ある研究では、重度外傷性脳損傷(TBI)患者が挿管前に静脈内リドカインを受けたかどうかにかかわらず血行動態に差が見られませんでした。12 現在、リドカイン前治療は推奨されていません。11、13 リドカインを前治療に使用する場合、典型的な用量は誘導3分前に1.5 mg/kgを投与します。3 この用量ではリドカインの作用開始時間は1分未満、作用時間は10〜20分です。 リドカインは肝臓で代謝され、肝機能障害が著しい患者では持続時間が2倍になることがあります。
誘発分娩の目的は、患者を迅速に全身麻酔状態に鎮静させ、麻痺薬の投与を可能にし、理想的な挿管に適した状態を促進することです。最適な誘発薬は、記憶喪失と鎮痛を提供しつつ、鎮静をスムーズかつ迅速に行う効果があります。この理想的な薬剤は血行力学的に中性で、即座に可逆的で、副作用も最小限に抑えられます。1 これらすべての特性を単一の薬剤が包含するわけではありませんが、患者特有の要因が臨床シナリオに最適な誘導薬の選択を左右します。2016年の米国の学術救急部門挿管の登録では、エトミデートがRSIの最も一般的な誘導剤であり、次いでケタミン、そしてプロポフォールが続きました。14
エトミデートは非バルビツール酸系催眠薬で、GABAの効果を高めることで鎮痛なしで迅速な鎮静を提供します。エトミドレートの人気は、その安定した血行動態プロファイルとICP低下の可能性、そして信頼性の高い薬理動態的および薬理動態的効果に起因しています。3、4 しかし、エトミド酸の単回投与は副腎抑制と関連しています。
敗血症以外の臨床的意義については議論がありますが、外傷患者の誘発分娩におけるエトミデートとケタミンを比較した研究では、死亡率、集中治療室(ICU)なし日数、人工呼吸器なし日数に差は見られませんでした。15 臨床医は、エトミダトによる迅速な誘導効果と血行動態の安定性の利点と、副腎抑制の可能性と比較検討しなければなりません。特に副腎不全のリスクが高い患者(例:敗血症や慢性疾患の患者)では、ケタミンやプロポフォールなどの代替薬が検討されることがあります。エトミデートは依然として価値ある薬剤ですが、その使用には慎重な検討が必要です。患者の状態に基づいたバランスの取れたアプローチが不可欠です。46
エトミデートの他の誘導薬に対する明確な利点の一つは、規制物質ではなく、未使用薬の保管や廃棄時に追加の書類作成を必要としないことです。RSIに対するエトミドレートの用量は0.3 mg/kgです。行動開始は1分未満で、行動時間は3〜5分です。16
誘発分娩におけるケタミンの使用は、その有利な血行動態プロファイルと、エトミデートによる副腎抑制への懸念に応えるため、人気が高まっています。ケタミンはNMDA受容体受容体を抑制するもので、迅速な鎮静、鎮痛、健忘をもたらします。興味深いことに、ケタミンは内因性カテコールアミンの再取り込みを阻害することで間接的な交感神経刺激効果を持ち、心拍数や血圧を上昇させます。15 しかし、ケタミンは直接的な心筋抑制作用も持ち、カテコールアミン不足患者ではより顕著になることがあります。15 重症化した敗血症患者において、心筋抑制が交感神経模倣効果を上回る可能性があるという懸念がある一方で、外傷患者のRSIに対するケタミン使用を具体的に検討した場合、この発見は持続していません。15、17 歴史的に、眼圧(IOP)が高い患者ではケタミンは避けられてきました。しかし、現在の証拠では、鎮静・人工呼吸(オックスフォードレベル2b、グレードC)で重度のTBI患者においてケタミンはICPを増加させないと示唆されています。実際、場合によってはICPを下げることさえあります。46 ケタミンの誘導用量は1〜2 mg/kgで、発症時間は約30秒、用量依存的な鎮静時間は5分から10分です。18 注目すべきは、ケタミンを60秒未満で急激に投与すると無呼吸を引き起こす可能性があるため、挿管を容易にする際にはタイミングが非常に重要であるということです。
RSI誘発剤としては、プロポフォールやミダゾラムなど、あまり一般的ではありません。プロポフォールは高度に脂溶性の高いGABA作動薬で、鎮静の開始が速いです。1 しかし、プロポフォールのボーラス投与は、前負荷、後負荷の減少、収縮力の低下を通じてMAPを減少させます。3 これらの特徴はプロポフォールのICP低下能力に寄与するため、ICPが高い血行動態的または高血圧患者にはプロポフォールが合理的な選択肢となる可能性があります。非プロポフォール誘導法(エトミデートまたはミダゾラム)と比較して、ある研究では年齢、損傷重症度スコア、RSI前低血圧を調整した結果、外傷性損傷患者で挿管後低血圧を引き起こす可能性がほぼ4倍に増加しました。19 プロポフォールは大豆油と卵レシチンを含んだ乳化液で製剤されますが、アメリカアレルギー喘息・免疫学会は、大豆や卵アレルギーのある患者は特別な注意なくプロポフォールを投与できると述べています。20 誘発時のプロポフォール用量は1.5〜2.5 mg/kgで、血行動態が不安定な患者には用量が減らされます。1、3ミダゾラムは作用の開始が遅く(最大5分)、鎮静のレベルも信頼性に欠けるため、RSIの唯一の誘発剤としてはあまり一般的ではありません。1 フェンタニルの併用投与により、発作時間は90秒に短縮できます。ミダゾラムの誘発用量は0.2〜0.3 mg/kgです。1、3 提供者は大量のミダゾラム投与に不慣れで不安を感じる場合があり、これらの用量が健忘を抑え、挿管条件を最適化するために必要な鎮静レベルを提供するために適正であることを確信する必要があるかもしれません。ミダゾラムは用量依存的に全身血管抵抗や心筋抑制の低下を示すため、血行動態不安定性の患者には注意して使用すべきです。1 ミダゾラムの誘発使用は、特定の適応症(けいれん発作)がある患者や、薬剤不足により他の薬剤が入手できない場合に限定されるべきです。
脱分極性の神経筋遮断薬であるスキニルコリンは、効果が早く、作用時間も短く、これらの特性により、外傷患者のRSIでの使用に理想的です。挿管後の鎮静レベルを正確に評価でき、気道の困難が懸念される場合や挿管直後に正確な神経学的評価が必要な場合に特に理想的です。1.5 mg/kgの用量では、45秒以内に発症し、持続時間は6〜10分です。21
しかし、特定の患者に対しての使用を制限するいくつかの考慮点があります。まず、悪性高体温症の個人または家族歴がある患者にはスクシニルコリンが禁忌とされています。2 つ目に、スクシニルコリンは一部の患者で重度の高カリウム血症を引き起こし、心室不整脈や心停止を引き起こすことがあります。ほとんどの患者では、スクシニルコリンは血清カリウムを平均0.3〜1 mEq/L増加させます。1、22 しかし、高カリウム血症の素因がある患者では、この上昇が5〜10 mEq/Lに達することがあり、心室性不整脈や心停止を引き起こすことがあります。21、23 したがって、症状性高カリウム血症、末期腎疾患、横紋筋融解症、または骨格筋の広範な脱神経を引き起こす疾患(例:多発性硬化症、筋ジストロフィー)の患者には、スクシニルコリンの使用を避けるべきです。1 スクシニルコリンによる重度の高カリウム血症は、圧迫損傷、脱神経損傷、火傷における急性期(損傷から約3〜5日後、または火傷後7〜10日)後に発生します。したがって、急性圧迫や火傷の最初の24〜48時間は、健康な患者に対してスクシニルコリンを使用しても安全です。また、小児患者にスクシニルコリンを使用すると、骨格筋筋症(すなわちデュシェンヌ型筋ジストロフィー)と診断された場合、急性横紋筋融解症や心停止のブラックボックス警告もあります。一部の センターでは、このリスクを避けるために小児患者に対してスクシニルコリンの使用を完全に避けていますが、ほとんどのセンターは健康な患者に対する緊急挿管には使用を検討しています。最後に、ある外傷センターでの回顧的研究では、重度TBI患者におけるサクシニルコリン使用と死亡率増加の関連が示されましたが、24 は禁忌がない場合でもTBIでの使用を推奨する者もいました。13
修正RSIの文脈では、ロクロニウムが唯一の代替手段として浮上します。この用途に必要な投与量は、ロクロニウムの標準誘導用量の約2倍であることは注目に値します。
ロクロニウムはアミノステロイドの非脱分極性神経筋遮断剤で、1 mg/kgの用量で約1〜2分間の発症を示します。25、26 国立緊急気道登録研究所の研究では、≥1.4 mg/kgの高用量が、低血圧≥14歳の患者における直接喉頭鏡検査の初発成功率向上と関連しています。ロ クロニウムの持続時間は用量と肝機能に依存します。通常の挿管用量では、持続時間は約40〜90分ですが、患者によっては120分以上続くこともあります。25 スクシニルコリンと対照的に、ロクロニウムには禁忌が一つだけあり、それはロクロニウムや他のNMBAに対するアナフィラキシーの既往です。したがって、病歴が不明であったり、検査値がまだ得られていない外傷患者に選ばれることが多いです。
ロクロニウムには外傷患者にとって2つの主な欠点があります。どちらも作用時間が著しく長いことによるものです。挿管後の鎮静で述べるように、不十分な用量や鎮静の開始遅延は起こりやすいです。28、29 長期的な麻痺は神経学的検査を受ける能力も妨げます。ロクロニウムの逆転剤は存在しますが、これらにもリスクがあります。コリンエステラーゼ阻害薬であるネオスチグミンは、患者が神経筋機能が回復した場合(すなわち4人中2人以上が4人連続で回復した場合)に投与可能です。30 アトロピンやグリコピロレートなどの抗コリン作動薬を併用して投与し、ムスカリン受容体の活性化による徐脈のリスクを減らす。21 シュガマデックスは、血漿中のロクロニウムまたはベクロニウムに結合する新規シクロデキストリンで、神経筋接合部のアセチルコリン受容体結合に有効なNMBA量を減少させます。Sugammadexは、深部ブロックを含むあらゆる程度の神経筋遮断を逆転させることができるという利点があります。スガマデックス-ロクロニウム複合体は腎内でクリアされており、クレアチニンクリアランスが< 30 mL/minの患者には、排出が長期間および反跳麻痺のリスクがあるため使用は推奨されません。また 、アナフィラキシー、徐脈、心停止とも関連しているため、注意が必要です。また、スガマデックスは使用後7日間、経口または非経口ホルモン避妊薬の効果を抑制し、バックアップ避妊法が必要です。31
他の2つの非脱分極剤は、その薬理動態のためRSIにはあまり使用されません。ベクロニウムはアミノステロイドで、標準用量0.08〜0.1 mg/kgで2〜3分の発効時間と60〜80分間の持続時間を持ちます。32 さらに、ベクロニウムは再構成が必要な粉末として供給され、緊急挿管時に薬剤を準備する過程にもう一つの工程を加えます。シサトラクリウムはベンジリソキノリニウムの非脱分極性NMBAで、0.15 mg/kgの挿管用量で2〜3分間の起作用、持続時間55〜80分で、スガマデックスでは逆転できません。33 ホフマン除去による臓器に依存しない代謝を持つ。ロクロニウムの薬剤不足時には、起始が遅いことを考慮すれば、両薬剤とも代替薬として検討される可能性があります。
患者が挿管された後は、患者の安全と快適さのために十分な鎮痛と鎮静を提供することが不可欠です。サクシニルコリンの作用時間が短いため、挿管後比較的迅速に患者の痛みや鎮静レベルを正確に評価できます。しかし、RSIにロクロニウムを使用する場合、誘導薬と麻痺剤の持続時間の不一致は、遅らせまたは不十分な鎮静と関連しており、患者が麻痺状態で意識を回復するリスクを高めています。26、27 最近の研究では、救急外来で挿管された患者の2.6%が麻痺を伴う意識を経験したことが判明し、このリスクはロクロニウムの方がスクシニルコリンよりも有意に高いことが示されました。34
2018年のPADISガイドラインでは、痛みや興奮の管理にはプロトコル駆動型鎮痛療法を推奨しており、鎮痛剤(通常はオピオイド)を鎮静剤の前または鎮静剤の代わりに使用します。35 トラウマベイの患者は痛みを伴うけがを負う可能性が高いことを考えると、この方法は賢明です。さらに、鎮静剤の記憶消去効果からも恩恵を受けることがあります。
鎮静には複数の戦略がありますが、オピオイドは依然として治療の主軸です。フェンタニルは、作用の発現が早く、血行動態が中立的で、単一ボーラスで投与しても短時間であることから、しばしば選ばれます。繰り返し投与または連続点滴を行うと、フェンタニルは2区画モデルの薬理動態を示し、特に心不全、肝疾患、または体重増加の患者において効果の持続時間が長くなります。36 初期ボーラス投与の後に連続的な点滴を行うことで、より速い滴定が可能となり、点滴ポンプを介してさらにボーラス投与が可能となります。これは安全性の両面で理想的であり、外傷評価や画像検査の残りの過程で看護師や薬剤師が自動調剤キャビネットに戻る必要を減らすことができます。フェンタニル点滴は一般的に混合型連続点滴として提供されており、他のオピオイド点滴よりも救急外来でより迅速に利用可能である可能性があります。
RSIにスクシニルコリンを使用する場合、標準尺度を用いた痛みと鎮静のレベルを追跡調査することで、フェンタニルの用量を増やすか鎮静剤を追加するかの決定が進むことがあります。37、38 しかし、ロクロニウムを用いて逆にしない場合、これらの尺度は痛みや鎮静の有効な評価とはなりません。したがって、患者の初期症状の情報をもとに、フェンタニルに加えて経験的に鎮静剤を開始すべきかどうかを判断することが重要です。例えば、メタンフェタミンやエタノールで最初に興奮し酩酊状態にある患者には、プロポフォールやベンゾジアゼピンが酩酊を和らげるための望ましい薬理学的効果をもたらします。
2018年のPADISガイドラインでは、ICUでの入院期間短縮、人工呼吸時間の短縮、せん妄のために、機械的換気患者の鎮静において、ベンゾジアゼピン系に代わって持続点滴プロポフォールまたはデクスメデトミジンの使用を推奨しています。35 連続点滴投与の場合、プロポフォールは迅速な効果と短時間の鎮静効果を持ち、患者の精神状態を評価するために中断が必要な場合に理想的です。プロポフォールは、その抗酸化特性や脳内膜圧(ICP)の減少の可能性により、鎮静中のTBI患者において神経保護効果を持つ可能性があります。39、40 低血圧はプロポフォールの既知の副作用ですが、深刻な場合があります。ある研究では、55歳以上の外傷患者、肥満、そしてベースラインSBPが低い患者で、SBPが約30 mmHg減少する可能性が高いことが示されました。41 初期プロポフォール点滴用量を低くし、患者に理想的な体重を適用することを考えましょう。低血圧は、プッシュドーズまたは連続輸液による血管圧迫剤、さらにATLSによる点滴および血液製剤による蘇生で軽減できます。
デクスメデトミジンは、オピオイドを抑える特性を持つα-2作動薬で、ICU鎮静に推奨される他の一般的な鎮静剤です。35 しかし、デクスメデトミジンは外傷患者の挿管直後には効果が長く、長時間作用型NMBAの影響下にある患者に対して十分な深度の鎮静を提供しないため、あまり理想的ではありません。
プロポフォールとデキスメデトミジンの両方が低血圧および徐脈の原因とされています。外傷患者室でプロポフォールと標準用量(≤0.7 mcg/kg/hr)および高用量(>0.7 mcg/kg/hr)デクスメデトミジンを比較した研究では、高用量デキスメデトミジンの点滴がICUでのLOS増加、低血圧の増加、鎮痛剤、鎮静剤、抗精神病薬の使用増加と関連していることが明らかになりました。42、43 特にTBI患者において、Pajoumandらはデキスメデトミジン単独療法を受けた患者が、デクスメデトミジン-プロポフォールまたは単剤療法と比較して入院後最初の2日間の平均最大ICPが高いことを示しました。これは、目標レベルの鎮静時間が長くなってものことでした。しかし 、より最近の研究では、ICUでデキスメデトミジンを投与した患者はプロポフォールに比べて目標鎮静レベルで過ごす時間が有意に長く、両群とも目標>90%の時間であったにもかかわらず、43 プロポフォールは適切な鎮痛に加えて、特にICP管理が必要な外傷患者の治療初期においてより望ましい鎮静剤となる可能性があります。
低血圧の外傷患者における即時鎮静の代替としてミダゾラムがあります。ミダゾラムは短時間作用型ベンゾジアゼピンで、静脈注射で3〜5分以内に発症し、成人では30〜60分、小児では15〜30分で効果がピークを迎えます。44 比較的中立的な血行動態効果があります。一般的な戦略の一つは、外傷検査や画像検査中にミダゾラムを断続的に投与し、ICUに移送後は推奨される連続点滴鎮静剤に切り替えることです。45
RSI前治療、誘発分娩、麻痺、挿管後の鎮静には多くの薬剤選択肢があります。外傷患者のための薬剤の選択は、症状の多さ、利用可能な病歴、血行動態プロファイル、望む戦略によって異なります。長期作用型NMBAがRSIに選ばれ逆転しない場合、麻痺による認識を避けるために経験的鎮静を開始することが重要です。
レベル1
-
- 以下の特徴を持つ外傷患者に適応症が見られます:
- 気道閉塞
- 低換気
- サプリメントO2にもかかわらず持続的な低酸素血症(SaO2 </90%)
- 重度の認知障害(GCS </8)
- 重度の出血性ショック
- 心停止
- 煙を吸い込むことおよび以下のいずれかの特徴を持つ患者に適応:
- 気道閉塞
- 重度の認知障害(GCS </8)
- 重度の皮膚火傷(>/40%)
- 重大な火傷および/または煙の吸入で、最終的な治療への搬送時間が長期間予想される場合、
- 気道閉塞の差し迫った症状は以下の通りです:
- 中等度から重度の顔面火傷
- 中等度から重度の口咽頭火傷、
- 内視鏡検査で中等度から重度の気道損傷が確認されました。
- 以下の特徴を持つ外傷患者に適応症が見られます:
レベル2—推奨なし
レベル3
-
- 以下の特徴を持つ外傷患者では挿管が適応となることがあります:
- 気道閉塞の可能性がある顔面または首の怪我。
- 中等度の認知障害(GCSスコア>9–12)。
- 薬理学的薬剤に対して持続的な抵抗性。
- 呼吸困難(低酸素症や低換気なし)。
- 以下の特徴を持つ外傷患者では挿管が適応となることがあります:
表2。 前治療、誘発、麻痺、挿管後鎮静に用いられる薬剤の特性
| 名称 | 用量 | 通常用量(成人用) | 行動の開始 | 訴訟期間 | 真珠 | 禁忌・警告 |
| フェンタニル(前治療) |
1〜3 mcg/kg |
100–200 mcg |
ラピッド | 30〜60分 | 交感神経サージに耐えられない患者を考えてみてください | 無呼吸を防ぐために>30〜60秒投与してください |
| アトロピン | 0.02 mg/kg | 0.5mg | ラピッド | 4分 |
小児患者<1歳またはスクシニルコリン投与中; RSI前または2回目のサクシニルコリン投与を受けた思春期・成人患者 |
|
| リドカイン |
1–1.5 mg/kg | 100mg | <1分 | 10〜20分 | 時間が許せば、誘導剤の3分前に投与してください | 肝機能障害の長期滞在 |
| エトミダテ | 0.3 mg/kg | 20mg | <1分 | 3〜5分 | 規制薬物ではありません | 管理期間中に燃え上がるかもしれません |
| ケタミン | 1〜2 mg/kg | 100〜200mg | 30秒 | 5〜10分(用量依存) | カテコールアミン不足患者の用量を減らす | 無呼吸を防ぐために>60秒を投与してください |
| プロポフォール(誘導療法) | 1.5〜2.5 mg/kg | 100〜200mg | ラピッド | 5分 | 血行動態が安定し、ICPが上昇している患者を考慮してください | 管理期間中に燃え上がるかもしれません |
| ミダゾラム(誘導投与) | 0.2〜0.3 mg/kg | 15〜20mg | 最大5分 | <2時間 | 発病時間を短縮するためにフェンタニルと併用する | |
| スクシニルコリン | 1.5 mg/kg | 100mg | 45秒 | 6〜10分 | 筋肉神経脱神経疾患、悪性高体温症、症状性高カリウム血症 | |
| ロクロニウム | 1.2 mg/kg | 80〜100mg | 60秒 | 40〜90分 | 用量依存の発症および作用時間(用量が高いほど=早く現れる+持続時間が長くなる) | 肝機能障害の長期滞在 |
| ベクロニウム | 0.08–0.1 mg/kg | 8〜10mg | 2〜3分 | 60〜80分 | 再編成が必要 | |
| フェンタニル輸液(挿管後) | 25〜300 mcg/hr |
初期:50–100mcgボーラス+。 |
ラピッド | 連続点滴後の延長 | ||
| 挿管後のプロポフォール点滴 | 5〜50mcg/kg/min | 初期:10–20 mcg/kg/min | ラピッド | 連続点滴後10〜15分 | 肥満患者には理想的な体重を使うことを検討してください | 低血圧 |
| デクスメデトミジン点滴(挿管後) | 0.2–1.4 mcg/kg/min | 初期:0.2–0.5 mcg/kg/min | 5〜10分 | 連続点滴後60〜240分 | 徐脈、低血圧 | |
| ミダゾラム(挿管後) |
IVP:1–5 mg 1/30分 PRN 点滴:1–10 mg/時間 |
初期:1–5mgボーラス+。 |
2〜5分 | 肥満期間や継続点滴後の長期投与 |
可能な限りIVPのPRNを活用してください。 ICUのLOS増加に関連する点滴 |
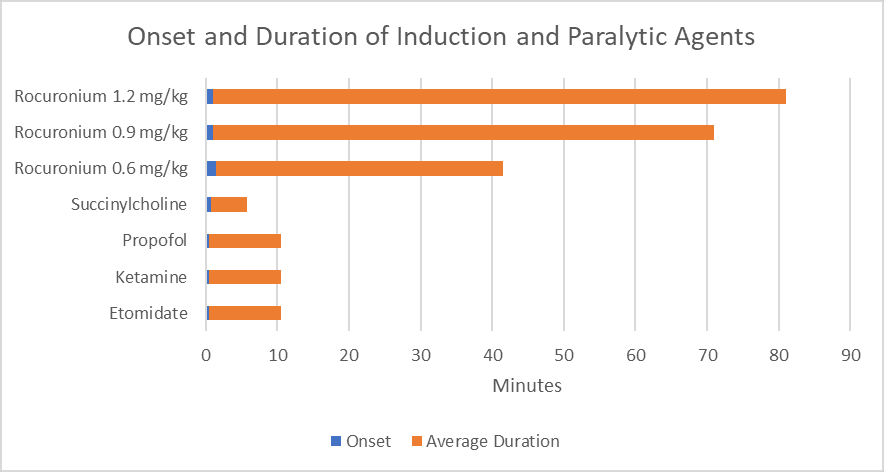 図1。誘発剤および麻痺剤の発症および持続時間。
図1。誘発剤および麻痺剤の発症および持続時間。
References
- Stollings JL、Diedrich DA、Oyen LJ、Brown Dr. Rapid-sequence挿管:薬剤選択時のプロセスと考慮事項のレビュー。 アン・ファーマカサー。2014;48(1):62-76. doi:10.1177/1060028013510488。
- Shafique MA、Haseeb A、Asghar B、Kumar A、Chaudhry ER、Mustafa MS. 病院前気道管理が重度の外傷性脳損傷に与える影響の評価:系統的レビューおよびメタアナリシス。 私は緊急医療です。2024;78:188-195. doi:10.1016/j.ajem.2024.01.030.
- Hampton JP, Hommer K, Musselman M, Bilhimer M. 迅速シーケンス挿管と救急医療薬剤師の役割:2022年更新。 Am Health Syst Pharm。2023年2月15日;80(4):182-195. DOI:10.1093/AJHP/ZXAC326。
- スコット・JA、ハードSO、ザヤルズニーM、ウォルツJM。重篤疾患における気道管理:最新情報。 胸。2020;157(4):877-887. doi:10.1016/j.chest.2019.10.026。
- コヴァチッチ(NJ)、ネルソンAC、マコーミックT、コーチャー(KA)。救急部門における小児急促挿管における徐脈の発生率およびアトロピンの使用。 小児緊急ケア。2022;38巻2号:e540-e543。 doi:10.1097/PEC.000000000002382.
- フェンタニルシトレートのパッケージ添付箋。イリノイ州レイクフォレスト:アコーン社;2012.
- サキニルコリン塩化物パッケージ添付箋。ニュージャージー州バークレーハイツ:ヒクマ・ファーマシューティカルズUSA Inc;2021.
- トプジアンAA、レイモンドTT、アトキンスDら;小児基礎および高度生命維持協力者。パート4:小児基礎・高度生命維持 2020年 アメリカ心臓協会の心肺蘇生および緊急心血管ケアガイドライン。 小児科。2021年1月;147(Suppl 1):e2020038505D。 doi:10.1542/peds.2020-038505D。
- エイサ・L、パッシ・Y、レルマン・J、ラチカ・M、ハードC。少量のアトロピン(<0.1 mg)が幼児の徐脈を引き起こすのでしょうか? 大人よ。2015;100(7):684-688. doi:10.1136/archdischild-2014-307868。
- 黄 WC、ヤン・AS、蔡 DH、シャオ SC、リン SJ、ライ EC。最近増加した抗コリン作動負荷と急性心血管イベントのリスクとの関連:全国的な症例・症例・時間・対照研究。 BMJ。2023;382:e076045。2023年9月27日公開。 DOI:10.1136/BMJ-2023-076045。
- エングストロムK、ブラウンCS、マットソンAE、ライオンズN、レチマサチューセッツ。救急部門における迅速シーケンス挿管のための薬物療法最適化。 私は緊急医療です。2023;70:19-29. doi:10.1016/j.ajem.2023.05.004.
- リン・CC、余JH、リン・CC、李WC、ウェン・YM、チェン・シー。重度の外傷性脳損傷における静脈内リドカインの挿管後血行動態的影響。 私は緊急医療です。2012;30(9):1782-1787. doi:10.1016/j.ajem.2012.02.013.
- クレイマー・N、レボウィッツ・D、ウォルシュ・M、ガンティ・L。外傷性脳損傷成人における迅速シーケンス挿管。 キュレウス。2018;10巻4号:e2530。2018年4月25日公開。 doi:10.7759/cureus.2530。
- エイプリルMD、アラナA、パリンDJほか。サクシニルコリンとロクロニウムの救急外来挿管成功:国立緊急気道登録研究所の研究。 アン・エマーグ・メッド。2018;72(6):645-653. DOI:10.1016/J.AnnemergMed.2018.03.042.
- アップチャーチ・CP、グリハルバ・CG、ラス・S他。成人外傷患者の急速シーケンス挿管時の誘発におけるエトミデートとケタミンの比較。 アン・エマーグ・メッド。2017;69巻1号:24-33.e2。 DOI:10.1016/J.AnnemergMed.2016.08.009.
- エトミダテの添付文書。イリノイ州レイクフォレスト:ホスピラ社;2017.
- モーアNM、ペイプSG、ルンデD、カジAH、ウォールズRM、ブラウンCA III。エトミデートの使用は救急外来の敗血症挿管においてケタミンよりも低血圧と関連しています:NEARコホート研究。 アカド・エマーグ・メッド。2020;27(11):1140-1149. doi:10.1111/acem.14070。
- ケタミンの添付文書。チェスナット・ライド(ニューヨーク州):パー・ファーマシューティカル;2017.
- ディートリッヒSK、ミクソンMA、ロゴシェフスキRJら。外傷を負った患者における急速シーケンス挿管誘導におけるプロポフォールの血行動態的効果。 外科です。2018;84(9):1504-1508.
- 大豆アレルギーおよび卵アレルギーの患者は安全に麻酔を受けることができます。アメリカアレルギー喘息免疫学会。2020年9月28日更新。2022年4月22日アクセス。入手可能: https://www.aaaai.org/Tools-for-the-Public/Conditions-Library/Allergies/soy-egg-anesthesia。
- Brown, CA et al. (2017) 『緊急気道管理の壁マニュアル』。フィラデルフィア:ウォルターズ・クルーワー。
- Rogachov A, Kitzerow C, Peterson J, Walker J. 外傷患者におけるスクシニルコリン使用後の高カリウム血症誘発性心停止および回復の疑い。 カンザス大学ジャーナル・メディカル。2023;16:299-301.2023年11月30日公開。 DOI:10.17161/KJM.vol16.21009。
- ストラチャン J、フリーゼ M. スクシニルコリン後の生命を脅かす高カリ血症。 ランセット。2020;395(10219):e9。 doi:10.1016/S0140-6736(19)32493-6。
- パタンワラAE、アースタッドBL、ローDJ、サクルズJC。スキニルコリンは、救急外来で重度脳損傷患者の急促配列挿管に使用される際に死亡率の増加と関連しています。 薬物療法。2016;36(1):57-63. DOI:10.1002/PHAR.1683。
- ロクロニウム・ブロマイドのパッケージインサート。イリノイ州ディアフィールド:バクスター・ヘルスケア・コーポレーション;2019.
- Vested M、Pape P、Kristensen CMら。ロクロニウム0.3または0.9 mg/kgを80歳以上の患者における発症時期、作用期間、挿管状態を比較:ランダム化研究。 Acta Anaesthesiol scand。2022;66(7):811-817. DOI:10.1111/AAS.14097。
- レビン(ニューメキシコ州)、フィックスML、エイプリルMD、アラナAA、ブラウン(カリフォルニア州)3位;NEAR捜査官たち。成人救急外来患者におけるロクロニウム投与量と初回挿管成功率の関連。 CJEM。2021;23(4):518-527. DOI:10.1007/S43678-021-00119-6。
- コリネクJD、トーマスRM、ゴダードLA、セントジョンAE、サクルスJC、パタンワラAE。救急外来における挿管後の鎮静剤および鎮痛剤投与におけるロクロニウムとスクシニルコリンの比較。 Eur J Emerg Med.2014;21(3):206-211. doi:10.1097/MEJ.0b013e3283606b89.
- ジョンソン EG、マイヤー A、シラクバリ A、ウェアント K、ベイカー ジャスティス S. ロクロニウムおよびスクシニルコリンが迅速配列挿管後の鎮静開始に与える影響。 J Emerg Med。2015;49(1):43-49. doi:10.1016/j.jemermed.2014.12.028.
- ネオスチグミンの添付書。ニュージャージー州プリンストン:Dr. Reddy's Laboratories, Inc.;2021.
- BRIDION(sugammadex)パッケージ添付。ホワイトハウス・ステーション(ニュージャージー州):メルク・シャープ&ドーム社;2021.
- ベクロニウム臭化物パッケージ添付箋。レイクズーリッヒ(イリノイ州):フレゼニウス・カビ;2019.
- NIMBEX(シサトラクリウム・ベシルレート)パッケージ添付書。イリノイ州ノースシカゴ:アビ社;2019.
- パッパルRD、ロバーツBW、モーアNM他。ED-AWARENESS研究:救急部門から入院した機械的人工呼吸患者の麻痺に対する意識に関する前向き観察コホート研究。 アン・エマーグ・メッド。2021;77(5):532-544. DOI:10.1016/J.AnnemergMed.2020.10.012.
- デヴリン JW、スクロビク Y、ジェリナス C ほかICUにおける成人患者の痛み、興奮・鎮静、せん妄、不動、睡眠障害の予防と管理に関する臨床実践ガイドライン。 クリットケアメッド。2018;46巻(9):e825-e873。 doi:10.1097/CCM.0000000000003299.
- チェ・L、フェレル BA、ヴァシレフスキス 電気工学 他重症患者におけるフェンタニルの集団薬理動態。 クリットケアメッド。2016;44(1):64-72. doi:10.1097/CCM.0000000000001347。
- Mondardini MC、Sperotto F、Daverio M、Amigoni A. 重症小児患者における鎮痛と鎮静:最近のガイドラインと視点からの最新情報。 Eur J Pediatr。2023;182(5):2013-2026. DOI:10.1007/S00431-023-04905-5。
- 蘇怡、ロックウッドC、ツォウYC、穆PF、廖SC、チェンWC。呼吸集中治療室におけるリッチモンド攪動鎮静尺度の実施:ベストプラクティスの実施プロジェクト。 JBIデータベースシステム リビジョン実装代表2019;17(8):1717-1726. doi:10.11124/JBISRIR-2017-004011。
- マサチューセッツ州ハウスブルク、バントンKL、ローマンPEなど。プロポフォールが虚血再灌流および外傷性脳損傷に与える影響。 Jクリットケア。2020;56:281-287. doi:10.1016/j.jcrc.2019.12.021.
- プロポフォール注射パッケージ添付。ユタ州レヒ:シビカ社;2020.
- シアリンAE、パタンワラAE、タンA、アースタッドBL。外傷患者におけるプロポフォールに関連する低血圧の予測因子。J トラウマナーズ。2014;21(1):4-8.doi:10.1097/JTN.0000000000000022.
- パジュマンM、クフェラJA、ボンズBWら。外傷性脳損傷患者の鎮静補助としてデクスメデトミジン。 J トラウマ急性期外科。2016;81(2):345-351. doi:10.1097/TA.000000000000001069。
- ウィニングスNA、デイリーBJ、ボリグRW他。重症外傷および外科患者における長期鎮静におけるデキスメデトミジンとプロポフォールの比較。 外科医。2021;19(3):129-134. DOI:10.1016/j.Surge.2020.04.003.
- ミダゾラム塩酸塩注射パッケージ添付箋。イリノイ州レイクフォレスト:ホスピラ社;2021.
- アクイストNM、モジアーJM、ビットナーEAらも含まれます。重症成人患者における迅速なシーケンス挿管に関する臨床実践ガイドライン。 クリットケアメッド。2023;51(10):1411-1430. doi:10.1097/CCM.0000000000006000。
- ツァイラーFA、タイテルバウムJ、ウェストM、ギルマンLM。外傷性脳損傷におけるケタミンがICPに与える影響。 ニューロクリットケア。2014;21(1):163-173. DOI:10.1007/S12028-013-9950-Y。
- ロガー:サイ、コエダム、TWA、ジャンナコプロス、GF、ヴァンデワレE、エルウテマンM、ズイデマWP。鈍的外傷患者における血行動態安定性の定義:オランダの外傷チームメンバーを対象とした体系的レビューと評価。 Eur J Trauma Emerg Surg。2017;43(6):823-833. DOI:10.1007/S00068-016-0744-8。
Cite this article
Ko CL, Celmins L. 外傷患者における迅速シーケンス挿管(RSI)気道管理のための薬理学。 J Med Insight。 2024;2024(299.11). doi:10.24296/jomi/299.11.

