Pharmakologie für die schnelle Sequenzintubation (RSI) Atemwegsmanagement bei Traumapatienten
Main Text
Table of Contents
Die primäre Befragung eines jeden Traumapatienten beginnt mit dem ABC: Atemwege, Atmung, Kreislauf. Wenn davon ausgegangen wird, dass der Patient eine Atemwegskontrolle benötigt, kann eine endotracheale Intubation mittels Schnellsequenz-Intubation (RSI) durchgeführt werden. Bei der RSI werden ein Induktionsmittel und ein schnell wirkender neuromuskulärer Blocker (NMBA oder paralytisch) verabreicht und die Intubation durchgeführt, sobald Bewusstlosigkeit und Lähmung erreicht sind. 1 Traumapatienten können aus einer Reihe von Gründen eine Intubation benötigen (Tabelle 1), einschließlich, aber nicht beschränkt auf Hypoxie, Hypoventilation, mögliche Verschlechterung des klinischen Status oder mangelnde Aufrechterhaltung oder Schutz der Atemwege aufgrund eines veränderten psychischen Zustands oder einer Verletzung des Kopfes oder Halses. 2 Historisch wurde RSI als eine Reihe von "sieben P's" beschrieben: (1) Vorbereitung, (2) Präoxygenierung, (3) Vorbehandlung, (4) Lähmung mit Induktion, (5) Schutz und Positionierung, (6) Platzierung des Schlauchs in der Luftröhre und (7) Postintubationsmanagement. 3 In dieser Übersichtsarbeit konzentrieren wir uns auf die Pharmakologie, Dosierung und andere Überlegungen zur Verwendung gängiger Medikamente zur Vorbehandlung, bei Lähmungen bei Induktion und nach der Intubation bei Traumapatienten.
Während der endotrachealen Intubation kann es zu einer Stimulation sowohl des Sympathikus als auch des Parasympathikus in den Atemwegen kommen. Die sympathische Stimulation kann zu einer Erhöhung der Herzfrequenz um bis zu 30 Schläge pro Minute und einem Anstieg des mittleren arteriellen Drucks (MAP) von etwa 25–50 mmHg führen, was zu einem Anstieg des intrakraniellen Drucks (ICP) beitragen kann. 4 Umgekehrt können pädiatrische Patienten Bradykardie durch parasympathische Stimulation aufgrund von Hypoxie oder direkte vagale Stimulation durch Manipulation des Laryngopharynx während der Intubation entwickeln. 5 Darüber hinaus stimuliert der physische Akt des Platzierens des Endotrachealtubus auch die Reflexe der oberen Atemwege, was zu Husten, Laryngospasmus und Bronchospasmus der unteren Atemwege führt, was ebenfalls zu einem Anstieg des ICP beitragen kann. 3 Das Ziel der Vorbehandlung ist es, diese physiologischen Reaktionen zu mildern.
Fentanyl kann verwendet werden, um die sympathische Reaktion auf die Intubation abzuschwächen. Erwägen Sie eine Vorbehandlung mit Fentanyl bei Patienten, die das größte Risiko für Schäden durch erhöhte Herzfrequenz, Blutdruck oder ICP haben. Zu diesen Patienten gehören Patienten mit erhöhtem ICP (mit oder ohne intrakranielle Blutung), bekanntem oder vermutetem Hirn- oder Aortenaneurysma oder großer Gefäßdissektion. 3 Vermeiden Sie eine Fentanyl-Vorbehandlung bei Patienten, die auf einen Sympathikusantrieb angewiesen sind, um ihr Herzzeitvolumen aufrechtzuerhalten, z. B. bei Patienten mit dekompensiertem Schock oder hämodynamisch instabil. Der Wirkungseintritt von Fentanyl ist nahezu augenblicklich und die Wirkungsdauer beträgt etwa 30–60 Minuten. 6 Fentanyl sollte etwa drei Minuten vor der Induktionsgabe in einer Dosis von 1–3 μg/kg i.v. verabreicht werden. Die Dosis vor der Behandlung sollte über 30–60 Sekunden verabreicht werden, um eine steile Atemdepression zu vermeiden. Höhere Dosen (5–10 μg/kg) Fentanyl wurden mit der Verursachung von übermäßiger Hypotonie, Apnoe und Steifheit der Brustwand in Verbindung gebracht. 4
Der Begriff "hämodynamische Instabilität" wird in der Literatur ohne vollständigen allgemeinen Konsens verwendet. Verschiedene Autoren verwenden unterschiedliche Kriterien, um hämodynamische Instabilität zu definieren. Zu diesen Kriterien gehören am häufigsten Störungen der Herzfrequenz, des systolischen Blutdrucks und der Atemfrequenz. Die Grenzwerte variieren ebenfalls, wobei die durchschnittlichen Werte bei >103 Schlägen pro Minute, <96 mmHg und <34 Atemzügen pro Minute liegen. 47
Atropin kann als Prämedikation für Patienten verwendet werden, die vor der Intubation bradykard sind oder bei denen das Risiko besteht, dass sie während der Intubation aufgrund einer vagalen Stimulation oder der Einnahme von Succinylcholin bradykard werden. Succinylcholin hat aufgrund seiner Wirkung auf Muskarinrezeptoren das Potenzial, Bradykardie zu verursachen oder zu verschlimmern. Die Inzidenz und der Schweregrad dieser Bradykardie ist bei Kindern häufiger als bei Erwachsenen. 7 In den PALS-Leitlinien von 2020 heißt es, dass es "vernünftig sein kann", Atropin als Prämedikation für die Intubation zu verwenden, um Bradykardie bei Hochrisikopatienten zu verhindern, wie z. B. bei Patienten unter einem Jahr oder bei Patienten, die Succinylcholin erhalten. 8 Erwägen Sie die Verabreichung von Atropin bei erwachsenen und jugendlichen Patienten, die eine zweite Dosis Succinylcholin erhalten. Die Dosis von Atropin zur Vorbeugung von Bradykardie beträgt 0,02 mg/kg (Höchstdosis 0,5 mg). 8, 9 Die Auswirkungen von Atropin auf die Herzfrequenz sind bei intravenöser Verabreichung nahezu sofort und halten bis zu vier Minuten an. 10
Lidocain wurde verwendet, um die Hustenreaktion auf die Intubation und ihre Wirkung auf die Hämodynamik und den ICP abzuschwächen. 3, 4 Die Bedeutung des Effekts ist unbekannt – es wurden keine Studien veröffentlicht, die die Auswirkungen von Lidocain und Intubation auf ICP oder patientenzentrierte Ergebnisse bewerten. 11 Eine Studie fand keinen Unterschied in der Hämodynamik bei Patienten mit schwerem Schädel-Hirn-Trauma (TBI), unabhängig davon, ob sie vor der Intubation intravenöses Lidocain erhielten oder nicht. 12 Derzeit wird eine Vorbehandlung mit Lidocain nicht empfohlen. 11, 13 Wenn Lidocain zur Vorbehandlung verwendet wird, beträgt die typische Dosis 1,5 mg/kg, die drei Minuten vor der Induktion verabreicht wird. 3 Bei dieser Dosis beträgt der Wirkungseintritt von Lidocain weniger als eine Minute und die Wirkungsdauer 10–20 Minuten. Lidocain wird von der Leber metabolisiert und die Dauer kann bei Patienten mit signifikanter Leberfunktionsstörung verdoppelt werden.
Das Ziel der Induktion ist es, den Patienten schnell in einen Zustand der Vollnarkose zu sedieren, was die Verabreichung von Lähmungsmitteln ermöglicht und die Bedingungen für eine ideale Intubation erleichtert. Das optimale Induktionsmittel sorgt für einen reibungslosen und schnellen Beginn der Sedierung und bietet gleichzeitig Amnesie und Analgesie. Dieses ideale Mittel wäre hämodynamisch neutral, sofort reversibel und hätte minimale Nebenwirkungen. 1 Obwohl kein einzelner Wirkstoff alle diese Eigenschaften umfasst, bestimmen patientenspezifische Faktoren die Auswahl des am besten geeigneten Induktionsmittels für das klinische Szenario. Ein 2016 veröffentlichtes Register von Intubationen in der US-Notaufnahme ergab, dass Etomidat das am häufigsten verwendete Induktionsmittel für RSI ist, gefolgt von Ketamin und Propofol. 14
Etomidat ist ein nicht-Barbiturat-Hypnotikum, das eine schnelle Sedierung ohne Analgesie ermöglicht, indem es die Wirkung von GABA verstärkt. Die Beliebtheit von Etomidat ist auf sein stabiles hämodynamisches Profil und sein Potenzial zur Senkung des ICP sowie auf seine zuverlässigen pharmakokinetischen und pharmakodynamischen Wirkungen zurückzuführen. 3, 4 Einzeldosen von Etomidat sind jedoch mit einer Nebennierensuppression verbunden.
Die klinische Bedeutung dieses Problems über die Sepsis hinaus wurde diskutiert, aber eine Studie, in der Etomidat mit Ketamin zur Induktion bei Traumapatienten verglichen wurde, fand keinen Unterschied in der Sterblichkeitsrate, den intensivstationsfreien Tagen oder den beatmungsfreien Tagen. 15 Ärzte müssen die Vorteile einer schnellen Induktion und hämodynamischen Stabilität durch Etomidat gegen die potenziellen Risiken einer Nebennierensuppression abwägen. Alternative Wirkstoffe wie Ketamin oder Propofol können in Betracht gezogen werden, insbesondere bei Patienten mit höherem Risiko für Nebenniereninsuffizienz (z. B. Patienten mit Sepsis oder chronischen Erkrankungen). Obwohl Etomidat ein wertvolles Mittel bleibt, erfordert seine Verwendung eine sorgfältige Überlegung. Ein ausgewogener Ansatz, der sich am Zustand des Patienten orientiert, ist von entscheidender Bedeutung. Nr. 46
Ein deutlicher Vorteil von Etomidat gegenüber anderen Induktionsmitteln besteht darin, dass es sich nicht um eine kontrollierte Substanz handelt und daher keine zusätzliche Dokumentation während der Lagerung oder Verschwendung von nicht verwendeten Medikamenten erforderlich ist. Die Dosis von Etomidat für RSI beträgt 0,3 mg/kg. Der Wirkungseintritt beträgt weniger als eine Minute und die Wirkungsdauer drei bis fünf Minuten. 16
Die Verwendung von Ketamin zur Induktion hat aufgrund seines günstigen hämodynamischen Profils und als Reaktion auf die Besorgnis über eine Nebennierensuppression mit Etomidat an Popularität gewonnen. Ketamin ist ein NMDA-Rezeptor-Antagonist, der eine schnelle Sedierung, Analgesie und Amnesie ermöglicht. Interessanterweise hat Ketamin indirekte sympathomimetische Wirkungen, indem es die Wiederaufnahme endogener Katecholamine hemmt, was zu einer erhöhten Herzfrequenz und einem erhöhten Blutdruck führt. 15 Ketamin hat jedoch auch direkte myokardiale depressive Wirkungen, die bei Patienten mit Katecholamin-Depletation ausgeprägter sein können. 15 Obwohl es Bedenken gibt, dass die myokardiale Depression die sympathomimetischen Wirkungen bei kritisch kranken septischen Patienten überwiegen könnte, hat sich dieser Befund nicht gehalten, wenn man sich speziell mit der Verwendung von Ketamin bei RSI bei Traumapatienten befasst. 15, 17 In der Vergangenheit wurde Ketamin bei Patienten mit erhöhtem Augeninnendruck (IOD) oder ICP vermieden. Aktuelle Erkenntnisse deuten jedoch darauf hin, dass Ketamin den ICP bei Patienten mit einem schweren SHT, die sediert und beatmet werden (Oxford Level 2b, GRADE C), nicht erhöht. In bestimmten Fällen kann es sogar den ICP senken. 46 Die Induktionsdosis von Ketamin beträgt 1–2 mg/kg mit einem Wirkungseintritt von etwa 30 Sekunden und einer dosisabhängigen Sedierungsdauer von fünf bis zehn Minuten. 18 Zu beachten ist, dass eine schnelle Verabreichung von Ketamin über weniger als 60 Sekunden zu Apnoe führen kann, so dass das Timing bei der Erleichterung der Intubation unerlässlich ist.
Zu den weniger gebräuchlichen Mitteln für die RSI-Induktion gehören Propofol und Midazolam. Propofol ist ein hoch fettlöslicher GABA-Agonist mit einem schnellen Sedierungsbeginn. 1 Bolusdosen von Propofol verringern jedoch die MAP durch Verringerung der Vor- und Nachlast und verminderte Kontraktilität. 3 Diese Eigenschaften tragen dazu bei, dass Propofol den ICP senken kann, so dass Propofol bei hämodynamisch stabilen oder hypertensiven Patienten mit erhöhtem ICP eine vernünftige Option sein kann. Im Vergleich zur Nicht-Propofol-Induktion (Etomidat oder Midazolam) ergab eine Studie, dass Propofol nach Berücksichtigung des Alters, des Schweregrads der Verletzung und der Prä-RSI-Hypotonie bei traumatisch verletzten Patienten fast viermal so wahrscheinlich eine Hypotonie nach der Intubation verursachte. 19 Während Propofol in einer Emulsion mit Sojaöl und Ei-Lecithin formuliert ist, gibt die American Academy of Allergy Asthma & Immunology an, dass Patienten mit Soja- oder Eiallergien Propofol ohne besondere Vorsichtsmaßnahmen erhalten können. 20 Die Dosis von Propofol zur Induktion beträgt 1,5–2,5 mg/kg, mit Dosisreduktionen für hämodynamisch instabile Patienten. 1, 3Midazolam wird aufgrund seines langsameren Wirkungseintritts (bis zu fünf Minuten) und seines unzuverlässigen Sedierungsniveaus selten als einziges Induktionsmittel für RSI verwendet. 1 Die Wirkungseintrittszeit kann durch die gleichzeitige Verabreichung von Fentanyl auf 90 Sekunden verbessert werden. Die Induktionsdosis von Midazolam beträgt 0,2-0,3 mg/kg. 1, 3 Anbieter sind möglicherweise mit der Verabreichung großer Dosen von Midazolam nicht vertraut und fühlen sich unwohl und benötigen möglicherweise die Gewissheit, dass diese Dosen indiziert sind, um das für die Amnesie erforderliche Sedierungsniveau zu gewährleisten und die Intubationsbedingungen zu optimieren. Midazolam zeigt eine dosisabhängige Abnahme des systemischen Gefäßwiderstands und der Myokarddepression und sollte bei Patienten mit hämodynamischer Instabilität mit Vorsicht angewendet werden. 1 Die Anwendung von Midazolam zur Induktion sollte Patienten mit bestimmten Indikationen (Krampfanfällen) vorbehalten sein oder wenn andere Wirkstoffe aufgrund von Medikamentenengpässen nicht verfügbar sind.
Succinylcholin, ein depolarisierendes neuromuskuläres Blockierungsmittel, hat einen schnellen Wirkungseintritt und eine kurze Wirkungsdauer. Diese Eigenschaften machen es ideal für den Einsatz in der RSI bei Traumapatienten. Es ermöglicht eine genaue Beurteilung des Sedierungsniveaus nach der Intubation und ist besonders ideal, wenn Bedenken hinsichtlich schwieriger Atemwege bestehen oder kurz nach der Intubation eine genaue neurologische Beurteilung erforderlich ist. Bei einer Dosis von 1,5 mg/kg bewirkt es einen Wirkungseintritt innerhalb von 45 Sekunden und eine Dauer von 6–10 Minuten. 21
Es gibt jedoch einige Überlegungen, die die Anwendung bei bestimmten Patienten einschränken können. Erstens ist Succinylcholin bei Patienten mit einer persönlichen oder familiären Vorgeschichte von maligner Hyperthermie kontraindiziert. 7 Zweitens kann Succinylcholin bei einigen Patienten eine tiefgreifende Hyperkaliämie verursachen, die zu ventrikulären Arrhythmien und Herzstillstand führt. Bei den meisten Patienten führt Succinylcholin zu einem durchschnittlichen Anstieg des Serumkaliums um 0,3–1 mEq/L. 1, 22 Bei Patienten mit einer Prädisposition für Hyperkaliämie kann dieser Anstieg jedoch 5–10 mEq/L betragen, was zu ventrikulären Arrhythmien und Herzstillstand führen kann. 21, 23 Daher sollte Succinylcholin auch bei Patienten mit symptomatischer Hyperkaliämie, Nierenerkrankung im Endstadium, Rhabdomyolyse oder anderen Krankheiten, die eine ausgedehnte Denervierung der Skelettmuskulatur verursachen (z. B. Multiple Sklerose, Muskeldystrophie), vermieden werden. 1 Das Risiko einer Succinylcholin-induzierten tiefgreifenden Hyperkaliämie bei Quetschverletzungen, Denervierungsverletzungen oder Verbrennungen entwickelt sich nach der akuten Phase (ca. 3–5 Tage nach der Verletzung oder 7–10 Tage nach der Verbrennung), so dass es sicher ist, Succinylcholin bei einem ansonsten gesunden Patienten während der ersten 24–48 Stunden nach akuten Quetsch- oder Verbrennungsverletzungen zu verwenden. Es gibt auch eine Black-Box-Warnung vor akuter Rhabdomyolyse und Herzstillstand, wenn Succinylcholin bei pädiatrischen Patienten angewendet wird, bei denen später eine Skelettmuskelmyopathie (d. h. Duchenne-Muskeldystrophie) festgestellt wird. 7 Einige Zentren vermeiden Succinylcholin bei pädiatrischen Patienten ganz, um dieses Risiko zu vermeiden, obwohl die meisten immer noch den Einsatz für Notfallintubationen bei ansonsten gesunden Patienten in Betracht ziehen würden. Schließlich fand eine retrospektive Studie in einem Traumazentrum einen Zusammenhang zwischen dem Konsum von Succinylcholin und einer erhöhten Mortalität bei Patienten mit schwerem SHT,24 obwohl andere immer noch die Anwendung von Succinylcholin bei SHT empfahlen, wenn keine Kontraindikationen bestehen. 13
Im Rahmen eines modifizierten RSI erweist sich Rocuronium als einzige Alternative. Es ist bemerkenswert, dass die erforderliche Dosierung für diese Anwendung ungefähr doppelt so hoch ist wie die Standard-Induktionsdosis von Rocuronium.
Rocuronium, ein nicht-depolarisierendes neuromuskuläres Aminosteroid-Blockierungsmittel, hat bei Dosen von 1 mg/kg einen Wirkungseintritt von etwa 1–2 Minuten. 25, 26 Höhere Dosen von ≥1,4 mg/kg waren in einer Studie des National Emergency Airway Registry mit einem verbesserten Erfolg beim ersten Versuch mit der direkten Laryngoskopie bei hypotensiven Patienten im Alter von ≥14 Jahren verbunden. 27 Die Dauer von Rocuronium hängt von der Dosis und der Leberfunktion ab. Bei üblichen intubierenden Dosen beträgt die Dauer etwa 40–90 Minuten, kann aber bei einigen Patienten bis zu 120 Minuten oder länger dauern. 25 Im Gegensatz zu Succinylcholin hat Rocuronium nur eine Kontraindikation – eine Anaphylaxie gegen Rocuronium oder andere NMBAs in der Vorgeschichte. So wird es oft bei Traumapatienten gewählt, bei denen die Anamnese unbekannt ist oder noch keine Laborwerte vorliegen.
Es gibt zwei Hauptnachteile von Rocuronium für Traumapatienten – beide als Folge seiner deutlich längeren Wirkungsdauer. Wie in der Sedierung nach der Intubation erörtert wird, ist es wahrscheinlicher, dass unzureichende Dosen oder ein verzögerter Beginn der Analgosedierung auftreten. 28, 29 Eine anhaltende Lähmung hemmt auch die Fähigkeit, eine neurologische Untersuchung zu erhalten. Es gibt Umkehrmittel für Rocuronium, aber diese bergen auch Risiken. Neostigmin, ein Cholinesterase-Hemmer, kann verabreicht werden, sobald der Patient eine gewisse neuromuskuläre Funktion wiedererlangt hat (d. h. ein Vierertraining von mindestens 2 von 4). 30 Ein Anticholinergikum wie Atropin oder Glycopyrrolat wird gleichzeitig verabreicht, um das Risiko einer Bradykardie aufgrund der Aktivierung des Muskarinrezeptors zu verringern. 21 Sugammadex ist ein neuartiges Cyclodextrin, das im Plasma an Rocuronium oder Vecuronium bindet und die effektive Menge an NMBA reduziert, die zur Bindung von Acetylcholinrezeptoren an der neuromuskulären Verbindung zur Verfügung steht. Sugammadex hat den Vorteil, dass es in der Lage ist, jeden Grad der neuromuskulären Blockade, einschließlich einer tiefen Blockade, rückgängig zu machen. Der Sugammadex-Rocuronium-Komplex wird renal gereinigt und wird aufgrund der verlängerten Elimination und des potenziellen Risikos einer Rebound-Lähmung nicht für die Anwendung bei Patienten mit einer Kreatinin-Clearance von < 30 ml/min empfohlen. 31 Sugammadex wurde auch mit Anaphylaxie, Bradykardie und Herzstillstand in Verbindung gebracht, so dass Vorsicht geboten ist. Sugammadex bindet und reduziert auch die Wirksamkeit der oralen oder nicht-oralen hormonellen Empfängnisverhütung für 7 Tage nach der Anwendung, was eine Backup-Verhütungsmethode erfordert. 31
Zwei weitere nicht-depolarisierende Mittel werden aufgrund ihrer pharmakokinetischen Eigenschaften nicht häufig für RSI verwendet. Vecuronium, ein Aminosteroid, hat einen Wirkungseintritt von 2–3 Minuten und eine Dauer von 60–80 Minuten bei einer Standarddosis von 0,08–0,1 mg/kg. 32 Darüber hinaus wird Vecuronium als Pulver geliefert, das rekonstituiert werden muss, wodurch der Prozess der Herstellung von Medikamenten bei einer dringenden Intubation um einen weiteren Schritt erweitert wird. Cisatracurium ist ein nicht depolarisierendes Benzylisochinolinium-NMBA mit einem Wirkungseintritt von 2–3 Minuten und einer Dauer von 55–80 Minuten bei einer intubierenden Dosis von 0,15 mg/kg und kann mit Sugammadex nicht rückgängig gemacht werden. 33 Es hat einen organunabhängigen Stoffwechsel durch Hofmann-Eliminierung. Beide Wirkstoffe könnten als Alternativen im Falle eines Medikamentenmangels an Rocuronium in Betracht gezogen werden, wobei der langsamere Wirkungseintritt zu berücksichtigen ist.
Sobald der Patient intubiert wurde, ist es unerlässlich, dass wir eine angemessene Analgesie und Sedierung für die Sicherheit und den Komfort unserer Patienten bereitstellen. Aufgrund der kürzeren Wirkungsdauer von Succinylcholin können wir das Schmerz- und Sedierungsniveau eines Patienten relativ schnell nach der Intubation genau beurteilen. Bei der Verwendung von Rocuronium für RSI wurde jedoch die Diskrepanz in der Dauer des Induktionsmittels im Vergleich zu einer Lähmung mit einer verzögerten oder unzureichenden Sedierung in Verbindung gebracht, wodurch der Patient dem Risiko einer Lähmung ausgesetzt ist. 26, 27 In einer kürzlich durchgeführten Studie wurde festgestellt, dass 2,6 % der Patienten, die in der Notaufnahme intubiert wurden, an Lähmungen litten, und es wurde festgestellt, dass dieses Risiko bei Rocuronium im Vergleich zu Succinylcholin signifikant höher war. 34
Die PADIS-Leitlinien von 2018 empfehlen eine protokollgesteuerte Analgosedierung zur Behandlung von Schmerzen und Unruhe, bei der ein Analgetikum (in der Regel ein Opioid) entweder vor einem Beruhigungsmittel oder anstelle eines Beruhigungsmittels verwendet wird. 35 In Anbetracht der Tatsache, dass Patienten in der Traumastation wahrscheinlich schmerzhafte Verletzungen erleiden, ist dieser Ansatz umsichtig. Darüber hinaus kann der Patient von der amnestischen Wirkung eines Beruhigungsmittels profitieren.
Es gibt mehrere Strategien zur Analgosedierung, aber Opiate bleiben die Hauptstütze der Therapie. Fentanyl wird oft aufgrund seines schnellen Wirkungseintritts, seiner neutralen hämodynamischen Wirkung und seiner kurzen Dauer gewählt, wenn es als einzelner Bolus verabreicht wird. Bei wiederholten Dosen oder einer kontinuierlichen Infusion zeigt Fentanyl eine Pharmakokinetik des Zwei-Kompartiment-Modells, was zu einer verlängerten Wirkungsdauer führt, insbesondere bei Patienten mit Herzinsuffizienz, Lebererkrankungen oder größerem Gewicht. 36 Die Verabreichung einer anfänglichen Bolusdosis, gefolgt von einer kontinuierlichen Infusion, ermöglicht schnellere Titrationen und gibt die Möglichkeit, weitere Bolusdosen über die Infusionspumpe zu verabreichen. Dies ist sowohl aus Sicherheitsgründen ideal als auch um die Notwendigkeit zu verringern, dass eine Krankenschwester oder ein Apotheker während des Rests der Traumabeurteilung und der bildgebenden Untersuchungen wiederholt zum automatischen Ausgabeschrank zurückkehren muss. Fentanyl-Infusionen sind in der Regel als vorgemischte kontinuierliche Infusionen erhältlich und können daher im Vergleich zu anderen Opiat-Infusionen in der Notaufnahme schneller zugänglich sein.
Wenn Succinylcholin für RSI verwendet wird, können Nachuntersuchungen des Schmerzniveaus und der Sedierung anhand von Standardskalen die Entscheidung beeinflussen, die Dosis von Fentanyl zu erhöhen oder ein Beruhigungsmittel hinzuzufügen. 37, 38 Wenn jedoch Rocuronium verwendet und nicht rückgängig gemacht wird, sind diese Skalen keine gültigen Bewertungen von Schmerzen und Sedierung. Daher ist es wichtig, anhand der Informationen aus der Erstvorstellung des Patienten festzustellen, ob zusätzlich zu Fentanyl empirisch mit einem Beruhigungsmittel begonnen werden sollte. Zum Beispiel wird bei einem Patienten, der anfänglich mit Methamphetamin oder Ethanol berauscht und berauscht ist, Propofol oder ein Benzodiazepin eine gewünschte pharmakologische Wirkung zur Bekämpfung der Vergiftung haben.
Die PADIS-Leitlinien von 2018 schlagen die Verwendung von Propofol oder Dexmedetomidin mit kontinuierlicher Infusion anstelle von Benzodiazepinen für die Sedierung von mechanisch beatmeten Patienten vor, da die Verweildauer auf der Intensivstation, die Dauer der mechanischen Beatmung und das Delir verkürzt sind. 35 Bei Verabreichung als kontinuierliche Infusion hat Propofol einen schnellen Wirkungseintritt und eine kurze Dauer der Sedierung, was ideal ist, wenn Unterbrechungen erforderlich sind, um den psychischen Zustand eines Patienten zu beurteilen. Propofol kann bei sedierten Patienten mit SHT aufgrund seiner inhärenten antioxidativen Eigenschaften sowie seines Potenzials, den zerebralen Sauerstoffverbrauch und den ICP zu reduzieren, neuroprotektiv wirken. 39, 40 Obwohl Hypotonie eine bekannte Nebenwirkung von Propofol ist, kann sie tiefgreifend sein. Eine Studie ergab, dass eine SBP-Abnahme um etwa 30 mmHg bei Traumapatienten über 55 Jahren, fettleibig und Patienten mit niedrigerem SBP zu Studienbeginn wahrscheinlicher war. 41 Erwägen Sie eine niedrigere anfängliche Propofol-Infusionsdosis und die Verwendung des idealen Körpergewichts für diese Patienten. Hypotonie kann zusätzlich zur ATLS-gesteuerten Wiederbelebung mit Flüssigkeiten und Blutprodukten entweder mit Push-Dosen oder kontinuierlichen Infusionsgefäßen gemildert werden.
Dexmedetomidin ist ein weiteres gängiges Beruhigungsmittel, ein Alpha-2-Agonist mit opiatsparenden Eigenschaften und ein bevorzugtes Mittel für die Sedierung auf der Intensivstation. 35 Dexmedetomidin ist jedoch in der unmittelbaren Zeit nach der Intubation bei einem Traumapatienten weniger ideal, da es einen längeren Wirkungseintritt aufweist und für einen Patienten, der unter den Auswirkungen einer lang wirkenden NMBA verbleibt, keine ausreichend tiefe Sedierung bietet.
Sowohl Propofol als auch Dexmedetomidin wurden mit der Entstehung von Hypotonie und Bradykardie in Verbindung gebracht. Eine Studie, in der Propofol mit Standarddosis (≤0,7 μg/kg/h) und hochdosiertem (>0,7 μg/kg/h) Dexmedetomidin auf der Trauma-Intensivstation verglichen wurde, ergab, dass hochdosierte Dexmedetomidin-Infusionen mit einer erhöhten LOS auf der Intensivstation, höheren Hypotonieraten und einem erhöhten Einsatz von Analgetika, Beruhigungsmitteln und Antipsychotika verbunden waren. 42, 43 Speziell bei SHT-Patienten zeigten Pajoumand und Kollegen, dass Patienten, die eine Dexmedetomidin-Monotherapie erhielten, in den ersten zwei Tagen nach der Aufnahme im Vergleich zu einer Dexmedetomidin-Propofol- oder Propofol-Monotherapie einen höheren mittleren maximalen ICP aufwiesen, obwohl die Zeit auf dem Zielniveau der Sedierung länger war. 42 Eine neuere Studie ergab jedoch, dass Patienten, die Dexmedetomidin erhielten, bei längerer Anwendung auf der Intensivstation im Vergleich zu Propofol signifikant mehr Zeit auf ihrem Zielniveau der Sedierung verbrachten, obwohl beide Gruppen >90 % der Zeit auf dem Zielwert lagen. 43 Propofol kann zusätzlich zu einer adäquaten Analgesie zu Beginn der Behandlung des Traumapatienten ein wünschenswerteres Beruhigungsmittel sein, insbesondere bei Patienten, die eine ICP-Behandlung erfordern.
Eine Alternative zur sofortigen Sedierung bei Patienten mit blutdrucksenkendem Trauma ist Midazolam. Midazolam ist ein kurzwirksames Benzodiazepin mit intravenösem Wirkungseintritt innerhalb von 3–5 Minuten und maximaler Wirkung nach 30–60 Minuten bei Erwachsenen und 15–30 Minuten bei der Pädiatrie. 44 Es hat relativ neutrale hämodynamische Wirkungen. Eine gängige Strategie besteht darin, Midazolam während der Traumauntersuchung und der bildgebenden Untersuchungen als intermittierende Boli zu dosieren und nach der Verlegung auf die Intensivstation zu einem bevorzugten Beruhigungsmittel mit kontinuierlicher Infusion überzugehen. 45
Es gibt viele Medikationsoptionen für die RSI-Vorbehandlung, Induktion, Lähmung und Sedierung nach der Intubation. Die Auswahl der Wirkstoffe für den Traumapatienten hängt von den vorliegenden Verletzungen, der verfügbaren Krankengeschichte, dem hämodynamischen Profil und der gewünschten Strategie ab. Wenn ein langwirksames NMBA für die RSI gewählt und nicht umgekehrt wird, ist es wichtig, eine empirische Analgosedierung zu beginnen, um ein Bewusstsein mit Lähmung zu vermeiden.
Tabelle 1. Indikationen für die Notfall-Trachealintubation2
Stufe 1
-
- Indiziert bei Traumapatienten mit den folgenden Merkmalen:
- Obstruktion der Atemwege
- Hypoventilation
- Persistierende Hypoxämie (SaO2 </ 90%) trotz Supplement O2
- Schwere kognitive Beeinträchtigung (GCS </8)
- Schwerer hämorrhagischer Schock
- Herzstillstand
- Indiziert für Patienten mit Rauchinhalation und einem der folgenden Merkmale:
- Obstruktion der Atemwege
- Schwere kognitive Beeinträchtigung (GCS </8)
- Schwere Hautverbrennungen (>/ 40%)
- Schwere Verbrennungen und/oder Rauchvergiftung mit einer zu erwartenden verlängerten Transportzeit bis zur endgültigen Behandlung und
- Drohende Obstruktion der Atemwege wie folgt:
- Mittelschwere bis schwere Verbrennungen im Gesicht
- Mittelschwere bis schwere oropharyngeale Verbrennungen und
- Mittelschwere bis schwere Atemwegsverletzung bei der Endoskopie.
- Indiziert bei Traumapatienten mit den folgenden Merkmalen:
Stufe 2 – Keine Empfehlungen
Stufe 3
-
- Eine Intubation kann bei Traumapatienten mit einem der folgenden Merkmale indiziert sein:
- Gesichts- oder Halsverletzung mit dem Potenzial für eine Obstruktion der Atemwege.
- Moderate kognitive Beeinträchtigung (GCS-Score >9–12).
- Anhaltende Kampfbereitschaft, refraktär gegenüber pharmakologischen Wirkstoffen.
- Atemnot (ohne Hypoxie oder Hypoventilation).
- Eine Intubation kann bei Traumapatienten mit einem der folgenden Merkmale indiziert sein:
Tabelle 2. Eigenschaften von Medikamenten, die zur Vorbehandlung, Induktion, Lähmung und Sedierung nach der Intubation verwendet werden
| Name | Dosis | Übliche Dosis (Erwachsene) | Beginn der Handlung | Dauer der Wirkung | Perlen | Kontraindikationen/Warnhinweise |
| Fentanyl (Vorbehandlung) |
1–3 μg/kg |
100–200 μg |
Schnell | 30–60 Minuten | Berücksichtigung bei Patienten, die einen sympathischen Anstieg nicht vertragen | Verabreichen Sie > 30–60 Sekunden, um Apnoe zu vermeiden |
| Atropin | 0,02 mg/kg | 0,5 mg | Schnell | 4 Minuten |
Pädiatrische Patienten <1 Jahr alt oder erhalten Succinylcholin; Jugendliche/Erwachsene Patienten, die vor der RSI bradykard sind oder die 2. Dosis von Succinylcholin erhalten haben |
|
| Lidocain |
1–1,5 mg/kg | 100 mg | <1 Minuten | 10–20 Minuten | 3 Minuten vor der Induktionsgabe geben, wenn die Zeit es erlaubt | Verlängerte Dauer bei Leberfunktionsstörungen |
| Etomidat | 0,3 mg/kg | 20 mg | <1 Minuten | 3–5 Minuten | Keine kontrollierte Substanz | Kann bei der Verabreichung brennen |
| Ketamin | 1–2 mg/kg | 100–200 mg | 30 Sek. | 5–10 min (dosisabhängig) | Reduzieren Sie die Dosis bei Patienten mit Katecholamin-Depletion | Verabreichen Sie >60 Sekunden, um Apnoe zu vermeiden |
| Propofol (Induktion) | 1,5–2,5 mg/kg | 100–200 mg | Schnell | 5 Minuten | Berücksichtigung bei hämodynamisch stabilen Patienten mit erhöhtem ICP | Kann bei der Verabreichung brennen |
| Midazolam (Induktion) | 0,2–0,3 mg/kg | 15–20 mg | bis zu 5 min | <2 Stunden | Gleichzeitige Verabreichung mit Fentanyl, um die Einwirkzeit zu verkürzen | |
| Succinylcholin | 1,5 mg/kg | 100 mg | 45 Sek. | 6–10 Minuten | Muskeldenervierende Erkrankungen, maligne Hyperthermie, symptomatische Hyperkaliämie | |
| Rocuronium | 1,2 mg/kg | 80–100 mg | 60 Sek. | 40–90 Minuten | Dosisabhängiger Wirkungseintritt und -dauer (höhere Dosis = schnellerer Wirkungseintritt + längere Dauer) | Verlängerte Dauer bei Leberfunktionsstörungen |
| Vecuronium | 0,08–0,1 mg/kg | 8-10 mg | 2–3 Minuten | 60–80 Minuten | Erfordert eine Rekonstitution | |
| Fentanyl-Infusion (nach der Intubation) | 25–300 μg/h |
Anfänglich: 50–100 μg Bolus + |
Schnell | Verlängert nach kontinuierlicher Infusion | ||
| Propofol-Infusion (nach der Intubation) | 5–50 μg/kg/min | Anfänglich: 10–20 μg/kg/min | Schnell | 10–15 min nach kontinuierlicher Infusion | Erwägen Sie die Verwendung des idealen Körpergewichts für adipöse Patienten | Hypotonie |
| Dexmedetomidin-Infusion (nach der Intubation) | 0,2–1,4 μg/kg/min | Anfänglich: 0,2–0,5 μg/kg/min | 5–10 Minuten | 60–240 min nach kontinuierlicher Infusion | Bradykardie, Hypotonie | |
| Midazolam (nach der Intubation) |
IVP: 1–5 mg alle 30 min PRN-Infusion: 1–10 mg/h |
Anfänglich: 1–5 mg Bolus + |
2–5 Minuten | Verlängert bei Fettleibigkeit oder nach kontinuierlicher Infusion |
Verwenden Sie nach Möglichkeit IVP PRN; Infusion im Zusammenhang mit erhöhter LOS auf der Intensivstation |
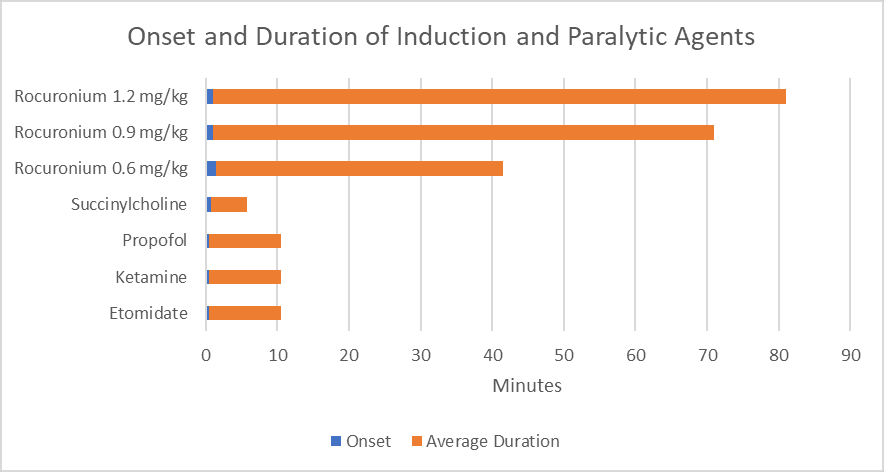 Abbildung 1. Beginn und Dauer von Induktions- und Lähmungsmitteln.
Abbildung 1. Beginn und Dauer von Induktions- und Lähmungsmitteln.
References
- Stollings JL, Diedrich DA, Oyen LJ, Brown DR. Schnellsequenz-Intubation: ein Überblick über den Prozess und Überlegungen bei der Auswahl von Medikamenten. Ann Pharmazeutin. 2014; 48(1):62-76. doi:10.1177/1060028013510488.
- Shafique MA, Haseeb A, Asghar B, Kumar A, Chaudhry ER, Mustafa MS. Bewertung der Auswirkungen des präklinischen Atemwegsmanagements auf schwere traumatische Hirnverletzungen: eine systematische Überprüfung und Metaanalyse. Am J Emerg Med. 2024;78:188-195. doi:10.1016/j.ajem.2024.01.030.
- Hampton JP, Hommer K, Musselman M, Bilhimer M. Schnelle Sequenzintubation und die Rolle des Apothekers in der Notfallmedizin: Update 2022. Am J Health Syst Pharm. 15. Februar 2023; 80(4):182-195. doi:10.1093/ajhp/zxac326.
- Scott JA, Heard SO, Zayaruzny M, Walz JM. Atemwegsmanagement bei kritischen Erkrankungen: ein Update. Brust. 2020; 157(4):877-887. doi:10.1016/j.chest.2019.10.026.
- Kovacich NJ, Nelson AC, McCormick T, Kaucher KA. Inzidenz von Bradykardie und die Verwendung von Atropin bei der pädiatrischen Schnellsequenz-Intubation in der Notaufnahme. Pädiatr Emerg Pflege. 2022; 38(2):e540-e543. doi:10.1097/PEC.0000000000002382.
- Packungsbeilage mit Fentanylcitrat. Lake Forest, Illinois: Akorn, Inc.; 2012.
- Packungsbeilage für Succinylcholinchlorid. Berkeley Heights, NJ: Hikma Pharmaceuticals USA Inc.; 2021.
- Topjian AA, Raymond TT, Atkins D, et al.; Pädiatrische Basis- und fortgeschrittene Lebenserhaltungsmitarbeiter. Teil 4: Pädiatrische grundlegende und erweiterte Lebenserhaltung 2020 Richtlinien der American Heart Association für Herz-Lungen-Wiederbelebung und kardiovaskuläre Notfallversorgung. Pädiatrie. Januar 2021; 147(Suppl 1):e2020038505D. doi:10.1542/peds.2020-038505D.
- Eisa L, Passi Y, Lerman J, Raczka M, Heard C. Verursachen kleine Dosen von Atropin (<0,1 mg) Bradykardie bei kleinen Kindern? Arch Dis Kind. 2015; 100(7):684-688. doi:10.1136/archdischild-2014-307868.
- Huang WC, Yang AS, Tsai DH, Shao SC, Lin SJ, Lai EC. Zusammenhang zwischen kürzlich erhöhter anticholinerger Belastung und dem Risiko akuter kardiovaskulärer Ereignisse: landesweite Fall-Fall-Zeit-Kontroll-Studie. BMJ. 2023; 382:e076045. Veröffentlicht 2023 Sep 27. doi:10.1136/bmj-2023-076045.
- Engstrom K, Brown CS, Mattson AE, Lyons N, Rech MA. Optimierung der Pharmakotherapie für die schnelle Sequenzintubation in der Notaufnahme. Am J Emerg Med. 2023;70:19-29. doi:10.1016/j.ajem.2023.05.004.
- Lin CC, Yu JH, Lin CC, Li WC, Weng YM, Chen SY. Postintubation hämodynamische Wirkungen von intravenösem Lidocain bei schweren traumatischen Hirnverletzungen. Am J Emerg Med. 2012; 30(9):1782-1787. doi:10.1016/j.ajem.2012.02.013.
- Kramer N, Lebowitz D, Walsh M, Ganti L. Schnelle Sequenzintubation bei traumatisch hirngeschädigten Erwachsenen. Kureus. 2018; 10(4):e2530. Veröffentlicht 2018 Apr 25. doi:10.7759/cureus.2530.
- April MD, Arana A, Pallin DJ et al. Erfolg bei der Intubation in der Notaufnahme mit Succinylcholin im Vergleich zu Rocuronium: eine Studie des National Emergency Airway Registry. Ann Emerg Med. 2018; 72(6):645-653. doi:10.1016/j.annemergmed.2018.03.042.
- Upchurch CP, Grijalva CG, Russ S, et al. Vergleich von Etomidat und Ketamin zur Induktion während der Schnellsequenzintubation von erwachsenen Traumapatienten. Ann Emerg Med. 2017; 69(1):24-33.e2. doi:10.1016/j.annemergmed.2016.08.009.
- Packungsbeilage von Etomidat. Lake Forest, Illinois: Hospira, Inc.; 2017.
- Mohr NM, Pape SG, Runde D, Kaji AH, Walls RM, Braun CA III. Die Anwendung von Etomidat ist mit einer geringeren Hypotonie als Ketamin bei Sepsis-Intubationen in der Notaufnahme verbunden: eine NEAR-Kohortenstudie. Acad Emerg Med. 2020; 27(11):1140-1149. doi:10.1111/acem.14070.
- Packungsbeilage für Ketamin. Chestnut Ride, NY: von Pharmaceutical; 2017.
- Dietrich SK, Mixon MA, Rogoszewski RJ, et al. Hämodynamische Wirkungen von Propofol zur Induktion einer schnellen Sequenzintubation bei traumatisch verletzten Patienten. Am Surg. 2018; 84(9):1504-1508.
- Soja-Allergiker und Ei-Allergiker können sicher eine Anästhesie erhalten. Amerikanische Akademie für Allergie, Asthma und Immunologie. Aktualisiert am 28. September 2020. Abgerufen am 22. April 2022. Verfügbar unter: https://www.aaaai.org/Tools-for-the-Public/Conditions-Library/Allergies/soy-egg-anesthesia.
- Brown, CA et al. (2017) Das Handbuch der Wände für das Notfall-Atemwegsmanagement. Philadelphia: Wolters Kluwer.
- Rogachov A, Kitzerow C, Peterson J, Walker J. Verdacht auf hyperkaliämieinduzierten Herzstillstand und Genesung nach Einnahme von Succinylcholin bei einem Traumapatienten. Kans J Med. 2023;16:299-301. Veröffentlicht 2023 Nov 30. doi:10.17161/kjm.vol16.21009.
- Strachan J, Frise M. Lebensbedrohliche Hyperkaliämie nach Succinylcholin. Lanzette. 2020; 395(10219):e9. doi:10.1016/S0140-6736(19)32493-6.
- Patanwala AE, Erstad BL, Roe DJ, Sakles JC. Succinylcholin ist mit einer erhöhten Mortalität verbunden, wenn es für eine schnelle Sequenzintubation von schwer hirnverletzten Patienten in der Notaufnahme verwendet wird. Pharmakotherapie. 2016; 36(1):57-63. doi:10.1002/phar.1683.
- Packungsbeilage von Rocuroniumbromid. Deerfield, Illinois: Baxter Healthcare Corporation; 2019.
- Vested M, Pape P, Kristensen CM, et al. Rocuronium 0,3 oder 0,9 mg/kg Vergleich von Wirkungseinbruchzeit, Wirkungsdauer und Intubationsbedingungen bei Patienten ab 80 Jahren: eine randomisierte Studie. Acta Anaesthesiol Scand. 2022; 66(7):811-817. doi:10.1111/aas.14097.
- Levin NM, Fix ML, April MD, Arana AA, Braun CA 3.; NEAR Ermittler. Der Zusammenhang zwischen der Dosierung von Rocuronium und dem Erfolg des ersten Intubationsversuchs bei erwachsenen Patienten in der Notaufnahme. EuGH. 2021; 23(4):518-527. doi:10.1007/s43678-021-00119-6.
- Korinek JD, Thomas RM, Goddard LA, St. John AE, Sakles JC, Patanwala AE. Vergleich von Rocuronium und Succinylcholin bei der Dosierung von Beruhigungsmitteln und Analgetika nach der Intubation in der Notaufnahme. Eur J Emerg Med. 2014; 21(3):206-211. doi:10.1097/MEJ.0b013e3283606b89.
- Johnson EG, Meier A, Shirakbari A, Weant K, Baker Justice S. Einfluss von Rocuronium und Succinylcholin auf die Sedierungsinitiierung nach schneller Sequenzintubation. J Emerg Med. 2015; 49(1):43-49. doi:10.1016/j.jemermed.2014.12.028.
- Neostigmin Packungsbeilage. Princeton, NJ: Dr. Reddy's Laboratorien, Inc.; 2021.
- BRIDION (Sugammadex) Packungsbeilage. Whitehouse Station, NJ: Merck Sharp & Dohme Corp.; 2021.
- Packungsbeilage für Vecuroniumbromid. Zürichsee, IL: Fresenius Kabi; 2019.
- NIMBEX (Cisatracurium Besylat) Packungsbeilage. Nord-Chicago, Illinois: AbbVie, Inc.; 2019.
- Pappal RD, Roberts BW, Mohr NM, et al. Die ED-AWARENESS-Studie: eine prospektive, beobachtende Kohortenstudie zum Bewusstsein mit Lähmungen bei mechanisch beatmeten Patienten, die aus der Notaufnahme aufgenommen wurden. Ann Emerg Med. 2021; 77(5):532-544. doi:10.1016/j.annemergmed.2020.10.012.
- Devlin JW, Skrobik Y, Gélinas C, et al. Leitlinien für die klinische Praxis zur Prävention und Behandlung von Schmerzen, Unruhe/Sedierung, Delirium, Immobilität und Schlafstörungen bei erwachsenen Patienten auf der Intensivstation. Crit Care Med. 2018; 46(9):e825-e873. doi:10.1097/CCM.0000000000003299.
- Choi L, Ferrell BA, Vasilevskis EE, et al. Populationspharmakokinetik von Fentanyl bei kritisch Kranken. Crit Care Med. 2016; 44(1):64-72. doi:10.1097/CCM.000000000001347.
- Mondardini MC, Sperotto F, Daverio M, Amigoni A. Analgesie und Sedierung bei kritisch kranken pädiatrischen Patienten: ein Update aus den jüngsten Leitlinien und aus der Sicht. Eur J Pädiatr. 2023; 182(5):2013-2026. doi:10.1007/s00431-023-04905-5.
- Su JY, Lockwood C, Tsou YC, Mu PF, Liao SC, Chen WC. Implementierung der Richmond Agitation-Sedation Scale auf einer Intensivstation für Atemwege: ein Best-Practice-Implementierungsprojekt. JBI Database System Rev Implement Rep. 2019; 17(8):1717-1726. doi:10.11124/JBISRIR-2017-004011.
- Hausburg MA, Banton KL, Roman PE, et al. Auswirkungen von Propofol auf Ischämie-Reperfusion und traumatische Hirnverletzungen. J Kritische Pflege. 2020;56:281-287. doi:10.1016/j.jcrc.2019.12.021.
- Packungsbeilage zur Propofol-Injektion. Lehi, UT: Civica, Inc.; 2020.
- Shearin AE, Patanwala AE, Tang A, Erstad BL. Prädiktoren für Hypotonie im Zusammenhang mit Propofol bei Traumapatienten. J Trauma-Krankenschwestern. 2014; 21(1):4-8. doi:10.1097/JTN.000000000000022.
- Pajoumand M, Kufera JA, Bonds BW, et al. Dexmedetomidin als Zusatz zur Sedierung bei Patienten mit traumatischen Hirnverletzungen. J Trauma-Akutversorgung Chirurgie. 2016; 81(2):345-351. doi:10.1097/TA.0000000000001069.
- Winings NA, Daley BJ, Bollig RW, et al. Dexmedetomidin versus Propofol für eine verlängerte Sedierung bei kritisch kranken Trauma- und chirurgischen Patienten. Chirurg. 2021; 19(3):129-134. doi:10.1016/j.surge.2020.04.003.
- Packungsbeilage zur Midazolamhydrochlorid-Injektion. Lake Forest, Illinois: Hospira, Inc.; 2021.
- Acquisto NM, Mosier JM, Bittner EA et al. Richtlinien der Society of Critical Care Medicine für die klinische Praxis der schnellen Sequenzintubation bei kritisch kranken erwachsenen Patienten. Crit Care Med. 2023; 51(10):1411-1430. doi:10.1097/CCM.000000000006000.
- Zeiler FA, Teitelbaum J, West M, Gillman LM. Die Wirkung von Ketamin auf den ICP bei traumatischen Hirnverletzungen. Neurokrit-Pflege. 2014; 21(1):163-173. doi:10.1007/s12028-013-9950-y.
- Holzfäller SAI, Koedam TWA, Giannakopoulos GF, Vandewalle E, Erwteman M, Zuidema WP. Definition der hämodynamischen Stabilität bei Patienten mit stumpfem Trauma: eine systematische Überprüfung und Bewertung unter den Mitgliedern des niederländischen Traumateams. Eur J Trauma Emerg Surg. 2017; 43(6):823-833. doi:10.1007/s00068-016-0744-8.
Cite this article
Ko CL, Celmins L. Pharmakologie für das Management der Atemwege mit schneller Sequenzintubation (RSI) bei Traumapatienten. J Med Insight. 2024; 2024(299.11). doi:10.24296/jomi/299.11.

