Colectomía izquierda abierta para el cáncer de colon: resección de colon izquierdo y sigmoide con formación de colostomía
Main Text
Table of Contents
Una colectomía abierta es la resección de todo o parte del colon, generalmente a través de una incisión en la línea media del abdomen. Este procedimiento suele estar indicado para el tratamiento de enfermedades colónicas como la obstrucción intestinal, la diverticulitis, la enfermedad inflamatoria intestinal y el cáncer de colon. El paciente en este caso era un varón cuadripléjico C6 que presentó cáncer de colon cerca de la flexión esplénica. También sufría de dismotilidad colónica y estreñimiento severo. Fue tratado con una colectomía abierta izquierda a través de una laparotomía de línea media superior. En cuanto al procedimiento, una vez ingresado al abdomen, se exploró la cavidad peritoneal y se identificó el tumor. Se movilizó el colon, comenzando por el colon transverso, que se extendió lateralmente para derribar la flexión hepática, seguido de la movilización del colon derecho de lateral a medial. A continuación, se movilizó la flexión esplénica seguida del colon descendente, de nuevo de forma lateral a medial. Una vez movilizado, se identificaron los márgenes de la transección y se ligó el mesocolon intermedio en forma de corte y amarre. A continuación, se seccionó el colon con una grapadora ILA para incluir el colon sigmoide transverso, descendente y proximal distal. Finalmente, el extremo cortado proximal del colon transverso se elevó a través de una colostomía del extremo izquierdo. En este video, se muestran los pasos clave del procedimiento y proporcionamos un análisis sobre nuestra toma de decisiones intraoperatorias.
El cáncer de colon es un proceso maligno que afecta el revestimiento epitelial del colon. Es el tercer cáncer más común en el mundo y representa aproximadamente el 9% de los nuevos diagnósticos de cáncer. 1 La incidencia del cáncer de colon es geográficamente variable, lo que sugiere que tanto los factores genéticos como los del estilo de vida contribuyen al desarrollo de la enfermedad. África occidental tiene la incidencia más baja, con una tasa de 3 a 4 casos por cada 100.000 personas por año, mientras que América del Norte tiene una incidencia anual de 26 por cada 100.000 personas. 2 Además, el cáncer de colon representa la cuarta causa más común de muerte relacionada con el cáncer, con más de 700,000 casos al año. 3 En conjunto, esta afección representa un importante problema de salud mundial tanto para los países desarrollados como para los países en desarrollo.
Los factores de riesgo para el cáncer de colon incluyen la edad, los factores ambientales y la predisposición genética. La mediana de edad del diagnóstico es de 67 años para los hombres y de 71 años para las mujeres. 4 Si bien el advenimiento de la colonoscopia de detección regular ha ayudado a reducir la incidencia de cánceres de colon en pacientes mayores de 50 años, la incidencia de cáncer de colon se ha duplicado entre los pacientes más jóvenes, principalmente de 40 a 49 años, en las últimas décadas. 5 Es probable que el aumento de la incidencia en las poblaciones más jóvenes esté asociado con el aumento de las tasas de obesidad, estilo de vida sedentario, dieta occidental, síndrome metabólico, así como el consumo de alcohol y tabaco. Estas observaciones se han observado de manera similar en otros países industrializados. Por último, los estudios familiares indican que hasta el 30% de los cánceres de colon están relacionados con una forma hereditaria de enfermedad, y aproximadamente el 5% de los casos están relacionados con síndromes de cáncer colorrectal altamente penetrantes, como la poliposis adenomatosa familiar (PAF), el síndrome de Lynch y las afecciones hamartomatosas. 6
La resección quirúrgica sigue siendo la única terapia curativa para el cáncer de colon. Una vez que se establece un diagnóstico, por lo general a través de una coloncopia de detección, los pacientes se estadifican completamente utilizando el sistema TNM del American Joint Committee on Cancer (AJCC). Para los pacientes con enfermedad localizada o regional, la colectomía con una producción de al menos 12 ganglios linfáticos es el estándar de atención. La quimioterapia adyuvante se considera para los pacientes con características de riesgo alto o estado ganglionar positivo. Por último, en el caso de los pacientes con enfermedad metastásica, la mayoría de estos casos se consideran incurables y los pacientes se tratan con quimioterapia paliativa. La supervivencia del cáncer de colon ha mejorado significativamente con mejores técnicas quirúrgicas y regímenes de quimioterapia. La tasa de supervivencia promedio a 5 años para la enfermedad en estadio temprano es superior al 90 %; La afectación de los ganglios linfáticos reduce esto a aproximadamente el 70%, y la enfermedad metastásica todavía se asocia con un pronóstico sombrío, con menos del 15% de los pacientes que sobreviven más de 5 años. 7
En este vídeo realizamos una colectomía abierta izquierda a un paciente de 65 años que presentó una obstrucción del intestino grueso secundaria a un tumor. En este procedimiento, el colon se moviliza bilateralmente, incluyendo el desmontaje de las flexuras hepática y esplénica. Se reseca el colon sigmoide distal transverso, descendente y proximal y se crea una colostomía final. Por lo tanto, este procedimiento reseca adecuadamente la porción enferma del colon, tratando eficazmente esta afección.
El paciente es un hombre de 65 años con cuadriplejia después de una lesión traumática del cordón C6 que acudió a un hospital externo con náuseas, vómitos y obstrucción de nueva aparición. Su examen incluyó una tomografía computarizada abdominal con evidencia de una masa obstructiva en el colon transverso. Estaba clínicamente estable y fue trasladado al Hospital General de Massachusetts para recibir atención adicional. Su historial médico es notable por estreñimiento crónico, úlceras recurrentes de decúbito tratadas con múltiples operaciones, incluido un procedimiento de Girdlestone, y pielonefritis recurrente secundaria a cálculos renales después de la litotricia y colocación de una sonda de nefrostomía percutánea del lado izquierdo. Tiene una puntuación de la Sociedad Americana de Anestesiólogos (ASA) de 3 y su índice de masa corporal (IMC) es de 25. Dado que se encontraba obstruido, el paciente fue trasladado directamente al quirófano para su tratamiento definitivo.
Al paciente se le realizó un examen físico sin complicaciones. En la oficina, se presentó en una silla de ruedas y no estaba en peligro aparente con signos vitales normales. Tenía un habitus normal. Su examen abdominal era significativo por cicatrices quirúrgicas previas, sin evidencia de hernias y sin sensibilidad a la palpación. Su abdomen estaba distendido pero blando.
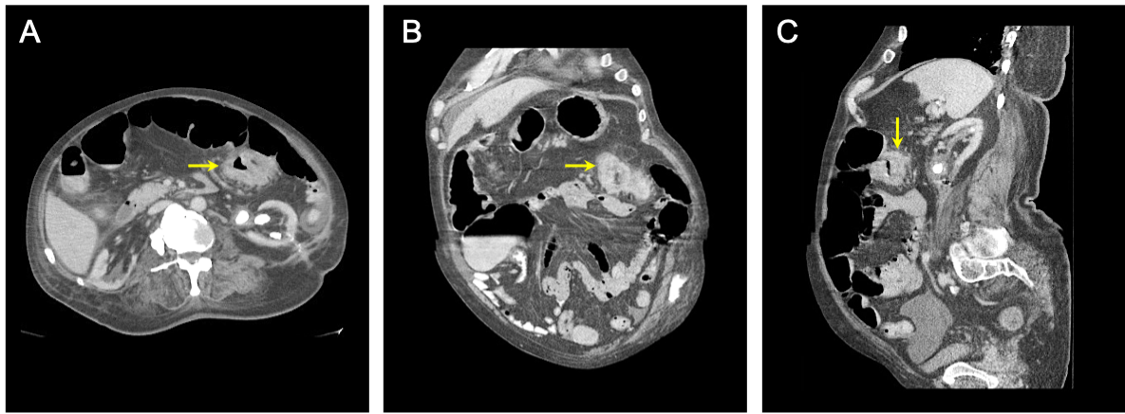
Figura 1: Tomografías computarizadas abdominales y pélvicas. Tomografía computarizada de abdomen y pelvis con contraste intravenoso y oral que muestra evidencia de una masa de colon transverso obstructiva. El tejido enfermo se muestra en las vistas axial (A), (B) coronal y (C) sagital. Las flechas amarillas apuntan hacia el segmento enfermo del colon.
Múltiples mecanismos patogénicos han sido implicados en el desarrollo del cáncer de colon. Para la mayoría de los pacientes, una secuencia escalonada de alteraciones genéticas y epigenéticas en los epitelios colónicos conduce al desarrollo de neoplasias de pólipos benignos que pueden progresar a carcinoma invasivo durante un período de años, como lo describieron inicialmente Vogelstein et al.8 Se ha demostrado que las alteraciones genéticas ocurren en tres mecanismos principales, que incluyen la inestabilidad cromosómica, la inestabilidad de los microsatélites y la metilación de la isla CpG. 9 Además, un subconjunto de pacientes puede desarrollar cáncer de colon secundario a una inflamación crónica significativa que puede provocar cambios displásicos sin formación de pólipos, generalmente en individuos con colitis ulcerosa o colitis de Crohn. De manera similar, las personas con síndrome de Lynch, una afección de la línea germinal que resulta en inestabilidad de microsatélites, desarrollarán cánceres de colon sin formación de pólipos. Una vez que se ha desarrollado un cáncer invasivo, las células malignas invaden y alteran los tejidos circundantes y pueden propagarse a sitios distantes a través de la invasión linfática, perineural y hematógena.
Para los pacientes con cáncer de colon oligometastásico localizado y regional o ciertos casos de cáncer de colon oligometastásico, la resección quirúrgica sigue siendo la única terapia curativa posible. No obstante, el paciente debe discutir los riesgos y beneficios de una operación con su cirujano. La quimioterapia adyuvante suele estar indicada para la enfermedad con características malignas o la enfermedad que se ha diseminado a los ganglios linfáticos o a sitios de órganos distantes. Sin embargo, la quimioterapia por sí sola no puede curar esta afección.
En general, el objetivo de la resección quirúrgica es la extirpación completa del tejido maligno, por lo tanto, una intención curativa.
Puede haber ciertos casos en los que el cáncer se ha diseminado a sitios distantes aunque se haya producido una complicación con el tumor primario, que incluye sangrado, perforación u obstrucción significativos. En estas situaciones, un cirujano puede decidir operar como una intervención aguda para salvar vidas sin un objetivo de eliminación de la enfermedad. En este video, el paciente presentó una complicación, una obstrucción del intestino grueso, pero afortunadamente no tenía evidencia de enfermedad metastásica.
Como hemos mostrado en este video, los principales pasos del procedimiento para esta operación son los siguientes: (1) realizar una laparotomía de línea media y estudiar la cavidad peritoneal, (2) movilizar el colon transverso mediante el desmontaje del ligamento gastrocólico y la entrada en el saco menor, (3) desmontaje de la flexión hepática y movilización lateral a medial del colon ascendente, (4) desmontaje de la flexión esplénica y movilización lateral a medial del colon descendente y sigmoide, (5) identificar los márgenes de resección y ligar el mesocolon intermedio, (6) seccionar el colon con una grapadora ILA 100 y (7) crear una colostomía final de forma escalonada. Este enfoque de una colectomía abierta da como resultado una movilización extensa de todo el colon, lo que permite una resección grande y una posterior colostomía final sin tensión en el lado izquierdo del abdomen. La arteria cólica media se conserva, lo que garantiza un suministro adecuado de sangre al colon transverso distal restante.
En el caso de la cirugía del cáncer de colon, el grado de rendimiento ganglionar y la escisión mesocólica sigue siendo un área de debate abierto. Le Voyer et al. demostraron previamente que el número de ganglios linfáticos analizados en muestras de cáncer de colon se asoció con la supervivencia. 10 En consecuencia, las directrices actuales recomiendan que se reseque un mínimo de 12 ganglios linfáticos con la muestra de cáncer para una estadificación adecuada. La razón por la cual un mayor rendimiento ganglionar está relacionado con mejores resultados de supervivencia no se comprende completamente. Se cree que la migración de etapas, en la que los cánceres se escalonan con rendimientos ganglionares más altos a medida que aumenta la probabilidad de encontrar un ganglio positivo, contribuye hasta cierto punto. 11 Sin embargo, también se ha propuesto que una escisión mesocólica más extensa proporciona una extirpación más adecuada de la enfermedad micrometastásica regional. 12 En apoyo de este razonamiento, múltiples estudios han demostrado que la escisión mesocólica extensa se asocia con mejores tasas de supervivencia general y libre de enfermedad entre los pacientes con cáncer de colon. 13 y 14 En este video, el mesocolon se tomó cerca de los despegues vasculares para proporcionar una muestra mesocólica más grande.
En el futuro, seguirá habiendo mejoras en los tratamientos no quirúrgicos para el cáncer de colon. Con tasas mejoradas de colonoscopia de detección, se ha demostrado que la detección temprana y la polipectomía endoscópica son suficientes para el tratamiento de cánceres muy tempranos, lo que evita la necesidad de una operación en un subconjunto de individuos. 15 Las terapias sistémicas también han experimentado una evolución y mejora significativas. Las terapias dirigidas de nuevo diseño contra el factor de crecimiento endotelial vascular (VEGF), el receptor del factor de crecimiento epidérmico (EGFR) y los componentes de la vía KRAS podrían tener un beneficio adicional a los regímenes de quimioterapia actuales y se están llevando a cabo en investigación clínica. 16, 17 Por último, el reciente desarrollo de la inmunoterapia podría ser prometedor para el subconjunto de cánceres de colon definidos por la inestabilidad de los microsatélites. 18
- Tiempo de operación: 90 minutos
- Pérdida de sangre estimada: 400 mL
- Fluidos: 4600 mL cristaloide
- Tiempo de estancia: alta hospitalaria a domicilio con asistencia de enfermería visitante en el día 9 del postoperatorio
- Morbilidad: sin complicaciones
- Patología final: pT4aN2bM0, 8 de 17 ganglios positivos; Histología: pobremente diferenciada con invasión linfovascular, márgenes quirúrgicos todos negativos
- Bisturí de 10 hojas
- Electrocauterización
- Pinzas DeBakey
- Retractor de mano de la pared abdominal
- Abrazadera Schnidt
- Lazos de seda 3-0 y 2-0 para ligadura de mesenterio
- Tijeras Metzenbaum
- Grapadora ILA de carga azul de 100 mm
- 4-0 Vicryl para la colostomía en maduración
- 1-0 Sutura de Prolene para cierre fascial
- Grapadora de piel
Nada que revelar.
El paciente al que se refiere este videoartículo ha dado su consentimiento informado para ser filmado y es consciente de que la información y las imágenes se publicarán en línea.
Nos gustaría agradecer a Theresa Kim, MD por ayudar en esta operación.
References
- Mattiuzzi C, Sanchis-Gomar F, Lippi G. Actualización concisa sobre la epidemiología del cáncer colorrectal. Ann Transl Med. 2019;7:609. doi:10.21037/atm.2019.07.91.
- Kuipers EJ, Grady WM, Lieberman D, et al. Colorectal cancer (Cáncer colorrectal). Nat Rev Dis Primers. 2015;1:15065. doi:10.1038/nrdp.2015.65.
- Mortalidad GBD, Causas de muerte C. Mortalidad mundial, regional y nacional por edad, sexo y todas las causas y por causas específicas para 240 causas de muerte, 1990-2013: un análisis sistemático para el Estudio de la Carga Mundial de Morbilidad 2013. Lanceta. 2015;385:117-71. doi:10.1016/S0140-6736(14)61682-2.
- Siegel R, Desantis C, Jemal A. Estadísticas de cáncer colorrectal, 2014. CA Cáncer J Clin. 2014;64:104-17. doi:10.3322/caac.21220.
- Stoffel EM, Murphy CC. Epidemiología y mecanismos del aumento de la incidencia de cánceres de colon y recto en adultos jóvenes. Gastroenterología. 2020;158:341-53. doi:10.1053/j.gastro.2019.07.055.
- Jasperson KW, Tuohy TM, Neklason DW, Burt RW. Cáncer de colon hereditario y familiar. Gastroenterología. 2010;138:2044-58. doi:10.1053/j.gastro.2010.01.054.
- DeSantis CE, Lin CC, Mariotto AB, et al. Estadísticas de tratamiento y supervivencia del cáncer, 2014. CA Cáncer J Clin. 2014;64:252-71. doi:10.3322/caac.21235.
- Vogelstein B, Fearon ER, Hamilton SR, et al. Alteraciones genéticas durante el desarrollo del tumor colorrectal. N Engl J Med. 1988;319:525-32. doi:10.1056/NEJM198809013190901.
- Erstad DJ, Tumusiime G, Cusack JC Jr. Biomarcadores pronósticos y predictivos en cáncer colorrectal: implicaciones para el cirujano clínico. Ann Surg Oncol. 2015;22:3433-50. doi:10.1245/s10434-015-4706-x.
- Le Voyer TE, Sigurdson ER, Hanlon AL, et al. La supervivencia del cáncer de colon se asocia con un mayor número de ganglios linfáticos analizados: una encuesta secundaria del ensayo intergrupal INT-0089. J Clin Oncol. 2003;21:2912-9. doi:10.1200/JCO.2003.05.062.
- Kim YW, Kim NK, Min BS, Lee KY, Sohn SK, Cho CH. Influencia del número de ganglios linfáticos recuperados en la estadificación y la supervivencia en pacientes con cáncer de recto en estadios II y III sometidos a escisión mesorrectal específica del tumor. Ann Surg. 2009;249:965-72. doi:10.1097/SLA.0b013e3181a6cc25.
- Rahbari NN, Bork U, Motschall E, et al. La detección molecular de células tumorales en los ganglios linfáticos regionales se asocia con la recurrencia de la enfermedad y la supervivencia precaria en el cáncer colorrectal con ganglios negativos: una revisión sistemática y metanálisis. J Clin Oncol. 2012;30:60-70. doi:10.1200/JCO.2011.36.9504.
- Bertelsen CA, Neuenschwander AU, Jansen JE, et al. Danish Colorectal Cancer G. Supervivencia libre de enfermedad después de la escisión mesocólica completa en comparación con la cirugía convencional de cáncer de colon: un estudio retrospectivo basado en la población. Lanceta Oncol. 2015;16:161-8. doi:10.1016/s1470-2045(14)71168-4.
- Hohenberger W, Weber K, Matzel K, Papadopoulos T, Merkel S. Cirugía estandarizada para el cáncer de colon: escisión mesocólica completa y ligadura central: notas técnicas y resultados. Dis. Colorrectal. 2009; 11:354-64; Discusión 64-5. doi:10.1111/j.1463-1318.2008.01735.x.
- Gangireddy VGR, Coleman T, Kanneganti P, et al. Polipectomía versus cirugía en el cáncer de colon temprano: el tamaño y la ubicación del cáncer de colon afectan la supervivencia a largo plazo. Int J Dis. Colorrectal. 2018;33:1349-57. doi:10.1007/s10350-007-9175-2.
- Hurwitz H, Fehrenbacher L, Novotny W, et al. Bevacizumab más irinotecán, fluorouracilo y leucovorina para el cáncer colorrectal metastásico. N Engl J Med. 2004;350:2335-42. doi:10.1056/NEJMoa032691.
- Dienstmann R, Salazar R, Tabernero J. Personalización de la terapia adyuvante para el cáncer de colon: selección de tratamientos óptimos para pacientes individuales. J Clin Oncol. 2015;33:1787-96. doi:10.1200/JCO.2014.60.0213.
- Dudley JC, Lin MT, Le DT, Eshleman JR. Inestabilidad de microsatélites como biomarcador para el bloqueo de PD-1. Clin Cáncer Res. 2016;22:813-20. doi:10.1158/1078-0432.CCR-15-1678.
Cite this article
Erstad DJ, Berger DL. Colectomía abierta izquierda para cáncer de colon: colon izquierdo y resección sigmoidea con formación de colostomía. J Med Insight. 2024; 2024(29). doi:10.24296/jomi/29.

