Réparation rétromusculaire Rives-Stoppa pour hernie incisionnelle
Massachusetts General Hospital
Main Text
Table of Contents
Il n’y a pas de consensus sur la méthode optimale de réparation d’une hernie ventrale, et le choix des techniques est généralement dicté par une combinaison de facteurs liés au patient et à l’expertise du chirurgien. Les techniques de séparation des composants permettent l’avancement médial du muscle droit de l’abdomen pour créer une fermeture fasciale médiane sans tension. Dans ce cas, nous décrivons une séparation des composants postérieurs avec placement du treillis rétrodroit, également connue sous le nom de réparation rétromusculaire Rives-Stoppa. Avec une faible morbidité et mortalité, cette technique offre une réparation durable avec de faibles taux de récidive et d’infection du site opératoire tout en fournissant un soutien musculaire dynamique et une tension physiologique, en prévenant l’éventration et en permettant l’incorporation du treillis dans la paroi abdominale existante.
Les hernies de la paroi abdominale touchent environ cinq millions d’Américains par an. Les hernies se forment à la suite d’une perte d’intégrité structurelle de la paroi abdominale. Les meilleures estimations disponibles suggèrent qu’environ un tiers de toutes les réparations de hernies aux États-Unis concernent des hernies ventrales, et de toutes les hernies ventrales réparées, les deux tiers sont des hernies ventrales primaires et un tiers sont des hernies incisionnelles. 1 Les troubles du tissu conjonctif, l’obésité, le tabagisme, l’utilisation de stéroïdes, le diabète et d’autres facteurs peuvent prédisposer les patients à la formation de hernies primaires, tandis que les hernies incisionnelles résultent, par définition, d’une rupture de la fermeture fasciale. Les facteurs de risque de formation d’une hernie incisionnelle comprennent les facteurs du patient, comme ci-dessus, ainsi que les facteurs techniques au moment de l’opération de référence, tels que l’infection de la plaie, la technique de fermeture fasciale, le type de chirurgie et le choix de l’incision. Une fois qu’une hernie s’est formée, son histoire naturelle est un élargissement progressif en raison d’une augmentation de la tension de la paroi à l’emplacement de la hernie. La réparation d’une hernie doit être fortement envisagée pour les hernies symptomatiques et est une nécessité pour les hernies incarcérées entraînant une occlusion intestinale ou des hernies étranglées. On estime que trois milliards de dollars sont dépensés chaque année en soins de santé liés aux hernies de la paroi abdominale. 2, 3 Dans ce cas, nous effectuons une réparation rétromusculaire Rives-Stoppa pour une hernie incisionnelle symptomatique.
Il s’agit d’une femme de 76 ans ayant des antécédents d’anévrisme de l’aorte abdominale après une réparation endovasculaire, une maladie pulmonaire obstructive chronique, ainsi qu’une colectomie droite pour un cancer du côlon entraînant une hernie incisionnelle qui s’est présentée pour une réparation élective de la hernie. La patiente était dans son état de santé habituel jusqu’en mai 2017, lorsqu’une coloscopie de dépistage a révélé la présence d’un cancer du côlon droit. Elle a ensuite subi une colectomie droite assistée par laparoscopie en juin 2017, suivie d’une chimiothérapie et d’une radiothérapie pour le traitement d’un adénocarcinome colique T4N2. Sa colectomie a été compliquée par une grosse hernie incisionnelle, et son traitement de chimiothérapie a été compliqué par l’anorexie et une perte de poids importante. Au cours de la surveillance, on a constaté qu’elle avait développé un anévrisme de l’aorte abdominale infrarénale de 5,2 cm pour lequel elle a subi une réparation endovasculaire en septembre 2018. Sa hernie s’est progressivement agrandie au fil du temps et est devenue de plus en plus symptomatique, ce qui a interféré avec ses activités de la vie quotidienne. La réparation avec la mise en place d’un treillis rétrodroit a été planifiée de manière élective. Son indice de masse corporelle (IMC) préopératoire était de 20,2, son albumine sérique était de 4,0 g/dl et son statut de l’American Society of Anesthesiologists (ASA) était de 3. Étant donné un côlon rempli de selles et distendu sur l’imagerie axiale préopératoire, une préparation intestinale préopératoire a été administrée pour décompresser le côlon. La céfazoline et l’énoxaparine ont été administrées en préopératoire.
À l’examen, on a remarqué qu’elle avait un abdomen mou avec une grande hernie ventrale qui était réductible et non sensible, sans changements cutanés sus-jacents.
La tomodensitométrie abdominale (TDM) a révélé une hypertrophie progressive d’une hernie ventrale abdominale centrale médiane contenant un petit et un gros intestin sans signe d’atteinte intestinale ou de dilatation intestinale en amont. Elle a également démontré qu’elle avait déjà subi une colectomie droite et une réparation endovasculaire de son anévrisme de l’aorte abdominale infrarénale (figure 1).
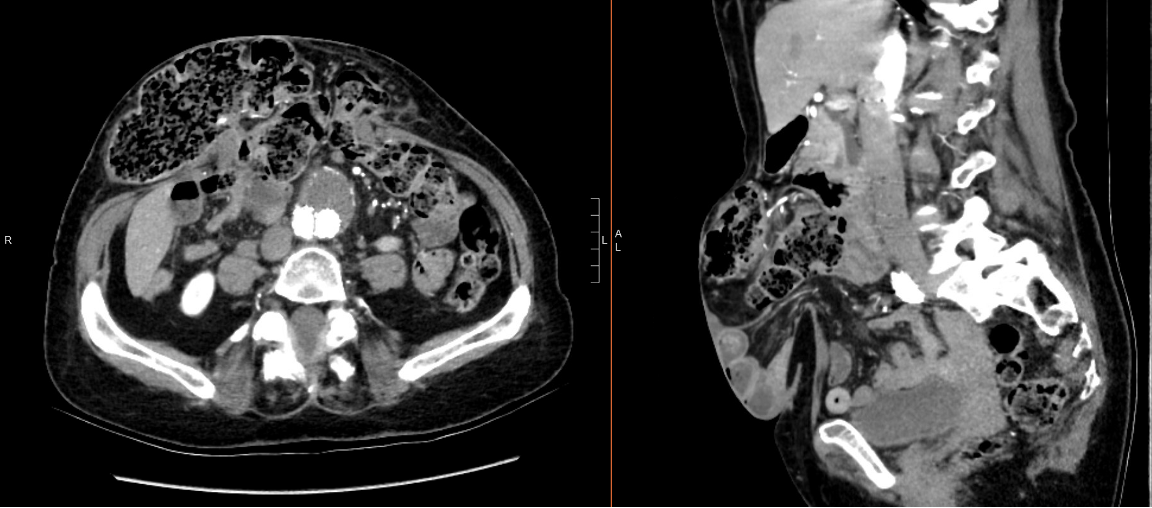
Figure 1 : TDM abdominale préopératoire du patient. Le plan axial (à gauche) et le plan sagittal (à droite) de la tomodensitométrie montrent une colectomie droite antérieure et une réparation endovasculaire antérieure de l’anévrisme abdominal infrarénal du patient.
Les hernies ventrales n’ont pas besoin d’être réparées à moins d’être symptomatiques étant donné que l’occlusion intestinale et l’étranglement sont rares. Même chez les patients symptomatiques, toutes les hernies n’ont pas besoin d’être réparées car la prise en charge non chirurgicale est une alternative sûre. La complexité de la réparation, les comorbidités du patient et la gravité des symptômes contribuent au profil risque-bénéfice d’un patient donné. Un consortium international de spécialistes des hernies a identifié le tabagisme, l’obésité (IMC supérieur à 35), le statut AAS 3 ou plus, une infection antérieure du site opératoire, des modifications cutanées superficielles et la formation d’une fistule entérocutanée comme les facteurs de risque les plus pertinents qui affectent le résultat opératoire après la réparation d’une hernie ventrale. 4 Les experts en hernie s’accordent à dire que la réparation élective d’une hernie ventrale n’est pas recommandée pour les patients ayant un IMC de 50 ou plus sans intervention de perte de poids, pour les fumeurs actifs ou pour ceux dont l’hémoglobine glycosylée (HbA1c) >8 %. 4 à 6
Dans le cadre d’une incarcération aiguë ou d’un étranglement, la réparation chirurgicale urgente est le traitement de choix et peut être la seule option, même chez les patients à haut risque qui pourraient ne pas se voir proposer de réparation élective. L’objectif de la réparation urgente est de soulager la douleur aiguë et l’occlusion intestinale, le cas échéant, et de prévenir ou de traiter l’infarctus intestinal. La technique optimale de réparation varie en fonction de la situation exacte, notamment de l’état nutritionnel, de la physiologie aiguë et de la présence d’une contamination, entre autres facteurs. En général, plus le degré de comorbidité du patient est élevé, plus la réparation doit être simple en cas d’urgence. Parfois, un patient bien nourri sans dérangement physiologique grave ou contamination peut présenter une exposition aiguë et être toujours candidat à une réparation complexe et définitive.
Il existe de nombreuses techniques pour la réparation des hernies ventrales ou incisionnelles médianes. Les réparations de hernie peuvent être effectuées avec ou sans treillis, et de manière ouverte, laparoscopique ou robotique. Le treillis peut être placé comme sous-couche (sous le péritoine), sous-couche (entre les muscles droits et la gaine du droit postérieur), onlay (au-dessus du fascia) ou incrustation (entre les bords fasciaux).
Selon les directives, la réparation du treillis doit être envisagée pour les défauts de >1 cm et est recommandée pour les défauts de >2 cm.5 La réparation du treillis soulage la tension de la paroi abdominale. Plusieurs essais randomisés démontrent des taux plus faibles de récidive avec le treillis. 7 à 9 Le treillis est cependant associé à un taux plus élevé de complications, notamment d’infections, d’érosions et de fistules, que les réparations sans treillis. 7, 10, 11 Une étude de cohorte basée sur un registre au Danemark a démontré que la réparation du treillis était associée à moins de réopérations pour les récidives (maille ouverte 12,3 %, maille laparoscopique 10,6 %, non-maille 17,1 %). 12 Lors d’un suivi de cinq ans, l’incidence cumulée des complications liées au treillis était de 5,6 % chez les patients ayant subi une réparation à treillis ouvert. 12
Le treillis herniaire peut généralement être classé en deux grandes classes : synthétique et biologique. La croissance tissulaire et l’adhérence du treillis synthétique sont attrayantes ; Cependant, il a l’inconvénient de provoquer des adhérences sur les surfaces sérosales. Certains produits en maille synthétique incorporent des anti-adhésifs sur le côté de la maille en contact avec les viscères pour permettre une mise en place intrapéritonéale avec moins de préoccupation pour l’érosion des tissus. Le treillis biologique offre une alternative pour une utilisation dans un champ contaminé et peut réduire la gravité des infections des plaies et la nécessité d’explanter le treillis en cas d’infection par rapport au treillis synthétique. Malgré ces avantages théoriques, le dogme selon lequel les produits biologiques sont préférables aux treillis synthétiques dans un champ infecté a été de plus en plus scruté, en partie en raison des coûts élevés ainsi que des taux élevés de récurrence et de complications associées aux treillis biologiques. Des études récentes offrent un soutien croissant à la pertinence du treillis synthétique ou biosynthétique dans des milieux contaminés tout en remettant en question les avantages présumés du treillis biologique. 13 à 15
Les comparaisons directes des techniques ouvertes et laparoscopique pour la réparation des hernies ont fait l’objet de nombreux essais randomisés. Une revue systématique de 2014 a démontré des taux plus faibles d’infection et de drainage des plaies, mais des taux plus élevés de lésions intestinales pour la laparoscopie par rapport à la réparation ouverte. 16 Une revue Cochrane et une méta-analyse ultérieure sont parvenues aux mêmes conclusions. 17, 18 Les circonstances dans lesquelles la réparation laparoscopique peut être avantageuse peuvent inclure une grande anomalie de la hernie, la suspicion de plusieurs anomalies et l’obésité. Avec la prolifération des plates-formes chirurgicales robotisées, les réparations de hernie assistées par robot sont devenues plus courantes. Bien qu’elles aient un ensemble d’indications similaires à celles de la réparation laparoscopique, la réparation assistée par robot n’améliore pas les résultats, mais prolonge le temps opératoire et augmente le coût. 19, 20
Des anomalies importantes ou complexes de la paroi abdominale représentent un problème chirurgical particulièrement difficile. La Société européenne de la hernie a classé les hernies présentant un défaut de >10 cm comme grandes. 21 Le choix de la technique pour traiter les anomalies importantes ou complexes des hernies est souvent dicté par l’expertise du chirurgien et la situation du patient. La séparation des composants postérieurs avec mise en place d’un treillis rétrodroit offre les avantages d’un faible taux de récidive, de faibles taux de complications de la plaie telles que le sérome ou l’infection, et d’une excellente incorporation d’un treillis peu coûteux et non enduit dans la paroi abdominale.
Les étapes d’une séparation de composants a posteriori avec placement de maillage sont les suivantes :
1) Incision et accès à la cavité abdominale.
2) Dissection et excision du sac herniaire.
3) Dissection et fermeture de la gaine postérieure du droit.
4) Placement du maillage.
5) Placement du drain.
6) Fermeture de la gaine du droit antérieur.
7) Fermeture de la peau.
Une fois l’accès à la cavité abdominale obtenu, une adhésiolyse peut être nécessaire en fonction du degré d’adhérence. Une fois que les viscères sont dégagés de la paroi abdominale, le sac herniaire doit être disséqué de la paroi abdominale et du fascia. Si vous pensez que vous pourriez avoir besoin du sac herniaire pour aider à la fermeture, ne l’excisez pas encore entièrement. Nous utilisons la dissection émoussée pour décoller le sac de la hernie, ce qui facilite une dissection rapide dans le bon plan et préserve ainsi l’épaisseur maximale de la peau sus-jacente et de la graisse sous-cutanée. Le sac herniaire est généralement excisé le long du bord fascial, bien qu’il puisse être préservé lors de réparations planifiées du rétrodroit pour être utilisé comme tissu supplémentaire pour la fermeture de la gaine postérieure. Les gaines postérieures du droit sont ensuite incisées et le fascia postérieur est séparé du droit de l’abdomen. Cela crée l’espace dans lequel le treillis du rétrorectus est placé. Cette dissection est portée latéralement vers la linea semilunaris, le bord latéral du muscle droit de l’abdomen. Il est important de visualiser la linea semilunaris, car la reconnaissance de cette structure et des faisceaux neurovasculaires perforants latéraux est essentielle pour éviter certaines des complications les plus potentiellement dévastatrices de la reconstruction de la paroi abdominale. Il est important de sortir juste de la médiale à la linea semilunaris, de descendre à Cooper dans l’espace de Retzius et de se lever sous le xiphoïde de manière supérieure constitue une dissection adéquate. Au fur et à mesure que cette dissection se produit, des vaisseaux perforants sont rencontrés. Médialement, ceux-ci doivent être sacrifiés pour développer cet espace, mais les perforateurs latéraux doivent être préservés. La dissection inférieure sous la ligne arquée entre dans l’espace de Retzius et peut s’étendre jusqu’aux ligaments de Cooper. La dissection supérieure dans l’espace sous-xiphoïde peut être difficile, car la gaine postérieure doit être détachée de la face postérieure de la linea alba sans pénétrer dans le fascia antérieur. Une fois que les deux côtés sont reliés aux parties supérieure et inférieure de la dissection, la gaine du droit postérieur est fermée. La gaine est fermée de manière courante avec de petites bouchées placées près les unes des autres pour répartir la tension. Cette couche de la fermeture n’est pas pour la force mais fonctionne pour fournir une couche de protection entre le maillage et les viscères intra-abdominaux. La gaine postérieure peut être faible et mince en raison de plusieurs sites de hernie, de réparations antérieures et de stomies, entre autres raisons. Dans ce cas, nous utilisons des bissections successives avec des sutures interrompues en forme de huit pour se rapprocher de la mince gaine postérieure. La fermeture de la gaine postérieure doit être sans tension. Si la gaine postérieure ne peut pas être fermée sur la ligne médiane, ou s’il y a trop de tension, une libération transverse de l’abdomen (TAR) peut être effectuée, l’espace peut être comblé avec le sac herniaire (qui doit être préservé au début du cas si cela est possible), ou bien un treillis enduit peut être utilisé. Dans ce cas, la décision de ne pas effectuer un TAR pourrait être controversée, mais nous n’avons pas estimé qu’il y avait de tension pour le justifier. Une fois que le fascia postérieur est fermé, l’attention est portée sur le placement du treillis. Dans ce cas, nous avons utilisé un treillis en polypropylène de 30 x 30 cm qui a été coupé à la bonne taille, remplissant l’espace du rétrorectus de la ligne semi-lunaire à la ligne semi-lunaire et de la marge costale au pubis. Le treillis enduit non barrière a l’avantage de permettre une incorporation rapide des deux côtés du treillis. Le treillis est maintenu en place avec des sutures transfasciales à travers le fascia antérieur. Il faut prendre soin de placer les sutures transfasciales de manière à ce qu’elles répartissent uniformément la tension sur le treillis et l’incision. La maille est fixée au niveau supérieur et inférieur, puis successivement des deux côtés, en alternant les côtés pour assurer une tension uniforme. La variation de cette technique est courante : certains chirurgiens fixent le treillis au fascia antérieur ou postérieur sans placer de sutures transfasciales, et d’autres n’utilisent aucune suture en s’appuyant sur la friction du treillis pour le maintenir en place. Les drains, dans ce cas deux drains Blake de 19 ronds, sont ensuite placés dans l’espace droit au-dessus du niveau du grillage. Le fascia antérieur est ensuite fermé de manière courante sur le dessus du grillage et s’écoule. Il s’agit d’une couche de résistance, et le fascia doit se rassembler sans tension excessive. La peau redondante est alors excisée, l’espace sous-cutané est drainé si nécessaire, et la peau est fermée.
La séparation des composants a été décrite pour la première fois en 1990. 22 Utilisé pour les hernies de taille modérée ou grande, ce terme englobe une variété de techniques impliquant des lambeaux d’avancement musculofascial pour permettre l’avancement médial du muscle droit de l’abdomen afin de créer une fermeture fasciale médiane sans tension. La séparation des composants peut être effectuée avec ou sans maillage ; Cependant, le taux de récidive reste plus élevé avec la réparation des sutures seule. Les techniques de séparation des composants peuvent être utilisées avec des défauts de hernie aussi grands que 20 cm et parfois même plus grands si un relâchement secondaire ou un treillis supplémentaire est utilisé pour combler le défaut résiduel.
Les éléments anatomiques et fonctionnels d’une technique de séparation des composants comprennent (1) la translation de la couche musculaire de la paroi abdominale pour agrandir la surface tissulaire ; (2) séparation des couches musculaires pour permettre une expansion maximale de chaque unité musculaire individuelle ; (3) la déconnexion de l’unité musculaire de sa gaine fasciale pour faciliter l’expansion ; (4) l’utilisation de la musculature de la paroi abdominale pour couvrir le contenu intra-abdominal ; et (5) l’utilisation de la mobilisation bilatérale pour équilibrer les forces de la paroi abdominale et centraliser la ligne médiane. 22, 23 La séparation des composants peut être effectuée à l’aide d’une approche antérieure ou postérieure avec ou sans libération secondaire pour fournir une progression supplémentaire. Le choix de la technique dépend généralement de l’expérience et de l’expertise du chirurgien, car les deux réussissent à faciliter l’avancement médial du droit pour la fermeture des hernies ventrales grandes et complexes. Une séparation des composants antérieurs implique la division de l’aponévrose oblique externe pour permettre l’avancement du lambeau musculofascial vers la ligne médiane. 24 La technique antérieure est cependant généralement réalisée avec la création de grands lambeaux sous-cutanés et présente donc des complications plus fréquentes de la plaie, bien que les techniques de préservation des perforateurs et d’endoscopie puissent atténuer certains de ces problèmes. 25 La libération oblique externe entraîne également la rupture latérale d’une couche de la paroi abdominale et nécessite une sous-couche intrapéritonéale ou un treillis d’onlay, si le treillis doit être utilisé. 24 Cela contraste avec la technique de séparation des composants postérieurs utilisée dans ce cas, dans laquelle toutes les couches de la paroi abdominale sont maintenues et il n’y a pas de grands lambeaux sous-cutanés. Pour les hernies plus grandes, la technique utilisée dans ce cas peut être étendue par l’utilisation d’un TAR, qui permet une mobilisation plus étendue de la paroi abdominale latérale vers la ligne médiane et permet la mise en place de prothèses à mailles plus grandes au prix d’une rupture latérale d’une couche de la paroi abdominale (dans ce cas, le transverse de l’abdomen). 24 à 27
De nombreux défenseurs préconisent l’utilisation d’un renfort de treillis lors d’une séparation de composants, en grande partie sur l’extrapolation des avantages susmentionnés du treillis pour réduire les taux de récidive des hernies ventrales. Une variété de produits de maille synthétique et biologique ont été utilisés. Il n’existe pas d’essai contrôlé randomisé à grande échelle comparant la séparation des composants avec et sans réparation du treillis. Une séparation des composants postérieurs facilite la mise en place du treillis dans une position de sous-couche extrapéritonéale si le treillis doit être utilisé. Théoriquement, cela permet l’incorporation de tissu vascularisé des deux côtés et peut entraîner des taux de récidive plus faibles. Comme mentionné ci-dessus, cette position, combinée à l’évitement de grands lambeaux sous-cutanés, peut réduire les complications de la plaie par rapport à la séparation des composants antérieurs, bien que les données comparatives directes soient rares. 28
Les patients dont l’évolution n’est pas compliquée sont généralement hospitalisés entre trois et cinq jours pour le contrôle de la douleur et l’avancement du régime alimentaire. Les drains sont retirés en fonction de leur emplacement, de la durée de leur mise en place et de leur rendement par jour. L’activité physique est souvent limitée à court terme, bien que cela n’ait pas été étudié rigoureusement. La morbidité et la mortalité associées à la séparation des composants postérieurs sont rares. Pour les hernies ventrales grandes ou complexes, une étude utilisant la séparation des composants pour réparer une hernie ventrale chez des patients obèses morbides a rapporté que la morbidité périopératoire majeure était de 8 % et la mortalité périopératoire de 1 %. 25 La morbidité est en grande partie attribuable à l’infection du site opératoire, au sérome/hématome et à la nécrose du lambeau cutané, qui se manifestent à des taux variables. Il existe peu d’études avec un suivi à long terme après la séparation des composants, mais les taux de récurrence pour la séparation des composants avec treillis semblent être inférieurs à 10 %.
Le cas détaillé ci-dessus a été réalisé en un peu moins de deux heures et demie avec une perte de sang estimée à 75 ml. Elle a eu une évolution postopératoire sans complication et a reçu son congé de la maison le jour postopératoire (POD) 4. Elle a été vue lors d’un suivi et s’est rétablie sans difficulté. Ses drains ont été enlevés sur les pods 13 et 17. Elle a subi une imagerie axiale par intervalles pour la surveillance de l’anévrisme de l’aorte abdominale qui a démontré l’intégrité de la réparation (Figure 2).
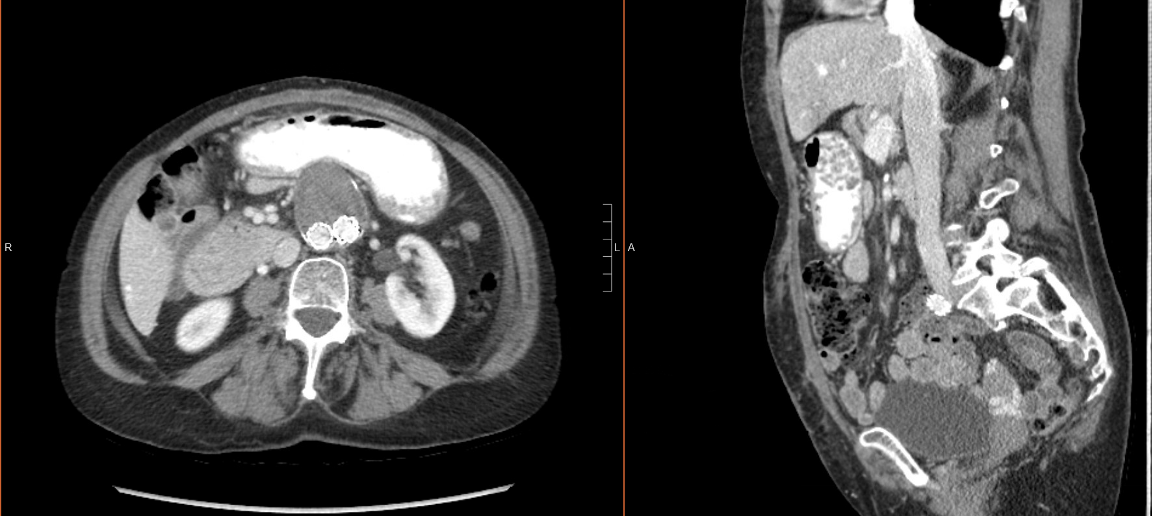
Figure 2 : TDM abdominale postopératoire du patient. Le plan axial (à gauche) et le plan sagittal (à droite) de la tomodensitométrie montrent l’intégrité de la réparation de la hernie ventrale.
Passe-suture laparoscopique ou aiguille Reverdin.
Maille en polypropylène 30x30 cm.
Rien à divulguer.
Le patient visé dans cet article vidéo a donné son consentement éclairé pour être filmé et est conscient que des informations et des images seront publiées en ligne. Il n’y a aucune information d’identification incluse dans la vidéo ou l’article texte.
References
- Rutkow IM. Aspects démographiques et socio-économiques de la réparation d’une hernie aux États-Unis en 2003. Surg Clin North Am. 2003; 83(5) :1045-1051, v-vi. doi :10.1016/S0039-6109(03)00132-4.
- Park AE, Roth JS, Kavic SM. Hernie de la paroi abdominale. Curr Probl Surg. 2006; 43(5):326-375. doi :10.1067/j.cpsurg.2006.02.004.
- Poulose BK, Beck WC, Phillips SE, Sharp KW, Nealon WH, Holzman MD. Les quelques élus : l’utilisation disproportionnée des ressources dans la réparation des hernies ventrales. Am Surg. août 2013 ; 79(8):815-8.
- Parker SG, Reid TH, Boulton R, Wood C, Sanders D, Windsor A. Proposition pour un système national de triage pour la prise en charge des hernies ventrales. Ann R Coll Surg Engl. 2018 février ; 100(2):106-110. doi :10.1308/rcsann.2017.0158.
- Liang MK, Holihan JL, Itani K, et al. Prise en charge de la hernie ventrale : consensus d’experts guidé par une revue systématique. Ann Surg. 2017; 265(1):80-89. doi :10.1097/SLA.000000000001701.
- Holihan JL, Alawadi ZM, Harris JW, et al. Hernie ventrale : sélection du patient, traitement et prise en charge. Curr Probl Surg. 2016; 53(7):307-354. doi :10.1067/j.cpsurg.2016.06.003.
- Luijendijk RW, Hop WCJ, Van Den Tol MP, et al. Une comparaison de la réparation des sutures avec la réparation du treillis pour la hernie incisionnelle. N Engl J Med. 2000; 343(6):392-398. doi :10.1056/NEJM200008103430603.
- Kaufmann R, Halm JA, Eker HH et al. Réparation par maille ou par suture de la hernie ombilicale chez l’adulte : un essai randomisé, en double aveugle, contrôlé et multicentrique. Lancet (Londres, Angleterre). 2018; 391(10123):860-869. doi :10.1016/S0140-6736(18)30298-8.
- Nguyen MT, Berger RL, Hicks SC, et al. Comparaison des résultats de la réparation du treillis synthétique par rapport à la réparation de la suture de l’herniorrhaphie ventrale primaire élective : une revue systématique et une méta-analyse. JAMA Surg. 2014; 149(5):415-421. doi :10.1001/jamasurg.2013.5014.
- den Hartog D, Dur AH, Tuinebreijer WE, Kreis RW. Procédures chirurgicales ouvertes pour les hernies incisionnelles. Base de données Cochrane Syst Rev. 16 juillet 2008 ; 2008(3) :CD006438. doi :10.1002/14651858.CD006438.pub2.
- Tuinebreijer WE, Amaragiri S, Dur AHM, Kreis RW, Den Hartog D. Procédures chirurgicales ouvertes pour les hernies incisionnelles. Base de données Cochrane Syst Rev. 2007; (2) :CD006438. doi :10.1002/14651858.CD006438.
- Kokotovic D, Bisgaard T, Helgstrand F. Récidive à long terme et complications associées à la réparation élective d’une hernie incisionnelle. JAMA. 2016; 316(15):1575-1582. doi :10.1001/jama.2016.15217.
- Majumder A, Winder JS, Wen Y, Pauli EM, Belyansky I, Novitsky YW. Analyse comparative des résultats des treillis biologiques et synthétiques dans les réparations de hernies contaminées. Surg (États-Unis). 2016; 160(4):828-838. doi :10.1016/j.surg.2016.04.041.
- Kissane NA, Itani KMF. Une décennie de réparations de hernies incisionnelles ventrales avec une matrice dermique acellulaire biologique : qu’avons-nous appris ? Plast Reconstr Surg. 2012; 130(5 Suppl. 2). doi :10.1097/prs.0b013e318265a5ec.
- Köckerling F, Alam NN, Antoniou SA, et al. Quelles sont les preuves de l’utilisation de treillis biologiques ou biosynthétiques dans la reconstruction de la paroi abdominale ? Hernie. 2018; 22(2):249-269. doi :10.1007/s10029-018-1735-y.
- Zhang Y, Zhou H, Chai Y, Cao C, Jin K, Hu Z. Réparation laparoscopique ou ouverte des hernies incisionnelles et ventrales : une revue systématique et une méta-analyse. World J Surg. 2014 ; 38(9):2233-2240. doi :10.1007/s00268-014-2578-z.
- Sauerland S, Walgenbach M, Habermalz B, Seiler CM, Miserez M. Techniques chirurgicales laparoscopique par rapport aux techniques chirurgicales ouvertes pour la réparation d’une hernie ventrale ou incisionnelle. 16 mars 2011 ; (3) :CD007781. doi :10.1002/14651858.CD007781.pub2.
- Al Chalabi H, Larkin J, Mehigan B, McCormick P. Une revue systématique de la réparation laparoscopique par rapport à la réparation d’une hernie incisionnelle abdominale ouverte, avec méta-analyse d’essais contrôlés randomisés. Int J Surg. 2015;20:65-74. doi :10.1016/j.ijsu.2015.05.050.
- Zayan NE, Meara MP, Schwartz JS, Narula VK. Une comparaison directe de la réparation robotique et laparoscopique des hernies : résultats rapportés par les patients et analyse des coûts. Hernie. 2019 décembre ; 23(6):1115-1121. doi :10.1007/s10029-019-01943-7.
- Meier J, Huerta S. La réparation robotisée de la hernie inguinale n’est pas supérieure à la réparation laparoscopique ou ouverte. Am J Surg. 2020 juil. 220(1):251. doi :10.1016/j.amjsurg.2019.11.015.
- Muysoms FE, Miserez M, Berrevoet F, et al. Classification des hernies primaires et incisionnelles de la paroi abdominale. Hernie. 2009; 13(4):407-414. doi :10.1007/s10029-009-0518-x.
- Ramirez OM. Création et évolution de la technique de séparation des composants : souvenirs personnels. Clin Plast Surg. 2006; 33(2) :241-246, vi. doi :10.1016/j.cps.2005.12.011.
- Shell IV DH, de la Torre J, Andrades P, Vasconez LO. Réparation ouverte des hernies incisionnelles ventrales. Surg Clin North Am. 2008; 88(1):61-83. doi :10.1016/j.suc.2007.10.008.
- Krpata DM, Blatnik JA, Novitsky YW, Rosen MJ. Séparations des composants antérieurs postérieurs et ouverts : une analyse comparative. Am J Surg. 2012; 203(3):318-322; Discussion 322. doi :10.1016/j.amjsurg.2011.10.009.
- Harth KC, Rosen MJ. Séparation endoscopique ou ouverte dans la reconstruction complexe de la paroi abdominale. Am J Surg. mars 2010 ; 199(3):342-6; Discussion 346-7. doi :10.1016/j.amjsurg.2009.09.015.
- Novitsky YW, Elliott HL, Orenstein SB, Rosen MJ. Relâchement du muscle transverse de l’abdomen : une nouvelle approche de la séparation des composants postérieurs lors d’une reconstruction complexe de la paroi abdominale. Am J Surg. 2012; 204(5):709-716. doi :10.1016/j.amjsurg.2012.02.008.
- Hodgkinson JD, Leo CA, Maeda Y, et al. Une méta-analyse comparant la séparation ouverte des composants antérieurs avec la séparation des composants postérieurs et la libération transverse de l’abdomen dans la réparation des hernies ventrales médianes. Hernie. 2018; 22(4):617-626. doi :10.1007/s10029-018-1757-5.
- Wegdam JA, Thoolen JMM, Nienhuijs SW, de Bouvy N, de Vries Reilingh TS. Revue systématique de la libération transverse de l’abdomen dans la reconstruction complexe de la paroi abdominale. Hernie. 2019; 23(1):5-15. doi :10.1007/s10029-018-1870-5.
Cite this article
Albutt K, Fagenholz P. Réparation rétromusculaire de Rives-Stoppa pour hernie incisionnelle. J Med Insight. 2023; 2023(285). doi :10.24296/jomi/285.

