Reparación retromuscular de Rives-Stoppa para la hernia incisional
Massachusetts General Hospital
Main Text
Table of Contents
No existe consenso sobre el método óptimo de reparación de la hernia ventral, y la elección de las técnicas suele estar dictada por una combinación de factores del paciente y la experiencia del cirujano. Las técnicas de separación de componentes permiten el avance medial del músculo recto abdominal para crear un cierre fascial libre de tensión en la línea media. En este caso, describimos una separación posterior de componentes con colocación de malla de retrorrecto, también conocida como reparación retromuscular de Rives-Stoppa. Con baja morbilidad y mortalidad, esta técnica proporciona una reparación duradera con bajas tasas de recurrencia e infección del sitio quirúrgico, al tiempo que proporciona soporte muscular dinámico y tensión fisiológica, previniendo eventraciones y permitiendo la incorporación de malla en la pared abdominal existente.
Las hernias de la pared abdominal afectan a un estimado de cinco millones de estadounidenses al año. Las hernias se forman como resultado de una pérdida de integridad estructural de la pared abdominal. Las mejores estimaciones disponibles sugieren que alrededor de un tercio de todas las reparaciones de hernias en los Estados Unidos son para hernias ventrales, y de todas las hernias ventrales reparadas, dos tercios son hernias ventrales primarias y un tercio son hernias incisionales. 1 Los trastornos del tejido conectivo, la obesidad, el tabaquismo, el uso de esteroides, la diabetes y otros factores pueden predisponer a los pacientes a la formación de hernias primarias, mientras que las hernias incisionales resultan, por definición, de la ruptura del cierre fascial. Los factores de riesgo para la formación de hernias incisionales incluyen factores del paciente, como se mencionó anteriormente, así como factores técnicos en el momento de la operación índice, como la infección de la herida, la técnica de cierre fascial, el tipo de cirugía y la elección de la incisión. Una vez que se ha formado una hernia, su historia natural es un agrandamiento progresivo debido a un aumento de la tensión de la pared en la ubicación de la hernia. La reparación de hernias debe considerarse seriamente para las hernias sintomáticas y es una necesidad para las hernias encarceladas que resultan en una obstrucción intestinal o hernias estranguladas. Se estima que cada año se gastan tres mil millones de dólares en gastos de atención médica relacionados con la hernia de la pared abdominal. 2, 3 En este caso, realizamos una reparación retromuscular Rives-Stoppa para una hernia incisional sintomática.
Se trata de una mujer de 76 años de edad con antecedentes de un estado de aneurisma de aorta abdominal después de la reparación endovascular, enfermedad pulmonar obstructiva crónica, así como una colectomía derecha por cáncer de colon con resultado de hernia incisional que se presentó para una reparación electiva de hernia. La paciente se encontraba en su estado de salud habitual hasta mayo de 2017, cuando una colonoscopia de detección identificó un cáncer de colon derecho. En junio de 2017 se sometió a una colectomía derecha asistida por laparoscopia, seguida de quimioterapia y radiación para el tratamiento de un adenocarcinoma de colon T4N2. Su colectomía se complicó por una gran hernia incisional, y su tratamiento de quimioterapia se complicó por anorexia y pérdida de peso significativa. Durante la vigilancia, se observó que había desarrollado un aneurisma de aorta abdominal infrarrenal de 5,2 cm por el que se sometió a una reparación endovascular en septiembre de 2018. Su hernia se agrandó progresivamente con el tiempo y fue cada vez más sintomática, interfiriendo con sus actividades de la vida diaria. La reparación con colocación de malla de retrorrecto se planificó de forma electiva. Su índice de masa corporal (IMC) preoperatorio era de 20,2, la albúmina sérica era de 4,0 g/dl y su estado de la Sociedad Americana de Anestesiólogos (ASA) era de 3. Dado un colon lleno de heces y distendido en las imágenes axiales preoperatorias, se administró una preparación intestinal preoperatoria para descomprimir el colon. En el preoperatorio se administraron cefazolina y enoxaparina.
En el examen, se observó que tenía un abdomen blando con una hernia ventral grande que era reducible y no dolorosa con cambios en la piel suprayacente.
La tomografía computarizada (TC) abdominal reveló un agrandamiento progresivo de una hernia ventral abdominal central de la línea media que contenía intestino delgado y grueso sin evidencia de compromiso intestinal o dilatación intestinal aguas arriba. También demostró su colectomía derecha previa y la reparación endovascular de su aneurisma de aorta abdominal infrarrenal (Figura 1).
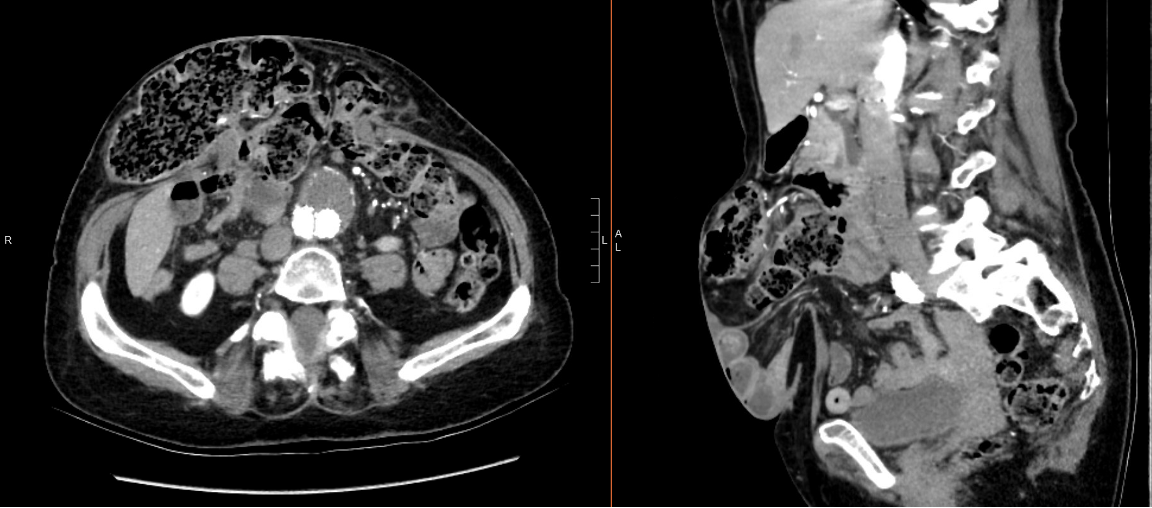
Figura 1: TAC abdominal preoperatorio del paciente. El plano axial (izquierda) y el plano sagital (derecha) de la tomografía computarizada muestran una colectomía derecha previa y una reparación endovascular previa del aneurisma abdominal infrarrenal del paciente.
Las hernias ventrales no necesitan ser reparadas a menos que sean sintomáticas, dado que la obstrucción intestinal y la estrangulación son raras. Incluso en pacientes sintomáticos, no es necesario reparar todas las hernias, ya que el tratamiento no quirúrgico es una alternativa segura. La complejidad de la reparación, las comorbilidades del paciente y la gravedad de los síntomas contribuyen al perfil de riesgo-beneficio de cualquier paciente. Un consorcio internacional de especialistas en hernias identificó el tabaquismo, la obesidad (IMC superior a 35), el estado de ASA 3 o superior, la infección previa del sitio quirúrgico, los cambios superficiales en la piel y la formación de fístulas enterocutáneas como los factores de riesgo más relevantes que afectan el resultado operatorio después de la reparación de la hernia ventral. 4 Los expertos en hernias están de acuerdo en que la reparación electiva de la hernia ventral no se recomienda para pacientes con un IMC de 50 o más sin una intervención para perder peso, para fumadores activos o para aquellos con hemoglobina glicosilada (HbA1c) >8%. De 4 a 6 años
En el contexto del encarcelamiento agudo o el estrangulamiento, la reparación quirúrgica urgente es el tratamiento de elección y puede ser la única opción, incluso en pacientes de alto riesgo a los que no se les puede ofrecer una reparación electiva. El objetivo de la reparación urgente es aliviar el dolor agudo y la obstrucción intestinal, cuando están presentes, y prevenir o tratar el infarto intestinal. La técnica óptima para la reparación varía en función de la situación exacta, incluyendo el estado nutricional, la fisiología aguda y la presencia de contaminación, entre otros factores. En general, cuanto mayor sea el grado de comorbilidad del paciente, más sencilla debe ser la reparación en circunstancias urgentes. Ocasionalmente, un paciente bien nutrido sin trastornos fisiológicos severos o cualquier contaminación puede presentarse de forma aguda y aún así ser candidato a una reparación compleja y definitiva.
Existen numerosas técnicas para la reparación de hernias ventrales o incisionales de la línea media. Las reparaciones de hernias se pueden realizar con o sin malla, y de manera abierta, laparoscópica o robótica. La malla se puede colocar como capa inferior (debajo del peritoneo), subcapa (entre los músculos rectos y la vaina posterior del recto), incrustación (por encima de la fascia) o incrustación (entre los bordes fasciales).
De acuerdo con las pautas, se debe considerar la reparación de la malla para defectos >1 cm y se recomienda para defectos >2 cm.5 La reparación de la malla descarga la tensión de la pared abdominal. Varios ensayos aleatorizados demuestran tasas más bajas de recurrencia con malla. De 7 a 9 años Sin embargo, la malla se asocia con una tasa más alta de complicaciones, incluidas infecciones, erosiones y fístula que las reparaciones sin malla. 7, 10, 11 Un estudio de cohorte basado en registros realizado en Dinamarca demostró que la reparación con malla se asoció con menos reintervenciones por recidivas (malla abierta 12,3 %, malla laparoscópica 10,6 %, malla no malla 17,1 %). 12 En un seguimiento de cinco años, la incidencia acumulada de complicaciones relacionadas con la malla fue de 5,6 % para los pacientes que se sometieron a reparación de malla abierta. 12
La malla para hernias se puede clasificar generalmente en dos grandes clases: sintética y biológica. El crecimiento tisular y la adherencia de la malla sintética son atractivos; sin embargo, tiene la desventaja de provocar adherencias a las superficies serosas. Algunos productos de malla sintética incorporan antiadhesivos en el lado de la malla en contacto con las vísceras para permitir la colocación intraperitoneal con menos preocupación por la erosión tisular. La malla biológica ofrece una alternativa para su uso en un campo contaminado y puede reducir la gravedad de las infecciones de la herida y la necesidad de explantación de la malla cuando se produce una infección en comparación con la malla sintética. A pesar de estas ventajas teóricas, el dogma de que la malla biológica es preferible a la malla sintética en un campo infectado ha sido cada vez más examinado debido en parte a los altos costos, así como a las altas tasas de recurrencia y complicaciones asociadas con la malla biológica. Estudios recientes ofrecen un apoyo cada vez mayor a la idoneidad de las mallas sintéticas o biosintéticas en entornos contaminados, al tiempo que cuestionan las supuestas ventajas de las mallas biológicas. De 13 a 15 años
Las comparaciones directas de las técnicas abiertas y laparoscópicas para la reparación de hernias han sido objeto de muchos ensayos aleatorizados. Una revisión sistemática de 2014 demostró tasas más bajas de infección y drenaje de la herida, pero tasas más altas de lesión intestinal para la reparación laparoscópica en comparación con la reparación abierta. 16 Una revisión Cochrane y un metanálisis posterior llegaron a las mismas conclusiones. 17 y 18 Las circunstancias en las que la reparación laparoscópica puede ser ventajosa pueden incluir un defecto herniario grande, sospecha de defectos múltiples y obesidad. Con la proliferación de plataformas quirúrgicas robóticas, las reparaciones de hernias asistidas por robots se han vuelto más comunes. Si bien tienen un conjunto de indicaciones similar al de la reparación laparoscópica, la reparación de hernias asistida por robot no mejora los resultados, pero prolonga el tiempo quirúrgico y aumenta el costo. 19 y 20
Los defectos grandes o complejos de la pared abdominal presentan un problema quirúrgico particularmente desafiante. La Sociedad Europea de Hernia clasificó las hernias con un defecto de >10 cm como grandes. 21 La elección de la técnica para tratar los defectos de hernia grandes o complejos a menudo está dictada por la experiencia del cirujano y las circunstancias del paciente. La separación posterior de los componentes con la colocación de una malla de retroceso ofrece las ventajas de bajas tasas de recurrencia, bajas tasas de complicaciones de la herida, como seroma o infección, y una excelente incorporación de una malla económica y sin recubrimiento en la pared abdominal.
Los pasos de una separación posterior de componentes con colocación de malla son los siguientes:
1) Incisión y acceso a la cavidad abdominal.
2) Disección y escisión del saco herniario.
3) Disección y cierre de la vaina del recto posterior.
4) Colocación de la malla.
5) Colocación del desagüe.
6) Cierre de la vaina del recto anterior.
7) Cierre de la piel.
Una vez obtenido el acceso a la cavidad abdominal, puede ser necesaria la adhesiólisis en función del grado de adherencias. Una vez que las vísceras están libres de la pared abdominal, el saco herniario debe ser diseccionado de la pared abdominal y la fascia. Si cree que podría necesitar el saco de hernia para ayudar con el cierre, no lo extirpe todo todavía. Utilizamos la disección roma para despegar el saco herniario, facilitando una disección rápida en el plano correcto y preservando así el máximo grosor de la piel suprayacente y la grasa subcutánea. Por lo general, el saco de la hernia se extirpa a lo largo del borde fascial, aunque se puede conservar en reparaciones retrorrectales planificadas para usarse como tejido adicional para el cierre posterior de la vaina. A continuación, se inciden las vainas de los rectos posteriores y se separa la fascia posterior del recto abdominal. Esto crea el espacio en el que se coloca la malla de retrorrectos. Esta disección se lleva a cabo lateralmente a la línea semilunar, el borde lateral del músculo recto abdominal. Es importante visualizar la línea semilunar, ya que el reconocimiento de esta estructura y de los haces neurovasculares perforantes laterales es clave para evitar algunas de las complicaciones potencialmente más devastadoras en la reconstrucción de la pared abdominal. Llegar a la parte medial de la línea semilunar es importante, bajar a la de Cooper en el espacio de Retzius es importante, y subir por debajo de la xifoides constituye una disección adecuada. A medida que se produce esta disección, se encuentran vasos perforantes. Medialmente, estos deben ser sacrificados para desarrollar este espacio, pero las perforantes laterales deben ser preservadas. La disección inferior por debajo de la línea arqueada entra en el espacio de Retzius y puede extenderse hasta los ligamentos de Cooper. La disección superior en el espacio subxifoides puede ser un desafío, ya que la vaina posterior debe separarse de la cara posterior de la línea alba sin entrar en la fascia anterior. Una vez que ambos lados están conectados en las porciones superior e inferior de la disección, se cierra la vaina del recto posterior. La vaina se cierra de forma corrida con pequeños bocados colocados muy juntos para repartir la tensión. Esta capa del cierre no es para la resistencia, sino que funciona para proporcionar una capa de protección entre la malla y las vísceras intraabdominales. La vaina posterior puede ser débil y delgada debido a múltiples sitios de hernia, reparaciones previas y ostomías, entre otras razones. En este caso, utilizamos bisecciones sucesivas con suturas interrumpidas en forma de ocho para aproximar la vaina posterior delgada. El cierre posterior de la vaina debe estar libre de tensión. Si la vaina posterior no se puede cerrar en la línea media, o hay demasiada tensión, se puede realizar una liberación transversa del abdomen (TAR), se puede salvar el espacio con el saco de la hernia (que debe conservarse al comienzo del caso si esto es posible), o alternativamente se puede usar una malla recubierta. En este caso, la decisión de no realizar un TIE puede ser controvertida, pero no sentimos que hubiera tensión que lo justificara. Una vez cerrada la fascia posterior, la atención se centra en la colocación de la malla. En este caso, se utilizó una malla de polipropileno de 30x30 cm que se cortó a medida, rellenando el espacio del retrorecto de línea semilunar a línea semilunar, y del margen costal al pubis. La malla recubierta sin barrera tiene la ventaja de permitir una rápida incorporación en ambos lados de la malla. La malla se asegura en su lugar con suturas transfasciales a través de la fascia anterior. Se debe tener cuidado de colocar las suturas transfasciales de tal manera que distribuyan uniformemente la tensión a través de la malla y la incisión. La malla se asegura en los aspectos superior e inferior y luego sucesivamente en ambos lados, alternando los lados para garantizar una tensión uniforme. La variación en esta técnica es común: algunos cirujanos sujetan la malla a la fascia anterior o posterior sin colocar suturas transfasciales, y algunos no usan suturas en absoluto confiando en la fricción de la malla para mantenerla en su lugar. Los drenajes, en este caso dos drenajes Blake de 19 rondas, se colocan en el espacio del rectrorecto por encima del nivel de la malla. A continuación, la fascia anterior se cierra de forma corrida sobre la parte superior de la malla y drena. Esta es una capa de resistencia, y la fascia debe unirse sin tensión excesiva. A continuación, se extirpa la piel redundante, se drena el espacio subcutáneo si es necesario y se cierra la piel.
La separación de componentes se describió por primera vez en 1990. 22 Utilizado para hernias de tamaño moderado o grande, este término abarca una variedad de técnicas que involucran colgajos de avance musculofascial para permitir el avance medial del músculo recto abdominal para crear un cierre fascial libre de tensión en la línea media. La separación de componentes se puede realizar con o sin malla; sin embargo, la tasa de recurrencia sigue siendo mayor con la reparación de suturas sola. Las técnicas de separación de componentes se pueden utilizar con defectos de hernia de hasta 20 cm y, a veces, incluso más grandes si se utiliza una malla de liberación secundaria o suplementaria para salvar el defecto residual.
Los elementos anatómicos y funcionales de una técnica de separación de componentes incluyen (1) la traslación de la capa muscular de la pared abdominal para ampliar la superficie del tejido; (2) separación de las capas musculares para permitir la máxima expansión de cada unidad muscular individual; (3) desconexión de la unidad muscular de su vaina fascial para facilitar la expansión; (4) uso de la musculatura de la pared abdominal para cubrir el contenido intraabdominal; y (5) el uso de la movilización bilateral para equilibrar las fuerzas de la pared abdominal y centralizar la línea media. 22 y 23 La separación de componentes se puede realizar mediante un abordaje anterior o posterior con o sin liberación secundaria para proporcionar un avance adicional. La elección de la técnica suele depender de la experiencia y los conocimientos del cirujano, ya que ambas tienen éxito en facilitar el avance medial del recto para el cierre de hernias ventrales grandes y complejas. Una separación de componentes anteriores implica la división de la aponeurosis oblicua externa para permitir el avance del colgajo musculofascial hacia la línea media. 24 Sin embargo, la técnica anterior se suele realizar con la creación de grandes colgajos subcutáneos y, por lo tanto, tiene complicaciones más frecuentes en la herida, aunque las técnicas endoscópicas y de conservación de la perforante pueden mitigar algunos de estos problemas. 25 La liberación oblicua externa también da lugar a la disrupción lateral de una capa de la pared abdominal y exige una base intraperitoneal o una malla de incrustación, si se va a utilizar la malla. 24 Esto contrasta con la técnica de separación de componentes posteriores utilizada en este caso, en la que se mantienen todas las capas de la pared abdominal y no hay colgajos subcutáneos grandes. Para hernias más grandes, la técnica utilizada en este caso puede ampliarse mediante el uso de un TAR, que proporciona una movilización más extensa de la pared abdominal lateral hacia la línea media y permite la colocación de prótesis de malla más grandes a costa de la disrupción lateral de una capa de la pared abdominal (en este caso el transverso abdominal). De 24 a 27 años
Muchos abogan por el uso de refuerzo de malla durante la separación de componentes, basándose en gran medida en la extrapolación de los beneficios antes mencionados de la malla para reducir las tasas de recurrencia de hernias en hernias ventrales. Se ha utilizado una variedad de productos de malla sintética y biológica. No existe un ensayo controlado aleatorizado grande que compare la separación de componentes con y sin reparación de malla. Una separación posterior de los componentes facilita la colocación de la malla en una posición de subposición extraperitoneal si se va a utilizar la malla. Teóricamente, esto permite la incorporación de tejido vascularizado en ambos lados y puede dar lugar a tasas de recurrencia más bajas. Como se mencionó anteriormente, esta posición, en combinación con la evitación de colgajos subcutáneos grandes, puede reducir las complicaciones de la herida en comparación con la separación de componentes anteriores, aunque los datos comparativos directos son escasos. 28
Los pacientes con un curso sin complicaciones suelen ser hospitalizados entre tres y cinco días para controlar el dolor y avanzar en la dieta. Los desagües se retiran en función de su ubicación, la duración del tiempo en su lugar y la producción por día. La actividad física suele estar restringida a corto plazo, aunque esto no se ha estudiado rigurosamente. La morbilidad y mortalidad asociadas con la separación posterior de los componentes son raras. En el caso de la hernia ventral grande o compleja, en un estudio en el que se utilizó la separación de componentes para reparar una hernia ventral en pacientes con obesidad mórbida, se notificó que la morbilidad perioperatoria mayor fue del 8 % y la mortalidad perioperatoria del 1 %. 25 La morbilidad se puede atribuir en gran medida a la infección del sitio quirúrgico, el seroma/hematoma y la necrosis del colgajo cutáneo, que ocurren en tasas variables. Hay estudios limitados con seguimiento a largo plazo después de la separación de componentes, pero las tasas de recurrencia para la separación de componentes con malla parecen ser inferiores al 10%.
El caso detallado anteriormente se completó en poco menos de dos horas y media con una pérdida de sangre estimada de 75 ml. Tuvo un postoperatorio sin complicaciones y fue dada de alta el día postoperatorio (POD) 4. Ha sido atendida en seguimiento y se ha recuperado sin dificultad. Sus drenajes fueron retirados en el POD 13 y el POD 17. Se le han realizado imágenes axiales interválticas para la vigilancia del aneurisma de aorta abdominal que demostraron la integridad de la reparación (Figura 2).
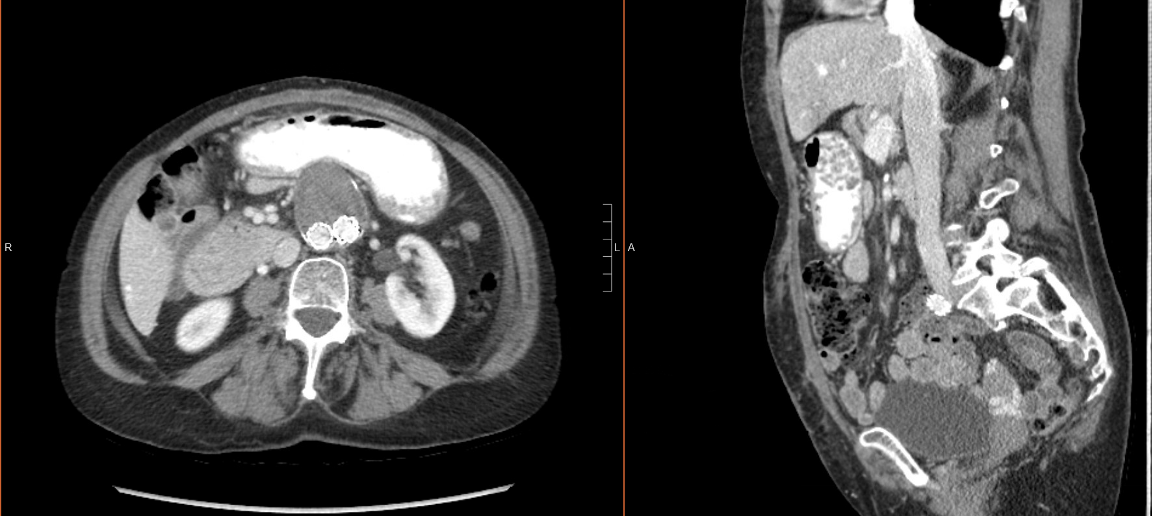
Figura 2: TAC abdominal postoperatorio del paciente. El plano axial (izquierda) y el plano sagital (derecha) de la tomografía computarizada muestran la integridad de la reparación de la hernia ventral.
Pasador de sutura laparoscópica o aguja Reverdin.
Malla de polipropileno de 30x30 cm.
Nada que revelar.
El paciente al que se hace referencia en este videoartículo ha dado su consentimiento informado para ser filmado y es consciente de que la información y las imágenes se publicarán en línea. No se incluye información de identificación ni en el video ni en el artículo de texto.
References
- Rutkow IM. Aspectos demográficos y socioeconómicos de la reparación de hernias en los Estados Unidos en 2003. Surg Clin North Am. 2003; 83(5):1045-1051, V-VI. doi:10.1016/S0039-6109(03)00132-4.
- Park AE, Roth JS, Kavic SM. Hernia de la pared abdominal. Curr Probl Surg. 2006; 43(5):326-375. doi:10.1067/j.cpsurg.2006.02.004.
- Poulose BK, Beck WC, Phillips SE, Sharp KW, Nealon WH, Holzman MD. Los pocos elegidos: el uso desproporcionado de recursos en la reparación de hernias ventrales. Am Surg. Agosto de 2013; 79(8):815-8.
- Parker SG, Reid TH, Boulton R, Wood C, Sanders D, Windsor A. Propuesta de un sistema nacional de triaje para el tratamiento de las hernias ventrales. Ann R Coll Surg Engl. febrero de 2018; 100(2):106-110. doi:10.1308/rcsann.2017.0158.
- Liang MK, Holihan JL, Itani K, et al. Manejo de la hernia ventral: consenso de expertos guiado por revisión sistemática. Ann Surg. 2017; 265(1):80-89. doi:10.1097/SLA.000000000000001701.
- Holihan JL, Alawadi ZM, Harris JW, et al. Hernia ventral: selección, tratamiento y manejo del paciente. Curr Probl Surg. 2016; 53(7):307-354. doi:10.1067/j.cpsurg.2016.06.003.
- Luijendijk RW, Hop WCJ, Van Den Tol MP, et al. Comparación de la reparación de suturas con la reparación con malla para la hernia incisional. N Engl J Med. 2000; 343(6):392-398. doi:10.1056/NEJM200008103430603.
- Kaufmann R, Halm JA, Eker HH, et al. Reparación con malla versus sutura de hernia umbilical en adultos: un ensayo aleatorizado, doble ciego, controlado y multicéntrico. Lancet (Londres, Inglaterra). 2018; 391(10123):860-869. doi:10.1016/S0140-6736(18)30298-8.
- Nguyen MT, Berger RL, Hicks SC, et al. Comparación de los resultados de la reparación con malla sintética frente a la reparación con sutura de la herniorrafia ventral primaria electiva: una revisión sistemática y metanálisis. JAMA Surg. 2014; 149(5):415-421. doi:10.1001/jamasurg.2013.5014.
- den Hartog D, Dur AH, Tuinebreijer WE, Kreis RW. Procedimientos quirúrgicos abiertos para hernias incisionales. Sistema de la Base de Datos Cochrane Rev. 16 de julio de 2008; 2008(3):CD006438. doi:10.1002/14651858.CD006438.pub2.
- Tuinebreijer WE, Amaragiri S, Dur AHM, Kreis RW, Den Hartog D. Procedimientos quirúrgicos abiertos para hernias incisionales. Sistema de la Base de Datos Cochrane Rev. 2007; (2):CD006438. doi:10.1002/14651858.CD006438.
- Kokotovic D, Bisgaard T, Helgstrand F. Recurrencia a largo plazo y complicaciones asociadas con la reparación electiva de la hernia incisional. JAMA. 2016; 316(15):1575-1582. doi:10.1001/jama.2016.15217.
- Majumder A, Winder JS, Wen Y, Pauli EM, Belyansky I, Novitsky YW. Análisis comparativo de los resultados de las mallas biológicas frente a las sintéticas en las reparaciones de hernias contaminadas. Surg (Estados Unidos). 2016; 160(4):828-838. doi:10.1016/j.surg.2016.04.041.
- Kissane NA, Itani KMF. Una década de reparación de hernias incisionales ventrales con matriz dérmica acelular biológica: ¿qué hemos aprendido? Plast Reconstr Surg. 2012; 130(5 Supl. 2). doi:10.1097/prs.0b013e318265a5ec.
- Köckerling F, Alam NN, Antoniou SA, et al. ¿Cuál es la evidencia para el uso de mallas biológicas o biosintéticas en la reconstrucción de la pared abdominal? Hernia. 2018; 22(2):249-269. doi:10.1007/s10029-018-1735-y.
- Zhang Y, Zhou H, Chai Y, Cao C, Jin K, Hu Z. Reparación de hernia ventral e incisional laparoscópica versus abierta: una revisión sistemática y metanálisis. World J Surg. 2014; 38(9):2233-2240. doi:10.1007/s00268-014-2578-z.
- Sauerland S, Walgenbach M, Habermalz B, Seiler CM, Miserez M. Técnicas quirúrgicas laparoscópicas versus abiertas para la reparación de hernias ventrales o incisionales. Sistema de la Base de Datos Cochrane Rev. 2011 16 de marzo; (3):CD007781. doi:10.1002/14651858.CD007781.pub2.
- Al Chalabi H, Larkin J, Mehigan B, McCormick P. Una revisión sistemática de la reparación de hernia incisional abdominal laparoscópica versus abierta, con metanálisis de ensayos controlados aleatorizados. Int J Surg. 2015;20:65-74. doi:10.1016/j.ijsu.2015.05.050.
- Zayan NE, Meara MP, Schwartz JS, Narula VK. Una comparación directa de la reparación robótica y laparoscópica de hernias: resultados informados por el paciente y análisis de costos. Hernia. Diciembre de 2019; 23(6):1115-1121. doi:10.1007/s10029-019-01943-7.
- Meier J, Huerta S. La reparación robótica de la hernia inguinal no es superior a la reparación laparoscópica o abierta. Am J Surg. Julio de 2020; 220(1):251. doi:10.1016/j.amjsurg.2019.11.015.
- Muysoms FE, Miserez M, Berrevoet F, et al. Clasificación de las hernias primarias e incisionales de la pared abdominal. Hernia. 2009; 13(4):407-414. doi:10.1007/s10029-009-0518-x.
- Ramirez OM. Inicio y evolución de la técnica de separación de componentes: recuerdos personales. Clin Plast Surg. 2006; 33(2):241-246, vi. doi:10.1016/j.cps.2005.12.011.
- Shell IV DH, de la Torre J, Andrades P, Vasconez LO. Reparación abierta de hernias incisionales ventrales. Surg Clin North Am. 2008; 88(1):61-83. doi:10.1016/j.suc.2007.10.008.
- Krpata DM, Blatnik JA, Novitsky YW, Rosen MJ. Separaciones de componentes posteriores y anteriores abiertos: un análisis comparativo. Am J Surg. 2012; 203(3):318-322; Discusión 322. doi:10.1016/j.amjsurg.2011.10.009.
- Harth KC, Rosen MJ. Separación endoscópica versus abierta de componentes en la reconstrucción compleja de la pared abdominal. Am J Surg. Marzo de 2010; 199(3):342-6; Discusión 346-7. doi:10.1016/j.amjsurg.2009.09.015.
- Novitsky YW, Elliott HL, Orenstein SB, Rosen MJ. Liberación del músculo transverso del abdomen: un enfoque novedoso para la separación de componentes posteriores durante la reconstrucción compleja de la pared abdominal. Am J Surg. 2012; 204(5):709-716. doi:10.1016/j.amjsurg.2012.02.008.
- Hodgkinson JD, Leo CA, Maeda Y, et al. Un metanálisis que compara la separación abierta de componentes anteriores con la separación de componentes posteriores y la liberación transversa del abdomen en la reparación de hernias ventrales de la línea media. Hernia. 2018; 22(4):617-626. doi:10.1007/s10029-018-1757-5.
- Wegdam JA, Thoolen JMM, Nienhuijs SW, de Bouvy N, de Vries Reilingh TS. Revisión sistemática de la liberación transversa del abdomen en la reconstrucción compleja de la pared abdominal. Hernia. 2019; 23(1):5-15. doi:10.1007/s10029-018-1870-5.
Cite this article
Albutt K, Fagenholz P. Reparación retromuscular de Rives-Stoppa para hernia incisional. J Med Insight. 2023; 2023(285). doi:10.24296/jomi/285.

