Rives-Stoppa retromuskuläre Reparatur für Inzisionshernie
Massachusetts General Hospital
Main Text
Table of Contents
Es gibt keinen Konsens über die optimale Methode der ventralen Hernienreparatur, und die Wahl der Techniken wird in der Regel durch eine Kombination aus Patientenfaktoren und der Expertise des Chirurgen bestimmt. Komponententrennungstechniken ermöglichen eine mediale Vorverlagerung des Musculus rectus abdominis, um einen spannungsfreien Faszienverschluss auf der Mittellinie zu schaffen. In diesem Fall sprechen wir von einer posterioren Komponententrennung mit retrorektus Netzplatzierung, die auch als retromuskuläre Rives-Stoppa-Reparatur bezeichnet wird. Mit geringer Morbidität und Mortalität bietet diese Technik eine dauerhafte Reparatur mit niedrigen Rezidivraten und Infektionen an der Operationsstelle, während sie gleichzeitig eine dynamische Muskelunterstützung und physiologische Spannung bietet, Eventrationen verhindert und die Eingliederung von Netzen in die bestehende Bauchdecke ermöglicht.
Bauchwandhernien betreffen schätzungsweise fünf Millionen Amerikaner pro Jahr. Hernien entstehen als Folge eines Verlustes der strukturellen Integrität der Bauchdecke. Die besten verfügbaren Schätzungen deuten darauf hin, dass etwa ein Drittel aller Hernienreparaturen in den Vereinigten Staaten auf ventrale Hernien zurückzuführen sind, und von allen reparierten ventralen Hernien sind zwei Drittel primäre ventrale Hernien und ein Drittel Narbenhernien. 1 Bindegewebserkrankungen, Fettleibigkeit, Rauchen, Steroidkonsum, Diabetes und andere Faktoren können Patienten für die Bildung einer primären Hernie prädisponieren, während Narbenhernien definitionsgemäß aus dem Zusammenbruch des Faszienverschlusses resultieren. Zu den Risikofaktoren für die Bildung einer Narbenhernie gehören die oben genannten Patientenfaktoren sowie technische Faktoren zum Zeitpunkt der Indexoperation, wie z. B. die Wundinfektion, die Technik des Faszienverschlusses, die Art der Operation und die Wahl des Schnitts. Sobald sich eine Hernie gebildet hat, ist ihr natürlicher Verlauf eine fortschreitende Vergrößerung aufgrund einer Erhöhung der Wandspannung an der Stelle der Hernie. Die Hernienreparatur sollte bei symptomatischen Hernien stark in Betracht gezogen werden und ist eine Notwendigkeit bei eingeklemmten Hernien, die zu einem Darmverschluss oder strangulierten Hernien führen. Schätzungsweise drei Milliarden Dollar werden jedes Jahr für Gesundheitsausgaben im Zusammenhang mit Bauchwandhernien ausgegeben. 2, 3 In diesem Fall führen wir eine retromuskuläre Rives-Stoppa-Reparatur bei einer symptomatischen Narbenhernie durch.
Es handelt sich um eine 76-jährige Frau mit einer Vorgeschichte mit einem abdominalen Aortenaneurysma-Status nach endovaskulärer Reparatur, chronisch obstruktiver Lungenerkrankung sowie einer rechten Kolektomie wegen Dickdarmkrebs, die zu einer Narbenhernie führte und sich für eine elektive Hernienreparatur vorstellte. Die Patientin befand sich bis Mai 2017 in ihrem gewohnten Gesundheitszustand, als bei einer Vorsorgekoloskopie ein rechter Darmkrebs festgestellt wurde. Im Juni 2017 unterzog sie sich einer laparoskopisch assistierten rechten Kolektomie, gefolgt von Chemotherapie und Bestrahlung zur Behandlung eines T4N2-Kolonadenokarzinoms. Ihre Kolektomie wurde durch einen großen Narbenbruch erschwert, und ihre Chemotherapie wurde durch Magersucht und erheblichen Gewichtsverlust erschwert. Während der Überwachung wurde festgestellt, dass sie ein 5,2 cm langes infrarenales Bauchaortenaneurysma entwickelt hatte, für das sie sich im September 2018 einer endovaskulären Reparatur unterzog. Ihre Hernie vergrößerte sich im Laufe der Zeit zunehmend und war zunehmend symptomatisch, was ihre Aktivitäten des täglichen Lebens beeinträchtigte. Die Reparatur mit retrorektus Netzplatzierung wurde elektiv geplant. Ihr präoperativer Body-Mass-Index (BMI) lag bei 20,2, ihr Serumalbuminwert bei 4,0 g/dl und ihr Status bei der American Society of Anesthesiologists (ASA) bei 3. Bei einem mit Stuhl gefüllten und aufgeblähten Dickdarm in der präoperativen axialen Bildgebung wurde eine präoperative Darmvorbereitung durchgeführt, um den Dickdarm zu dekomprimieren. Cefazolin und Enoxaparin wurden präoperativ verabreicht.
Bei der Untersuchung wurde festgestellt, dass sie einen weichen Bauch mit einer großen ventralen Hernie hatte, die reduzierbar und nicht druckempfindlich war und keine darüber liegenden Hautveränderungen aufwies.
Die abdominelle Computertomographie (CT) zeigte eine fortschreitende Vergrößerung einer zentralen ventralen Hernie des Abdomens in der Mittellinie, die Dünn- und Dickdarm enthielt, ohne Hinweise auf eine Darmkompromittierung oder eine vorgelagerte Darmdilatation. Es zeigte auch ihre vorherige rechte Kolektomie und endovaskuläre Reparatur ihres infrarenalen abdominalen Aortenaneurysmas (Abbildung 1).
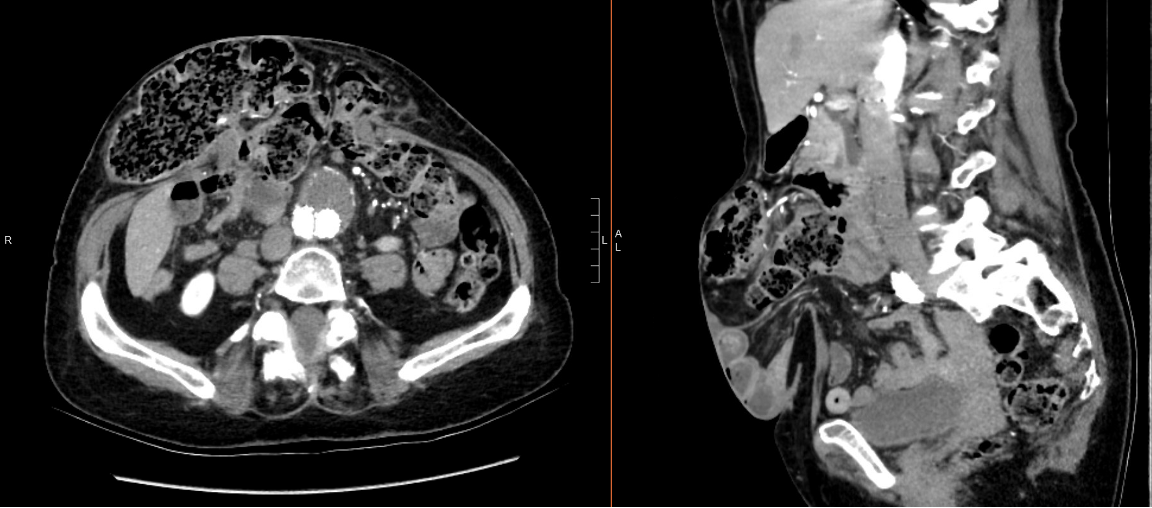
Abbildung 1: Präoperativer abdominaler CT-Scan des Patienten. Die axiale Ebene (links) und die sagittale Ebene (rechts) des CT-Scans zeigen eine vorherige rechte Kolektomie und eine vorherige endovaskuläre Reparatur des infrarenalen abdominalen Aneurysmas des Patienten.
Ventrale Hernien müssen nicht repariert werden, es sei denn, sie sind symptomatisch, da Darmverschluss und Strangulation selten sind. Selbst bei symptomatischen Patienten müssen nicht alle Hernien repariert werden, da die nicht-operative Behandlung eine sichere Alternative darstellt. Die Komplexität der Reparatur, die Komorbiditäten der Patienten und die Schwere der Symptome tragen zum Risiko-Nutzen-Profil für jeden Patienten bei. Ein internationales Konsortium von Hernienspezialisten identifizierte Raucherstatus, Adipositas (BMI größer als 35), ASS-Status 3 oder höher, frühere Infektionen an der Operationsstelle, oberflächliche Hautveränderungen und enterokutane Fistelbildung als die relevantesten Risikofaktoren, die das operative Ergebnis nach ventraler Hernienreparatur beeinflussen. 4 Hernienexperten sind sich einig, dass eine elektive ventrale Hernienreparatur für Patienten mit einem BMI von 50 oder mehr ohne Gewichtsverlustintervention, für aktive Raucher oder für Patienten mit glykosyliertem Hämoglobin (HbA1c) >8 %) nicht empfohlen wird. 4–6
Im Falle einer akuten Inkarzeration oder Strangulation ist eine dringende chirurgische Reparatur die Behandlung der Wahl und kann die einzige Option sein, auch bei Hochrisikopatienten, denen möglicherweise keine elektive Reparatur angeboten wird. Das Ziel der dringenden Reparatur ist es, akute Schmerzen und Darmverschluss, falls vorhanden, zu lindern und Darminfarkt zu verhindern oder zu behandeln. Die optimale Technik für die Reparatur hängt von der genauen Situation ab, einschließlich des Ernährungszustands, der akuten Physiologie und des Vorhandenseins einer Kontamination, neben anderen Faktoren. Im Allgemeinen gilt: Je größer der Grad der Komorbidität des Patienten, desto einfacher sollte die Reparatur in dringenden Fällen sein. Gelegentlich kann ein gut ernährter Patient ohne schwere physiologische Störung oder Kontamination akut auftreten und dennoch ein Kandidat für eine komplexe, endgültige Reparatur sein.
Es gibt zahlreiche Techniken zur Reparatur von ventralen Mittellinien- oder Narbenhernien. Hernienreparaturen können mit oder ohne Netz und offen, laparoskopisch oder robotergestützt durchgeführt werden. Das Netz kann als Unterlage (unterhalb des Bauchfells), als Sublay (zwischen den Rektusmuskeln und der hinteren Rektusscheide), als Onlay (über der Faszie) oder als Inlay (zwischen den Faszienkanten) platziert werden.
Gemäß den Richtlinien sollte bei Defekten >1 cm eine Netzreparatur in Betracht gezogen werden und wird bei Defekten >2 cm empfohlen.5 Die Netzreparatur entlastet die Bauchdecke. Mehrere randomisierte Studien zeigen niedrigere Rezidivraten mit Mesh. 7–9 Netze sind jedoch mit einer höheren Rate an Komplikationen wie Infektionen, Erosionen und Fisteln verbunden als Reparaturen ohne Netz. 7, 10, 11 Eine registerbasierte Kohortenstudie in Dänemark zeigte, dass die Netzreparatur mit weniger Reoperationen für Rezidive verbunden war (offenes Netz 12,3 %, laparoskopisches Netz 10,6 %, Nicht-Netz 17,1 %). 12 Bei einer fünfjährigen Nachbeobachtung betrug die kumulative Inzidenz von netzbedingten Komplikationen 5,6 % bei Patienten, die sich einer offenen Netzreparatur unterzogen hatten. 12
Herniennetze können im Allgemeinen in zwei große Klassen eingeteilt werden: synthetisch und biologisch. Das Einwachsen von Gewebe und das Anhaften von synthetischen Netzen sind ansprechend; Es hat jedoch den Nachteil, dass es zu Verklebungen an serosalen Oberflächen kommt. Einige synthetische Netzprodukte enthalten Antiadhäsive an der Seite des Netzes, die mit den Eingeweiden in Kontakt kommt, um eine intraperitoneale Platzierung mit weniger Bedenken hinsichtlich der Gewebeerosion zu ermöglichen. Biologisches Netz bietet eine Alternative für den Einsatz in einem kontaminierten Feld und kann im Vergleich zu synthetischen Netzen die Schwere von Wundinfektionen und die Notwendigkeit einer Netzexplantation bei einer Infektion verringern. Trotz dieser theoretischen Vorteile wurde das Dogma, dass biologische Netze in einem infizierten Feld synthetischen Netzen vorzuziehen sind, zunehmend hinterfragt, was zum Teil auf die hohen Kosten sowie die hohen Rezidivraten und Komplikationen im Zusammenhang mit biologischen Netzen zurückzuführen ist. Jüngste Studien belegen zunehmend die Eignung von synthetischen oder biosynthetischen Netzen in kontaminierten Umgebungen und stellen gleichzeitig die angeblichen Vorteile biologischer Netze in Frage. 13–15 Uhr
Kopf-an-Kopf-Vergleiche von offenen und laparoskopischen Techniken zur Hernienreparatur waren Gegenstand vieler randomisierter Studien. Eine systematische Übersichtsarbeit aus dem Jahr 2014 zeigte niedrigere Raten von Wundinfektionen und -drainagen, aber höhere Raten von Darmverletzungen bei laparoskopischen Eingriffen im Vergleich zur offenen Reparatur. 16 Ein Cochrane-Review und eine anschließende Metaanalyse kamen zu den gleichen Schlussfolgerungen. 17, 18 Zu den Umständen, unter denen eine laparoskopische Reparatur von Vorteil sein kann, gehören ein großer Herniendefekt, der Verdacht auf mehrere Defekte und Fettleibigkeit. Mit der Verbreitung von robotergestützten chirurgischen Plattformen sind robotergestützte Hernienreparaturen immer häufiger geworden. Obwohl sie ähnliche Indikationen wie die laparoskopische Reparatur haben, verbessert die robotergestützte Hernienreparatur nicht die Ergebnisse, sondern verlängert die Operationszeit und erhöht die Kosten. 19, 20
Große oder komplexe Bauchwanddefekte stellen ein besonders herausforderndes chirurgisches Problem dar. Die Europäische Herniengesellschaft stufte Hernien mit einem Defekt von >10 cm als groß ein. 21 Die Wahl der Technik zur Behandlung großer oder komplexer Herniendefekte wird oft von der Expertise des Chirurgen und den Umständen des Patienten bestimmt. Die posteriore Komponententrennung mit retrorektusartiger Netzplatzierung bietet die Vorteile niedriger Rezidivraten, geringer Raten von Wundkomplikationen wie Serom oder Infektionen und einer hervorragenden Einarbeitung von kostengünstigem, unbeschichtetem Netz in die Bauchdecke.
Die Schritte einer posterioren Bauteiltrennung mit Netzplatzierung sind wie folgt:
1) Inzision und Zugang zur Bauchhöhle.
2) Herniensackdissektion und Exzision.
3) Dissektion und Verschluss der hinteren Rektusscheide.
4) Platzierung des Netzes.
5) Platzierung des Abflusses.
6) Verschluss der vorderen Rektusscheide.
7) Verschluss der Haut.
Sobald der Zugang zur Bauchhöhle erhalten ist, kann je nach Grad der Verwachsungen eine Adhäsiolyse erforderlich sein. Sobald die Eingeweide von der Bauchdecke befreit sind, muss der Bruchsack von der Bauchdecke und den Faszien entfernt werden. Wenn du glaubst, dass du den Bruchsack brauchst, um den Verschluss zu unterstützen, schneide noch nicht alles heraus. Wir verwenden die stumpfe Dissektion, um den Bruchsack abzuschälen, was eine schnelle Dissektion in der richtigen Ebene ermöglicht und so die maximale Dicke der darüber liegenden Haut und des Unterhautfettgewebes erhält. Der Bruchsack wird in der Regel entlang des Faszienrandes herausgeschnitten, kann aber bei geplanten retrorektus Reparaturen erhalten bleiben, um als zusätzliches Gewebe für den Verschluss der hinteren Scheide verwendet zu werden. Anschließend werden die hinteren Rektusscheiden eingeschnitten und die hintere Faszie vom Rectus abdominis getrennt. Dadurch entsteht der Raum, in dem das Retrorectus-Netz platziert wird. Diese Dissektion wird seitlich zur Linea semilunaris, dem lateralen Rand des Musculus rectus abdominis, durchgeführt. Es ist wichtig, die Linea semilunaris zu visualisieren, da das Erkennen dieser Struktur und der seitlich perforierenden neurovaskulären Bündel der Schlüssel ist, um einige der potenziell verheerendsten Komplikationen bei der Bauchwandrekonstruktion zu vermeiden. Es ist wichtig, nur medial zur Linea semilunaris zu gelangen, es ist wichtig, zu Cooper im Raum von Retzius zu gelangen, und das Aufstehen unter dem Xiphoid stellt eine angemessene Sektion dar. Bei dieser Dissektion treten perforierende Gefäße auf. Medial müssen diese geopfert werden, um diesen Raum zu entwickeln, aber laterale Perforatoren sollten erhalten bleiben. Die untere Dissektion unterhalb der Bogenlinie tritt in den Retziusraum ein und kann sich bis zu den Cooper-Bändern erstrecken. Die obere Dissektion im subxiphoiden Raum kann eine Herausforderung darstellen, da die hintere Scheide von der hinteren Seite der Linea alba gelöst werden muss, ohne in die vordere Faszie einzudringen. Sobald beide Seiten am oberen und unteren Teil der Dissektion verbunden sind, wird die hintere Rektusscheide verschlossen. Die Hülle wird laufend geschlossen, wobei kleine Bisse dicht beieinander liegen, um die Spannung zu verteilen. Diese Schicht des Verschlusses dient nicht der Festigkeit, sondern dient dazu, eine Schutzschicht zwischen dem Netz und den intraabdominalen Eingeweiden zu bieten. Die hintere Scheide kann unter anderem aufgrund mehrerer Hernienstellen, früherer Reparaturen und Stomas schwach und dünn sein. In diesem Fall verwenden wir eine sukzessive Halbierung mit einer unterbrochenen Achternaht, um die dünne hintere Hülle anzunähern. Der hintere Mantelverschluss sollte spannungsfrei sein. Wenn die hintere Scheide in der Mittellinie nicht verschlossen werden kann oder zu viel Spannung vorhanden ist, kann ein Transversus abdominis Release (TAR) durchgeführt werden, die Lücke kann mit dem Bruchsack überbrückt werden (der zu Beginn des Falles erhalten werden muss, wenn dies möglich ist) oder alternativ kann ein beschichtetes Netz verwendet werden. In diesem Fall mag die Entscheidung, keine TAR durchzuführen, umstritten sein, aber wir hatten nicht das Gefühl, dass es Spannungen gibt, die dies rechtfertigen würden. Sobald die hintere Faszie geschlossen ist, richtet sich die Aufmerksamkeit auf die Platzierung des Netzes. In diesem Fall haben wir ein 30 x 30 cm großes Polypropylennetz verwendet, das auf Maß geschnitten wurde und den retrorektus von halbmondförmiger Linie zu halbmondförmiger Linie und vom Rippenrand bis zum Schambein ausfüllt. Barrierefreies Gewebe hat den Vorteil, dass es eine schnelle Einarbeitung auf beiden Seiten des Gewebes ermöglicht. Das Netz wird mit transfaszialen Nähten durch die vordere Faszie fixiert. Es sollte darauf geachtet werden, dass die transfaszialen Nähte so platziert werden, dass sie die Spannung gleichmäßig über das Netz und den Schnitt verteilen. Das Netz wird an den oberen und unteren Seiten befestigt und dann nacheinander auf beiden Seiten, wobei die Seiten abwechselnd befestigt werden, um eine gleichmäßige Spannung zu gewährleisten. Variationen in dieser Technik sind üblich – einige Chirurgen heften das Netz an die vordere oder hintere Faszie, ohne transfasziale Nähte zu platzieren, und andere verwenden überhaupt keine Nähte und verlassen sich auf die Reibung des Netzes, um es an Ort und Stelle zu halten. Die Drainagen, in diesem Fall zwei 19-Round-Blake-Drainagen, werden dann in den Rectrorectus-Raum über dem Niveau des Gitters gelegt. Die vordere Faszie wird dann laufend über die Oberseite des Netzes geschlossen und drainiert. Dies ist eine Festigkeitsschicht, und die Faszien sollten ohne übermäßige Spannung zusammenkommen. Überflüssige Haut wird dann entfernt, der Unterhautraum bei Bedarf drainiert und die Haut verschlossen.
Die Komponententrennung wurde erstmals 1990 beschrieben. 22 Dieser Begriff, der bei mittelgroßen oder großen Hernien verwendet wird, umfasst eine Vielzahl von Techniken, bei denen muskulofasziale Vorschublappen verwendet werden, um eine mediale Vorverlagerung des Musculus rectus abdominis zu ermöglichen, um einen spannungsfreien Faszienverschluss in der Mittellinie zu schaffen. Die Bauteiltrennung kann mit oder ohne Netz erfolgen; Die Rezidivrate bleibt jedoch bei der reinen Nahtreparatur höher. Bei Herniendefekten von bis zu 20 cm und manchmal sogar noch größer, wenn ein sekundäres Trenn- oder Ergänzungsnetz zur Überbrückung des Restdefekts verwendet wird, können Komponententrenntechniken eingesetzt werden.
Zu den anatomischen und funktionellen Elementen einer Komponententrennungstechnik gehören (1) die Translation der Muskelschicht der Bauchwand zur Vergrößerung der Gewebeoberfläche; (2) Trennung der Muskelschichten, um eine maximale Ausdehnung jeder einzelnen Muskeleinheit zu ermöglichen; (3) Trennung der Muskeleinheit von ihrer Faszienhülle, um die Expansion zu erleichtern; (4) Verwendung der Bauchwandmuskulatur zur Abdeckung des intraabdominellen Inhalts; und (5) Nutzung der bilateralen Mobilisation, um die Kräfte der Bauchdecke auszugleichen und die Mittellinie zu zentralisieren. 22, 23 Die Komponententrennung kann mit einem anterioren oder posterioren Zugang mit oder ohne sekundäre Freisetzung durchgeführt werden, um einen zusätzlichen Vorschub zu erzielen. Die Wahl der Technik hängt in der Regel von der Erfahrung und dem Fachwissen des Chirurgen ab, da beide erfolgreich sind, um das mediale Vorschieben des Rektus für den Verschluss großer und komplexer ventraler Hernien zu erleichtern. Bei einer vorderen Komponententrennung wird die Aponeurose der äußeren schrägen Aponeurose geteilt, um das Vorrücken des muskulofaszialen Lappens in die Mittellinie zu ermöglichen. 24 Die anteriore Technik wird jedoch in der Regel mit großen subkutanen Lappen durchgeführt und führt daher zu häufigeren Wundkomplikationen, obwohl perforatorerhaltende und endoskopische Techniken einige dieser Probleme lindern können. 25 Die externe schräge Freisetzung führt auch zu einer seitlichen Störung einer Schicht der Bauchdecke und erfordert eine intraperitoneale Unterlage oder ein Onlaynetz, wenn das Netz verwendet werden soll. 24 Dies steht im Gegensatz zu der im vorliegenden Fall angewandten Technik der posterioren Komponententrennung, bei der alle Schichten der Bauchdecke erhalten bleiben und keine großen subkutanen Lappen vorhanden sind. Bei größeren Hernien kann die in diesem Fall verwendete Technik durch die Verwendung einer TAR erweitert werden, die eine umfassendere Mobilisierung der lateralen Bauchwand zur Mittellinie ermöglicht und die Platzierung größerer Netzprothesen auf Kosten einer lateralen Unterbrechung einer Schicht der Bauchdecke (in diesem Fall des Transversus abdominis) ermöglicht. 24-27
Viele befürworten die Verwendung von Netzverstärkungen während einer Komponententrennung, die weitgehend auf der Extrapolation der oben genannten Vorteile von Netzen zur Verringerung der Hernienrezidivraten bei ventralen Hernien basiert. Es wurde eine Vielzahl von synthetischen und biologischen Netzprodukten verwendet. Es gibt keine große randomisierte Kontrollstudie, in der die Komponententrennung mit und ohne Netzreparatur verglichen wird. Eine posteriore Komponententrennung erleichtert das Platzieren des Netzes in einer extraperitonealen Sublay-Position, wenn das Netz verwendet werden soll. Theoretisch ermöglicht dies den Einbau von vaskularisiertem Gewebe in beide Seiten und kann zu niedrigeren Rezidivraten führen. Wie oben angedeutet, kann diese Position in Kombination mit der Vermeidung großer subkutaner Lappen Wundkomplikationen im Vergleich zur Trennung der vorderen Komponenten reduzieren, obwohl direkte Vergleichsdaten spärlich sind. Nr. 28
Patienten mit einem unkomplizierten Verlauf werden in der Regel zwischen drei und fünf Tagen zur Schmerzkontrolle und Diät ins Krankenhaus eingeliefert. Abflüsse werden basierend auf ihrem Standort, der Dauer der Verweildauer und der Leistung pro Tag entfernt. Körperliche Aktivität ist oft kurzfristig eingeschränkt, obwohl dies nicht gründlich untersucht wurde. Morbidität und Mortalität im Zusammenhang mit einer posterioren Komponententrennung sind selten. Für große oder komplexe ventrale Hernien berichtete eine Studie, in der die Komponententrennung zur Reparatur einer ventralen Hernie bei krankhaft adipösen Patienten verwendet wurde, dass die schwere perioperative Morbidität 8 % und die perioperative Mortalität 1 % betrug. 25 Die Morbidität ist weitgehend auf Infektionen an der Operationsstelle, Serome/Hämatome und Hautlappennekrose zurückzuführen, die mit unterschiedlicher Häufigkeit auftreten. Es gibt nur begrenzte Studien mit Langzeit-Follow-up nach Bauteiltrennung, aber die Rezidivraten für die Bauteiltrennung mit Netz scheinen weniger als 10% zu betragen.
Der oben beschriebene Fall wurde in knapp zweieinhalb Stunden mit einem geschätzten Blutverlust von 75 ml abgeschlossen. Sie hatte einen unkomplizierten postoperativen Verlauf und wurde am postoperativen Tag (POD) 4 nach Hause entlassen. Sie wurde in der Nachsorge gesehen und hat sich ohne Schwierigkeiten erholt. Ihre Drainagen wurden an POD 13 und POD 17 entfernt. Sie hatte eine axiale Intervallbildgebung zur Überwachung des Bauchaortenaneurysmas, die die Integrität der Reparatur demonstrierte (Abbildung 2).
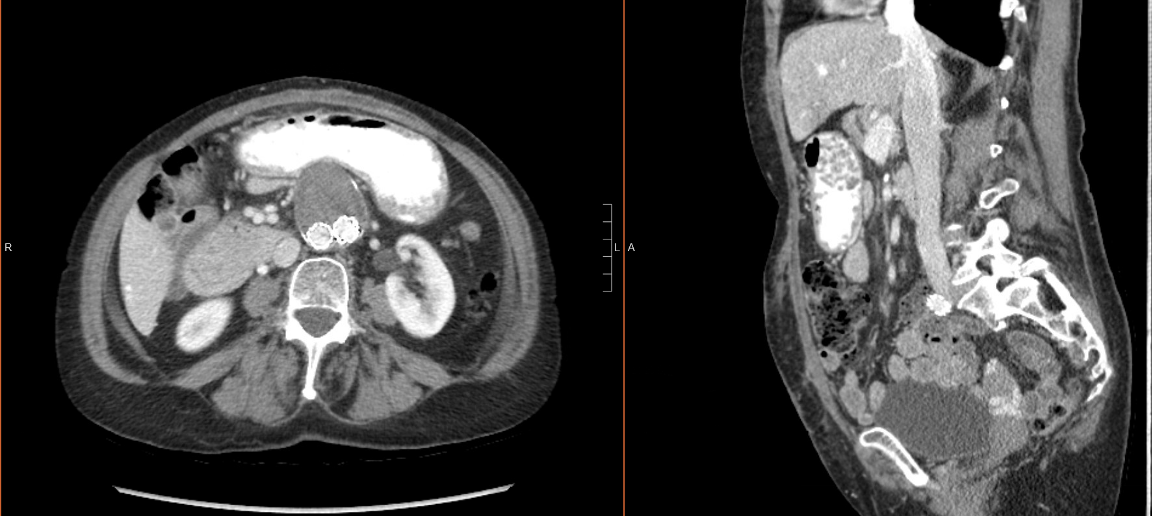
Abbildung 2: Postoperativer abdominaler CT-Scan des Patienten. Die axiale Ebene (links) und die sagittale Ebene (rechts) des CT-Scans zeigen die Integrität der Reparatur der ventralen Hernie.
Laparoskopischer Nahtpasser oder Reverdin-Nadel.
30x30 cm Polypropylen-Netz.
Nichts zu verraten.
Der Patient, auf den in diesem Videoartikel Bezug genommen wird, hat sein Einverständnis gegeben, gefilmt zu werden, und ist sich bewusst, dass Informationen und Bilder online veröffentlicht werden. Weder im Video noch im Textartikel sind identifizierende Informationen enthalten.
References
- Rutkow IM. Demographische und sozioökonomische Aspekte der Hernienreparatur in den Vereinigten Staaten im Jahr 2003. Surg Clin Nord Am. 2003; 83(5):1045-1051, V-VI. doi:10.1016/S0039-6109(03)00132-4.
- Park AE, Roth JS, Kavic SM. Bauchwandhernie. Curr Probl Surg. 2006; 43(5):326-375. doi:10.1067/j.cpsurg.2006.02.004.
- Poulose BK, Beck WC, Phillips SE, Sharp KW, Nealon WH, Holzman MD. Die wenigen Auserwählten: unverhältnismäßiger Ressourcenverbrauch bei der ventralen Hernienreparatur. Am Surg. 2013 Aug; 79(8):815-8.
- Parker SG, Reid TH, Boulton R, Wood C, Sanders D, Windsor A. Vorschlag für ein nationales Triage-System zur Behandlung ventraler Hernien. Ann R Coll Surg Engl. 2018 Februar; 100(2):106-110. doi:10.1308/rcsann.2017.0158.
- Liang MK, Holihan JL, Itani K, et al. Ventrales Hernienmanagement: Expertenkonsens geleitet durch systematische Übersichtsarbeit. Ann Surg. 2017; 265(1):80-89. doi:10.1097/SLA.00000000000001701.
- Holihan JL, Alawadi ZM, Harris JW, et al. Ventrale Hernie: Patientenauswahl, -behandlung und -management. Curr Probl Surg. 2016; 53(7):307-354. doi:10.1067/j.cpsurg.2016.06.003.
- Luijendijk RW, Hop WCJ, Van Den Tol MP, et al. Ein Vergleich der Nahtreparatur mit der Netzreparatur bei Narbenhernie. N engl J Med. 2000; 343(6):392-398. doi:10.1056/NEJM200008103430603.
- Kaufmann R, Halm JA, Eker HH, et al. Netz- versus Nahtreparatur bei Nabelbrüchen bei Erwachsenen: eine randomisierte, doppelblinde, kontrollierte, multizentrische Studie. Lancet (London, England). 2018; 391(10123):860-869. doi:10.1016/S0140-6736(18)30298-8.
- Nguyen MT, Berger RL, Hicks SC, et al. Vergleich der Ergebnisse von synthetischem Netz vs. Nahtreparatur bei elektiver primärer ventraler Herniorrhaphie: eine systematische Übersichtsarbeit und Metaanalyse. JAMA Surg. 2014; 149(5):415-421. doi:10.1001/jamasurg.2013.5014.
- den Hartog D, Dur AH, Tuinebreijer WE, Kreis RW. Offene chirurgische Eingriffe bei Narbenbrüchen. Cochrane Datenbank Syst Rev. 16. Juli 2008; 2008(3):CD006438. doi:10.1002/14651858.CD006438.pub2.
- Tuinebreijer WE, Amaragiri S, Dur AHM, Kreis RW, Den Hartog D. Offene chirurgische Eingriffe bei Narbenhernien. Cochrane Datenbank Syst Rev. 2007; (2):CD006438. doi:10.1002/14651858.CD006438.
- Kokotovic D, Bisgaard T, Helgstrand F. Langzeitrezidiv und Komplikationen im Zusammenhang mit der elektiven Inzisionshernienreparatur. JAMA. 2016; 316(15):1575-1582. doi:10.1001/jama.2016.15217.
- Majumder A, Winder JS, Wen Y, Pauli EM, Belyansky I, Novitsky YW. Vergleichende Analyse der Ergebnisse von biologischen und synthetischen Netzen bei kontaminierten Hernienreparaturen. Surg (Vereinigte Staaten). 2016; 160(4):828-838. doi:10.1016/j.surg.2016.04.041.
- Kissane NA, Itani KMF. Ein Jahrzehnt ventraler Inzisionshernienreparaturen mit biologischer azellulärer dermaler Matrix: Was haben wir gelernt? Plast Reconstr Surg. 2012; 130 Abs. 5 Suppl 2. doi:10.1097/prs.0b013e318265a5ec.
- Köckerling F, Alam NN, Antoniou SA, et al. Welche Evidenz gibt es für den Einsatz von biologischen oder biosynthetischen Netzen bei der Bauchwandrekonstruktion? Hernie. 2018; 22(2):249-269. doi:10.1007/s10029-018-1735-y.
- Zhang Y, Zhou H, Chai Y, Cao C, Jin K, Hu Z. Laparoskopische versus offene Inzisions- und ventrale Hernienreparatur: Eine systematische Überprüfung und Metaanalyse. Welt J Surg. 2014; 38(9):2233-2240. doi:10.1007/s00268-014-2578-z.
- Sauerland S, Walgenbach M, Habermalz B, Seiler CM, Miserez M. Laparoskopische versus offene Operationstechniken zur ventralen oder inzisionalen Hernienreparatur. Cochrane Database Syst Rev. 16. März 2011; (3):CD007781. doi:10.1002/14651858.CD007781.pub2.
- Al Chalabi H, Larkin J, Mehigan B, McCormick P. Eine systematische Übersichtsarbeit zur laparoskopischen versus offenen abdominalen Inzisionshernienreparatur mit Metaanalyse randomisierter kontrollierter Studien. Int J Surg. 2015;20:65-74. doi:10.1016/j.ijsu.2015.05.050.
- Zayan NE, Meara MP, Schwartz JS, Narula VK. Ein direkter Vergleich von robotergestützter und laparoskopischer Hernienreparatur: patientenberichtete Ergebnisse und Kostenanalyse. Hernie. 2019 Dezember; 23(6):1115-1121. doi:10.1007/s10029-019-01943-7.
- Meier J, Huerta S. Die robotergestützte Reparatur von Leistenhernien ist der laparoskopischen oder offenen Reparatur nicht überlegen. Am J Surg. 2020 Juli; 220(1):251. doi:10.1016/j.amjsurg.2019.11.015.
- Muysoms FE, Miserez M, Berrevoet F, et al. Klassifikation von primären und inzisionalen Bauchwandhernien. Hernie. 2009; 13(4):407-414. doi:10.1007/s10029-009-0518-x.
- Ramirez OM. Anfänge und Entwicklung der Technik der Komponententrennung: persönliche Erinnerungen. Clin Plast Surg. 2006; 33(2):241-246, vi. doi:10.1016/j.cps.2005.12.011.
- Shell IV DH, de la Torre J, Andrades P, Vasconez LO. Offene Reparatur von ventralen Narbenhernien. Surg Clin Nord Am. 2008; 88(1):61-83. doi:10.1016/j.suc.2007.10.008.
- Krpata DM, Blatnik JA, Novitsky YW, Rosen MJ. Trennungen von posterioren und offenen Frontzahnkomponenten: eine vergleichende Analyse. Am J Surg. 2012; 203(3):318-322; Diskussion 322. doi:10.1016/j.amjsurg.2011.10.009.
- Harth KC, Rosen MJ. Endoskopische versus offene Komponententrennung bei komplexen Bauchwandrekonstruktionen. Am J Surg. 2010 Mär; 199(3):342-6; Diskussion 346-7. doi:10.1016/j.amjsurg.2009.09.015.
- Novitsky YW, Elliott HL, Orenstein SB, Rosen MJ. Transversus abdominis Muscle Release: ein neuartiger Ansatz zur posterioren Komponententrennung während einer komplexen Bauchwandrekonstruktion. Am J Surg. 2012; 204(5):709-716. doi:10.1016/j.amjsurg.2012.02.008.
- Hodgkinson JD, Leo CA, Maeda Y, et al. Eine Metaanalyse, in der die offene anteriore Komponententrennung mit der posterioren Komponententrennung und der transversus abdominis-Freisetzung bei der Reparatur von ventralen Mittellinienhernien verglichen wird. Hernie. 2018; 22(4):617-626. doi:10.1007/s10029-018-1757-5.
- Wegdam JA, Thoolen JMM, Nienhuijs SW, de Bouvy N, de Vries Reilingh TS. Systematische Übersichtsarbeit zur Freisetzung von Transversus abdominis bei komplexer Bauchwandrekonstruktion. Hernie. 2019; 23(1):5-15. doi:10.1007/s10029-018-1870-5.
Cite this article
Albutt K, Fagenholz P. Rives-Stoppa retromuskuläre Reparatur bei Narbenhernie. J Med Insight. 2023; 2023(285). doi:10.24296/jomi/285.

