오른쪽에 피질 절약이 있는 양측 후방 후복막경 부신 절제술
Main Text
피질 보존 부신 절제술은 부신 종양을 절제하는 동시에 부신 부전을 예방하기 위해 영향을 받지 않은 부신 조직을 보존할 수 있습니다. 이는 양측 부신 종양, 일반적으로 갈색세포종에 영향을 받는 환자에게 특히 중요합니다.
후방 후복막경 부신절제술(PRA)은 기존의 복강경 경복부 부신절제술 및 개방 접근법에 비해 부신 절제술에 대한 최소 침습적 접근법을 허용합니다. PRA 기법은 전 세계적으로 대량 내분비 외과 의사들에 의해 점점 더 많이 사용되고 있습니다. 이 접근법은 양측성 질환이 있는 환자를 치료하는 데 이상적이며, 다발성 내분비 종양 2A 증후군 환경에서 양측 갈색세포종을 앓고 있는 환자의 이 경우에 사용되었습니다.
후방 후복막 내시경 부신절제술(PRA)은 Walz와 동료들에 의해 독일에서 처음 대중화되었습니다. 부신은 복강경 기구와 CO2 주입을 사용하는 후복막 접근법을 통해 접근합니다. 1 그렇게 함으로써, 외과 의사는 복막강으로 들어가는 것을 피하고, 장, 간, 비장, 췌장을 포함한 주위 내장이 움직이지 않게 한다. 개복 및 복강경 경복부 부신절제술(LTA) 접근법과 비교할 때 이 기술은 입원 기간을 줄이고 통증을 줄이며 장폐색증 위험을 줄여 환자의 회복을 촉진합니다. 2-4
PRA의 장점 중 하나는 수술 중 환자의 체위를 변경할 필요 없이 최소 침습적 접근 방식을 통해 양쪽 부신에 양측으로 접근할 수 있다는 것입니다. 2 Von Hippel Lindau(VHL) 또는 다발성 내분비 신생물 2형(MEN2) 증후군으로 인한 갈색세포종과 같은 양측 부신 종양이 있는 환자는 이 접근법에 이상적인 후보입니다. 두 질환 과정 모두에서 양측 종양이 자주 발생합니다. 따라서 환자는 생화학적 치료를 달성하기 위해 양측 부신절제술이 필요할 수 있습니다.
수술 후 급성 부신부전(Addisonian crisis)을 예방하기 위해 피질 보존 부신 절제술을 시행할 수 있습니다. 이 과정에서 정상적인 부신 조직을 보존하면서 원인 종양 조직을 제거합니다. 5 전통적으로 이 기법은 개방형 및 LTA 접근법과 함께 설명되었습니다. 그러나 양측성 질환의 경우 PRA 접근법이 점점 더 성공적으로 활용되고 있습니다.
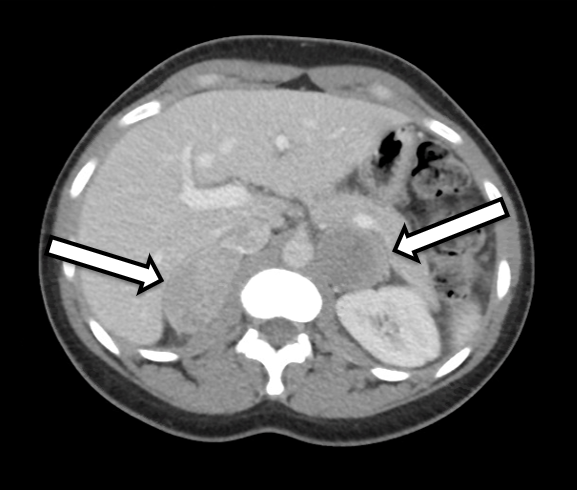
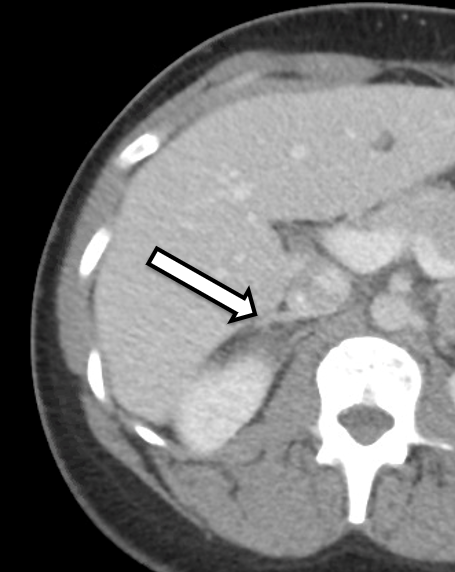
환자는 31세 여성으로 생화학적으로 명백한 양측 갈색세포종을 내원했습니다. 그녀는 고혈압과 심계항진 증상을 보였고, 이로 인해 주치의가 추가 조사를 하게 되었습니다. 그녀의 실험실 정밀 검사는 642pg/ml(참조 범위 < 57pg/mL)의 유리 혈장 메타네프린 상승 및 2284pg/ml(참조 <범위 148pg/ml)의 노르메타네프린 및 갈색세포종과 일치하는 소변 메타네프린 상승에 대해 중요했습니다. 단면 영상에는 IV 조영제를 이용한 복부 CT가 포함되었습니다. CT는 조영제 전 Hounsfield 단위를 가진 양측 부신 결절과 양측 갈색세포종의 전반적인 영상 특성을 보여주었습니다(그림 1). 그녀의 영상을 면밀히 검토한 결과, 오른쪽의 부신 피질 조직이 정상으로 보이는 것으로 나타났으며(그림 2), 이 조직은 이 쪽의 피질을 보존하는 부신 절제술에 도움이 될 수 있습니다.
그녀의 어린 나이와 양측 종양의 존재 때문에 그녀는 다른 MEN2A 관련 종양, 특히 갑상선 수질암 및 원발성 부갑상선 기능 항진증에 대해 추가 조사를 받았습니다. 실제로 혈청 칼시토닌 수치가 229pg/ml(참고 < 5pg/ml)로 상승한 것으로 확인되었으며, 초음파 및 세침 흡인 소견은 우측 갑상선엽의 갑상선 수질암 과 일치했습니다. 그녀의 혈청, 온전한 부갑상선 호르몬 및 칼슘 수치는 눈에 띄지 않았습니다.
CT와 MRI는 정상 및 비정상 부신을 촬영하는 데 사용되는 주요 방사선 기술입니다. CT에서 갈색세포종은 종종 주변 조직으로부터 잘 정의되며 일반적으로 30-40의 조영전 Hounsfield 단위를 보여줍니다. 작은 병변은 단순하고 단단하게 보이는 경향이 있는 반면, 큰 병변은 더 낭포성 특성과 다른 복잡한 특징을 가질 수 있습니다. MRI에서 갈색세포종은 T2 가중 이미지에서 전형적인 "전구" 모양을 가지고 있습니다. 기능적 영상도 얻을 수 있으며, 특히 전이성 질환이 우려되는 경우 더욱 그렇습니다. 가장 일반적인 방법은 노르에피네프린의 유사체인 131 I- 및 123 I-메타요오도벤질구아니딘(MIBG)을 사용하는 것이며, 이는 노에피네프린의 유사체이며 대칭 둔부 조직에 우선적으로 국한됩니다. 6 개
우리는 환자가 수술 계획을 위해 수술 후 약 3-6개월 이내에 부신 프로토콜 CT 또는 MRI를 받는 것을 선호합니다. 이 경우, 환자는 갈색세포종으로 의심되는 영상 특성을 가진 양측 부신 종괴를 보여주는 CT를 받은 후 저희에게 의뢰되었습니다. 상세한 문헌고찰 또는 그녀의 영상에서, 우측 부신의 하내측 사지에는 절제 중에 잠재적으로 보존될 수 있는 부신 피질 조직에 영향을 미치지 않는 것이 분명했다.
갈색세포종은 부신 수질의 신경능선 세포에서 유래하며 과도한 양의 카테콜아민을 분비합니다. 갈색세포종의 전반적인 유병률은 1:6500에서 1:2500 사이로 추정되며, 평균 발병 연령은 40-50세이며 여성에서 약간 더 높은 유병률을 보입니다. 대부분의 종양은 양성입니다. 6 흥미롭게도, 다양한 예측 알고리즘이 만들어졌음에도 불구하고, 크기, 유사분열 속도, 혈관 또는 수정체 침범을 포함하여 악성 가능성을 정확하게 예측할 수 있는 단일 병리학적 특성은 없습니다. 7 종양의 약 10-15%는 악성 변형을 나타내는 전이성 질환을 동반하거나 발병할 수 있습니다. 8 악성 갈색세포종의 질병별 생존율은 SEER(Surveillance, Epidemiology, and End Results) 데이터베이스 분석을 기반으로 5년 시점에서 약 70%로 추정됩니다. 9 개
갈색세포종의 표준 치료법은 외과적 절제입니다. 수술 전에 환자는 카테콜아민 차단술을 받아야 하는데, 이는 일반적으로 비선택적 알파 수용체 차단제인 페녹시벤자민 또는 독사조신과 같은 선택적 알파 차단제를 사용하여 수행됩니다. 베타 차단제를 포함한 추가적인 항고혈압제도 필요할 수 있습니다. 그러나 베타 차단제는 환자가 알파 차단제를 투여한 후에만 시작해야 하며, 이는 반대되지 않는 베타 수용체 차단으로 인한 고혈압 위기를 예방하기 위한 것입니다. 또한 환자는 만성적으로 탈수 상태이며 수술 전 수액 소생술이 필요합니다. 10명
갈색세포종을 앓고 있는 환자는 종종 심한 고혈압 및 심계항진, 두통, 공황 발작 및 발한을 포함한 과도한 카테콜아민 생성의 기타 임상 증상을 겪습니다. 11 혈압약이 부분적인 완화를 줄 수 있지만, 장기적이고 지속적인 유일한 치료법은 원인이 되는 병변을 절제하는 것입니다. 더욱이, 개입 없이 계속하는 사람들은 심각한 고혈압 위기의 위험에 처해 있으며, 잠재적으로 사망에 이를 수 있습니다. 12 그러므로, 갈색세포종 환자는 신속하게 수술적 치료를 받아야 합니다.
양측 갈색세포종을 동반한 환자에서 피질 보존 부신 절제술은 원인 조직을 절제하면서 부신 기능 부전의 발생을 예방할 수 있습니다. 이전 연구에 따르면 전체 부신 절제술은 매우 병적일 수 있습니다. 예를 들어, Lairmore et al.이 발표한 시리즈에서 43명의 환자가 양측 갈색세포종에 대한 완전 부신 절제술을 받았고, 23%는 부신 기능 부전을 겪었으며, 한 환자는 Addisonian 위기로 사망했습니다. 13 또한, 부신 절제술을 받은 환자들은 삶의 질이 떨어지고 부신 기능 부전과 관련된 잦은 입원을 보고합니다. 14명
피질 보존 부신 절제술은 갈색세포종과 관련된 유전 증후군이 있는 환자에게 매우 유용한 옵션입니다. 이러한 증후군에는 MEN2, VHL, 신경섬유종증 1형(NF1) 등이 포함됩니다. 양측 갈색세포종으로 진단된 환자는 유전자 검사를 의뢰해야 한다는 점에 유의하는 것이 중요합니다. 칼시토닌 검사는 유전자 검사를 수행하고 적절하게 해석하는 데 몇 개월이 걸릴 수 있기 때문에 MEN2 환자를 식별하는 데 유용한 보조 수단이 될 수 있습니다. MEN2A 또는 VHL 환자의 약 40-80%에서 양측 갈색세포종이 발생하며, 이러한 종양은 일반적으로 양성입니다. 15 따라서 피질을 보존하는 부신 절제술은 부신기능 부전을 예방할 수 있는 충분한 조직을 남기면서 재발 위험을 최소화하면서 영향을 받은 조직을 제거할 수 있습니다.
대뇌 피질 보존 부신 절제술의 첫 번째 사례는 1983년 Irvin et al. 에 의해 설명되었습니다. 16 그 이후로, 일부 기관들은 개복 또는 최소 침습적 접근법을 통해 재발률이 상당히 낮고, 중요하게는 부신 기능 부전의 발생률이 낮다는 점에서 대뇌 피질 보존 부신 절제술을 성공적으로 수행했다고 보고했습니다. 14 PRA의 사용은 대량 내분비 외과 의사들이 이 기술을 시행함에 따라 증가하고 있습니다. PRA는 1995년에 처음 기술된 후 Walz와 그의 동료들의 경험을 통해 더욱 발전되었습니다. 1, 4, 17 PRA와 LTA를 비교한 후향적 연구에서는 수술 시간 단축, 출혈 감소, 장기 결과에는 차이가 없는 것으로 나타났습니다.
최근에는 PRA가 피질을 보존하는 부신절제술에도 활용되고 있습니다. 최근 시리즈에서는 RPA 접근법을 사용하여 양측 갈색세포종에 대한 피질 보존 부신절제술을 25년 동안 수행한 경험에 대해 설명했습니다. 66명의 환자를 대상으로 수술을 받았으며 총 101회의 부신절제술을 시행했습니다. 양측 수술의 평균 수술 시간은 128분이었으며, 주요 합병증은 두 건에 불과했다. 그들은 89명의 환자에서 피질 보존 수술을 시행할 수 있었고 그 중 91%는 수술 후 스테로이드가 필요하지 않았습니다. 단 한 명의 환자만이 지속적인 질병을 앓고 있었고 재발은 보고되지 않았습니다. 18 환자는 수술 후에 얼마의 부신 기능 부전이 있을 수 있으므로 주의를 기울여야 합니다. 이것은 잔여 부신 조직의 크기와 혈류의 보존에 달려 있습니다. 일시적인 부신 기능 부전은 내분비내과 및 적절한 실험실 검사와 긴밀한 상담을 통해 관리됩니다.
시술은 기관내 삽관과 함께 전신 마취하에 수행됩니다. 종양으로 인해 수술 중 발생할 수 있는 혈역학적 변화로 인해 혈압 모니터링을 위해 동맥 라인을 배치하고 마취과 의사는 필요에 따라 혈관 활성 약물을 투여합니다. 폴리 카테터를 삽입하여 소변 배출량을 모니터링합니다. 카테콜아민 상승 정도 및 기타 환자 요인에 따라 추가 정맥 접근 및 중심 정맥압 모니터링을 위해 중심 정맥 라인을 배치할 수 있습니다.
전신 마취 유도 및 기관 내 삽관 후 환자는 엉덩이를 90도로 구부린 상태에서 엎드린 잭나이프 자세를 취합니다. Cloward Surgical Saddle이 있는 Cloward 테이블을 사용하여 복부가 종속적인 방식으로 매달릴 수 있도록 합니다. 잭나이프 위치와 Cloward Surgical Saddle은 후복막 공간을 열어 노출을 극대화합니다. 얼굴, 팔, 엉덩이, 다리를 포함한 모든 압박 지점은 광범위하게 패딩되어 있습니다. 장골 능선, 11번째와 12번째 갈비뼈의 끝부분, 척추 주위 근육의 가장자리는 외과 의사가 표시하는 중요한 이정표입니다. 초기 절개는 12번째 갈비뼈의 끝 부분보다 약간 아래쪽에 위치합니다. 가위는 연조직을 날카롭게 나누고 후복막으로 들어가는 데 사용됩니다. 그런 다음 외과 의사의 손가락을 사용하여 공간을 무디게 청소하고 내측 및 측면으로 5mm 포트의 배치를 안내하며, 둘 다 약 30도 각도로 부신의 위치를 향하게 합니다. 그런 다음 10mm 풍선 포트를 중간 절개 부위에 배치합니다. retroperitoneum은 고유량 튜브를 통해 25mmHg의 흡입 압력까지 CO2 로 주입됩니다.
5mm 30도 내시경을 10mm 포트에 삽입하고 LigaSure 장치를 사용하여 후복막 공간을 만듭니다. 해부는 내측으로 척추 주위 근육을 확인하는 것으로 시작하고, 그 다음에는 신장을 하부로 식별합니다. 그런 다음 카메라는 일반적으로 내측 포트로 이동하고 외과의는 LigaSure 장치와 장 그립기를 각각 측면 및 중앙 포트를 통해 사용합니다. 박리는 신장의 상극을 통해 그리고 척추 주위 근육을 따라 내측으로 부신 방향으로 계속됩니다. 노출은 부분적으로 신장에 가해지는 하향 압력에 의해 촉진됩니다. 부신이 확인됨에 따라 부신의 하부 범위와 부신 정맥과의 관계가 결정됩니다. 오른쪽에서 이 절개부는 IVC를 보여주며, 부신을 절개하여 부신 정맥을 드러냅니다. 왼쪽에서 부신 정맥은 왼쪽 신장 정맥에서 시작됩니다.
이 시점에서, 변하지 않은 대뇌 피질 부신 조직과 원인 종양의 정확한 관계가 결정된다. 이는 부분적으로 수술 중 소견과 함께 수술 전 영상에 대한 상세한 평가에 의해 결정됩니다. 경우에 따라 수술 중 초음파가 유용할 수 있습니다. 적합한 평면이 확인되면 LigaSure 장치를 사용하여 갈색세포종을 정상 부신 조직과 분리합니다. 부신은 혈관화가 심한 곳이기 때문에 부신이 절제될 때 지혈에 세심한 주의를 기울입니다. 이 경우, 본래 우측 부신의 하측 내측 사지가 보존에 적합하였다. 가능하면 정맥을 보존해야 합니다. 그러나 이것은 작은 부신 동맥을 따라 추가적인 정맥 배액이 있다는 점을 감안할 때 필요하지도 않고 항상 가능하지도 않습니다. 이번 수술 중에는 부신 정맥이 종양으로 직접 들어가는 것이 확인되어 클립으로 나뉘었습니다. 이 시점에서, 종양의 내측 및 외측 부착물이 제거되고, 상부 부착부는 종양이 늘어질 수 있도록 하고 우수한 반대 견인 부위를 제공할 수 있도록 남습니다. 외측 및 두부 절개 중에 복막강으로 들어가지 않도록 주의합니다. 종양을 원주방향으로 절개한 후에는 상부 부착물을 채취하고 Endocatch 장치를 사용하여 후복막 공간에서 분비샘을 제거합니다. 10mm 포트는 층으로 닫혀 있는 반면 5mm 포트 사이트는 피부 수준에서만 닫힙니다.
최종 병리검사에서 5.2cm의 우측 갈색세포종과 5.6cm의 좌측 갈색세포종이 발견되었다. 수술 후 첫날에 실시한 검사에서는 코르티솔 생성이 약간 감소한 것으로 나타났습니다. 따라서 환자는 임시로 저용량의 경구용 스테로이드를 투여받았습니다. 환자는 수술 후 2주 후에 병원에서 진찰을 받았을 때 수술 후 2일째 되는 날에 훌륭한 회복 상태로 퇴원했으며, 저용량의 프레드니손을 끊을 계획을 가지고 있었습니다.
Andrew 프레임, Cloward Surgical Saddle, LigaSure 장치 및 Endocatch 회수 백.
저자는 공개하지 않습니다.
이 비디오 기사에 언급된 환자는 촬영에 대해 사전 동의를 제공했으며 정보와 이미지가 온라인에 게시될 것임을 알고 있습니다.
References
- Walz MK, Peitgen K, Hoermann R, Giebler RM, Mann K, Eigler FW. 부신 절제술을위한 새로운 최소 침습적 접근법으로서의 후방 후 복막 내시경 검사 : 27 명의 환자에서 30 건의 부신 절제술 결과. 월드 J 서지. 1996;20(7):769-774. doi:10.1007/s002689900117.
- 칼렌더 GG, 케나머 DL, 그럽스 EG, 리 JE, 에반스 DB, 페리에 ND. 후방 후 복막 경 부신 절제술. 어드밴스 서지. 2009;43(1):147-157. 도이 : 10.1016 / J.Yasu.2009.02.017.
- Perrier ND, Kennamer DL, Bao R, et al. 후방 후 복막 경 부신 절제술 : 양성 종양 및 고립 된 전이를 제거하는 데 선호되는 기술. 앤 서지. 2008;248(4):666-674. 도이 : 10.1097 / SLA.0b013e31818a1d2a.
- Walz MK, Peitgen K, Walz MV, et al. 후방 후 복막 내시경 부신 절제술 : 5 년 이내에 배운 교훈. 월드 J 서지. 2001;25(6):728-734. 도이 : 10.1007 / S00268-001-0023-6.
- Lee JE, Curley SA, Gagel RF, Evans DB, Hickey RC. 양측 갈색 세포종 환자를위한 피질 보존 부신 절제술. 외과. 1996;120(6):1064-1071. doi : 10.1016 / S0039-6060 (96) 80056-0.
- Farrugia FA, Martikos G, Tzanetis P, et al. 갈색 세포종, 진단 및 치료 : 문헌 검토. 내분비 조절. 2017;51(3):168-181. 도이 : 10.1515 / ENR-2017-0018.
- 톰슨 LD. 양성과 악성 신 생물을 분리하기위한 부신 척도 점수 (PASS)의 갈색 세포종 : 100 건의 임상 병리학 및 면역 표현형 연구. Am J Surg Pathol. 2002;26(5):551-566. doi:10.1097%2F00000478-200205000-00002.
- Pacak K, Wimalawansa SJ. 갈색 세포종 및 부신경절종. 내분비 실습. 2015;21(4):406-412. 도이 : 10.4158 / EP14481. 라.
- 고프레도 P, 소사 JA, 로만 SA. 악성 갈색 세포종 및 부신경절종 : 2 년 동안의 장기 생존에 대한 인구 수준 분석. J 서그 온콜. 2013;107(6):659-664. 도이 : 10.1002 / jso.23297.
- Li J, Yang CH. 부신 갈색 세포종 환자의 수술 전 관리 개선. Int J Clin Exp Med. 2014;7(12):5541-5546. http://www.ncbi.nlm.nih.gov/pmc/articles/PMC4307515.
- 첸 H, 시펠 RS, 오도리시오 MS, 비닉 AI, 로이드 RV, 파칵 K; 북미 신경 내분비 종양 학회 (NANETS). 신경 내분비 종양의 진단 및 관리를위한 북미 신경 내분비 종양 학회 합의 지침 : 갈색 세포종, 부신경절종 및 갑상선 수질암. 췌. 2010;39(6):775-783. 도이 : 10.1097 / MPA.0b013e3181ebb4f0.
- Sutton MG, Sheps SG, Lie JT. 임상 적으로 의심되지 않는 갈색 세포종의 유병률 : 50 년 부검 시리즈 검토. 메이요 클린 프록. 1981;56(6):354-360.
- Lairmore TC, Ball DW, Baylin SB, Wells SA Jr. 다발성 내분비 신 생물 제 2 형 증후군 환자의 갈색 세포종 관리. 앤 서지. 1993;217(6):595-603. doi:10.1097/00000658-199306000-00001.
- Walz MK. 부신 신 생물에 대한 부신 절제술의 범위 : 피질 절약 (소계) 대 전체 부신 절제술. 서그 클린 노스 암. 2004;84(3):743-753. 도이 : 10.1016 / J.Suc.2004.01.003.
- Renard J, Clerici T, Licker M, Triponez F. 갈색 세포종 및 복부 부신경절종. J 비스크 서지. 2011;148(6):e409-e416. doi:10.1016/j.jviscsurg.2011.07.003.
- 어빈 GL 3위, 피쉬맨 LM, 셔 JA. 가족 성 갈색 세포종. 외과. 1983;94(6):938-940. https://www.surgjournal.com/article/0039-6060(83)90403-8/전문.
- 메르칸 S, 세븐 R, 오자르마간 S, 테젤만 S. 내시경 후복막 부신 절제술. 외과. 1995;118(6):1071-1076. doi : 10.1016 / S0039-6060 (05) 80116-3.
- Alesina PF, Hinrichs J, Meier B, Schmid KW, Neumann HP, Walz MK. 양측 갈색 세포종에 대한 최소 침습적 피질 보존 수술. 랑겐벡스 아치 서지. 2012;397(2):233-238. 도이 : 10.1007 / S00423-011-0851-2.
Cite this article
브라운 TC, 칼링 T. 오른쪽에 피질 절약을 통한 양측 후방 후 복막 경 부신 절제술. J 메드 인사이트. 2021;2021(282). 도이 : 10.24296 / 조미 / 282.