신경내분비 종양에 대한 개복 전절제술 및 십이지장 절제술
Main Text
Table of Contents
이 비디오는 십이지장 구근의 신경 내분비 종양에 대해 수행된 개방 십이지장 절제술 및 전방 절제술을 위한 수술 기술을 설명합니다. 이 절차에서는 상부 정중선 개복술로 시작하여 원위 위, 십이지장 및 췌장 머리의 가동을 진행합니다. 동원하기 위해 십이지장을 코체라이징한 다음 우측 위동맥을 결찰하고 위간인대를 절개한 다음 우측 위상피혈관을 결찰하고 하낭을 노출시키는 복인대를 제거합니다. 구조물이 적절하게 동원되면 췌장 머리에서 십이지장의 첫 번째 부분을 절개하고 TA 스테이플러로 횡단합니다. 다음으로 전방 절제술을 시행하여 검체를 제거합니다. 재건을 위해, 우리는 후배통 끝에서 옆으로 손으로 꿰매어진 위제장루술을 수행합니다. 이 기술은 소화성 궤양 질환 및 antrum, pylorus 또는 십이지장 구의 기타 종괴 병변을 포함한 여러 적응증에 사용할 수 있습니다.
코처 기동; 안절제술; 십이지장 절제술; 신경내분비종양; 위절개술.
신경내분비종양(NET)은 소화관과 췌장을 포함하는 미만성 신경내분비계의 분비 세포에서 발생합니다. NETs는 대장암에 이어 두 번째로 흔한 소화기암입니다. NET의 약 70%는 소장 또는 결장에서, 12%는 췌장에서, 5%는 맹장에서 발생합니다. 1 NET은 특성이 이질적이고, 대다수는 성장이 느려지며, 하위 집합은 호르몬 또는 생체 활성 아민을 분비하여 기능 장애를 일으킵니다. 2 암종종양은 세로토닌을 생성하는 엔테로크로마핀 세포에서 발생하는 종양의 일종입니다. 다른 유형의 NET은 인슐린, 글루카곤, 소마토스타틴, 가스트린 또는 혈관 활성 장 펩타이드(VIP)를 생산할 수 있습니다. NET은 임상 양상, 생화학적 마커, 병리학 및 이미징의 조합을 사용하여 진단됩니다. 3 NETs의 공격성은 주로 종양 등급에 의해 결정되며, 이는 위치에 따라 다릅니다. 4 발병률은 지난 40년 동안 증가해 왔지만, 이는 부분적으로 진단 영상의 증가에 기인하는 것으로 생각됩니다. 환자의 27%는 진단 시점에 전이성 질환을 앓고 있습니다. 5 개
생물학적 공격성과 생체 활성 화학 물질의 분비에서 가변성을 보이는 NET의 이질성을 감안할 때 이러한 종양을 관리하려면 종종 개인화된 접근 방식이 필요합니다. 외과적 절제술은 일반적으로 NET에 대한 유일한 치료법으로 남아 있습니다. 내시경 절제술은 직경이 1cm 미만인 십이지장 병변에 대해서도 고려할 수 있습니다. 그러나 이 절차는 십이지장의 해부학적 특성으로 인해 기술적으로 어렵습니다. 또한, 천공의 위험이 있으며 점막하층으로의 침투로 인해 양의 수직 마진이 있습니다. 6,11
이 비디오에서는 48세 여성의 십이지장 NET에 대한 전절제술을 통한 십이지장 절제술을 시행합니다. 종괴는 임상 정밀 검사에서 양성 특징을 가지고 있었습니다. 그러나 감시 내시경 검사에서 병변의 크기가 증가함에 따라 치료 목적으로 수술적 절제를 진행하기로 결정했습니다.
환자는 위식도 역류 질환 병력이 있는 48세 여성으로, 식도 위십이지장 내시경 검사에서 십이지장 구근에 종양이 발견되었습니다. 병변의 특성을 추가로 규명하기 위해 내시경 초음파를 시행한 결과, 최대 크기가 5mm이고 점막하로 보였다. 병변에 문신을 새겼고, 종괴를 모니터링하기 위해 환자를 정기적인 내시경 검사로 추적했습니다. 2년 후, 종괴는 완만하게 커졌고, 그녀는 절제 수술을 위해 외과 클리닉에 의뢰되었습니다. 그녀의 다른 병력은 비만, 당뇨병 및 고혈압으로 유명합니다. 그녀는 이전에 복부 수술 이력이 없습니다. 그녀의 마지막 대장 내시경 검사는 3년 전이었고 정상이었습니다. 그녀는 미국 마취과 학회 점수(ASA)가 2이고 체질량 지수(BMI)가 31입니다.
환자는 별다른 특이하지 않은 신체 검사를 받았다. 사무실에서, 그녀는 정상적인 바이탈로 고통스러워 보이지 않았다. 그녀는 정상적인 습관을 가지고 있었다. 그녀의 복부 검사는 이전의 수술 흉터, 탈장 또는 촉진에 대한 압통의 증거가 없어 눈에 띄지 않았습니다. 그녀의 복부는 부드러웠고 팽창하지 않았다.
관련 이미징은 그림 1에서 볼 수 있습니다.
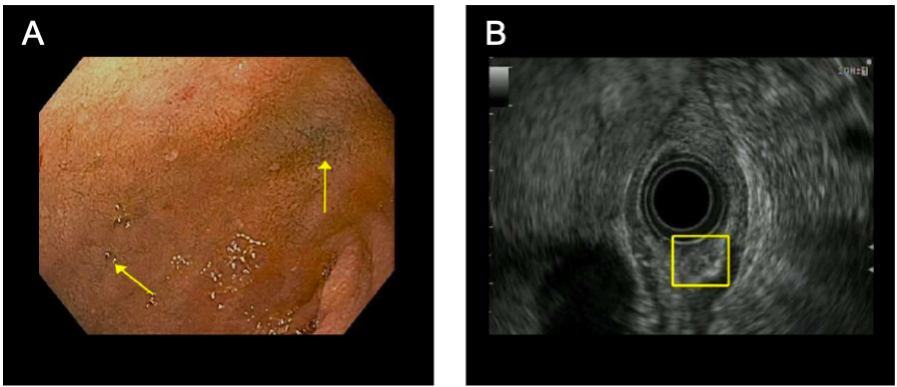
그림 1. 관련 이미징. (A) 십이지장의 내시경 이미지. 노란색 화살표는 종괴의 이전 내시경 표시에서 가져온 파란색 잉크 문신을 가리킵니다. 병변은 작으며 기존 내시경에서는 볼 수 없습니다. (B) 노란색 상자 안에 캡처된 신경내분비 종양의 내시경 초음파 이미지. 병변은 초음파에서 상피하부에 있습니다.
NETs의 임상 경과는 매우 다양합니다. 낮은 등급의 잘 분화된 병변은 일반적으로 전이 가능성이 낮은 나태한 경과를 보이는 반면, 고등급 NET은 원거리 전이로 빠르게 진행됩니다. 생존율은 종양의 위치와도 관련이 있으며, 등급이 높은 췌장골은 5년 생존율이 10% 미만으로 암울합니다. 7 NET 발달을 주도하는 유전적 및 후성유전학적 변화의 순서는 저등급 병변과 고등급 병변을 비교할 때 가변적일 뿐만 아니라 세포 유형의 기원을 비교할 때도 가변적이며, 이는 분자 병리학 및 후속 임상 과정이 NET들 간에 이질적임을 나타냅니다.
NETs에 대한 유일한 잠재적 완치 요법은 종양을 외과적으로 절제하는 것입니다. 그럼에도 불구하고 외과 의사는 수술의 위험과 이점에 대해 환자와 논의해야 합니다. 어떤 경우에는 내시경 절제술을 시도하는 것이 위험도가 낮은 작은 병변에 합리적입니다. 전이성 질환의 경우, 질병 전체가 소멸 가능하거나 호르몬 분비 질량의 삶의 질을 크게 향상시킬 수 있는 상황에서 수술이 필요할 수 있습니다. 그러나 대부분의 전이성 질환의 경우 세포독성 화학요법과 항호르몬 요법이 치료의 주류입니다.
비전이성 NET에 대한 외과적 절제술의 근거는 치료 의도를 가진 완전한 질병 제거입니다.
NET의 외과적 절제술에는 몇 가지 주의 사항이 있습니다. 첫째, 직경이 1cm 미만이고 위험이 낮은 십이지장 NET에 대한 감시를 고려할 수 있으며, 내시경 절제가 허용됩니다.8 둘째, 고등급 병변의 경우, 원격 전이의 위험이 증가하고 예후가 좋지 않기 때문에 수술의 역할이 명확하지 않습니다. 셋째, 호르몬 분비 종양의 삶의 질을 향상시키기 위해 특정 전이성 질환의 경우 비근치적 외과적 용적 축소를 고려할 수 있습니다.
이 비디오에서 보여준 것처럼 이 수술의 주요 절차 단계는 다음과 같습니다: (1) 상부 정중선 개복술, 팔시폼 인대 제거, 복막강 탐색; (2) 십이지장의 Kocherization; (3) 우측 위동맥을 결찰하고 위간인대를 제거합니다. (4) 우측 위상피동맥을 결찰하고, 위인대를 제거하고, 하낭으로 진입합니다. (5) 췌장 머리에서 십이지장의 첫 번째 부분을 동원하는 것; (6) TA 스테이플러로 십이지장을 횡단합니다. (7) ILA 스테이플러로 위의 앞부분을 가로질렀습니다. (8) 후배통 종단 간 Hoffmeister 위장루술로 Billroth II 재건을 수행합니다. 이 접근법은 십이지장과 원위 위를 광범위하게 동원하여 부정적인 절제 마진을 보장할 수 있습니다.
위절개술에는 전산통(antecolic)과 후산골(retrocolic)의 두 가지 옵션이 있습니다. 후행적 접근법에서 jejunum은 횡결장의 장간막 창을 통해 전달되어 구심성 루프가 짧아지고 구심성 루프 증후군의 위험이 감소합니다. 반면에, 산전 접근법은 기술적으로 더 쉬운 것으로 간주되며, 악성 종양의 경우에 선호됩니다. 12명
십이지장 NET은 드물며, 원발성 십이지장 신생물의 5% 미만과 모든 NET의 10% 미만을 차지합니다. 9 대부분의 십이지장 NET은 기능이 없고 직경이 2cm 미만이며 무증상 환자에서 우연히 발견됩니다. 8 이러한 종양은 일반적으로 심부 점막에 존재하며 내시경 검사에서 점막하 모양으로 나타납니다. 십이지장 NETs의 표준 치료는 외과적 절제입니다. 그러나 등급이 낮고 크기가 작으며 기능하지 않는 병변의 경우 내시경 절제술을 고려할 수 있습니다. 10 림프절 전이의 위험 때문에 낮은 등급의 작은 병변에 대한 관찰은 권장되지 않습니다.
외과적 절제술의 유형은 십이지장 내 병변의 위치와 크기에 따라 다릅니다. 양압 종양은 예후가 나쁜 경향이 있으며 종종 음의 마진과 적절한 결절 수율을 위해 췌장 십이지장 절제술이 필요합니다. 장의 항장간막 경계에 있는 십이지장 그물은 충분히 작고 위험이 낮은 특징을 가진 경우 때때로 쐐기 방식으로 절제할 수 있습니다. 다른 경우에는 분절 십이지장 절제술이 필요합니다. 우리 환자의 경우, 우리는 전절제술과 함께 D1 절제를 시행하기로 결정했습니다. 우리가 이 시술을 선택한 이유는 수술 중 병변의 국소화가 불가능했기 때문에 쐐기 절제술이 불가능했기 때문입니다.
- 수술 시간: 68분
- 예상 출혈량: 50mL
- 유체: 1700mL 결정질
- 입원 기간: 수술 후 4일째 되는 날 서비스 없이 병원에서 집으로 퇴원
- 이환율: 합병증 없음
- 최종 병리학: 신경내분비 종양, 1등급, 가스트린 염색 양성
- 10날 메스
- 전기 소작
- DeBakey 겸자
- 복부 벽 휴대용 견인기
- 슈니트 클램프
- 장간막 결찰을 위한 3-0 및 2-0 실크 넥타이
- Metzenbaum 가위
- ILA 스테이플러
- TA 스테이플러
- 3-0 Vicryl 및 3-0 위장관절개술용 실크
- 1-0 근막 봉합을 위한 프롤렌 봉합사
- 스킨 스테이플러
공개할 것이 없습니다.
이 비디오 기사에 언급된 환자는 촬영에 대해 사전 동의를 했으며 정보와 이미지가 온라인에 게시될 것임을 알고 있습니다.
이 작업에 도움을 주신 Theresa Kim 의학박사님께 감사드립니다.
References
- 프릴링 A, Akerstrom G, Falconi M 등 신경내분비종양질환: 진화하는 환경. 내분비 관련 암. 2012; 19:R163-85. 도:10.1530/ERC-12-0024.
- Cives M, Strosberg JR. 위장 엽장 신경 내분비 종양. 캘리포니아 암 J 클린. 2018;68:471-87. doi:10.3322/caac.21493입니다.
- Oberg K, Couvelard A, Delle Fave G, et al, Antibes Consensus Conference p. 신경 내분비 종양의 표준 치료에 대한 ENETS 합의 지침: 생화학적 마커. 신경내분비학. 2017;105:201-11. https://doi.org/10.1159/000461583.
- Kloppel G, La Rosa S. Ki67 라벨링 지수: 위장 신경내분비 신생물에서의 평가 및 예후 역할. 버쇼 아치. 2018;472:341-9. 도:10.1007/S00428-017-2258-0.
- 다사리 A, 쉔 C, 할페린 D 등 미국에서 신경내분비종양 환자의 발병률, 유병률 및 생존 결과의 추세. JAMA 온콜. 2017;3:1335-42. 도:10.1001/jamaoncol.2017.0589.
- Partelli S, Bartsch DK, Capdevila J, et al, Antibes Consensus Conference p. 신경 내분비 종양의 표준 치료에 대한 ENETS 합의 지침 : 소장 및 췌장 신경 내분비 종양에 대한 수술. 신경내분비학. 2017;105:255-65. 도:10.1159/000464292.
- Strosberg JR, Cheema A, Weber J, Han G, Coppola D, Kvols LK. 췌장 신경내분비 종양에 대한 새로운 미국 암 병기 분류 공동 위원회(American Joint Committee on Cancer Staging Classification)의 예후 타당성. J Clin 온콜. 2011;29:3044-9. 도:10.1200/JCO.2011.35.1817.
- 사토 Y, 하시모토 S, 미즈노 K, 타케우치 M, 테라이 S. 위 및 십이지장 신경 내분비 종양의 관리. 세계 J Gastroenterol 2016;22:6817-28. doi:10.3748/wjg.v22.i30.6817입니다.
- Yao JC, Hassan M, Phan A 등 "암" 이후 100년: 미국에서 35,825건의 사례에서 신경내분비 종양의 역학 및 예후 요인. J Clin 온콜. 2008;26:3063-72. 도:10.1200/JCO.2007.15.4377.
- Kulke MH, Shah MH, Benson AB III 등; 국가 종합 암 네트워크. 신경내분비종양, 버전 1.2015. J Natl Compr Canc Netw. 2015년 1월; 13(1):78-108. 도:10.6004/jnccn.2015.0011.
- Furukawa K, Nakamura M, Kawashima H, Fujishiro M. 십이지장 신경 내분비 종양의 내시경 절제술. Rev esp enferm 발굴. 2022; 114(5):291-292. 도:10.17235/reed.2021.8232/2021.
- 미야자키 Y, 오다 T, 시모무라 O 외 췌장 십이지장 절제술 후 후배통 위정장절개술: 만족스러운 지연 위 배출률. 췌장. 2019; 48(4):579-584. doi:10.1097/MPA.0000000000001295입니다.
Cite this article
Erstad DJ, 버거 DL. 신경내분비 종양에 대한 개복 전절제술 및 십이지장 절제술. J 메드 인사이트. 2024; 2024(28). 도:10.24296/조미/28.

