Offene Antrektomie und Zwölffingerdarmresektion bei neuroendokrinen Tumoren
Main Text
Table of Contents
Dieses Video beschreibt die Operationstechnik für eine offene Zwölffingerdarmresektion und Antrektomie, die bei einem neuroendokrinen Tumor des Zwölffingerdarmbulbus durchgeführt wurde. Bei diesem Verfahren beginnen wir mit einer Laparotomie der oberen Mittellinie und fahren mit der Mobilisierung des distalen Magens, des Zwölffingerdarms und des Pankreaskopfes fort. Zur Mobilisierung kochen wir den Zwölffingerdarm, ligieren dann die rechte Magenarterie und präparieren das gastroepipatische Band, gefolgt von der Ligatur der rechten gastroepiploischen Gefäße und entfernen das gastrokolische Band, wodurch der kleine Sack freigelegt wird. Sobald die Strukturen ausreichend mobilisiert sind, präparieren wir den ersten Teil des Zwölffingerdarms vom Kopf der Bauchspeicheldrüse und durchtrennen ihn mit einem TA-Stapler. Als nächstes wird die Antrektomie durchgeführt, bei der die Probe entfernt wird. Für die Rekonstruktion führen wir eine retrokolische Ende-zu-Seite-Handgenähte Gastrojejunostomie durch. Diese Technik kann bei mehreren Indikationen eingesetzt werden, einschließlich Magengeschwüren und anderen Massenläsionen des Antrums, des Pylorus oder des Zwölffingerdarmbulbus.
Kocher-Manöver; Antrektomie; Duodenektomie; neuroendokriner Tumor; Gastrojejunostomie.
Neuroendokrine Tumoren (NETs) entstehen aus den sekretorischen Zellen des diffusen neuroendokrinen Systems, zu dem auch der Verdauungstrakt und die Bauchspeicheldrüse gehören. NETs sind nach Darmkrebs die zweithäufigste Krebserkrankung des Verdauungstrakts. Etwa 70 % der NETs treten im Dünndarm oder Dickdarm auf, 12 % in der Bauchspeicheldrüse und 5 % im Blinddarm. 1 NETs sind heterogen in ihrem Charakter, die Mehrheit hat ein indolentes Wachstum, und eine Untergruppe sezerniert Hormone oder bioaktive Amine, was zu Funktionsstörungen führt. 2 Karzinoidtumoren sind eine Art von NET, die aus enterochromaffinen Zellen entstehen, die Serotonin produzieren. Andere Arten von NETs können Insulin, Glucagon, Somatostatin, Gastrin oder vasoaktives intestinales Peptid (VIP) produzieren. NETs werden anhand einer Kombination aus klinischem Erscheinungsbild, biochemischen Markern, Pathologie und Bildgebung diagnostiziert. 3 Die Aggressivität von NETs wird in erster Linie durch den Tumorgrad bestimmt, der je nach Lokalisation variabel ist. 4 Die Inzidenz hat in den letzten vier Jahrzehnten zugenommen, aber es wird angenommen, dass dies zum Teil auf die Zunahme der diagnostischen Bildgebung zurückzuführen ist. Siebenundzwanzig Prozent der Patienten weisen zum Zeitpunkt der Diagnose eine metastasierende Erkrankung auf. 5
Angesichts der Heterogenität der NETs, die eine Variabilität in der biologischen Aggressivität und der Sekretion bioaktiver Chemikalien aufweisen, erfordert die Behandlung dieser Tumoren oft einen personalisierten Ansatz. Die chirurgische Resektion ist nach wie vor die einzige kurative Therapie für NETs im Allgemeinen. Eine endoskopische Resektion kann auch bei Zwölffingerdarmläsionen mit einem Durchmesser von weniger als einem Zentimeter in Betracht gezogen werden. Dieses Verfahren ist jedoch aufgrund der anatomischen Eigenschaften des Zwölffingerdarms technisch anspruchsvoll. Darüber hinaus birgt es die Gefahr einer Perforation und eines positiven vertikalen Randes durch Infiltration in die Submukosa. 6,11 kg
In diesem Video führen wir bei einer 48-jährigen Frau eine Zwölffingerdarmresektion mit Antrektomie für ein Zwölffingerdarm-NET durch. Die Masse wies bei der klinischen Abklärung gutartige Merkmale auf; Aufgrund einer Vergrößerung der Läsion bei der Überwachungsendoskopie wurde jedoch die Entscheidung getroffen, mit der chirurgischen Resektion in kurativer Absicht fortzufahren.
Bei der Patientin handelt es sich um eine 48-jährige Frau mit gastroösophagealer Refluxkrankheit in der Vorgeschichte, bei der bei der Ösophagogastroduodenoskopie ein Tumor in ihrem Zwölffingerdarmknollen festgestellt wurde. Ein endoskopischer Ultraschall wurde durchgeführt, um die Läsion weiter zu charakterisieren, die eine maximale Dimension von 5 mm hatte und submukös erschien. Die Läsion wurde tätowiert und der Patient wurde mit einer routinemäßigen Endoskopie überwacht, um die Masse zu überwachen. Zwei Jahre später war die Masse leicht gewachsen und sie wurde zur Resektion in die chirurgische Klinik überwiesen. Ihre andere Krankengeschichte ist bemerkenswert für Fettleibigkeit, Diabetes mellitus und Bluthochdruck. Sie hat keine Vorgeschichte von Bauchoperationen. Ihre letzte Darmspiegelung lag drei Jahre zurück und verlief normal. Sie hat einen ASA-Score (ASA) der American Society of Anesthesiologist (ASA) und einen Body-Mass-Index (BMI) von 31.
Der Patient wurde einer unauffälligen körperlichen Untersuchung unterzogen. In der Praxis stellte sie sich in keiner offensichtlichen Not mit normalen Vitalwerten vor. Sie hatte einen normalen Habitus. Ihre Bauchuntersuchung verlief unauffällig, es gab keine Hinweise auf frühere Operationsnarben, Hernien oder Druckempfindlichkeit beim Abtasten. Ihr Bauch war weich und nicht aufgebläht.
Relevante Bildgebung ist in Abbildung 1 zu sehen.
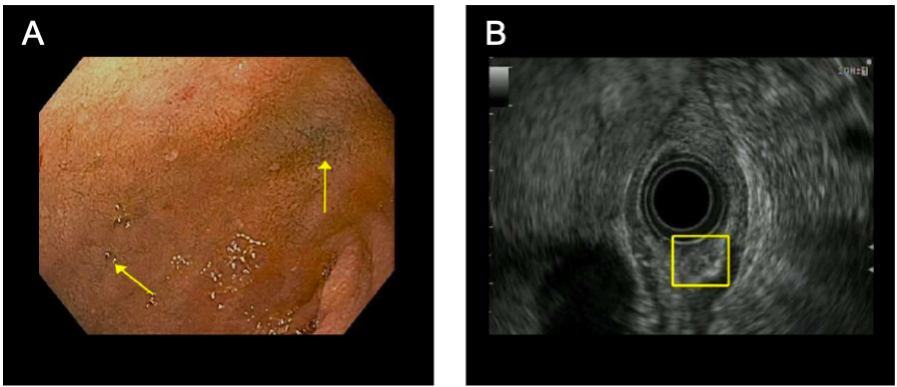
Abbildung 1. Relevante Bildgebung. (A) Endoskopisches Bild des Zwölffingerdarms. Gelbe Pfeile zeigen auf eine Blautintentätowierung von der vorherigen endoskopischen Markierung der Masse. Die Läsion ist klein und in der konventionellen Endoskopie nicht sichtbar. (B) Endoskopisches Ultraschallbild des neuroendokrinen Tumors, das in der gelben Box erfasst ist. Die Läsion ist im Ultraschall subepithelial.
Der klinische Verlauf von NETs ist sehr variabel. Niedriggradige, gut differenzierte Läsionen haben typischerweise einen indolenten Verlauf mit geringem Metastasierungspotenzial, während hochgradige NETs mit Fernausbreitung schnell fortschreiten. Das Überleben ist auch mit der Tumorlokalisation verbunden, und Pankreas-NETs mit hochgradigen Merkmalen haben düstere 5-Jahres-Überlebensraten von weniger als 10%. 7 Die Abfolge der genetischen und epigenetischen Veränderungen, die die NET-Entwicklung vorantreiben, ist variabel beim Vergleich von niedrig- und hochgradigen Läsionen, aber auch beim Vergleich der Herkunft des Zelltyps, was darauf hindeutet, dass die molekulare Pathologie und der anschließende klinische Verlauf bei NETs heterogen sind.
Die einzige mögliche kurative Therapie für NETs ist die chirurgische Resektion des Tumors. Nichtsdestotrotz sollte der Chirurg die Risiken und Vorteile einer Operation mit dem Patienten besprechen. In bestimmten Fällen ist ein Versuch einer endoskopischen Resektion bei kleinen Läsionen mit geringem Risiko sinnvoll. Bei metastasierenden Erkrankungen kann eine Operation indiziert sein, wenn die Gesamtheit der Krankheit auslöschbar ist oder in Situationen, in denen das Debulking die Lebensqualität der hormonsekretierenden Massen signifikant verbessern könnte. In den meisten Fällen von metastasierten Erkrankungen sind jedoch zytotoxische Chemotherapien und antihormonelle Therapien die Hauptstützen der Behandlung.
Die Begründung für die chirurgische Resektion bei nicht-metastasiertem NET ist die vollständige Entfernung der Erkrankung mit kurativer Absicht.
Es gibt mehrere Vorbehalte bei der chirurgischen Resektion bei NETs. Erstens kann eine Überwachung in Betracht gezogen werden, für Zwölffingerdarm-NETs mit einem Durchmesser von weniger als 1 cm und geringen Risikomerkmalen ist eine endoskopische Resektion akzeptabel.8 Zweitens ist bei hochgradigen Läsionen die Rolle der Operation aufgrund des erhöhten Risikos einer Fernausbreitung und der schlechten Prognose weniger klar. Drittens kann in bestimmten Fällen von metastasierender Erkrankung ein nicht-kuratives chirurgisches Debulking in Betracht gezogen werden, um die Lebensqualität von hormonsezernierenden Tumoren zu verbessern.
Wie wir in diesem Video gezeigt haben, sind die wichtigsten Verfahrensschritte für diese Operation wie folgt: (1) Laparotomie der oberen Mittellinie, Entfernung des falciformen Bandes, Untersuchung der Peritonealhöhle; (2) Kocherisierung des Zwölffingerdarms; (3) Ligatur der rechten Magenarterie, Entfernung des gastrophatischen Bandes; (4) Ligatur der rechten gastroepiploischen Arterie, Entfernung des gastrokolischen Bandes und Eintritt in den kleinen Sack; (5) Mobilisierung des ersten Teils des Zwölffingerdarms vom Kopf der Bauchspeicheldrüse; (6) den Zwölffingerdarm mit einem TA-Stapler durchschneiden; (7) das Antrum des Magens mit einem ILA-Stapler durchschneiden; und (8) eine Billroth-II-Rekonstruktion mit einer retrokolischen End-to-Side-Hoffmeister-Gastrojejunostomie durchzuführen. Dieser Ansatz ermöglicht eine großflächige Mobilisation des Zwölffingerdarms und des distalen Magens, um negative Resektionsränder zu gewährleisten.
Es gibt zwei Optionen für die Gastrojejunostomie: antekolisch und retrokolike. Beim retrokolischen Zugang wird das Jejunum durch ein mesenteriales Fenster des Dickdarms transversal eingebracht, was zu einer kürzeren afferenten Schleife und einem verringerten Risiko für ein afferentes Schleifensyndrom führt. Auf der anderen Seite gilt der antekolische Ansatz als technisch einfacher und wird bei Malignomen bevorzugt. 12
Duodenale NETs sind selten und machen weniger als 5 % der primären Duodenalneoplasien und weniger als 10 % aller NETs aus. 9 Die Mehrzahl der Zwölffingerdarm-NETs ist nicht funktionsfähig, hat einen Durchmesser von weniger als 2 cm und wird zufällig bei ansonsten asymptomatischen Patienten entdeckt. 8 Diese Tumoren treten typischerweise in der tiefen Schleimhaut auf und haben in der Endoskopie ein submuköses Aussehen. Die Standardbehandlung für Zwölffingerdarm-NETs ist die chirurgische Resektion. Bei Läsionen, die geringgradig, klein und nicht funktionsfähig sind, kann jedoch eine endoskopische Resektion in Betracht gezogen werden. 10 Die Beobachtung bei geringgradigen, kleinen Läsionen wird aufgrund des Risikos von Lymphknotenmetastasen nicht empfohlen.
Die Art der chirurgischen Resektion hängt von der Lage und Größe der Läsion innerhalb des Zwölffingerdarms ab. Ampulläre Tumoren haben tendenziell eine schlechtere Prognose und erfordern oft eine Pankreatikoduodenektomie bei negativen Rändern und ausreichender Knotenausbeute. Zwölffingerdarm-NETs an der antimesenterialen Grenze des Darms können manchmal verkeilt reseziert werden, wenn sie klein genug sind und risikoarme Merkmale aufweisen. In anderen Fällen ist eine segmentale Zwölffingerdarmresektion notwendig. Im Falle unserer Patientin haben wir uns für eine D1-Resektion mit Antrektomie entschieden. Wir haben uns für dieses Verfahren entschieden, da die Läsion intraoperativ nicht lokalisierbar war und daher nicht für eine Keilresektion geeignet war.
- Betriebszeit: 68 Minuten
- Geschätzter Blutverlust: 50 ml
- Flüssigkeiten: 1700 mL kristalloid
- Aufenthaltsdauer: Entlassung aus dem Krankenhaus nach Hause ohne Versorgung am 4. Tag der Operation
- Morbidität: keine Komplikationen
- Endgültige Pathologie: neuroendokriner Tumor, Grad 1, färbt sich positiv auf Gastrin
- 10-Klingen-Skalpell
- Elektrokauterisation
- DeBakey Pinzette
- Handretraktor für Bauchdecke
- Schnidt Klemme
- 3-0 und 2-0 Seidenkrawatten für die Ligatur des Mesenteriums
- Metzenbaum Schere
- ILA-Tacker
- TA Tacker
- 3:0 Vicryl und 3:0 Seide für die Gastrojejunostomie
- 1-0 Prolene Naht für Faszienverschluss
- Hautklammerer
Nichts offenzulegen.
Der Patient, auf den sich dieser Videoartikel bezieht, hat seine Einverständniserklärung gegeben, gefilmt zu werden, und ist sich bewusst, dass Informationen und Bilder online veröffentlicht werden.
Wir danken Theresa Kim, MD, für die Unterstützung bei dieser Operation.
References
- Rüschen A, Akerstrom G, Falconi M, et al. Neuroendokrine Tumorerkrankung: eine sich wandelnde Landschaft. Endokr Relat Krebs. 2012; 19:R163-85. doi:10.1530/ERC-12-0024.
- Cives M, Strosberg JR. Gastroenteropankreatische neuroendokrine Tumoren. CA Krebs J Clin. 2018;68:471-87. doi:10.3322/caac.21493.
- Oberg K, Couvelard A, Delle Fave G, et al., Antibes Consensus Conference S. ENETS Consensus Guidelines for standard of care in Neuroendocrine Tumours: Biochemical Markers. Neuroendokrinologie. 2017;105:201-11. https://doi.org/10.1159/000461583.
- Kloppel G, La Rosa S. Ki67-Markierungsindex: Bewertung und prognostische Rolle bei gastroenteropankreatischen neuroendokrinen Neoplasien. Virchows-Bogen. 2018;472:341-9. doi:10.1007/s00428-017-2258-0.
- Dasari A, Shen C, Halperin D, et al. Trends bei der Inzidenz, Prävalenz und Überlebensrate bei Patienten mit neuroendokrinen Tumoren in den Vereinigten Staaten. JAMA Oncol. 2017;3:1335-42. doi:10.1001/jamaoncol.2017.0589.
- Partelli S., Bartsch DK., Capdevila J., et al., Antibes Consensus Conference S. ENETS Consensus Guidelines for standard of care in neuroendocrine Tumours: Surgery for small intestinal and pancreatic neuroendocrine tumors. Neuroendokrinologie. 2017;105:255-65. doi:10.1159/000464292.
- Strosberg JR, Cheema A, Weber J, Han G, Coppola D, Kvols LK. Prognostische Validität eines neuartigen American Joint Committee on Cancer Staging Classification für neuroendokrine Tumoren der Bauchspeicheldrüse. J Clin Oncol. 2011;29:3044-9. doi:10.1200/JCO.2011.35.1817.
- Sato Y, Hashimoto S, Mizuno K, Takeuchi M, Terai S. Behandlung von neuroendokrinen Tumoren des Magens und des Zwölffingerdarms. Welt J Gastroenterol 2016;22:6817-28. doi:10.3748/wjg.v22.i30.6817.
- Yao JC, Hassan M, Phan A, et al. Hundert Jahre nach "Carcinoid": Epidemiologie und prognostische Faktoren für neuroendokrine Tumoren in 35.825 Fällen in den Vereinigten Staaten. J Clin Oncol. 2008;26:3063-72. doi:10.1200/JCO.2007.15.4377.
- Kulke MH, Shah MH, Benson AB III, et al.; Nationales umfassendes Krebsnetzwerk. Neuroendokrine Tumoren, Version 1.2015. J Natl Compr Canc Netw. Januar 2015; 13(1):78-108. doi:10.6004/jnccn.2015.0011.
- Furukawa K, Nakamura M, Kawashima H, Fujishiro M. Endoskopische Resektion eines duodenalen neuroendokrinen Tumors. Rev Esp Enferm Dig. 2022; 114(5):291-292. doi:10.17235/reed.2021.8232/2021.
- Miyazaki Y, Oda T, Shimomura O, et al. Retrokolische Gastrojejunostomie nach Pankreatikoduodenektomie: eine zufriedenstellende verzögerte Magenentleerungsrate. Bauchspeicheldrüse. 2019; 48(4):579-584. doi:10.1097/MPA.000000000001295.
Cite this article
Erstad DJ, Berger DL. Offene Antrektomie und Zwölffingerdarmresektion bei neuroendokrinen Tumoren. J Med Insight. 2024; 2024(28). doi:10.24296/jomi/28.

