Pankreas-Debridement über Sinustrakt-Endoskopie
Main Text
Table of Contents
Die Sinus-Trakt-Endoskopie (STE) ist eine minimal-invasive Technik zum Debridement von totem oder infiziertem Gewebe. STE wird normalerweise zur Behandlung von infizierter Pankreas- oder Peripankreasnekrose eingesetzt, obwohl andere Anwendungen beschrieben wurden. STE beinhaltet die Platzierung eines perkutanen Abflusses, gefolgt von einer fluoroskopisch geführten Erweiterung des Abflusskanals, um die Platzierung einer Arbeitshülle zu ermöglichen. Ein Endoskop wird dann durch die Scheide eingeführt und verwendet, um nekrotisches Gewebe zu debridieren. Ein Abfluss wird dann am Ende des Verfahrens durch den gleichen Trakt ersetzt. In diesem Fall verwenden wir STE, um infizierte peripankreasische Nekrose zu debridieren, die durch eine traumatische Pankreasverletzung verursacht und durch eine enterische Fistel kompliziert wird.
Akute Pankreatitis betrifft über 275.000 Menschen pro Jahr in den Vereinigten Staaten. Ungefähr 20% entwickeln Nekrose und 10-20% davon entwickeln infizierte Nekrose. Infizierte Pankreas- oder Peripankreasnekrose ist die primäre Indikation für eine Intervention bei nekrotisierender Pankreatitis. 1, 2
Unser Patient ist ein 58-jähriger Mann, der in eine Kollision mit einem Kraftfahrzeug verwickelt war und mehrere Verletzungen erlitt, darunter auch an der Bauchspeicheldrüse. Er wurde zunächst in einem anderen Krankenhaus behandelt, wo er sich einer endoskopischen retrograden Cholangiopankreatikographie und Pankreaskanalstenting unterzog. Er entwickelte eine symptomatische akute Peripankreasflüssigkeitssammlung und unterzog sich einer perkutanen Drainage, die eine Infektion aufdeckte. Als sich seine peripankreatische Sammlung nicht auflöste, wurden seine Drainagen vergrößert. Eine minderwertige linke retroperitoneale Sammlung verbesserte sich signifikant, aber er entwickelte eine persistierende nekrotische Sammlung neben dem Pankreasschwanz, die sich mit perkutaner Drainage nicht verbesserte. Eine fluoroskopische Abflussinjektion zeigte, dass die Sammlung mit dem Dünndarm kommunizierte. Er hatte anhaltende Bauchschmerzen und war zeitweise fieberhaft und wurde daher an uns überwiesen.
Die körperliche Untersuchung ergab einen gesund aussehenden Mann mit normalen Vitalzeichen. Kopf-, Hals- und Herz-Lungen-Untersuchung waren alle normal. Sein Bauch war weich und leicht zart im linken Hemiabdomen. Er hatte zwei 24 Fr Drainagen, die aus dem seitlichen Bauch mit eitrigem Ausgang herausragten.
Ein abdominaler CT-Scan zeigte eine anhaltende 9 cm x 6 cm große Ansammlung von abgemauerten Nekrosen neben dem Pankreasschwanz im linken oberen Quadranten (Abbildung 1).
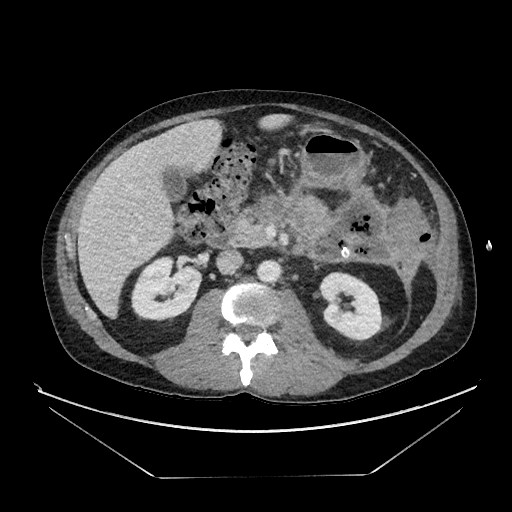
Abbildung 1. CT-Scan des Patienten, der eine nekrotische Ansammlung in der Nähe des lufthaltigen Pankreasschwanzes und mit perkutanem Abfluss zeigt.
Die meisten peripankreatischen Nekrosen resultieren aus einer akuten Pankreatitis, die am häufigsten durch Ethanolgebrauch oder Gallensteine verursacht wird. Trauma-induzierte Nekrose wie in diesem Fall ist relativ selten. Die meiste Pankreatitis ist mild und führt nicht zu lokalen Komplikationen wie Peripankreasflüssigkeitsansammlungen oder Nekrose. Wenn diese auftreten, sollten sie zunächst nicht-interventionell behandelt werden, und Nekrose- oder Flüssigkeitsansammlungen werden in den meisten Fällen verschwinden. Wenn Nekrose oder Flüssigkeitsansammlungen bestehen bleiben, besteht wie in diesem Fall ein Infektionsrisiko. Wenn eine Infektion auftritt, sollte sie mit einem Step-up-Ansatz behandelt werden, bei dem ein minimal-invasives Drainageverfahren (entweder endoskopisch oder perkutan) der erste Schritt ist. In 20-40% der Fälle löst dies die Infektion auf. Wenn dies nicht der Fall ist, ist im Allgemeinen eine Nekrosektomie erforderlich. 2–4
Zum Zeitpunkt der Präsentation bei uns gab es mehrere Möglichkeiten für den Patienten. Eine fortgesetzte perkutane Entwässerung hätte die Sammlung in diesem Fall möglicherweise gelöst, jedoch auf Kosten vieler Wochen laufender externer Entwässerung. Die nekrotische Ansammlung dieses Patienten war nicht für eine transgastrische Drainage zugänglich, da sie nicht an den Magen anstieß. Videoassistiertes retroperitoneales Debridement (VARD) oder Sinus-Trakt-Endoskopie (STE) sind minimal-invasive Optionen für diesen Patienten. Auch eine offene chirurgische Nekrosektomie wäre möglich gewesen.
Wir haben uns in diesem Fall für STE entschieden, weil die Gesamtgröße der Sammlungen relativ klein war und das Vorhandensein von enterischen Fisteln die Wahrscheinlichkeit von Wundkomplikationen erhöhte, die durch STE minimiert würden.
In den letzten Jahren hat sich die offene Operation zu einem minimal-invasiven Step-up-Ansatz für die Behandlung infizierter Pankreasnekrose verlagert. 2–4 Dieser Artikel beschreibt STE, eine wichtige Technik der minimal-invasiven Nekrosektomie. 5 Der Step-up-Ansatz und der Einsatz von STE und anderen minimal-invasiven Techniken haben die Morbidität und Mortalität bei Patienten, die sich einer Intervention wegen infizierter Pankreasnekrose unterziehen, signifikant verringert. 6 Unabhängig von der genauen angewandten Technik umfassen die gemeinsamen Managementprinzipien ein frühzeitiges nicht-interventionelles Management, damit sich die Nekrose abschotten kann, ein anfängliches Eingreifen mit minimal-invasiver Drainage und eine minimal-invasive Nekrosektomie, die eine klar abgegrenzte Nekrose behandelt.
Während dieser Artikel die Verwendung von STE zur Behandlung von infizierter peripankreatischer Nekrose demonstriert, ist es wichtig zu verstehen, welche anderen Techniken zur Optimierung von STE zur Verfügung stehen. Die wichtigsten anderen verwendeten Techniken sind VARD und transgastrische Nekrosektomie, die endoskopisch oder chirurgisch durchgeführt werden können. VARD benötigt ein retroperitoneales Fenster in die Nekrose und eignet sich optimal für das schnelle Debridement von großvolumigen Nekrose-Tracking zu den parakolischen Dachrinnen. Es beinhaltet eine Abschneidung, die über den Abfluss durchgeführt wird, um auf die Nekrosehöhle zuzugreifen. 7 Die transgastrische Nekrosektomie ist ein bevorzugter Weg, wenn ein klares transgastrisches Fenster in die Nekrosehöhle vorhanden ist, wobei der Großteil der Nekrosebelastung in Kontinuität mit dem hinteren Magen liegt. Endoskopische transgastrische Drainage und Debridement und VARD wurden in zwei kürzlich durchgeführten randomisierten Studien positiv mit der offenen Nekrosektomie verglichen. 3,8,9 Es wurde gezeigt, dass beide die Häufigkeit von neu auftretendem Organversagen nach dem Debridement reduzieren. Endoskopisches Debridement führte auch zu einer Verringerung der Mortalität und der äußeren Fistelbildung im Vergleich zur chirurgischen Nekrosektomie. Seine Hauptnachteile sind die anatomischen Anforderungen an den transgastrischen Zugang und die häufige Notwendigkeit mehrerer Reinterventionen (Median 3, in zwei verschiedenen randomisierten Studien). 9,10 VARD, das als Teil eines Step-up-Protokolls durchgeführt wurde, führte zu niedrigeren Kosten und niedrigeren Raten von Diabetes mellitus im Vergleich zur Nekrosektomie, die über eine Laparotomie durchgeführt wurde, führte jedoch weder zu einem Mortalitätsvorteil noch zu einer Verringerung der Fistelbildungsrate. 8 VARD und endoskopische transgastrische Nekrosektomie wurden nun in einer randomisierten Kopf-an-Kopf-Studie direkt miteinander verglichen, die keinen Unterschied im Tod oder bei größeren Komplikationen, aber einen Vorteil für die endoskopische Nekrosektomie bei einigen sekundären Endpunkten einschließlich Pankreasfistel zeigte. 10 Einwohner
Die chirurgische transgastrische Nekrosektomie kann offen oder laparoskopisch durchgeführt werden, macht mehrere Verfahren überflüssig und ermöglicht eine gleichzeitige Cholezystektomie, wenn sie bei biliärer Pankreatitis benötigt wird. Es unterliegt jedoch immer noch den gleichen anatomischen Einschränkungen wie die endoskopische transgastrische Nekrosektomie. Eine kürzlich durchgeführte randomisierte Studie, in der eine Kombination der chirurgischen transgastrischen Nekrosektomie mit VARD verglichen wurde, zeigte höhere Komplikationsraten mit den chirurgischen Ansätzen, aber keinen Unterschied in der Mortalität. 11 Zwar wurden darin chirurgische mit endoskopischen transgastrischen Ansätzen nicht direkt verglichen, doch legt sie nahe, dass der chirurgische Ansatz selektiv angewandt werden sollte. Die Kombination der endoskopischen transgastrischen Drainage mit der perkutanen Drainage, die als "Dual-Modality-Drainage" (DMD) bezeichnet wird, ergibt den Hauptvorteil der endoskopischen Drainage - die niedrige Rate der externen Fistel -, ermöglicht aber auch den Zugang zu Teilen der Sammlungen, die endoskopisch schwer zu erreichen sind. 12 In der ursprünglichen Beschreibung von DMD wurde auf beiden Wegen keine Nekrosektomie durchgeführt. Wir kombinieren jetzt routinemäßig die transgastrische Drainage mit der Nekrosektomie, die entweder von STE oder VARD durchgeführt wird. 13 Wir haben festgestellt, dass dies die Hauptvorteile der chirurgischen Nekrosektomie (schnelles Debridement und die Fähigkeit, leichter auf Nekrose zuzugreifen, die nicht an den Magen angrenzt) und der endoskopischen transgastrischen Nekrosektomie (Kontrolle externer Fisteln) kombiniert.
Wenn man VARD gegenüber STE betrachtet, hat jeder Vor- und Nachteile. VARD verwendet Geräte, die Chirurgen vertraut sind, wie ein Laparoskop für die Visualisierung und einen Ring oder eine laparoskopische Pinzette für das Debridement, und der eigentliche Akt des Debridements, sobald der Hohlraum betreten wird, ist der offenen chirurgischen Nekrosektomie sehr ähnlich. Aus diesen Gründen können viele Chirurgen feststellen, dass es eine einfachere Technik ist. VARD, wie die offene Nekrosektomie, ermöglicht ein schnelles Debridement großer Nekrosebrocken und hat unserer Erfahrung nach noch keine wiederholten Verfahren erfordert. Es gibt zwei Hauptnachteile von VARD. Eine davon ist, dass Wundkomplikationen, obwohl sie im Allgemeinen geringfügig sind, relativ häufig sind. Die andere ist die Anforderung eines retroperitonealen Weges in die Nekrose, der breit genug ist, um eine sichere Abholzung entlang des Abflusskanals zu ermöglichen und auch in den Hohlraum an einer Stelle eintritt, die ein vollständiges Debridement ermöglicht.
Im Vergleich zur VARD- oder endoskopischen transgastrischen Drainage ist STE relativ frei von anatomischen Anforderungen. Praktisch jede nekrotische Sammlung, auf die perkutan zugegriffen werden kann, kann von STE abgerufen werden. Dies ist ein Vorteil, wenn der einzige oder beste Weg in die Nekrose transperitoneal, interkostal ist oder wenn das Fenster in die Nekrose so eng ist, dass die für VARD erforderliche Reduzierung Schäden an lebenswichtigen Strukturen riskiert. Diese Flexibilität ist vielleicht der größte Vorteil von STE, da sie die Patientenberechtigung erheblich erweitert und die Notwendigkeit einer morbideren offenen Nekrosektomie oder einer sehr langen perkutanen Drainage für die Behandlung von Sammlungen, die über transgastrische oder retroperitoneale Ansätze nicht zugänglich sind, überflüssig macht. Darüber hinaus ist STE im Wesentlichen frei von Wundkomplikationen, da der einzige Schnitt die eigentliche Abflussstelle ist. STE erfordert jedoch eine Vertrautheit mit Geräten, die von Chirurgen seltener verwendet werden, wie z. B. ein starres Nephroskop und eine intraoperative Durchleuchtung. Die relativ geringe Instrumentierung bedeutet auch, dass für große nekrotische Sammlungen häufig mehrere Verfahren erforderlich sind.
In diesem Fall, mit einer relativ kleinen Sammlung von Nekrose, wurde das komplette Debridement in einem Verfahren durchgeführt. Wenn dies aufgrund eines großen Nekrosevolumens oder aufgrund einer engen Haftung der Nekrose an lebenswichtigen Strukturen wie Milzgefäßen nicht möglich ist, kann ein Abfluss mit einem geplanten Wiederholungsverfahren an Ort und Stelle belassen werden. Wenn eine Wiederholung geplant ist, platzieren wir einen 7 Fr-Katheter neben dem größeren Drainagekatheter durch den gleichen Hautschnitt, durch den die Bewässerung eingeflößt werden soll. Wir führen in der Regel eine kontinuierliche Bewässerung mit 0,9% Kochsalzlösung bei 200 ml / Stunde für 48-72 Stunden zwischen den Verfahren durch. Falls vorhanden, kann der Spülkatheter an einer Infusionspumpe befestigt werden, und der Drainagekatheter ist mit einem Drainagebeutel verbunden, und die Haut wird mit unterbrochenen Nähten um den Katheter geschlossen. Nach einer Phase der Bewässerung ist es sehr üblich, dass die Restnekrose lose anhaftend und viel schneller und sicherer debridiert ist, als es möglich gewesen wäre, wenn sie beim ersten Eingriff beibehalten worden wäre. Aus diesem Grund sollte die Versuchung, die Wände des Hohlraums aggressiv zu debridieren, aufgrund des Blutungsrisikos vermieden werden, und die Schwelle zur Wiederholung des Verfahrens sollte niedrig sein. Selbst wenn wir dieser Leitlinie folgen, bleibt unsere mittlere Anzahl von Verfahren 1 mit einem Mittelwert von 1,8 (Bereich 1–4). 7
Schließlich zeigt dieser Fall eine enterische Fistel zum Jejunum. Darmfisteln im Dünndarm, Magen und Dickdarm sind keine Seltenheit. Bis heute mussten wir nie direkt an der Fistel eingreifen, und alle Fisteln haben sich mit vollständigem Debridement der Nekrosehöhle geschlossen, wie in diesem Fall. Die chirurgische Reparatur oder Resektion des proximalen Darms oder der Diversion (im Falle von distalen Dünndarm- oder Dickdarmfisteln) sollte sehr selektiv eingesetzt werden. Dieser Patient wurde am Tag nach dem Eingriff nach Hause entlassen. Seine Abflüsse wurden am postoperativen Tag 12 entfernt.
- Radioluzenter OP-Tisch
- C-Bogen
- Amplatz Super Stiff Guidewire (.035" Durchmesser), Boston Scientific
- Hochdruck-Nephrostomie-Ballonkatheter und -scheide (30 Fr), Boston Scientific
- Starres Nephroskop (30 Fr), Storz
- 16-28 Fr perkutaner Abfluss
Nichts zu offenbaren.
Der Patient, auf den in diesem Videoartikel Bezug genommen wird, hat seine Einverständniserklärung gegeben, gefilmt zu werden, und ist sich bewusst, dass Informationen und Bilder online veröffentlicht werden.
Citations
- Peery AF, Crockett SD, Barritt AS, et al. Belastung durch Magen-Darm-, Leber- und Bauchspeicheldrüsenerkrankungen in den Vereinigten Staaten. Gastroenterologie. 2015;149(7):1731-1741. doi:10.1053/j.gastro.2015.08.045
- Tenner S, Baillie J, DeWitt J, Vege SS; Amerikanisches College für Gastroenterologie. American College of Gastroenterology Richtlinie: Management von akuter Pankreatitis. Am J Gastroenterol. 2013;108(9):1400-1416. doi:10.1038/ajg.2013.218
- Hollemans RA, Bakker OJ, Boermeester MA, et al.; Niederländische Pankreatitis-Studiengruppe. Überlegenheit des Step-up-Ansatzes gegenüber der offenen Nekrosektomie in der Langzeit-Follow-up von Patienten mit nekrotisierender Pankreatitis. Gastroenterologie. 2019;156(4):1016-1026. doi:10.1053/j.gastro.2018.10.045
- Arbeitsgruppe IAP/APA Acute Pancreatitis Guidelines. IAP/APA evidenzbasierte Leitlinien für die Behandlung von akuter Pankreatitis. Pankreatologie. 2013;13(4 suppl 2):e1-15. doi:10.1016/j.pan.2013.07.063
- Carter CR, McKay CJ, Imrie CW. Perkutane Nekrosektomie und Sinustrakt-Endoskopie bei der Behandlung von infizierter Pankreasnekrose: eine erste Erfahrung. Ann Surg 2000;232(2):175-180. doi:10.1097%2F00000658-200008000-00004.
- van Brunschot S, Hollemans RA, Bakker OJ, et al. Minimalinvasive und endoskopische versus offene Nekrosektomie bei nekrotisierender Pankreatitis: eine gepoolte Analyse individueller Daten für 1980 Patienten. Darm. 2018;67(4):697-706. doi:10.1136/gutjnl-2016-313341
- Fong ZV, Fagenholz PJ. Minimal-invasives Debridement bei infizierter Pankreasnekrose. J Gastrointest Surg. 2019;23(1):185-191. doi:10.1007/s11605-018-3908-5
- van Santvoort HC, Besselink MG, Bakker OJ, et al.; Niederländische Pankreatitis-Studiengruppe. Ein Step-up-Ansatz oder eine offene Nekrosektomie bei nekrotisierender Pankreatitis. N Engl J Med. 2010;362(16):1491-1502. doi:10.1056/NEJMoa0908821
- Bakker OJ, van Santvoort HC, van Brunschot S, et al.; Niederländische Pankreatitis-Studiengruppe. Endoskopische transgastrische vs. chirurgische Nekrosektomie bei infizierter nekrotisierender Pankreatitis: eine randomisierte Studie. JAMA. 2012;307(10):1053-1061. doi:10.1001/jama.2012.276
- van Brunschot S, van Grinsven J, van Santvoort HC, et al.; Niederländische Pankreatitis-Studiengruppe. Endoskopischer oder chirurgischer Step-up-Ansatz für infizierte nekrotisierende Pankreatitis: eine multizentrische randomisierte Studie. Lanzette. 2018;391(10115):51-58. doi:10.1016/S0140-6736(17)32404-2
- Bang JY, Arnoletti JP, Holt BA, et al. Ein endoskopischer transluminaler Ansatz reduziert im Vergleich zur minimal-invasiven Chirurgie Komplikationen und Kosten für Patienten mit nekrotisierender Pankreatitis. Gastroenterologie. 2019;156(4):1027-1040.e3 doi:10.1053/j.gastro.2018.11.031
- Ross AS, Irani S, Gan SI, et al. Dual-Modality-Drainage von infizierten und symptomatischen abgeschirmten Pankreasnekrose: langfristige klinische Ergebnisse. Gastrointest Endosc. 2014;79(6):929-935. doi:10.1016/j.gie.2013.10.014
- Fagenholz PJ, Thabet A, Müller PR, Forcione DG. Kombinierte endoskopische trangastrische Drainage und videogestütztes retroperitoneales Pankreasdebridement - das Beste aus beiden Welten für ausgedehnte Pankreasnekrose mit enterischen Fisteln. Pankreatologie. 2016;16(5):788-790. doi:10.1016/j.pan.2016.06.009
Cite this article
Fagenholz P. Pankreasdebridement mittels Sinustrakt-Endoskopie. J Med Einblick. 2021;2021(250). doi:10.24296/jomi/250.

