皮質腺腫に対する経腹腔鏡下右副腎摘出術
Main Text
原発性高アルドステロン症、またはコン症候群は、片方または両方の副腎が過剰量のアルドステロンを産生し、高血圧および低カリウム血症を引き起こす疾患です。この障害を引き起こす一般的な状態には、副腎の腺腫または両方の副腎の過形成が含まれます。まれに、副腎皮質の悪性増殖または家族性高アルドステロン症によって引き起こされます。高血圧は頭痛やかすみ目を引き起こす可能性があります。低カリウムは、倦怠感、筋肉のけいれん、筋力低下、しびれ、または一時的な麻痺を引き起こす可能性があります。
原発性高アルドステロン症は、アルドステロン、レニン、およびカリウムの血清レベルを測定することによって診断されます。患者は古典的にアルドステロンレベルが高く、レニンレベルが抑制され、カリウムレベルが低い。診断が確立されると、画像検査を使用してソースの局在化が実行されます。副腎静脈サンプリングも行われ、過剰なアルドステロンを産生している側をより正確かつ直接的に決定する。
副腎腫瘍によって引き起こされる原発性高アルドステロン症は、副腎摘出術で治療されます。患者の約95%は、手術が成功した後、高血圧の有意な改善に気付くでしょう。症例は58歳の女性で,低カリウム血症と長年の高血圧治療に抵抗性の1例を経験したので報告する.彼女の血液検査は、高アルドステロンレベルと低レニンレベルを示し、高アルドステロン症の診断を確認しました。CT検査では両側に副腎結節を認めた.副腎静脈サンプリングにより、右副腎結節が原因として特定されました。腹腔鏡下アクセスが得られ、副腎を解剖して露出させ、副腎静脈を結紮し、副腎を切除した。
原発性アルドステロン症は、1956年にジェロームコンによって最初に記述されました。1 コン博士の名前を冠した症候群は、低カリウム血症と高血圧を特徴とし、どちらも医学的管理に比較的難治性です。原発性アルドステロン症は一般的ですが、二次性高血圧の原因は過小評価されています。高血圧患者の1〜10%が根底にある原発性高アルドステロン症があると考えられています。.2
原発性アルドステロン症の最も一般的な原因は、原発性アルドステロン産生腫瘍または副腎の糸球体帯の過形成です。3
薬剤耐性高血圧症の患者には、コン症候群の精密検査が必要です。片側性腫瘍が過剰なアルドステロンの発生源として特定された場合、腫瘍を除去する手術が必要です。
症例は58歳の女性で,長年の高血圧症を患っている.彼女は3つの薬で治療されていましたが、高血圧の十分な緩和はありませんでした。彼女の臨床検査は長期の低カリウム血症で顕著であり、彼女の記録された最低値は2.3 mmol / L(正常範囲3.6〜5.2 mmol / L)でした。
彼女の血清アルドステロンおよび血漿レニン活性(PRA)を測定して、彼女のアルドステロン対レニン比(ARR)を決定しました。血清アルドステロンは24 ng/dl,PRAは0.6 ng/ml/hでARRは40(正常<30 ng/mL/hの範囲)であった。
CTスキャンで両側性副腎病変を示した後、副腎静脈サンプリングを行い、アルドステロンとコルチゾールのレベルを測定し、対照として下大静脈を使用してそれらの比率を決定しました(表1)。4 右腎静脈のアルドステロン濃度は左右腎静脈でそれぞれ3,800 ng/dl,78 ng/dlであった。下大静脈からの対照値は66 ng/dlであった。コルチゾール測定を含むこれらの値に基づいて、計算された右対左のアルドステロン/コルチゾール比は13.75でした。4を超える比率は、肯定的な所見と見なされます。まとめると、検査所見は、右副腎が過剰なアルドステロンの発生源であったことを示唆しています。
原発性アルドステロン症は、身体検査の特定の徴候によって特徴付けられるものではありません。それにもかかわらず、長年の高血圧は左心室肥大を引き起こし、聴診時にS4音を生成する可能性があります。その他の非特異的兆候には、頸動脈打撲傷、筋力低下、高血圧性脳症に関連する精神状態の変化などがあります。.3
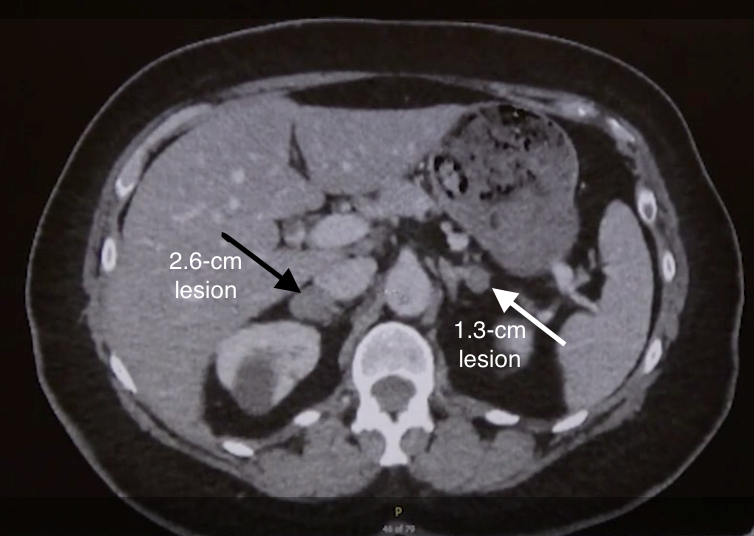
腹部CTで右副腎に2.6cm,左副腎に1.3cmの病変を認めた(図1)。
治療せずに放置すると、原発性高アルドステロン症の経過は、低カリウム血症および慢性高血圧症の後遺症を特徴とする。低カリウム血症に続発する筋力低下と血清クレアチンキナーゼレベルの上昇は、症状と兆候として報告されています。.5 慢性高血圧は、心房細動、心筋梗塞、脳卒中などの主要な有害な心臓イベントのリスクが高くなります。3
片側性副腎腫瘍の腹腔鏡下切除は、コン症候群に最適な治療法です。6 ただし、一部の患者は降圧薬でうまく管理されます。手術は一般的に両側性疾患の患者には禁忌です。そのような患者は、ミネラルコルチコイド拮抗薬を含む降圧剤で医学的に最もよく管理されます。.外科的アプローチは、主に腹腔鏡または後腹膜鏡検査です。7
治療の目標は、患者の低カリウム血症と高血圧を逆転させることです。この手順は、事実上100%の症例で低カリウム血症を逆転させます。しかし、高血圧の程度は一般的に減少しますが、患者は降圧薬を中止できるのは症例の35%にすぎません。8
片側性副腎摘出術は、疾患が片側性である場合に最も効果的です。両側性過形成または両側性アルドステロン産生腫瘍(非常にまれ)の患者は、一般に手術の候補者ではなく、血圧降下薬およびスピロノラクトンなどのアルドステロン遮断薬で医学的に治療する必要があります。.
腹腔鏡下アプローチを用いて、原発性アルドステロン症の58歳の女性から2.5cmの皮質腺腫を切除しました。注目に値するこの症例の特徴の1つは、患者がCTで両側性腫瘍の証拠を持っていたことです。しかし、副腎静脈サンプリングは、右側腫瘍が彼女の過剰なアルドステロンの発生源であることを示唆しました。
現在、私たちは通常、重大な併存疾患がない限り、手術当日(外来患者)に患者を帰宅させます。彼らは、少なくとも1日2回血圧を監視し続け、処方されたとおりに血圧薬を服用することをお勧めします(通常、薬剤の数と投与量を大幅に削減します)。退院後は、同日後、翌日に電話で綿密にフォローしています。
この患者は彼女のベータ遮断薬のみで退院しました。フォローアップでは、彼女の血圧とカリウムレベルを監視しました。この患者の目標は、最終的にすべての血圧薬から彼女を引き離すことでした。
- 遠藤パドル
- 遠藤キャッチバッグ
何一つ。
このビデオ記事で言及されている患者は、撮影についてインフォームドコンセントを与えており、情報や画像がオンラインで公開されることを認識しています。
References
- コンJW、ルイLH。原発性アルドステロン症、新しい臨床実体。アンインターンメッド。1956;44(1):1-15.DOI: 10.7326/0003-4819-44-1-1.
- Piaditis G、Markou A、Papanastasiou L、Androulakis II、Kaltsas G.アルドステロン症の進歩:高血圧前および高血圧における原発性アルドステロン症の有病率のレビュー。ユーロJエンドクリノール。2015;172:R191-203.DOI: 10.1530/EJE-14-0537.
- コブA、アエドゥラNR。原発性高アルドステロン症。[2019年4月21日更新]。で:スタットパール。トレジャーアイランド(フロリダ州):スタットパールズパブリッシング;2019.から入手可能: https://www.ncbi.nlm.nih.gov/books/NBK539779/?report=classic。
- デイポリイA、ベイリンA、ウィッキーS、アランサリS、オクルR.コン症候群の副腎静脈サンプリング:診断と臨床転帰。診断。2015;5(2):254-71.DOI: 10.3390/diagnostics5020254.
- Olt S、Yaylaci S、Tatli L、Gunduz Y、Garip T、Tamer A.低カリウム血症誘発性ミオパチーおよび大量のクレアチンキナーゼ上昇をコン症候群の最初の症状として。ニジェールメッドJ.2013;54(4):283.DOI: 10.4103/0300-1652.119658.
- キム・K、キム・JK、リー・CR、他原発性高アルドステロン症に対する腹腔鏡下副腎摘出術の外科的転帰:単一の施設での20年の経験。アンサーグトリートレス。2019;96(5):223-9.DOI: 10.4174/astr.2019.96.5.223.
- Wierdak M, Sokołowski G, Natkaniec M, et al.Conn症候群に対する腹腔鏡下副腎摘出術の短期および長期の結果。Wideochir Inne Tech maloinwazyjne.2018年9月;13(3):292。DOI: 10.5114/wiitm.2018.74833.
- パルタサラシーHK、メナールJ、ホワイトWB、他高血圧患者におけるエプレレノンとスピロノラクトンの降圧効果と原発性アルドステロン症の証拠を比較する二重盲検無作為化研究。J高血圧。2011年5月;29(5):980-90。DOI: 10.1097/HJH.0b013e3283455ca5.
Cite this article
コーエンS、ホディンR.皮質腺腫に対する経腹腔鏡下右副腎摘出術。Jメッドインサイト。2023;2023(240).DOI: 10.24296/jomi/240.

.png)