개방 원위 위절제술
Main Text
완전 마진 음성(R0) 절제술은 위 선암에 대한 유일한 잠재적 치료 치료법으로 남아 있습니다. 수술 선택은 종양의 위치와 질병의 단계에 따라 다릅니다. 이 환자는 증상이 있는 빈혈을 보였고, 정밀 검사 결과 위염과 위말단부에 작은 종양이 있는 것으로 나타났습니다. 조직검사 결과 선암이 확인되었고, 내시경 초음파(EUS)에서 이 종양을 T2 N0으로 진단했습니다. 병기 결정 스캔에서는 원격 전이성 질환의 증거가 발견되지 않았습니다. 이 환자가 비교적 초기 단계의 종양을 가지고 있었기 때문에 우리는 선행 수술을 진행하기로 결정했으며, 이 경우 원위 위 절제술을 수반했습니다. 이 비디오는 "확장된" D1 림프절 절제술로 개복 원위 절제술을 수행하는 숙련된 위 외과 의사의 기술을 보여줍니다.
지난 수십 년 동안 미국에서 위암 발병률이 급격히 감소했지만, 위암은 여전히 암 관련 사망의 중요한 원인입니다. 병기 결정 방식, 수술 요법 및 수술 전후 관리의 상당한 개선에도 불구하고 대부분의 위암 환자의 예후는 여전히 좋지 않습니다. 이것은 주로 이 암의 공격적인 생물학과 대부분의 환자가 임상의에게 제시하는 질병의 진행된 단계의 결과입니다. 위험 요인으로는 헬리코박터 파일로리 및 엡스타인-바 바이러스(EBV) 감염, 악성 빈혈, 이전 위 절제술, 흡연, 고염분 섭취 등이 있습니다. 위암의 약 10%는 E-cadherin(CDH1) 유전자의 생식세포 돌연변이를 특징으로 하는 유전성 미만성 위암(HDGC)과 DNA 불일치 복구 유전자의 생식세포 돌연변이를 특징으로 하는 유전성 비용종증 대장암(HNPCC) 증후군을 포함한 유전성 암 증후군에 기인합니다. 최근 위암에 대한 포괄적인 분자 평가는 EBV 감염 종양(9%), 현미부수체 불안정(MSI 높음) 종양(22%), 유전체 안정 종양(20%), 염색체 불안정 종양(50%)의 4가지 주요 게놈 아형과 대략적인 빈도를 정의하는 분류 체계로 이어졌습니다. 1개
위암 진단을 암시하는 전형적인 증상은 거의 없으며, 이는 이 암이 진행된 단계에서 자주 진단되는 이유를 설명합니다. 상복부 통증, 소화불량, 위산 역류와 같은 초기 증상은 매우 비특이적이어서 대부분의 환자는 추가 조사 없이 단순히 경험적으로 제산제로 치료합니다. 병이 진행됨에 따라 증상이 더욱 두드러지고 불길해지며 삼킴곤란, 메스꺼움, 구토, 조기 포만감, 식욕 부진, 피로, 체중 감소와 같은 증상이 나타납니다. 위암의 위치와 조직학적 유형에 따라 근위 종양의 삼킴곤란부터 원위부 종양 폐쇄를 위한 구토, 미만형(linitis plastica) 종양의 경우 조기 포만감과 체중 감소에 이르기까지 증상 복합체가 결정되는 경우가 많습니다. 2,3호
이 환자는 위염과 만성 위식도 접합부 협착 병력이 있는 84세 남성으로, 피로와 호흡 곤란 증상으로 주치의에게 내원했습니다. 전체 혈구 수를 측정한 결과 환자가 빈혈 상태임을 알 수 있었습니다. 그는 복통, 메스꺼움, 구토, 배변 습관의 변화, 식사 장애, 체중 감소 등을 부인했다.
위암 환자의 신체 검사는 일반적으로 상복부 압통을 제외하고는 눈에 띄지 않으며 만져지는 상복부 종괴의 가능성은 적습니다. 버쇼 결절, 메리 조셉 수녀의 회음부 결절, 블루머 선반과 같은 고전적인 시조 신체 소견은 드물게 나타나지만 볼 수 있는 경우 진행된 전이성 질환을 나타냅니다. 마찬가지로, 위암 환자에서 악액질, 황달, 복수 및 간비대증의 존재는 일반적으로 불치의 전이성 질환을 의미합니다. 우리 환자는 건강해 보였고, 진찰 결과 복부가 부드러웠고 만져지는 종괴는 없었다.
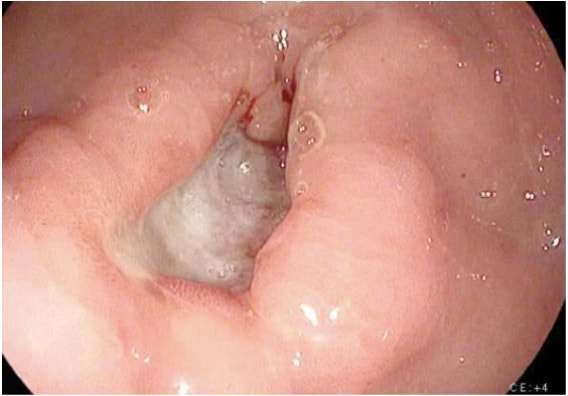
위암 정밀 검사를 위한 영상에는 다양한 연구가 포함됩니다. 위암의 진단은 일반적으로 조직검사를 통한 내시경 검사로 쉽게 확인할 수 있습니다(그림 1). 내시경 검사는 위 내 종양의 위치와 범위를 정의하며, 내시경 초음파(EUS)와 결합하면 종양 침범 깊이(T 병기)를 정확하게 추정할 수 있습니다. EUS는 위암의 T 단계를 확립하는 데 가장 민감한 양식이며, EUS는 국소 림프절을 평가하고 의심스러운 림프절의 바늘 생검을 통해 결절 침범(N 단계)을 확인할 수 있습니다. 흉부, 복부 및 골반의 CT 스캔을 수행하여 절제 부위 외부의 폐, 간, 복막 또는 림프절과 같은 원격 전이성 전이를 평가해야 합니다. 또한 CT 스캔은 복막 종양 전이를 나타낼 수 있고 세포학적 검사를 위해 이미지 유도 수단으로 샘플링할 수 있는 소량의 복수를 감지하는 데 민감합니다. PET 및 PET-CT 스캔은 위암의 수술 전 병기 결정에서 일상적으로 권장되지는 않지만 유용한 추가 정보를 제공할 수 있습니다. PET는 원발성 종양, 특히 초기 및 미만성 위암을 검출하는 데 민감도가 낮지만 국소 림프절 전이 검출에 있어 CT보다 특이도가 높고(90% 대 60%) 간, 폐 및 원격 림프절 전이의 검출에 합리적인 민감도를 가지고 있습니다. 4 또한 PET는 초기 단계에서 치료에 대한 반응자를 정확하게 감지하여 임상의가 환자를 가능한 한 적극적인 화학 요법 요법으로 유지할 수 있도록 하기 때문에 선행 화학 요법에 대한 종양 반응을 모니터링하는 데 사용할 수 있습니다.
국소 진행성 암(T3+/N+) 환자는 복강경 검사에 의한 추가 병기 결정이 고려됩니다. 병기 결정 복강경 검사는 계획된 개복술 직전에 수행하거나 수술 전 요법을 고려하는 환자에게 수행되는 치료 전 절차로 수행할 수 있습니다. 병기 결정 복강경 검사는 방사선 촬영상 잠복 복막 및 간 전이의 확인과 양성 세포학을 통해 환자의 30% 이상을 병기상으로 병기합니다. 5 개
위암은 일반적으로 림프절을 통해 전이되거나 혈액성으로 전이되며 일반적으로 간, 폐 또는 복막으로 전이됩니다. 또한 췌장과 횡결장과 같은 인접 장기를 침범하기 위해 직접 퍼질 수 있습니다. 위암을 치료할 수 있는 유일한 치료법은 수술입니다. 완전한 마진 음성 절제술과 (신)보조 요법을 시행하더라도 5년 생존율은 ~40%로 낮게 유지됩니다.
미국에서 위암에 대한 가장 일반적인 치료 패러다임은 역사적으로 고위험군(T3/4, 결절 양성, 응집력이 좋지 않은 유형) 환자에 대한 보조 화학방사선 요법(그룹 간 0116 시험에서 설명됨)이 그 뒤를 이었습니다. 6 그러나 이 임상시험에 참여한 환자의 64%만이 계획대로 수술 후 화학방사선 요법을 받을 수 있었으며, 영국 의학 연구 위원회(British Medical Research Council)가 실시한 MAGIC 임상시험에서 기술된 바와 같이 많은 환자들이 수술 전후 화학요법을 선호합니다. 이 임상시험에서 환자는 수술 전후 화학요법(수술 전후 에피루비신, 시스플라틴, 5-플루오로우라실(ECF)의 3주기)과 수술 또는 수술 단독으로 받도록 무작위 배정되었습니다. 5년 생존율은 수술 단독 요법군에 비해 수술 전후 화학요법군이 더 높았다(36% 대 23%). 7 환자의 ~40%만이 이 치료 접근법으로 권장되는 모든 요법을 완료하지만, 85% 이상의 환자가 수술 전 화학 요법의 계획된 3주기 모두를 받고 모든 환자는 적어도 한 주기의 화학 요법을 받습니다. 고위험 종양 환자를 위한 수술 전에 적어도 몇 주기의 전신 요법을 투여하는 것은 몇 가지 이점을 제공합니다: (1) 가능한 미세 전이성 질환의 조기 치료를 허용합니다. (2) PET-CT 스캔 영상과 같은 치료에 대한 생체 내 종양 반응을 모니터링할 수 있습니다. (3) 초기 전이성 질환이 발병하여 위절제술로 생존 혜택을 얻지 못하는 특히 나쁜 종양 생물학 환자를 선택할 수 있습니다. 7 개
완전 마진 음성(R0) 절제술은 위 선암에 대한 유일한 잠재적 치료 치료법으로 남아 있습니다. 수술 선택은 종양의 위치와 질병의 단계에 따라 다릅니다. 조직학적 등급이 양호한 표면 침습성(T1a) 위암은 감시림프절 생검을 병행하거나 동반하지 않고 내시경 점막 절제술 또는 쐐기 절제술로 치료할 수 있습니다. 이러한 시술은 일본의 외과 동료들에 의해 광범위하게 설명되었으며, 일본에서는 선별 내시경 검사가 널리 보급되어 있기 때문에 위암이 조기에 진단되는 경우가 많습니다. 미국 환자의 대다수는 증상이 있는 국소 진행성 종양을 가지고 있기 때문에 주요 수술 질문은 어떤 시술이 허용 가능한 이환율과 사망률로 완치 가능성이 가장 높은가 하는 것입니다. 많은 환자들이 의학적으로 부적합하거나 수술 전 영상 검사 또는 복강경 수술 시 전이성 질환이 있기 때문에 수술 대상이 아닙니다. 위 절제술을 받을 수 있는 환자의 경우 전체 위, 근위 및 원위 위 절제술을 선택할 수 있습니다. 전 세계적으로 복강경 시술을 시행하는 경험이 증가하고 있으며, 단기 결과와 결절 수율이 개선되고 생존 결과가 기존의 개복 시술과 동등합니다. 그러나 미국에서 위암 절제술의 대다수는 여전히 개방 접근법을 통해 시행되고 있습니다.
즉각적인 외과적 절제술을 고려해야 하는 환자에는 초기 단계(T1/T2 N0) 위암 환자와 출혈 또는 고등급 종양 관련 내강 폐쇄의 즉각적인 완화가 필요한 환자가 포함됩니다. 그러나 이 후자의 환자 집단에서 수술 전후 이환율과 사망률은 중요하며 절제술의 가능한 이점과 신중하게 비교해야 합니다. 국소적으로 진행된 위암 환자는 수술 전 화학요법 또는 화학방사선 요법을 받을 수 있습니다.
이 환자는 비교적 초기 단계의 종양(uT2N0)을 가지고 있었고 나이에 비해 매우 건강했기 때문에 원위 위 절제술을 받은 선행 수술을 받았습니다. 우리는 개방 원위 위절제술이 잠재적으로 저위험 암에 대한 선행 화학요법으로 과잉 치료의 위험을 제한하는 동시에 최종 병리학 보고서에서 더 진행된(예: T3+/N+) 암으로 판명될 경우 보조 요법을 제공할 수 있는 옵션을 남겨 두었다고 느꼈습니다.
위 절제술의 범위는 원발성 종양의 위치와 범위에 따라 결정됩니다. 전향적 무작위 임상시험에서는 위위부원위종양 환자에 대한 원위부절제술에 비해 위전절제술의 생존 우위를 입증하지 못했다. 8 그러므로, 적당한 크기의 위 잔여물을 유지하면서 종양으로부터 5 내지 6cm의 여유를 얻을 수 있는 환자들의 경우, 전체 위 절제술보다 이환율이 낮고 삶의 질이 더 좋기 때문에 보다 보존적인 위 절제술을 시행해야 합니다. 8 그럼에도 불구하고, R0 절제술을 위해 필요한 경우 전체 위절제술을 시행해야 하는데, 양성 절제술(R1 절제술)은 생존율이 매우 낮기 때문입니다. 네덜란드 위암 임상시험에서는 10%의 환자가 절제술이 양성이었고 그에 따라 3년 생존율이 마이너스 환자에 비해 열등했다(18% 대 63%). 9 그러나 현미경으로 침범된 가장자리는 림프절 전이가 5개 이하인 환자에서만 장기 생존에 영향을 미치는 것으로 보입니다. 근위 위암의 경우, 많은 외과 의사들이 근위 위절제술보다 전체 위절제술을 선호하는데, 이는 후자의 시술로 증상이 있는 위산 역류의 장기적인 후유증 때문입니다.
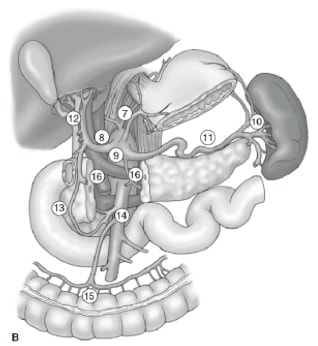
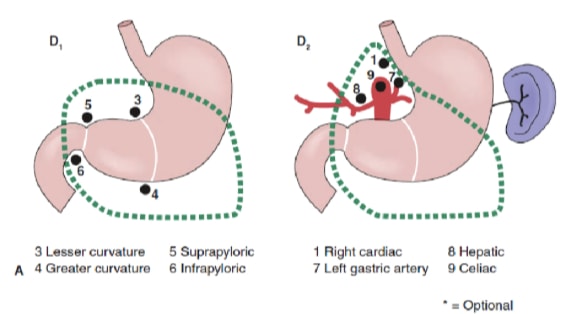
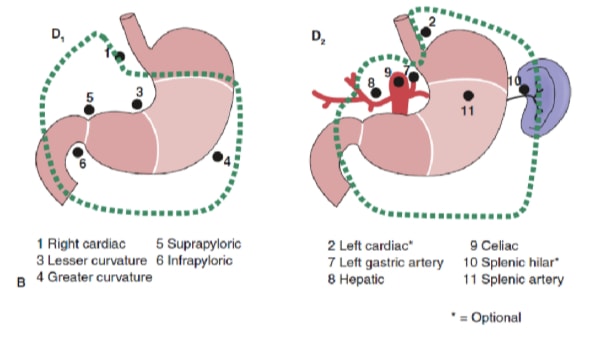
림프절 절제술의 정도는 위암 관리에서 가장 논란이 되는 문제 중 하나입니다. 위암 등록부(Gastric Cancer Registry)의 보고서와 기타 후향적 연구는 장기(D2) 림프절 절제술을 동반한 근치적 위절제술을 일본에서 치료 가능한 위암 치료를 위한 표준 치료법으로 만들었습니다. 10,11 일본 위암 연구회(Japanese Research Society for Gastric Cancer)는 위의 배수 림프절 분지를 6개의 복부 주위 스테이션(그림 2a)과 주요 혈관을 따라 췌장에 인접한 10개의 국소 스테이션을 포함하여 16개의 스테이션으로 분류합니다(그림 2b). 림프절 절제술의 범위는 D라는 명칭으로 표시됩니다. D1 절개에는 복부 결절(스테이션 1 - 6)만 포함됩니다. a D2 박리에는 총간동맥, 좌위동맥, 셀리악동맥, 비장동맥(스테이션 7-11)을 따라 림프절이 포함된다. D3 절제는 간장 간엽 내부와 대동맥에 인접한 추가 결절(스테이션 12-16)을 포함합니다(그림 3).
D1 절제술의 결과와 D2 절제술의 결과를 비교하는 두 건의 대규모 전향적 무작위 임상시험이 서양 환자를 대상으로 수행되었다. 이 두 연구 중 더 큰 규모의 연구인 네덜란드 위암 그룹 임상시험(Dutch Gastric Cancer Group Trial)의 15년 추적 관찰에서는 D2 림프절 절제술이 장기적 전체 생존 이득을 보여주지 못했지만(29%% 대 21%, P=.34), 위암 관련 사망률이 현저히 감소했으며(37% 대 48%, P=.01), D1 수술보다 국소 재발률이 낮았다. 9 그러나 더 광범위한 D2 림프절 절제술을 받은 환자에서 수술 후 이환율(43% 대 25%)과 사망률(10% 대 4%)이 훨씬 더 높았는데, 이는 대부분 완전한 결절 절제술을 달성하기 위해 이 그룹에서 더 많은 수의 비장 절제술과 췌장 절제술을 시행했기 때문입니다. 9 이와 유사하게, 의학연구위원회(Medical Research Council)가 실시한 영국 협력 임상시험에서는 D2 절제술에 무작위 배정된 환자들의 전체 생존율 또는 무재발 생존율에 도움이 되지 않은 높은 비장 절제술과 췌장 절제술의 높은 비율과 관련된 이환율 증가를 보고했습니다. 12의
이 두 연구의 결과에도 불구하고, 연구자들은 D2 림프절 절제술을 연장한 후 합병증 발생률을 낮출 수 있다면, 아시아의 경험 많은 센터에서 보고한 바와 같이 D2 절제술이 주는 생존 혜택이 위암을 앓고 있는 서양 환자들에게로 옮겨질 수 있다고 주장했다. 13 따라서 이탈리아 위암 연구 그룹은 일본의 마스터 외과 의사의 관찰을 통해 기술에 대한 엄격한 교육을 이수한 외과 의사가 환자를 대량 센터에서 췌장 보존 D2 림프절 절제술 또는 D1 림프절 절제술에 무작위 배정하는 3상 시험을 수행했습니다. 그들은 직접적인 종양 침범에 대해서만 췌장 절제술 또는 비장 절제술을 시행하는 D2 절제술을 받은 환자에서 이환율(17.9%)과 사망률(3.0%)이 매우 낮았다고 보고했습니다. 14 그러나 D1 그룹과 D2 그룹 간의 5년 전체 생존율에는 차이가 없음을 발견했습니다(66.5% 대 64.2%; P = 0.695), 하위 그룹 분석에서는 D2 림프절 절제술이 T2–T4 및/또는 결절 양성 종양 환자에게 도움이 될 수 있음을 시사했습니다. 14의
D2 림프절 절제술이 단순히 철저한 병기 결정인지 또는 특정 환자군(예를 들어, N2 질환 환자)에 대한 치료적 이점이 있을 수 있는지는 아직 불분명하다. 미국 암 합동 위원회(AJCC) 병기 편람의 가장 최근 제7판에 따르면 위암 환자의 정확한 병기 결정은 최소 15개의 림프절을 평가해야 한다는 점에 유의해야 합니다. 15 그런 다음 노드 스테이징은 N1 (1 - 2 포지티브 노드), N2 (3 - 6 포지티브 노드), N3a (7 - 15 포지티브 노드) 및 N3b (16+ 포지티브 노드) 범주를 갖는 포지티브 노드의 수를 기반으로 합니다. 연구에 따르면 환자 생존율 향상과 검체에서 검사한 림프절 수 증가 사이의 상관관계가 나타났습니다. 16 물론, 이것은 시술로 인한 치료상의 유익이 아니라 단지 더 정확한 병기 결정의 결과일 수 있습니다. 그러나 더 광범위한 림프절 절제술이 국소 재발률을 낮춘다는 간접적인 증거가 있으며, 이는 생존에 도움이 될 수 있습니다. 실제로, 대만의 한 센터에서 실시된 무작위 임상시험에서는 D1 절개술을 받은 환자(53.6%)에 비해 D3 절제술을 받은 환자(59.5%)의 전체 5년 생존율이 높은 것으로 확인되었습니다. 13의
지난 10년 동안 MGH에서 치료받은 환자의 경우, 위 절제술과 D2 림프절 절제술 후 이환율과 사망률이 각각 17%와 0%로 보고되었으며, 검체의 체외 절제술을 통한 림프절 수율 중앙값은 40마디로 증가했습니다. 미국에서 소계 및 전체 위절제술의 평균 입원 기간은 평균 9-10일이지만 많은 환자가 7일 이내에 퇴원합니다. 소계 및 전체 위 절제술의 장기 합병증에는 비타민 및 미네랄 결핍, 특히 비타민 B12, 비타민 D, 철분 및 칼슘의 결핍과 알칼리성 역류 위염, 덤핑 증후군, 루 정체 증후군 및 구심성 사지 증후군과 같은 전형적인 위절제술 후 증후군이 포함됩니다.
국소 위암에 대한 유일한 잠재적 완치 치료법은 수술이지만, R0 절제가 가능한 환자에서도 수술 전후 화학요법 또는 수술 후 화학방사선 요법으로 5년 생존율이 35%에서 40%에 불과합니다. 위암 치료의 미래 발전은 조기 진단을 위한 기술뿐만 아니라 더 나은 전신 치료법의 개발에 달려 있습니다.
A. 위 원위 절제술:
위 선암, 세뇨관형, 불일치 복구 단백질 발현 불안정. (시놉틱 보고서 참조).
B. 림프절 생검, 스테이션 8:
4개의 림프절에서 악성종양의 증거는 없다(0/4).
C. 림프절 생검, 스테이션 11:
두 개의 림프절에서 악성종양의 증거는 없다(0/2).
D. 림프절 생검, 스테이션 7:
두 개의 림프절에서 악성종양의 증거는 없다(0/2).
E. 림프절 생검, 스테이션 3:
한쪽 림프절에서 악성종양의 증거는 없다(0/1).
시놉틱 보고서:
종양 단계 요약: pT1bN0.
특정 부위 : 위 antrum.
종양 크기(최대 치수): 0.3cm(슬라이드에서 측정).
WHO 분류: 세뇨관 선암종.
조직학적 등급: G1(잘 분화됨)
침습 범위: pT1b(종양이 점막하를 침범함).
소혈관(혈액/림프관) 침습: 없음.
대형 선박 (정맥) 침입 : 없음.
신경 주위 침공: 없음.
근위 위 가장자리: 침습성 암종에 의해 침범되지 않음.
원위 십이지장 가장자리: 침습성 암종에 의해 침범되지 않음. (간격=0.4cm).
국소 림프절: pN0(국소 림프절 전이 없음): 31개의 림프절을 검사했습니다.
*림프절 총계는 모든 검체 부분을 포함합니다. 주 검체(검체 A)에는 22개의 림프절이 포함되어 있었습니다.
HER2 면역조직화학: Her 2 점수 0/음성(종양 세포의 < 10%에서 반응성 또는 매우 희미한 막질 염색 없음).
추가 연구:
MLH1 및 PMS가 손실되었습니다.
MSH2 및 MSH6 온전함.
추가 결과:
장 화생과 고급 이형성증을 동반한 위 전방 점막.
안저샘 용종.
엡스타인-바 바이러스 인코딩 RNA(EBER)는 음성입니다.
저희 환자는 수술 후 회복이 잘 되어 수술 후 5일째에 퇴원했습니다. 그의 최종 병리학 보고서는 그의 종양을 T1bN0으로 판정했고, 절제술의 가장자리는 음성이었다. 우리는 우수한 결절 채취(림프절 31개)를 달성했기 때문에 이 단계 할당의 정확성을 확신할 수 있습니다. 따라서 보조 요법이 필요하지 않으며 장기 예후가 우수합니다.
고정 복벽 견인기 시스템은 이 작업에 매우 유용할 수 있습니다. 우리는 Bookwalter를 사용했지만 다른 옵션으로는 Thompson 및 Omni 견인기 시스템이 있습니다. 십이지장과 위는 스테이플러(이 경우 Endo-GIA 스테이플러)로 절제됩니다. LigaSure 장치 또는 Harmonic 메스와 같은 혈관 밀봉 장치는 작은 혈관을 효율적으로 제어하는 데 매우 유용합니다. 좌측 위 동맥과 같은 더 큰 혈관은 혈관 스테이플러로 나누거나 전통적인 봉합 결찰로 조절할 수 있습니다.
저자는 공개할 갈등이 없습니다.
이 영상에 언급된 환자는 촬영에 대해 사전 동의를 했으며 자신의 개인 건강 정보가 확인되지 않은 방식으로 온라인에 게시될 것임을 알고 있습니다.
References
- 암 게놈 아틀라스 연구 네트워크. 위 선암의 포괄적인 분자 특성 분석. 자연. 2014; 513(7517):202-209. doi:10.1038/nature13480입니다.
- Mullen JT. 위암. 에서: Fischer J, ed. 수술의 숙달. 7 판 펜실베이니아 주 필라델피아: Lippincott Williams & Wilkins; 2017.
- 윤SS, 박 DJ. 위 선암. 에서: Cameron JL, Cameron AM, eds. 현재 외과 치료. 11 판 펜실베니아 주 필라델피아 : Saunders, 2014 : 87-95.
- Yun M. 18 F-FDG PET/CT를 이용한 위암 대사 영상. J 위암. 2014; 14(1):1-6. doi:10.5230/jgc.2014.14.1.1입니다.
- Ikoma N, Blum M, Chiang YJ 등 위암의 방사선학적 잠복막 암종증에 대한 병기 결정 복강경 및 세척 세포학의 수율. 앤 서그 온콜(Ann Surg Oncol.) 2016; 23(13):4332-4337. 도:10.1245/s10434-016-5409-7.
- 맥도날드 JS, 스몰리 SR, 베네데티 J 등 수술 후 화학방사선 요법은 위 또는 위식도 접합부의 선암에 대한 단독 수술과 비교됩니다. N Engl J Med. 2001; 345(10):725-730. doi:10.1056/NEJMoa010187입니다.
- 커닝햄 D, Allum WH, 스텐닝 SP 등 절제 가능한 위식도암에 대한 수술 전후 화학 요법 대 수술만. N Engl J Med. 2006; 355(1):11-20. doi:10.1056/NEJMoa055531입니다.
- 보제티 F, 마루비니 E, 본판티 G, 미첼리 R, 피아노 C, 겐나리 L; 이탈리아 위장 종양 연구 그룹. 위암에 대한 소계 대 전체 위절제술: 다기관 무작위 이탈리아 시험에서 5년 생존율. 앤 서그(Ann Surg). 1999; 230(2):170-178. doi:10.1097/00000658-199908000-00006입니다.
- Bonenkamp JJ, Hermans J, Sasako M, et al; 네덜란드 위암 그룹. 위암에 대한 확장된 림프절 절제술. N Engl J Med. 1999; 340(12):908-914. doi:10.1056/NEJM199903253401202입니다.
- 마루야마 K, 오카바야시 K, 키노시타 T. 일본의 위 수술의 발전과 그 근본성의 한계. 월드 J Surg. 1987; 11(4):418-425. 도:10.1007/BF01655804.
- 사사코 M, 맥컬록 P, 키노시타 T, 마루야마 K. 위암에 대한 림프절 절제술의 치료 가치를 평가하는 새로운 방법. BR J 수술 1995; 82(3):346-351. doi:10.1002/bjs.1800820321입니다.
- Cuschieri A, Weeden S, Fielding J 등; 외과 협동 그룹. 위암에 대한 D1 및 D2 절제 후 환자 생존: MRC 무작위 수술 시험의 장기 결과. Br J 암. 1999; 79(9-10):1522-1530. 도:10.1038/sj.bjc.6690243..
- Wu CW, Hsiung CA, Lo SS 등 위암 환자를 위한 결절 절제술: 무작위 대조 시험. 랜싯 온콜. 2006; 7(4):309-315. 도:10.1016/S1470-2045(06)70623-4.
- 데줄리 M, 사사코 M, 폰티 A; 이탈리아 위암 연구 그룹. 이탈리아 위암 연구 그룹의 이환율 및 사망률은 위암에 대한 D1 대 D2 절제술의 무작위 임상 시험입니다. BR J 수술 2010; 97(5):643-649. doi:10.1002/bjs.6936입니다.
- Edge SB, Byrd DR, Compton CC, Fritz AG, Greene F, Trotti A, eds. AJCC 암 병기 핸드북. 7 판 뉴욕, 뉴욕 : 스프링거; 2010.
- 스미스 DD, 슈바르츠 RR, 슈바르츠 RE. 위암에 대한 위절제술 후 병기 결정 및 생존에 대한 총 림프절 수의 영향: 대규모 미국 인구 데이터베이스의 데이터. J Clin 온콜. 2005; 23(28):7114-7124. doi:10.1200/JCO.2005.14.621입니다.
Cite this article
Merrill AL, Mullen JT. 개원 위절제술. J 메드 인사이트. 2024; 2024(191). doi:10.24296/jomi/191입니다.


.jpg&w=3840&q=75&dpl=dpl_DRq22chi3FG6HemihCK8Jf6po1Fs)
.jpg&w=3840&q=75&dpl=dpl_DRq22chi3FG6HemihCK8Jf6po1Fs)