ओपन डिस्टल गैस्ट्रेक्टॉमी
Main Text
Table of Contents
एक पूर्ण मार्जिन-नकारात्मक (R0) लकीर गैस्ट्रिक एडेनोकार्सिनोमा के लिए एकमात्र संभावित उपचारात्मक उपचार है। ऑपरेशन का विकल्प ट्यूमर के स्थान के साथ-साथ बीमारी के चरण पर निर्भर करता है। इस रोगी को रोगसूचक एनीमिया के साथ प्रस्तुत किया गया, और वर्कअप ने गैस्ट्र्रिटिस और डिस्टल पेट में एक छोटे ट्यूमर का प्रदर्शन किया। बायोप्सी ने एडेनोकार्सिनोमा की पुष्टि की, और एक एंडोस्कोपिक अल्ट्रासाउंड (ईयूएस) ने इस ट्यूमर को टी 2 एन 0 के रूप में मंचित किया। स्टेजिंग स्कैन ने दूर के मेटास्टेटिक रोग का कोई सबूत नहीं दिखाया। यह देखते हुए कि इस रोगी के पास अपेक्षाकृत प्रारंभिक चरण का ट्यूमर था, हमने अग्रिम सर्जरी के साथ आगे बढ़ने के लिए चुना, जिसमें इस मामले में एक डिस्टल गैस्ट्रेक्टोमी शामिल थी। यह वीडियो एक "विस्तारित" डी 1 लिम्फ नोड विच्छेदन के साथ एक खुले डिस्टल गैस्ट्रेक्टोमी करने के लिए एक अनुभवी गैस्ट्रिक सर्जन की तकनीक दिखाता है।
यद्यपि पिछले कई दशकों के दौरान संयुक्त राज्य अमेरिका में गैस्ट्रिक कैंसर की घटनाओं में नाटकीय रूप से कमी आई है, गैस्ट्रिक कैंसर कैंसर से संबंधित मौत का एक महत्वपूर्ण कारण बना हुआ है। स्टेजिंग तौर-तरीकों, सर्जिकल थेरेपी और पेरीऑपरेटिव देखभाल में महत्वपूर्ण सुधार के बावजूद, गैस्ट्रिक कैंसर वाले अधिकांश रोगियों का पूर्वानुमान खराब रहता है। यह काफी हद तक इस कैंसर के आक्रामक जीव विज्ञान के साथ-साथ बीमारी के उन्नत चरण का परिणाम है, जिस पर अधिकांश रोगी चिकित्सक को पेश करते हैं। जोखिम कारकों में हेलिकोबैक्टर पाइलोरी और एपस्टीन-बार वायरस (ईबीवी) संक्रमण, घातक एनीमिया, पूर्व गैस्ट्रिक लकीर, धूम्रपान और उच्च नमक का सेवन शामिल है। लगभग 10% गैस्ट्रिक कैंसर विरासत में मिले कैंसर सिंड्रोम के कारण होते हैं, जिसमें वंशानुगत फैलाना गैस्ट्रिक कैंसर (एचडीजीसी) शामिल है, जो ई-कैडरिन (सीडीएच 1) जीन में जर्मलाइन म्यूटेशन की विशेषता है, और वंशानुगत नॉनपोलिपोसिस कोलोरेक्टल कैंसर (एचएनपीसीसी) सिंड्रोम, डीएनए बेमेल मरम्मत जीन में जर्मलाइन म्यूटेशन की विशेषता है। हाल ही में, गैस्ट्रिक कैंसर के एक व्यापक आणविक मूल्यांकन ने एक वर्गीकरण योजना का नेतृत्व किया है जो 4 प्रमुख जीनोमिक उपप्रकारों और उनकी अनुमानित आवृत्तियों को परिभाषित करता है: ईबीवी-संक्रमित ट्यूमर (9%), माइक्रोसेटेलाइट अस्थिर (एमएसआई-उच्च) ट्यूमर (22%), जीनोमिक रूप से स्थिर ट्यूमर (20%), और गुणसूत्र अस्थिर ट्यूमर (50%)। 1
पेट के कैंसर के निदान के विचारोत्तेजक कुछ, यदि कोई हो, क्लासिक लक्षण हैं, जो बताते हैं कि इस कैंसर का अक्सर उन्नत चरण में निदान क्यों किया जाता है। प्रारंभिक लक्षण, जैसे कि अधिजठर दर्द, अपच और एसिड भाटा, इतने निरर्थक हैं कि अधिकांश रोगियों को बिना किसी जांच के एंटासिड के साथ अनुभवजन्य रूप से इलाज किया जाता है। जैसे-जैसे बीमारी बढ़ती है, लक्षण अधिक प्रमुख और अधिक अशुभ हो जाते हैं और इसमें डिस्पैगिया, मतली, उल्टी, प्रारंभिक तृप्ति, एनोरेक्सिया, थकान और वजन घटाने जैसी शिकायतें शामिल होती हैं। गैस्ट्रिक कैंसर का स्थान और हिस्टोलॉजिक प्रकार अक्सर लक्षण जटिल को निर्धारित करता है, समीपस्थ ट्यूमर के लिए डिस्पैगिया से लेकर डिस्टल ट्यूमर को बाधित करने के लिए उल्टी से लेकर प्रारंभिक तृप्ति और फैलाना-प्रकार (लिनिटिस प्लास्टिक) ट्यूमर के लिए वजन घटाने तक। 2,3
यह रोगी गैस्ट्र्रिटिस के इतिहास और एक पुरानी गैस्ट्रोओसोफेगल जंक्शन सख्ती के साथ एक 84 वर्षीय सज्जन है जो थकान और सांस की तकलीफ के लक्षणों के साथ अपने प्राथमिक देखभाल चिकित्सक को प्रस्तुत करता है। एक पूर्ण रक्त गणना प्राप्त की गई और पता चला कि रोगी एनीमिक था। उन्होंने पेट दर्द, मतली, उल्टी, आंत्र की आदतों में बदलाव, खाने में कठिनाई या वजन घटाने से इनकार किया।
गैस्ट्रिक कैंसर वाले रोगी की शारीरिक परीक्षा आमतौर पर एपिगैस्ट्रिक पेट की कोमलता के अपवाद के साथ अचूक होती है और, कम संभावना है, एक स्पष्ट अधिजठर द्रव्यमान की। क्लासिक नामांकित भौतिक निष्कर्ष जैसे कि विरचो का नोड, सिस्टर मैरी जोसेफ का पेरिम्बिलिकल नोड, और ब्लूमर का शेल्फ शायद ही कभी मौजूद होते हैं, लेकिन जब देखा जाता है तो उन्नत मेटास्टेटिक बीमारी का संकेत मिलता है। इसी तरह, गैस्ट्रिक कैंसर रोगी में कैशेक्सिया, पीलिया, जलोदर और हेपेटोमेगाली की उपस्थिति आमतौर पर लाइलाज मेटास्टेटिक बीमारी का प्रतीक है। हमारा रोगी अच्छी तरह से दिखाई दे रहा था, और परीक्षा में उसके पास एक नरम पेट था और कोई स्पष्ट द्रव्यमान नहीं था।
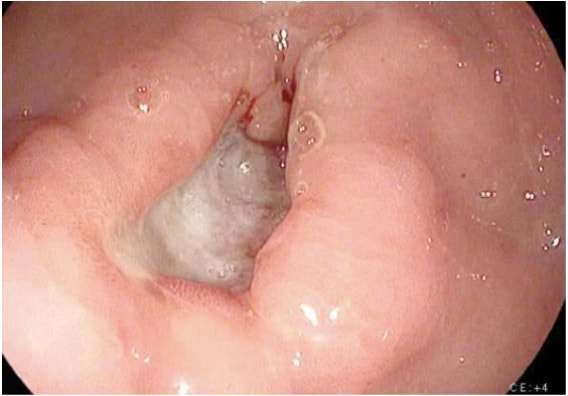
गैस्ट्रिक कैंसर के वर्कअप के लिए इमेजिंग में विभिन्न प्रकार के अध्ययन शामिल हैं। गैस्ट्रिक कैंसर का निदान आमतौर पर बायोप्सी (छवि 1) के साथ एंडोस्कोपी द्वारा आसानी से स्थापित किया जाता है। एंडोस्कोपी पेट के भीतर ट्यूमर के स्थान और सीमा को परिभाषित करता है और, जब एंडोस्कोपिक अल्ट्रासाउंड (ईयूएस) के साथ संयुक्त होता है, तो ट्यूमर आक्रमण (टी चरण) की गहराई का सटीक अनुमान लगाने की अनुमति देता है। ईयूएस गैस्ट्रिक कैंसर के टी चरण को स्थापित करने में सबसे संवेदनशील साधन है, और ईयूएस नोडल भागीदारी (एन चरण) की पुष्टि करने के लिए क्षेत्रीय लिम्फ नोड्स और संदिग्ध नोड्स की सुई बायोप्सी के आकलन को सक्षम बनाता है। छाती, पेट और श्रोणि का एक सीटी स्कैन दूर के मेटास्टेटिक प्रसार के मूल्यांकन के लिए किया जाना चाहिए, जैसे कि फेफड़े, यकृत, पेरिटोनियम, या लकीर के क्षेत्र के बाहर लिम्फ नोड्स। इसके अलावा, एक सीटी स्कैन जलोदर की थोड़ी मात्रा का पता लगाने में संवेदनशील है जो पेरिटोनियल ट्यूमर प्रसार का प्रतिनिधित्व कर सकता है और जिसे साइटोलॉजिकल परीक्षा के लिए छवि-निर्देशित साधनों द्वारा नमूना लिया जा सकता है। हालांकि गैस्ट्रिक कैंसर के प्रीऑपरेटिव स्टेजिंग में पीईटी और पीईटी-सीटी स्कैन नियमित रूप से अनुशंसित नहीं हैं, वे निश्चित रूप से अतिरिक्त उपयोगी जानकारी प्रदान कर सकते हैं। पीईटी प्राथमिक ट्यूमर का पता लगाने में एक कम संवेदनशीलता है, विशेष रूप से जल्दी और फैलाना प्रकार गैस्ट्रिक कैंसर में, लेकिन पीईटी सीटी की तुलना में एक उच्च विशिष्टता है ( ̃90% बनाम ̃60%) क्षेत्रीय लिम्फ नोड मेटास्टेस का पता लगाने में और एक उचित संवेदनशीलता है जिगर, फेफड़े, और दूर लिम्फ नोड मेटास्टेस का पता लगाने के लिए. 4 इसके अलावा, पीईटी का उपयोग नियोएडजुवेंट कीमोथेरेपी के लिए ट्यूमर प्रतिक्रिया की निगरानी के लिए किया जा सकता है, क्योंकि यह प्रारंभिक चरण में चिकित्सा के लिए उत्तरदाताओं का सटीक रूप से पता लगाता है, इस प्रकार चिकित्सक को रोगियों को यथासंभव सक्रिय कीमोथेरेपी आहार पर बनाए रखने में सक्षम बनाता है।
लोकोरीजनल रूप से उन्नत कैंसर (टी 3 + / एन +) वाले मरीजों को लैप्रोस्कोपी द्वारा अतिरिक्त स्टेजिंग के लिए माना जाता है। स्टेजिंग लैप्रोस्कोपी नियोजित लैपरोटॉमी से तुरंत पहले या प्रीऑपरेटिव थेरेपी पर विचार करने वाले रोगियों में किए गए प्रीट्रीटमेंट प्रक्रिया के रूप में किया जा सकता है। स्टेजिंग लैप्रोस्कोपी रेडियोग्राफिक रूप से मनोगत पेरिटोनियल और यकृत मेटास्टेस और सकारात्मक कोशिका विज्ञान की पहचान के माध्यम से 30% से अधिक रोगियों को ऊपर उठाता है। 5
गैस्ट्रिक कैंसर आमतौर पर लिम्फ नोड्स या हेमटोजेनस के माध्यम से फैलता है और आमतौर पर यकृत, फेफड़े या पेरिटोनियम को मेटास्टेसाइज करता है। यह सीधे आसन्न अंगों, जैसे अग्न्याशय और अनुप्रस्थ बृहदान्त्र को शामिल करने के लिए भी फैल सकता है। गैस्ट्रिक कैंसर के लिए एकमात्र संभावित उपचारात्मक चिकित्सा सर्जरी है। पूर्ण, मार्जिन-नकारात्मक लकीर और (नव) सहायक चिकित्सा के साथ भी, 5 साल की जीवित रहने की दर ~ 40% पर कम रहती है।
संयुक्त राज्य अमेरिका में गैस्ट्रिक कैंसर के लिए सबसे आम उपचार प्रतिमान ऐतिहासिक रूप से अग्रिम सर्जरी रहा है, इसके बाद उच्च जोखिम वाले (टी 3/4, नोड पॉजिटिव, खराब सामंजस्यपूर्ण प्रकार) ट्यूमर वाले रोगियों के लिए सहायक केमोरेडिएशन थेरेपी (जैसा कि इंटरग्रुप 0116 परीक्षण में वर्णित है)। 6 हालांकि, इस परीक्षण में केवल 64% रोगियों को योजना के अनुसार पोस्टऑपरेटिव केमोरेडियोथेरेपी प्राप्त हो सकती है, और ऐसे रोगियों के लिए कई पक्ष पेरिऑपरेटिव कीमोथेरेपी, जैसा कि ब्रिटिश मेडिकल रिसर्च काउंसिल द्वारा आयोजित मैजिक परीक्षण में वर्णित है। इस परीक्षण में, रोगियों को या तो पेरीऑपरेटिव कीमोथेरेपी (एपिरूबिसिन, सिस्प्लैटिन और 5-फ्लूरोरासिल (ईसीएफ) के तीन चक्र) प्रीऑपरेटिव और पोस्टऑपरेटिव रूप से) और अकेले सर्जरी या सर्जरी प्राप्त करने के लिए यादृच्छिक किया गया था। सर्जरी-अकेले समूह (36% बनाम 23%) की तुलना में पेरिऑपरेटिव कीमोथेरेपी समूह में पांच साल की जीवित रहने की दर बेहतर थी। हालांकि केवल ~ 40% रोगी इस उपचार दृष्टिकोण के साथ सभी अनुशंसित चिकित्सा को पूरा करते हैं, 85% से अधिक रोगियों को प्रीऑपरेटिव कीमोथेरेपी के सभी 3 नियोजित चक्र प्राप्त होते हैं, और सभी रोगियों को कीमोथेरेपी का कम से कम एक चक्र प्राप्त होता है। उच्च जोखिम वाले ट्यूमर वाले रोगियों के लिए सर्जरी से पहले प्रणालीगत चिकित्सा के कम से कम कुछ चक्रों का प्रशासन कई फायदे प्रदान करता है: (1) यह संभावित माइक्रोमेटास्टेटिक बीमारी के प्रारंभिक उपचार की अनुमति देता है; (2) कोई चिकित्सा के लिए विवो ट्यूमर प्रतिक्रिया की निगरानी कर सकता है, जैसे कि पीईटी-सीटी स्कैन इमेजिंग के साथ; और (3) कोई विशेष रूप से खराब ट्यूमर जीव विज्ञान वाले उन रोगियों के लिए चयन कर सकता है जो प्रारंभिक मेटास्टेटिक बीमारी विकसित करते हैं और जो इस प्रकार गैस्ट्रेक्टोमी से कोई जीवित लाभ प्राप्त नहीं करेंगे। 7
एक पूर्ण मार्जिन-नकारात्मक (R0) लकीर गैस्ट्रिक एडेनोकार्सिनोमा के लिए एकमात्र संभावित उपचारात्मक उपचार है। ऑपरेशन का विकल्प ट्यूमर के स्थान के साथ-साथ बीमारी के चरण पर निर्भर करता है। अनुकूल हिस्टोलॉजिक ग्रेड के सतही रूप से आक्रामक (टी 1 ए) गैस्ट्रिक कैंसर का इलाज एंडोस्कोपिक म्यूकोसल लकीर या वेज एक्सिशन द्वारा सहवर्ती प्रहरी लिम्फ नोड बायोप्सी के साथ या बिना किया जा सकता है। जापान के हमारे सर्जिकल सहयोगियों द्वारा इस तरह की प्रक्रियाओं का बड़े पैमाने पर वर्णन किया गया है, जहां गैस्ट्रिक कैंसर का अक्सर प्रारंभिक चरण में निदान किया जाता है, उस देश में स्क्रीनिंग एंडोस्कोपिक परीक्षाओं की व्यापकता को देखते हुए। क्योंकि संयुक्त राज्य अमेरिका में अधिकांश रोगी रोगसूचक, लोकोरेगनल रूप से उन्नत ट्यूमर के साथ मौजूद हैं, प्राथमिक सर्जिकल प्रश्न यह है कि कौन सी प्रक्रिया स्वीकार्य रुग्णता और मृत्यु दर के साथ इलाज के लिए सबसे बड़ा मौका प्रदान करती है। कई रोगी किसी भी शल्य चिकित्सा प्रक्रिया के लिए उम्मीदवार नहीं होते हैं क्योंकि या तो वे चिकित्सकीय रूप से अयोग्य होते हैं या प्रीऑपरेटिव इमेजिंग अध्ययन पर या लैप्रोस्कोपी के समय देखी गई मेटास्टेटिक बीमारी की उपस्थिति के कारण। उन रोगियों के लिए जो गैस्ट्रिक लकीर के लिए उम्मीदवार हैं, विकल्पों में कुल, समीपस्थ और डिस्टल गैस्ट्रेक्टोमी शामिल हैं। इन प्रक्रियाओं को लैप्रोस्कोपिक रूप से करने में दुनिया भर में अनुभव बढ़ रहा है, बेहतर अल्पकालिक परिणामों और नोडल पैदावार के साथ, और उत्तरजीविता परिणाम जो पारंपरिक खुली प्रक्रियाओं के बराबर हैं। हालांकि, संयुक्त राज्य अमेरिका में गैस्ट्रिक कैंसर के लिए अधिकांश लकीरें अभी भी खुले दृष्टिकोण के माध्यम से की जाती हैं।
जिन रोगियों को तत्काल सर्जिकल लकीर के लिए विचार किया जाना चाहिए, उनमें प्रारंभिक चरण (टी 1 / टी 2 एन 0) गैस्ट्रिक कैंसर वाले लोग शामिल हैं और जिन्हें रक्तस्राव या उच्च श्रेणी के ट्यूमर से जुड़े ल्यूमिनल रुकावट के तत्काल उपशामक की आवश्यकता होती है। हालांकि, रोगियों की इस बाद की आबादी में पेरिऑपरेटिव रुग्णता और मृत्यु दर महत्वपूर्ण हैं और लकीर के संभावित लाभों के खिलाफ सावधानीपूर्वक तौला जाना चाहिए। लोकोरेगनल रूप से उन्नत गैस्ट्रिक कैंसर वाले मरीज़ प्रीऑपरेटिव कीमोथेरेपी या कीमोरेडिएशन थेरेपी के लिए अच्छे उम्मीदवार हैं।
क्योंकि इस रोगी के पास अपेक्षाकृत प्रारंभिक चरण का ट्यूमर (uT2N0) था और वह अपनी उम्र के लिए उल्लेखनीय रूप से अच्छे स्वास्थ्य में था, इसलिए उसे डिस्टल गैस्ट्रेक्टोमी के साथ अग्रिम सर्जरी की पेशकश की गई थी। हमने महसूस किया कि एक ओपन डिस्टल गैस्ट्रेक्टोमी ने संभावित रूप से कम जोखिम वाले कैंसर के लिए नियोएडजुवेंट कीमोथेरेपी के साथ ओवरट्रीटमेंट के जोखिम को सीमित कर दिया है, जबकि हमें अंतिम पैथोलॉजी रिपोर्ट में अधिक उन्नत (जैसे, टी 3 + / एन +) कैंसर का पता चलने पर उसे सहायक चिकित्सा की पेशकश करने का विकल्प छोड़ दिया गया है।
गैस्ट्रिक लकीर की सीमा प्राथमिक ट्यूमर के स्थान और सीमा से निर्धारित होती है। संभावित, यादृच्छिक परीक्षण डिस्टल पेट के ट्यूमर वाले रोगियों के लिए डिस्टल गैस्ट्रेक्टोमी पर कुल गैस्ट्रेक्टोमी के लिए जीवित रहने का लाभ प्रदर्शित करने में विफल रहे। 8 इसलिए, उन रोगियों के लिए जिनमें ट्यूमर से 5- से 6 सेमी का मार्जिन प्राप्त किया जा सकता है, जबकि अभी भी एक उचित आकार के गैस्ट्रिक अवशेष को बनाए रखा जा सकता है, एक अधिक रूढ़िवादी गैस्ट्रिक लकीर का प्रदर्शन किया जाना चाहिए, क्योंकि यह कम रुग्णता के साथ एक समान जीवित रहने की दर प्रदान करता है और कुल गैस्ट्रेक्टोमी की तुलना में जीवन की बेहतर गुणवत्ता। 8 फिर भी, R0 लकीर प्राप्त करने के लिए यदि आवश्यक हो तो कुल गैस्ट्रेक्टोमी की जानी चाहिए, क्योंकि सकारात्मक लकीर मार्जिन (R1 लकीर) बहुत खराब अस्तित्व की ओर ले जाते हैं। डच गैस्ट्रिक कैंसर परीक्षण में, 10% रोगियों में एक सकारात्मक लकीर मार्जिन था और नकारात्मक लकीर मार्जिन वाले लोगों की तुलना में एक समान रूप से अवर 3 साल का अस्तित्व (18% बनाम 63%) था। 9 हालांकि, सूक्ष्म रूप से शामिल मार्जिन केवल पांच या उससे कम लिम्फ नोड मेटास्टेस वाले रोगियों में दीर्घकालिक अस्तित्व को प्रभावित करते हैं। समीपस्थ गैस्ट्रिक कैंसर के लिए, कई सर्जन बाद की प्रक्रिया के साथ रोगसूचक एसिड भाटा के दीर्घकालिक अनुक्रम के कारण एक समीपस्थ गैस्ट्रेक्टोमी पर कुल गैस्ट्रेक्टोमी पसंद करते हैं।
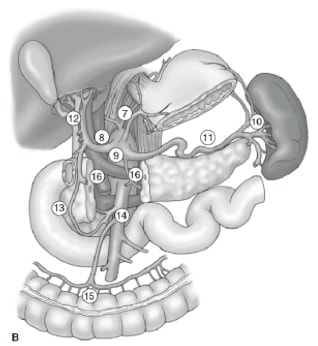
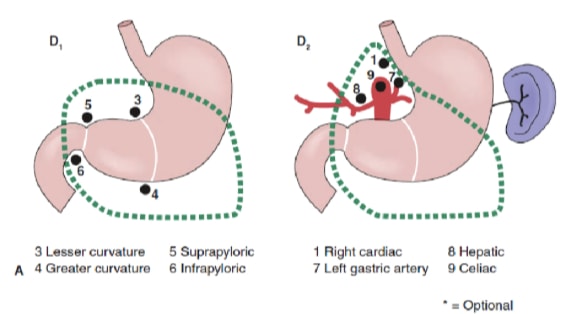
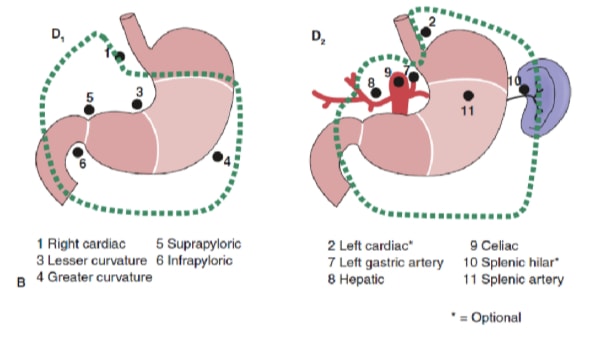
लिम्फ नोड विच्छेदन की सीमा गैस्ट्रिक कैंसर के प्रबंधन में सबसे विवादास्पद मुद्दों में से एक है। गैस्ट्रिक कैंसर रजिस्ट्री और अन्य पूर्वव्यापी अध्ययनों की रिपोर्ट ने जापान में इलाज योग्य गैस्ट्रिक कैंसर के उपचार के लिए विस्तारित (डी 2) लिम्फैडेनेक्टोमी के साथ कट्टरपंथी गैस्ट्रेक्टोमी को देखभाल का मानक बना दिया है। 10,11 गैस्ट्रिक कैंसर के लिए जापानी रिसर्च सोसाइटी पेट के निकासी लिम्फ नोड बेसिन को 16 स्टेशनों में वर्गीकृत करती है, जिसमें 6 पेरिगैस्ट्रिक स्टेशन(चित्रा 2ए)और प्रमुख जहाजों के साथ 10 क्षेत्रीय स्टेशन और अग्न्याशय(चित्रा 2बी)से सटे शामिल हैं। लिम्फ नोड विच्छेदन की सीमा पदनाम डी द्वारा इंगित की जाती है। एक डी 1 विच्छेदन में केवल पेरिगैस्ट्रिक नोड्स (स्टेशन 1 से 6) शामिल हैं; एक डी 2 विच्छेदन में सामान्य यकृत, बाएं गैस्ट्रिक, सीलिएक और प्लीहा धमनियों (स्टेशन 7 से 11) के साथ लिम्फ नोड्स शामिल हैं; और एक डी 3 विच्छेदन पोर्टा हेपेटिस के भीतर और महाधमनी (स्टेशनों 12 से 16) (चित्रा 3) के निकट अतिरिक्त नोड्स शामिल हैं।
पश्चिमी रोगियों में डी 2 विच्छेदन के साथ डी 1 विच्छेदन के परिणामों की तुलना करने वाले दो बड़े, संभावित यादृच्छिक परीक्षण आयोजित किए गए हैं। इन दो अध्ययनों में से बड़े के पंद्रह साल के अनुवर्ती, अर्थात्, डच गैस्ट्रिक कैंसर समूह परीक्षण, डी 2 लिम्फ नोड विच्छेदन (29% बनाम 21%, पी = .34) के साथ कोई दीर्घकालिक समग्र अस्तित्व लाभ का प्रदर्शन नहीं किया, लेकिन गैस्ट्रिक कैंसर से संबंधित मृत्यु दर (37% बनाम 48%, पी = .01) और डी 1 सर्जरी की तुलना में कम लोकोरेजनल पुनरावृत्ति दर दिखाई। 9 हालांकि, अधिक व्यापक डी 2 लिम्फैडेनेक्टोमी से गुजरने वाले उन रोगियों में पोस्टऑपरेटिव रुग्णता (43% बनाम 25%) और मृत्यु दर (10% बनाम 4%) की काफी अधिक दर थी, बड़े हिस्से में स्प्लेनेक्टोमी और अग्नाशय-उच्छेदन की अधिक संख्या के परिणामस्वरूप इस समूह में प्रदर्शन किया गया एक पूर्ण नोड विच्छेदन प्राप्त करने के लिए। 9 इसी तरह, मेडिकल रिसर्च काउंसिल द्वारा आयोजित ब्रिटिश सहकारी परीक्षण ने एक बढ़ी हुई रुग्णता की सूचना दी, जो सहवर्ती स्प्लेनेक्टोमी और अग्नाशय-उच्छेदन की उच्च दर से जुड़ी हुई है, उन रोगियों में समग्र या पुनरावृत्ति मुक्त अस्तित्व में लाभ के बिना जो डी 2 विच्छेदन के लिए यादृच्छिक हैं। 12
इन दो अध्ययनों के निष्कर्षों के बावजूद, जांचकर्ताओं ने तर्क दिया है कि यदि एक विस्तारित डी 2 लिम्फ नोड विच्छेदन के बाद जटिलता दर को कम किया जा सकता है, तो डी 2 विच्छेदन द्वारा प्रदत्त उत्तरजीविता लाभ, जैसा कि एशिया में अनुभवी केंद्रों द्वारा रिपोर्ट किया गया है, गैस्ट्रिक कैंसर वाले पश्चिमी रोगियों में अनुवाद किया जा सकता है। 13 इस प्रकार, इतालवी गैस्ट्रिक कैंसर अध्ययन समूह ने जापान में मास्टर सर्जनों के अवलोकन के माध्यम से तकनीक में कठोर प्रशिक्षण पूरा करने वाले सर्जनों द्वारा उच्च मात्रा वाले केंद्रों पर या तो अग्न्याशय-संरक्षण डी 2 लिम्फैडेनेक्टोमी या डी 1 लिम्फैडेनेक्टोमी के लिए रोगियों को यादृच्छिक बनाने के लिए एक चरण III परीक्षण आयोजित किया। उन्होंने डी 2 विच्छेदन से गुजरने वाले रोगियों में प्रभावशाली रूप से कम रुग्णता (17.9%) और मृत्यु दर (3.0%) की सूचना दी, जिसमें केवल प्रत्यक्ष ट्यूमर आक्रमण के लिए एक अग्नाशय-उच्छेदन या स्प्लेनेक्टोमी किया गया था। 14 हालांकि, उन्हें डी 1 और डी 2 समूहों के बीच 5 साल के समग्र अस्तित्व में कोई अंतर नहीं मिला (66.5% बनाम 64.2%; पी = 0.695), हालांकि उपसमूह विश्लेषणों ने सुझाव दिया कि डी 2 लिम्फैडेनेक्टोमी टी 2-टी 4 और / या नोड-पॉजिटिव ट्यूमर वाले रोगियों के लिए लाभ का हो सकता है। 14
यह स्पष्ट नहीं है कि क्या डी 2 लिम्फ नोड विच्छेदन केवल एक संपूर्ण मंचन प्रक्रिया है या क्या रोगियों के कुछ सबसेट (जैसे, एन 2 रोग वाले रोगियों) के लिए चिकित्सीय लाभ हो सकता है। यह ध्यान दिया जाना चाहिए कि गैस्ट्रिक कैंसर के रोगियों का सटीक मंचन, अमेरिकन ज्वाइंट कमेटी ऑन कैंसर (एजेसीसी) स्टेजिंग मैनुअल के सबसे हालिया सातवें संस्करण के अनुसार, कम से कम 15 लिम्फ नोड्स के मूल्यांकन की मांग करता है। 15 नोडल स्टेजिंग तब N1 (1 से 2 पॉजिटिव नोड्स), N2 (3 से 6 पॉजिटिव नोड्स), N3a (7 से 15 पॉजिटिव नोड्स), और N3b (16+ पॉजिटिव नोड्स) श्रेणियों के साथ सकारात्मक नोड्स की संख्या पर आधारित होती है। अध्ययनों ने बेहतर रोगी अस्तित्व और नमूने में जांच की गई लिम्फ नोड्स की बड़ी संख्या के बीच एक संबंध दिखाया है। 16 बेशक, यह प्रक्रिया से चिकित्सीय लाभ के विपरीत अधिक सटीक मंचन को प्रतिबिंबित कर सकता है। हालांकि, अप्रत्यक्ष सबूत हैं कि अधिक व्यापक लिम्फैडेनेक्टोमी के परिणामस्वरूप लोकोरेजनल पुनरावृत्ति की कम दर होती है, और यह एक जीवित लाभ में अनुवाद कर सकता है। दरअसल, ताइवान में एक एकल केंद्र में किए गए एक यादृच्छिक परीक्षण ने डी 3 विच्छेदन (59.5%) से गुजरने वाले रोगियों के लिए समग्र 5 साल के अस्तित्व के लाभ की पहचान की, जो डी 1 विच्छेदन (53.6%) से गुजर रहे थे। 13
पिछले एक दशक में एमजीएच में इलाज किए गए रोगियों के लिए, हमने क्रमशः 17% और 0% के गैस्ट्रेक्टोमी और डी 2 लिम्फैडेनेक्टोमी के बाद रुग्णता और मृत्यु दर की सूचना दी है, और नमूने के पूर्व विवो विच्छेदन के साथ हमारी औसत लिम्फ नोड उपज 40 नोड्स तक बढ़ गई है। संयुक्त राज्य अमेरिका में उप-योग और कुल गैस्ट्रेक्टोमी के लिए रहने की औसत लंबाई औसतन 9-10 दिन है, हालांकि कई रोगियों को 7 दिनों के भीतर छुट्टी दे दी जाती है। सबटोटल और कुल गैस्ट्रेक्टोमी की दीर्घकालिक जटिलताओं में विटामिन और खनिज की कमी शामिल है, विशेष रूप से विटामिन बी 12, विटामिन डी, लोहा और कैल्शियम, और क्लासिक पोस्टगैस्ट्रेक्टोमी सिंड्रोम, जैसे क्षारीय भाटा गैस्ट्रिटिस, डंपिंग सिंड्रोम, रॉक्स स्टैसिस सिंड्रोम, और अभिवाही अंग सिंड्रोम।
स्थानीयकृत गैस्ट्रिक कैंसर के लिए सर्जरी एकमात्र संभावित उपचारात्मक चिकित्सा है, फिर भी उन रोगियों के लिए भी जिनमें R0 लकीर संभव है, केवल 35% से 40% 5 साल का अस्तित्व या तो पेरीऑपरेटिव कीमोथेरेपी या पोस्टऑपरेटिव केमोरेडियोथेरेपी के साथ प्राप्त किया जाता है। गैस्ट्रिक कैंसर के उपचार में भविष्य की प्रगति बेहतर प्रणालीगत उपचारों के विकास के साथ-साथ पहले निदान के लिए तकनीकों पर निर्भर करती है।
A. डिस्टल पेट की लकीर:
गैस्ट्रिक एडेनोकार्सिनोमा, ट्यूबलर प्रकार, बेमेल मरम्मत प्रोटीन अभिव्यक्ति अस्थिर। (सिनॉप्टिक रिपोर्ट देखें)।
बी लिम्फ नोड बायोप्सी, स्टेशन 8:
चार लिम्फ नोड्स (0/4) में दुर्दमता का कोई सबूत नहीं है।
C. लिम्फ नोड बायोप्सी, स्टेशन 11:
दो लिम्फ नोड्स (0/2) में दुर्दमता का कोई सबूत नहीं है।
D. लिम्फ नोड बायोप्सी, स्टेशन 7:
दो लिम्फ नोड्स (0/2) में दुर्दमता का कोई सबूत नहीं है।
ई. लिम्फ नोड बायोप्सी, स्टेशन 3:
एक लिम्फ नोड (0/1) में दुर्दमता का कोई सबूत नहीं है।
सिनॉप्टिक रिपोर्ट:
ट्यूमर स्टेज सारांश: pT1bN0।
विशिष्ट साइट: गैस्ट्रिक एंट्रम।
ट्यूमर का आकार (सबसे बड़ा आयाम): 0.3 सेमी (स्लाइड पर मापा गया)।
डब्ल्यूएचओ वर्गीकरण: ट्यूबलर एडेनोकार्सिनोमा।
हिस्टोलॉजिक ग्रेड: जी 1 (अच्छी तरह से विभेदित)
आक्रमण की सीमा: pT1b (ट्यूमर सबम्यूकोसा पर हमला करता है)।
छोटा पोत (रक्त/लसीका) आक्रमण: अनुपस्थित।
बड़ा पोत (शिरापरक) आक्रमण: अनुपस्थित।
पेरिनुरल आक्रमण: अनुपस्थित।
समीपस्थ गैस्ट्रिक मार्जिन: आक्रामक कार्सिनोमा द्वारा असंबद्ध।
डिस्टल डुओडेनल मार्जिन: इनवेसिव कार्सिनोमा द्वारा असंबद्ध। (निकासी = 0.4 सेमी)।
क्षेत्रीय लिम्फ नोड्स: pN0 (कोई क्षेत्रीय लिम्फ नोड मेटास्टेसिस नहीं): 31 लिम्फ नोड्स की जांच की गई।
*लिम्फ नोड कुल सभी नमूना भागों में शामिल है। मुख्य नमूने (नमूना ए) में 22 लिम्फ नोड्स थे।
HER2 इम्यूनोहिस्टोकेमिस्ट्री: उसका 2 स्कोर 0/नकारात्मक (ट्यूमर कोशिकाओं के 10% < में कोई प्रतिक्रियाशीलता या बहुत बेहोश झिल्लीदार धुंधला नहीं है)।
अतिरिक्त अध्ययन:
MLH1 और PMS हार गए।
MSH2 और MSH6 बरकरार।
अतिरिक्त निष्कर्ष:
आंतों के मेटाप्लासिया और उच्च ग्रेड डिस्प्लेसिया के साथ गैस्ट्रिक एंट्रल म्यूकोसा।
फंडिक ग्रंथि पॉलीप।
एपस्टीन-बार वायरस एन्कोडेड आरएनए (ईबीईआर) नकारात्मक है।
हमारा मरीज सर्जरी से अच्छी तरह से ठीक हो गया और ऑपरेशन के बाद 5 वें दिन छुट्टी दे दी गई। उनकी अंतिम पैथोलॉजी रिपोर्ट ने उनके ट्यूमर को T1bN0 के रूप में मंचित किया, और लकीर के मार्जिन नकारात्मक थे। हमने एक उत्कृष्ट नोडल फसल (31 लिम्फ नोड्स) हासिल की, इसलिए हम इस चरण असाइनमेंट की सटीकता में आश्वस्त हो सकते हैं। जैसे, उसे सहायक चिकित्सा की आवश्यकता नहीं है, और उसका दीर्घकालिक पूर्वानुमान उत्कृष्ट है।
एक निश्चित पेट की दीवार प्रतिकर्षक प्रणाली इस ऑपरेशन के लिए बहुत सहायक हो सकती है; हमने बुकवाल्टर का उपयोग किया, लेकिन अन्य विकल्पों में थॉम्पसन और ओमनी रिट्रैक्टर सिस्टम शामिल हैं। ग्रहणी और पेट को स्टेपलर के साथ स्थानांतरित किया जाता है - इस मामले में एक एंडो-जीआईए स्टेपलर। एक पोत सील डिवाइस, जैसे कि लिगाश्योर डिवाइस या हार्मोनिक स्केलपेल, छोटे रक्त वाहिकाओं के कुशल नियंत्रण में काफी सहायक होते हैं। बाएं गैस्ट्रिक धमनी जैसे बड़े जहाजों को संवहनी स्टेपलर के साथ विभाजित किया जा सकता है या पारंपरिक सिवनी बंधाव द्वारा नियंत्रित किया जा सकता है।
लेखकों के पास खुलासा करने के लिए कोई संघर्ष नहीं है।
इस वीडियो लेख में संदर्भित रोगी ने फिल्माए जाने के लिए अपनी सूचित सहमति दी है और वह जानता है कि उसकी व्यक्तिगत स्वास्थ्य जानकारी अज्ञात फैशन में ऑनलाइन प्रकाशित की जाएगी।
References
- कैंसर जीनोम एटलस रिसर्च नेटवर्क। गैस्ट्रिक एडेनोकार्सिनोमा का व्यापक आणविक लक्षण वर्णन। प्रकृति। 2014; 513(7517):202-209. डीओआइ:10.1038/प्रकृति13480.
- मुलेन जेटी। गैस्ट्रिक कैंसर। इन: फिशर जे, एड। सर्जरी की महारत। 7 वां संस्करण। फिलाडेल्फिया, पीए: लिपिनकॉट विलियम्स और विल्किंस; 2017.
- यूं एसएस, पार्क डीजे। गैस्ट्रिक एडेनोकार्सिनोमा। में: कैमरून जेएल, कैमरून एएम, एड्स। वर्तमान सर्जिकल थेरेपी। 11 वां संस्करण। फिलाडेल्फिया, पीए: सॉन्डर्स, 2014: 87-95।
- यूं एम. 18 एफ-एफडीजी पीईटी/सीटी का उपयोग करके गैस्ट्रिक कैंसर चयापचय की इमेजिंग। 14(1):1-6. डीओआइ:10.5230/जेजीसी.2014.14.1.1.
- इकोमा एन, ब्लम एम, चियांग वाईजे, एट अल। गैस्ट्रिक कैंसर के रेडियोलॉजिकल रूप से मनोगत पेरिटोनियल कार्सिनोमैटोसिस के लिए लेप्रोस्कोपी और लैवेज साइटोलॉजी के मंचन की उपज। एन सर्जन Oncol. 2016; 23(13):4332-4337. डीओआइ:10.1245/एस10434-016-5409-7.
- मैकडोनाल्ड जेएस, स्माली एसआर, बेनेडेटी जे, एट अल। पेट या गैस्ट्रोओसोफेगल जंक्शन के एडेनोकार्सिनोमा के लिए अकेले सर्जरी की तुलना में सर्जरी के बाद केमोरेडियोथेरेपी। एन इंग्लैंड जे मेड। 2001; 345(10):725-730. डीओआइ:10.1056/एनईजेएमओए010187.
- कनिंघम डी, एलम डब्ल्यूएच, स्टेनिंग एसपी, एट अल। पेरीऑपरेटिव कीमोथेरेपी बनाम सर्जरी अकेले रिसेक्टेबल गैस्ट्रोओसोफेगल कैंसर के लिए। एन इंग्लैंड जे मेड। 2006; 355(1):11-20. डीओआइ:10.1056/एनईजेएमओए055531.
- Bozzetti एफ, Marubini ई, Bonfanti जी, Miceli आर, पियानो सी, Gennari एल ; इतालवी गैस्ट्रोइंटेस्टाइनल ट्यूमर अध्ययन समूह। गैस्ट्रिक कैंसर के लिए सबटोटल बनाम कुल गैस्ट्रेक्टोमी: एक बहुस्तरीय यादृच्छिक इतालवी परीक्षण में पांच साल की जीवित रहने की दर। एन सर्जरी। 1999; 230(2):170-178. डीओआइ:10.1097/00000658-199908000-00006.
- बोनेनकैंप जेजे, हरमन जे, सासाको एम, एट अल ; डच गैस्ट्रिक कैंसर समूह। गैस्ट्रिक कैंसर के लिए विस्तारित लिम्फ-नोड विच्छेदन। एन इंग्लैंड जे मेड। 1999; 340(12):908-914. डीओआइ:10.1056/NEJM199903253401202.
- Maruyama K, Okabayashi K, Kinoshita T. जापान में गैस्ट्रिक सर्जरी में प्रगति और कट्टरता की अपनी सीमाओं. वर्ल्ड जे सर्जरी। 1987; 11(4):418-425. डीओआइ:10.1007/BF01655804.
- सासाको एम, मैककुलोच पी, किनोशिता टी, मारुयामा के। गैस्ट्रिक कैंसर के लिए लिम्फ नोड विच्छेदन के चिकित्सीय मूल्य का मूल्यांकन करने के लिए नई विधि। बीआर जे सर्जरी. 1995; 82(3):346-351. डीओआइ:10.1002/बीजेएस.1800820321.
- कुस्चिएरी ए, वीडेन एस, फील्डिंग जे, एट अल ; सर्जिकल सहकारी समूह। गैस्ट्रिक कैंसर के लिए डी1 और डी2 लकीरों के बाद रोगी का अस्तित्व: एमआरसी यादृच्छिक सर्जिकल परीक्षण के दीर्घकालिक परिणाम। बीआर जे कैंसर। 1999; 79(9-10):1522-1530. डीओआइ:10.1038/एसजे.बीजेसी.6690243..
- वू सीडब्ल्यू, हसिउंग सीए, लो एसएस, एट अल। गैस्ट्रिक कैंसर वाले रोगियों के लिए नोडल विच्छेदन: एक यादृच्छिक नियंत्रण परीक्षण। लैंसेट ओन्कोल। 2006; 7(4):309-315. डीओआइ:10.1016/एस1470-2045(06)70623-4.
- डेगिउली एम, सासाको एम, पोंटी ए ; इतालवी गैस्ट्रिक कैंसर अध्ययन समूह। इतालवी गैस्ट्रिक कैंसर अध्ययन समूह में रुग्णता और मृत्यु दर गैस्ट्रिक कैंसर के लिए डी 1 बनाम डी 2 लकीर के यादृच्छिक नैदानिक परीक्षण। बीआर जे सर्जरी. 2010; 97(5):643-649. डीओआइ:10.1002/बीजेएस.6936.
- एज एसबी, बर्ड डीआर, कॉम्पटन सीसी, फ्रिट्ज एजी, ग्रीन एफ, ट्रॉटी ए, एड्स। एजेसीसी कैंसर स्टेजिंग हैंडबुक। 7वां संस्करण। न्यूयॉर्क, एनवाई: स्प्रिंगर; 2010.
- स्मिथ डीडी, श्वार्ज आरआर, श्वार्ज आरई। गैस्ट्रिक कैंसर के लिए गैस्ट्रेक्टोमी के बाद स्टेजिंग और अस्तित्व पर कुल लिम्फ नोड गिनती का प्रभाव: एक बड़े यूएस-जनसंख्या डेटाबेस से डेटा। जे क्लिन ओन्कोल। 2005; 23(28):7114-7124. डीओआइ:10.1200/जेसीओ.2005.14.621.
Cite this article
मेरिल अल, Mullen संयुक्त. ओपन डिस्टल gastrectomy. जे मेड अंतर्दृष्टि। 2024; 2024(191). डीओआइ:10.24296/जोमी/191.


.jpg&w=3840&q=75&dpl=dpl_8D2zDMD8DCtbijFTya2eJLHRA7sZ)
.jpg&w=3840&q=75&dpl=dpl_8D2zDMD8DCtbijFTya2eJLHRA7sZ)