胸部鏡手術による右下葉肺ウェッジ切除術の複合手術
Main Text
スクリーニングや診断検査におけるコンピュータ断層撮影(CT)の利用が増加するにつれて、肺結節を持つ患者が増加しています。この症例の患者は視力の変化、首の筋力低下、嚥下障害を訴えました。検査の結果、非胸腺性重症筋無力症と、画像的特徴、間隔成長、乳がんの既往に悪性腫瘍の疑いがある右下葉肺結節が偶然発見されました。診断および治療の目的で肺切除が必要でした。さらに、重症筋無力症の症状をコントロールするために胸腺切除術が推奨されました。その結果、合同アプローチが実施されました。
重症筋無力症(MG)は自己免疫疾患で、神経筋接合部の後シナプス膜の成分(アセチルコリン受容体または受容体関連タンパク質)に自己抗体が作用し、眼筋、球筋、四肢、呼吸筋の疲労性弱化を引き起こします。ほとんどの患者はアセチルコリン受容体または筋肉特異的チロシンキナーゼ受容体に対して検出可能な抗体を持っています。
MG患者は、日中や運動後に悪化する変動性の骨格筋の筋力低下を示します。眼瞼下垂および/または複視は患者の50%で初発症状です。患者のうち、構音障害、嚥下障害、疲労性咀嚼などの球茎症状を呈する患者は少なく、近位肢の筋力低下はまれです。呼吸筋の筋力低下が呼吸不全を引き起こす場合、これは「筋無力危機」と呼ばれ、生命を脅かす状況です。筋無力危機は、薬物療法、手術、炎症や感染症など多くの要因によって引き起こされます。
この女性は69歳で、重症筋無力症、高血圧、糖尿病、左乳がんの既往があり、乳房腫瘍切除術、補助放射線治療、ホルモン療法を受けており、右下葉のスパイキュー化した肺結節を訴えました。患者は発診の約1年前から筋無力症の症状が現れ始めました。彼女は複視、垂れ下がる頭、不安定な歩行、嚥下障害を抱えていました。
検査の結果、患者は眼球運動が弱いものの瞳孔機能は正常であることを示します。顔面の筋肉が関与しているため無表情に見えることがあり、後部の首筋が弱いため「頭が垂れ下がっている」ことがあります。この患者は両側の肺音が明確でした。彼女は疲労性の両側眼瞼下垂で、右眼瞼下垂が左眼より重くなっていました。彼女は外眼運動時に疲労性左眼遠視を患っていました。首の屈曲筋力が低下していました。神経学的検査の残りは特に異常はありませんでした。
MGの診断は自己抗体の血清学的検査や筋電図検査によって確認できます。エドロフォニウム塩化物(テンシロン)検査は感度が高いですが、偽陽性率が高いです。胸膜がないことを証明するために胸部CTまたはMRIを撮ってください。MG患者の約60〜70%が胸腺過形成を有し、10〜15%の患者には基礎的な胸腺腫があります。
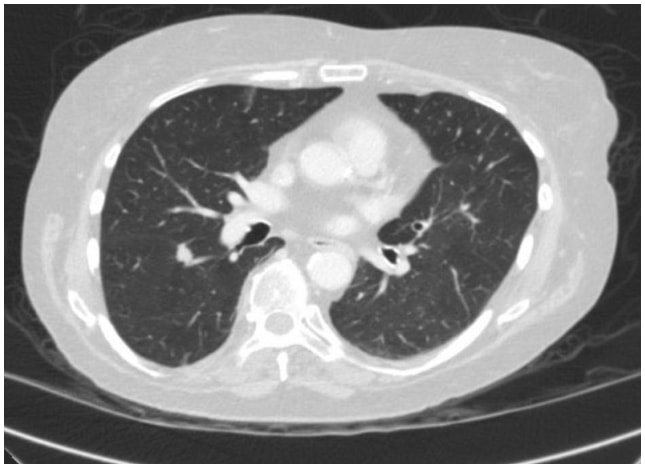
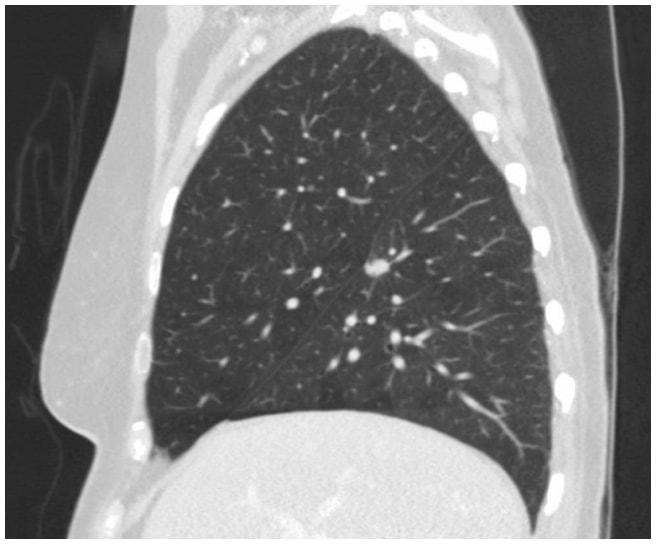
このケースでは、胸部CTにより右下葉上節の裂肛面に1.3cmの棘状病変が認められ、肺癌の可能性が非常に疑わしいものでした(図1)。その後、PET/CT検査を受け、FDGの悪性疑いが示されました。
MGの自然病程は、症状が出ない期間が徐々に短くなり、発症から2〜3年以内にピークを迎えるものです。その後、患者は通常、持続的で安定した病気を持ち、感染や薬物、その他の臨床的変化の場で悪化することがあります。第三段階では、約10〜20%の患者が自然寛解を迎えることがあります。
MGの医療的管理は、症状のコントロール(抗コリンエステラーゼ薬剤)と免疫調節(ステロイド、免疫抑制、血漿交換、静脈内免疫グロブリン投与)を含みます。非胸腺腫性MGの患者は、症状の改善や寛解の可能性を高めるために胸腺切除術の恩恵を受ける可能性があります。米国重症筋無力症財団(MGFA)によるMG重症度の分類によると、眼性MG(MGFA I型)のみの患者は胸腺切除術の恩恵を受けない一方、全身性MG(MGFA >II)患者は症状改善が見られる可能性があります。1 重要な注意点として、眼性MG患者の50〜70%が診断後2〜3年で全般性MGに進行するという点です。したがって、早期胸腺切除術はこの集団の一部を「救済」する可能性がある。
この患者は右下葉の肺結節があり、悪性腫瘍および非胸腺腫性重症筋無力症の疑いがありました。診断および治療のために肺切除が必要であり、重症筋無力症の症状をコントロールするために胸腺切除術も受けました。その結果、合同アプローチが実施されました。
経頸椎胸腺切除術は最も侵襲の少ない開放的アプローチです。しかし、胸膜組織の完全な切除は限られています。これは重要で、胸腺は解剖学的境界(無名静脈は上方、横隔神経は側方)を超えて伸びており、患者の約75%が前縦隔全体に異所性胸腺組織を持つことがあるからです。ビデオ支援胸腔鏡手術(VATS)やロボット胸腺切除術などの低侵襲技術は、切除の可視化と完全性の向上をもたらします。外科医の好みや腫瘍の側面の位置に応じて、左胸または右胸から行われます。
外科医は神経内科医と連携し、術後の筋無力症危機を防ぎ呼吸不全を防ぐために術前に最適な患者を調整すべきです。強制肺活量および最大呼吸能力(1分間の呼吸量に周波数を掛けたもの)を測定し、呼吸力低下を評価するべきです。MGの症状は、手術前にコリンエステラーゼ阻害剤、免疫抑制、血漿換出、または静脈内免疫グロブリン治療で十分にコントロールされなければなりません。
麻酔チームとの術前計画は非常に重要であり、神経筋遮断症は、MG患者がスクシニルコリンに耐性を持ち、非脱分極剤に対して非常にかつ予測不能な感受性を示すため、完全に回避されます。鎮静剤や麻酔薬は、麻酔解除時の呼吸抑制を最小限に抑えるため、短時間作用であるべきです。吸入麻酔と静脈内麻酔の組み合わせがよく用いられます。神経筋伝達を妨げることが知られている他の薬剤は避けるべきです。
胸腺切除術後のMG症状の改善や寛解は、胸腺摘出術から数年後に見られることがあります。
MGに対する長期免疫抑制療法の期待を踏まえ、特定の感染症や攻撃的な腫瘍疾患を除外するために単発性肺結節の診断が望ましい。
A. 右下葉の肺くさび形生検:
カルチノイド腫瘍、典型的だ。
くさび形切除のリンパ節の一つはカルチノイド腫瘍に関与しています。
注:腫瘍細胞は広まってシナプトフィシンとクロモグラニン陽性です。ERの染色は陰性です。Ki-67は腫瘍細胞の1%を染色します。細胞変性の微小な焦点が1分ずつ存在します。細胞学的非定型は最小限です。有糸分裂は特定されていません。
腫瘍島は腫瘍結節に隣接する一部の肺胞に存在します。腫瘍のリンパ管による転移は限定的ですが、切除縁には広がりません。切除の縁には腫瘍がありません。カルチノイド腫瘍の一部は高密度硬化性です。
組織学的特徴の一部は異常ですが、所見は非定型カルチノイド腫瘍の診断にはなりません。選ばれたスライドは会議でレビューされました。
B. ステーション12 メジャー・フィッシャー:
1つのリンパ節に悪性腫瘍の証拠はありません(0/1)。
C. ステーション12リンパ節生検:
1つのリンパ節に転移性カルチノイド腫瘍(1/1)。
D. ステーション7リンパ節生検:
2つのリンパ節に悪性腫瘍の証拠はありません(0/2)。
胸腺切除術:
脂肪代替品。胸腺組織は特定されていません。
MGに対する子宮頸切除術は、1939年にアルフレッド・ブラロックによって初めて記述されました。これは、胸腺腫を持つ若い女性の症例で、胸腺切除術後に筋無力症状が寛解したケースです。1941 年には、胸腺切除術を受けた非胸腺腫性MG患者でも症状改善が得られることをさらに示しました。3 MGに対する胸摘出術は、マウントサイナイおよびマサチューセッツ総合病院の1,355人の患者を対象とした縦断的研究の発表により確立された治療パラダイムとなりました。4 本研究は、40歳未満の中等度から重度の全般性非胸腺腫性MGを持つ女性が胸腺切除術を受けた場合、有意な(全寛解率38%、症状改善51%)および持続的な利益を示しました。4
唯一の対照ランダム化胸腺摘出試験は2016年に発表されました。これは多施設間の試験で、経胸腺切除術とプレドニゾン単独を比較しました。5,126名の患者は以下の基準で対象となりました:年齢18歳から65歳、非胸腺腫性MG、病<期間5年、MGFAクラスII〜IV、血清アセチルコリン受容体抗体の上昇。胸腺切除術群は、3年間の追跡調査で定量的重症筋無力スコアの改善が高く、免疫抑制の必要性が低いことが示されました。これらの効果がより長期間持続するかどうか、より侵襲の少ない手術法でも同様の効果が得られるか、そしてこれらの効果が長期の高用量ステロイド併用治療なしで得られるかどうかがまだ明らかになっています。
胸腺切除術の手術中罹患率と死亡率はそれぞれ20%と1%です。6.7 比較試験では、VATS胸腺切除術後に4%、経胸骨胸腺切除術後は16%であった。8 MG管理に関する最新の国際コンセンサスガイドラインでは、非胸腺腫性の全身性MG患者に対して、免疫抑制治療を回避または最小限に抑えるために選択的手術として9(1 )を行うことが推奨されています。(2) 胸腺腫性MGの全患者は完全な胸腺切除術を受け、不完全切除胸腺腫は補助化学療法および/または放射線治療で治療すべきです。(3) 胸膜切除術の非侵襲的アプローチ(胸部鏡的、ロボット手術)は、より積極的なアプローチと同様の結果をもたらすようですが、これはランダム化比較試験で示されていません。
この患者は術後出血があり、術後1日目に手術室に戻って検査を行いました。十分なモニタリング、アクセス、蘇生が確立された後、患者は二重内腔の気管内チューブで挿管され、左側デキュビタス姿勢に置かれました。右胸は以前の開胸切開から挿入されました。約1リットルの血腫を除去しました。内乳静脈の胸骨側で出血が確認されました。これは縫合結紮で管理されました。患者の術後の経過は特に異常なしでした。現在はステロイドの減薬中で、筋力が向上しています。最終病理では、典型的なカルチノイド腫瘍で陽性12リンパ節が認められました。胸腺標本は脂肪置換術で胸腺組織は特定されませんでした。
肛門切除術は、免疫抑制やステロイドの長期投与を回避できるため、最も魅力的なMG治療法です。免疫抑制薬の進歩や造血幹細胞移植などの技術の新たな応用が将来的にMG治療の一部となる可能性があります。10
典型的なカルチノイド腫瘍の治療は、完全切除とリンパ節の採取を含みます。裂肛のリンパ節に転移性カルチノイド腫瘍が見られました。併存症を考慮すると、外科的切除の範囲は十分です。より健康な患者にとっては、根治的リンパ節郭清術が選択肢だったかもしれません。コンピュータ断層撮影による観察は、患者にとって満足のいく管理方法です。
開示すべきことは何もありません。
この動画で言及されている患者は撮影に同意しており、情報や画像がオンラインで公開されることを認識しています。
References
- ヤレツキ・A・III、バロン・RJ、エルンストフ・RMら;米国重症筋無力症財団医療科学諮問委員会タスクフォース。重症筋無力症:臨床研究基準の推奨事項。 アン胸部外科。 2000;70(1):327-334. doi:10.1016/S0003-4975(00)01595-2。
- ブラロックA、メイソンMF、モーガンHJ、リヴェンSS. 重症筋無力症および胸腺領域腫瘍:腫瘍摘出症例の報告。 アン・サージ。 1939;110(4):544-561. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1391425/。
- ペンシルベニア州カーシュナー。アルフレッド・ブラロックと重症筋無力症の胸腺切除術。 アン胸部外科。 1987;43(3):348-349. doi:10.1016/S0003-4975(10)60635-2。
- Perlo VP、Poskanzer DC、Schwab RS、Viets HR、Osserman KE、Genkins G. 重症筋無力症:1,355人の患者における治療評価。 神経学です。 1966;16(5):431-439. doi:10.1212/WNL.16.5.431.
- ウルフGI、カミンスキーHJ、アバンIB他。重症筋無力症における胸腺摘出術のランダム化試験。 N Engl J Med. 2016;375(6):511-522. doi:10.1056/NEJMoa1602489。
- バッハマンK、ブルクハルトD、シュライターIら。重症筋無力症に対する開胸および胸部鏡下胸腺切除術後の長期予帰と生活の質:131人の患者の解析。 内視外科です。 2008;22(11):2470-2477. DOI:10.1007/S00464-008-9794-2。
- グロンセスGS、バローンRJ。実践パラメータ:自己免疫性重症筋無力症の胸腺切除術(エビデンスに基づくレビュー)。 神経学です。 2000;55(1):7-15. doi:10.1212/WNL.55.1.7.
- マイヤーDM、ハーバートMA、ソバニNCら。経胸骨および低侵襲的アプローチによる重症筋無力症の胸腺切除術の臨床転帰の比較。 アン胸部外科。 2009;87(2):385-391. DOI:10.1016/J.athoracsur.2008.11.040。
- サンダースDB、ウルフGI、ベナターM他。重症筋無力症管理に関する国際合意指針:エグゼクティブサマリー。 神経学です。 2016;87(4):419-425. doi:10.1212/WNL.00000000000002790.
- ブライアント・A、アトキンス・H、プリングル・CEら。重症筋無力症は自己造血幹細胞移植で治療されました。 JAMAニューロール。 2016;73(6):652-658. DOI:10.1001/JamaNeurol.2016.0113。
Cite this article
マダリアガML、ガイサートHA。胸膜切除術と右下葉肺ウェッジ切除術を胸部鏡手術で組み合わせて行いました。 J Med Insight。 2024;2024(181). doi:10.24296/jomi/181。