Biopsia cerebral de un presunto linfoma cerebeloso
Main Text
Table of Contents
En neurocirugía, la biopsia cerebral es una herramienta esencial para proporcionar un muestreo histológico adecuado en lesiones neoplásicas y no tumorales. Existen dos técnicas principales para obtener muestras de tejido: la biopsia abierta que requiere craneotomía o la biopsia con aguja. Las biopsias con aguja permiten un diagnóstico tisular mínimamente invasivo con menos riesgo de morbilidad operatoria para el paciente. Aquí mostramos una biopsia con aguja sin marco de una lesión cerebelosa utilizando el sistema VarioGuide de Brainlab.
La lesión a tratar se localiza adyacente al cuarto ventrículo en el parénquima cerebeloso. No es una lesión del tronco encefálico y no compromete los pedúnculos cerebelosos. Hay realce homogéneo del contraste en las imágenes de RM y algo de edema perifocal. No se detectaron signos de hemorragia ni isquemia.
El paciente no ha tenido enfermedades graves hasta el momento y no hay antecedentes de malignoma. Solo se observaron hipertensión arterial leve y polineuropatía leve. Las terapias inmunosupresoras anteriores que podrían aumentar el desarrollo del linfoma también estaban ausentes.
Esta mujer de 72 años desarrolló una ataxia severa de la marcha, que hasta ahora era desconocida para ella. No había otros signos cerebelosos como disartria o temblor intencionado.
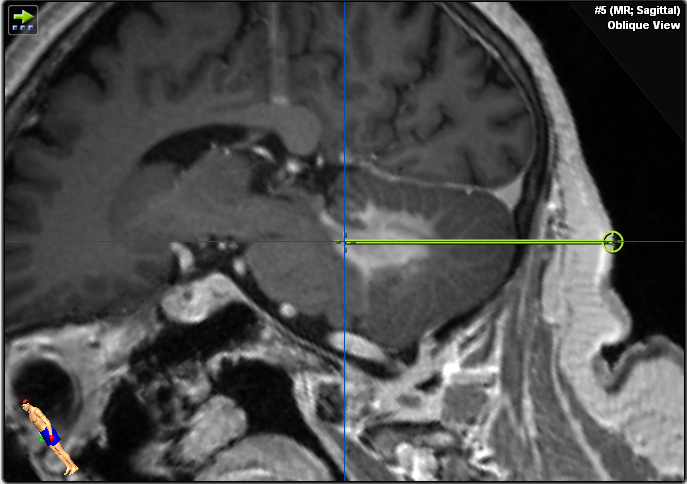
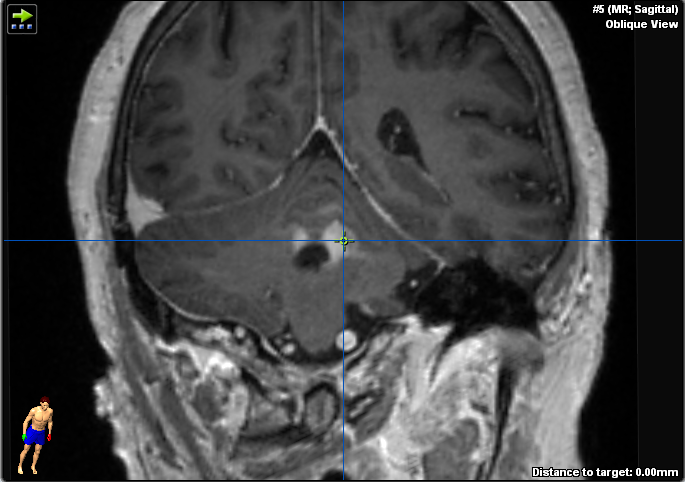
Se le realizó una resonancia magnética que mostró una lesión homogénea con contraste adyacente al cuarto ventrículo en el tejido cerebeloso y edema perifocal moderado (figuras 1-2). El tronco encefálico y los pedúnculos cerebelosos no estaban afectados. No se detectaron signos de hemorragia ni isquemia.
Debido al realce homogéneo del contraste, sospechamos de linfoma del SNC. Otros diagnósticos posibles incluyen isquemia, vasculitis, metástasis, glioma e inflamación.
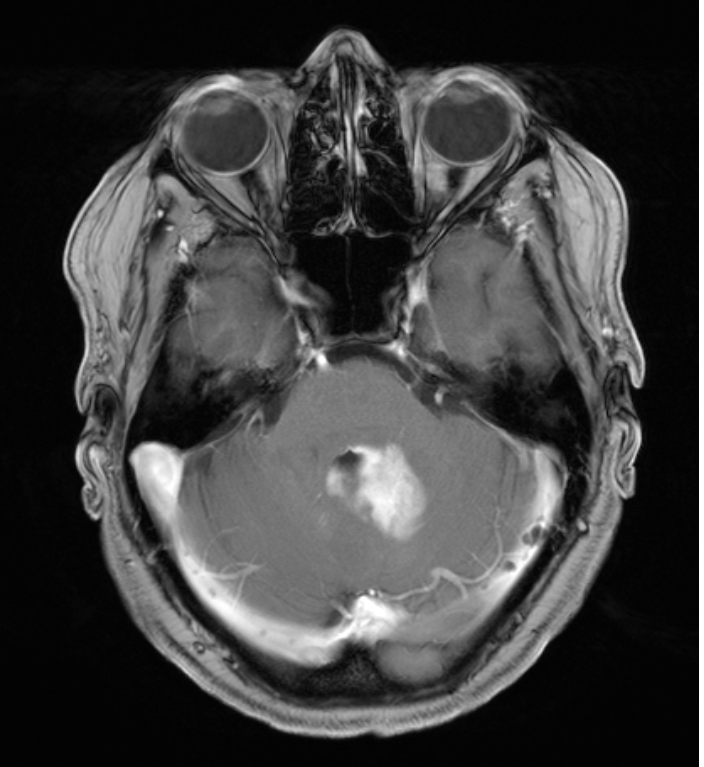
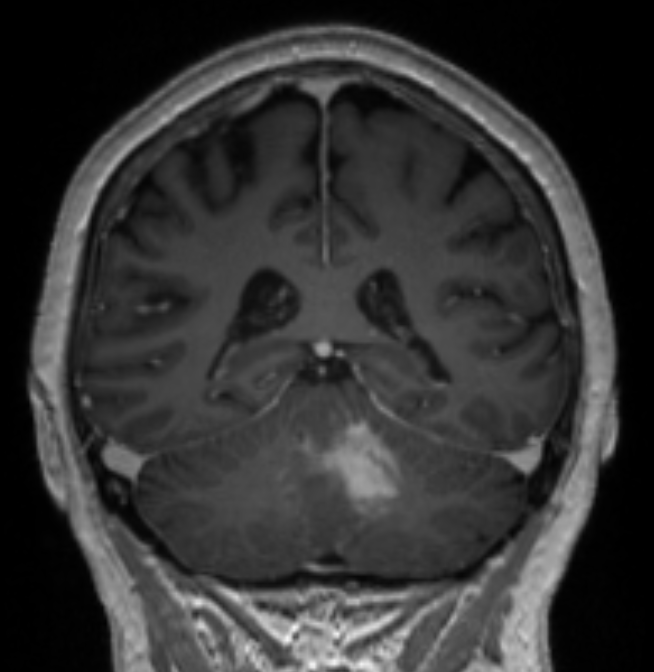
Figura 1. Estas imágenes ponderadas en T1 realzadas con gadolinio muestran una lesión infratentorial en el cerebelo y el pedúnculo cerebeloso izquierdo adyacente al cuarto ventrículo. Obsérvese el realce homogéneo del contraste sospechoso de linfoma del SNC y la falta de infiltración del tronco encefálico.
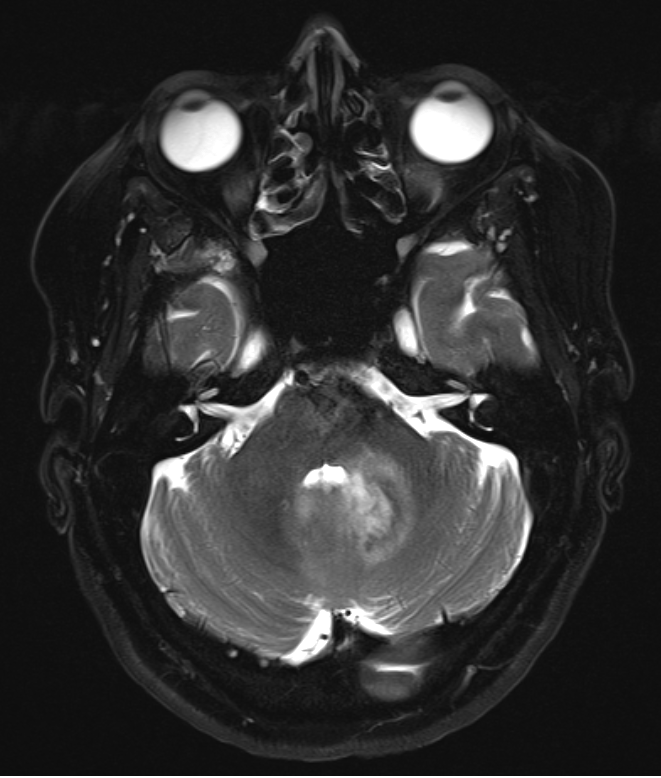 Figura 2. Esta vista axial muestra hiperintensidad periventricular T2, demostrando edema perifocal moderado. La luz del cuarto ventrículo todavía está abierta, lo que permite el paso del líquido cefalorraquídeo. Tenga en cuenta la ausencia de efecto de masa significativo o signos de hernia transtentorial.
Figura 2. Esta vista axial muestra hiperintensidad periventricular T2, demostrando edema perifocal moderado. La luz del cuarto ventrículo todavía está abierta, lo que permite el paso del líquido cefalorraquídeo. Tenga en cuenta la ausencia de efecto de masa significativo o signos de hernia transtentorial.Si no se trata, esta lesión provocaría hidrocefalia oclusiva, coma y muerte. Si progresara en tamaño, los síntomas cerebelosos aumentarían (p. ej., disartria, temblor intencional, ataxia) y es probable que los síntomas del tronco encefálico empeoren (déficits de nervios craneales, p. ej., dificultades para tragar, paresia, desregulación vegetativa, coma).
Las opciones de tratamiento en los casos de linfoma incluirían quimioterapia; En el caso de glioma o metástasis, la radioterapia puede administrarse en función del hallazgo histológico exacto. Ambos diagnósticos posibles requerirán tratamiento antineoplásico porque ambas entidades tumorales muestran una progresión rápida si no se tratan. El diagnóstico tisular es importante para demostrar la presencia de un tumor, proporcionar una caracterización molecular de la lesión y permitir terapias dirigidas. El diagnóstico de tejidos sería posible con la cirugía transcortical abierta, pero esto requeriría un tiempo de anestesia más prolongado y un mayor riesgo de fuga de líquido cefalorraquídeo y problemas de cicatrización de heridas en comparación con la aplicación de una biopsia con aguja. En los casos de linfoma, es importante que el paciente no tome corticosteroides antes de obtener muestras de tejido, ya que la cortisona puede impedir un diagnóstico adecuado de los tejidos.
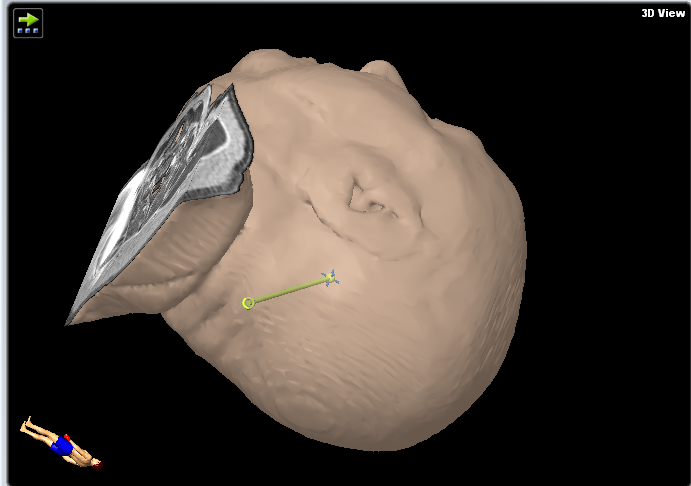
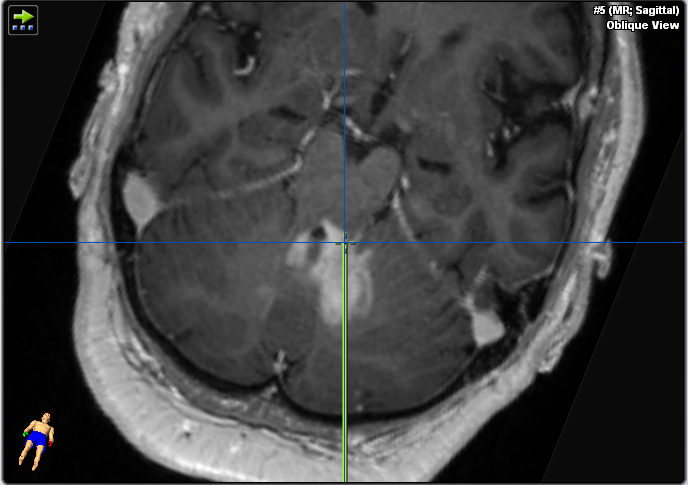
Decidimos realizar una biopsia cerebral en lugar de una cirugía transcortical abierta para detectar linfoma por las razones expuestas en la sección anterior (Figura 3). La precisión del sistema de neuronavegación es más precisa en posición supina en comparación con la posición prona debido a la mejora de la visibilidad de la cara y la superficie de convexidad para la cámara de navegación. Por lo tanto, optamos por la posición supina para permitir la máxima precisión espacial en este procedimiento. La biopsia estereotáctica sería más difícil técnicamente debido al procedimiento basado en el marco, que requeriría una posición semisentada y un mayor riesgo de embolia gaseosa. En las lesiones puramente del tronco encefálico, la biopsia estereotáctica basada en rongeur sería la técnica más favorable, ya que causaría menos trauma tisular (aguja de biopsia más pequeña, pero también menor volumen de muestra). El suelo del cuarto ventrículo debe evitarse en los procedimientos quirúrgicos debido a su papel fundamental en la función del tronco encefálico.
Figura 3. Estas imágenes muestran el plan de la trayectoria.
Solo unos pocos pacientes no se someten a la toma de muestras de tejido: se trata de pacientes de alto riesgo que tienen probabilidades de morir por el procedimiento quirúrgico o por complicaciones de la anestesia (p. ej., enfermedad coronaria grave, pacientes sépticos) o pacientes que no se someterán a quimioterapia debido a su estado clínico reducido.
Mostramos aquí un procedimiento que permite la toma de muestras histológicas mínimamente invasivas en una lesión de fosa posterior. Existe una clara ventaja de la biopsia con aguja sobre un procedimiento abierto debido a las menores complicaciones quirúrgicas, como la fuga de líquido cefalorraquídeo y los problemas de cicatrización de heridas. 9
Además, se puede obtener una biopsia con aguja con la misma precisión y tasa de diagnóstico histológico concluyente que una biopsia estereotáctica. 1,10
La precisión espacial del sistema de navegación es más precisa en posición supina porque la nariz, la glabela, las sienes y la frente son más fácilmente accesibles y pueden ser detectadas más fácilmente por la cámara del sistema de navegación. En posición prona, el registro del paciente puede llevar más tiempo, requerir más tiempo de anestesia y puede ser menos preciso. Especialmente en pacientes de edad avanzada o pacientes con riesgos anestésicos de moderados a altos, la biopsia VarioGuide permite un tiempo de operación más corto (Miltiadis 2017) y menos riesgo de procedimiento para el paciente. 9
La biopsia estereotáctica basada en el marco sería más exigente desde el punto de vista técnico porque el marco estereotáctico puede no permitir la trayectoria deseada. La estereotaxia basada en el marco también puede requerir una posición semisentada del paciente y albergar un mayor riesgo de embolia gaseosa venosa y sus complicaciones conocidas). 3,5,7,8 Sin embargo, el estudio realizado por Nakagawa et al. en 80 pacientes demuestra el uso seguro de la biopsia estereotáctica suboccipital en posición supina, con la cabeza girada e inclinada. 12 En las lesiones puramente intrínsecas del tronco encefálico anterior, una biopsia estereotáctica basada en rongeur sería la técnica más favorable, ya que resulta en menos trauma tisular debido a una aguja de biopsia más pequeña. Sin embargo, una biopsia estereotáctica basada en rongeur también da como resultado un menor volumen de muestra. Lesiones como la de este caso no pueden alcanzarse anatómicamente con este abordaje porque las biopsias estereotácticas basadas en rongeur requieren un punto de entrada supratentorial 4 cm lateral a la línea media a nivel de la sutura coronal. En consecuencia, se procedió a una biopsia con aguja. 1,7
Los puntos de referencia críticos que deben evitarse para las complicaciones hemorrágicas son el seno transverso, la arteria vertebral y la arteria cerebelosa inferior posterior. Por lo tanto, elegimos un punto de entrada muy por debajo del seno transverso y muy por encima de la arteria vertebral. La trayectoria de la biopsia debe evitar pasar el tronco encefálico (demasiado anterior) o el ventrículo y el plexo coroideo (muy vascularizado y con mayor riesgo de sangrado). La entrada al ventrículo también puede dar lugar a la obtención de solo líquido cefalorraquídeo porque no se puede aplicar ninguna "succión" al parénquima sobre la aguja de autocorte.
Las muestras de la zona fronteriza pueden demostrar posteriormente que la trayectoria es precisa y pueden permitir el diagnóstico de un tumor vital (p. ej., en el glioma de alto grado). 6 Las muestras del núcleo de la lesión pueden indicar necrosis o la necesidad de obtener más muestras del tumor vital. Una muestra tumoral vital es esencial para establecer el diagnóstico molecular y permitir la terapia dirigida. 11
Las muestras de biopsia se examinan bajo un microscopio de luz de fluorescencia para determinar si las muestras provienen del tejido patológico. Las muestras fluorescentes se asemejan a regiones de barrera hematoencefálica alterada y demuestran que la lesión fue realmente dirigida durante la biopsia. 2 Si ninguna de las lesiones es fluorescente, se podría agregar fácilmente otra trayectoria de biopsia en la misma operación. número arábigo
El muestreo histológico en este paciente descartó linfoma y demostró rombencefalitis no infecciosa. El tratamiento para esta enfermedad incluyó una terapia de refuerzo de cortisona en dosis altas que condujo al alivio de los síntomas y a la mejora de los hallazgos de la resonancia magnética. Sin embargo, el paciente desarrolló posteriormente una recaída de la enfermedad que resultó ser refractaria a otra terapia con cortisona. Por lo tanto, el tratamiento se cambió a plasmaféresis. 4
En este procedimiento se utilizaron el sistema de navegación de Brainlab, el sistema de biopsia VarioGuide y la aguja de biopsia de corte lateral. La planificación de la trayectoria preoperatoria se llevó a cabo con el software iPlan net de Brainlab.
No hay divulgaciones financieras para ninguno de los autores.
El paciente al que se refiere este artículo de vídeo ha dado su consentimiento informado para ser filmado y es consciente de que la información y las imágenes se publicarán en línea.
References
- Bradac O, Steklacova A, Nebrenska K, Vrana J, de Lacy P, Benes V. Precisión del sistema estereotáctico sin marco VarioGuide frente a la estereotaxia basada en marcos: estudio prospectivo, aleatorizado y unicéntrico. Neurocirugía Mundial. 2017;104:831-840. doi:10.1016/j.wneu.2017.04.104.
- Bowden SG, Neira JA, Gill BJA, et al. La fluoresceína sódica facilita la toma de muestras guiadas del tejido tumoral diagnóstico en gliomas sin realce. Neurocirugía. 2017. doi:10.1093/neuros/nyx271.
- Fàbregas N, Hurtado P, Gracia I, Craen R. Anestesia para la neurocirugía mínimamente invasiva. Rev. Colomb Anestesiol. 2015; 43(Supl. 1):15-21. doi:10.1016/j.rca.2015.07.004.
- Fukata M, Yokoi N, Fukata Y. Neurobiología de la encefalitis autoinmune. Curr Opin Neurobiol. 2017;48:1-8. doi:10.1016/j.conb.2017.07.012.
- Gracia I, Fábregas N. Craneotomía en posición sentada: manejo anestésico. Curr Opin Anestesiol. 2014; 27(5):474-483. doi:10.1097/ACO.00000000000000104.
- Louis DN, Perry A, Reifenberger G, et al. Clasificación de tumores del sistema nervioso central de la Organización Mundial de la Salud de 2016: un resumen. Acta Neuropathol. 2016; 131(6):803-820. doi:10.1007/s00401-016-1545-1.
- Georgiopoulos M, Ellul J, Chroni E, Constantoyannis C. Eficacia, seguridad y duración de una biopsia cerebral sin marco frente a una biopsia estereotáctica basada en marco: un estudio aleatorizado prospectivo. J Neurol Surg A Cent Eur Neurosurg. 2017. doi:10.1055/s-0037-1602697.
- Prabhakar H, Mahajan C, Kapoor I. Anestesia para la neurocirugía mínimamente invasiva. Curr Opin Anestesiol. 2017; 30(5):546-550. doi:10.1097/ACO.00000000000000499.
- Pulhorn H, Quigley DG, Bosma JJ, et al. Impacto de la biopsia cerebral en el tratamiento de pacientes con trastornos neurológicos no neoplásicos no diagnosticados. Neurocirugía. 2008; 62(4):833-837. doi:10.1227/01.neu.0000318168.97966.17.
- Ringel F, Ingerl D, Ott S, Meyer B. VarioGuide: un nuevo estudio de precisión y evaluación clínica del sistema estereotáctico guiado por imágenes sin marco. Neurocirugía. 2009; 64(5 Supl 2):365-371. doi:10.1227/01.NEU.0000341532.15867.1C.
- Weller M, van den Bent M, Tonn JC, et al. Guía de la Asociación Europea de Neurooncología (EANO) sobre el diagnóstico y el tratamiento de los gliomas astrocíticos y oligodendrogliales en adultos. Lanceta Oncol. 2017; 18(6):E315-E329. doi:10.1016/S1470-2045(17)30194-8.
- Nakagawa JM, Trippel M, Doostkam S, Mader I, Coenen VA, Reinacher PC. El abordaje suboccipitaltranscerebeloso estereotáctico de las lesiones del tronco encefálico y el cerebelo. 2018;166:10-15. doi:10.1016/j.clineuro.2018.01.015.
Cite this article
Misch M, Vajkoczy P, Czabanka M. Biopsia cerebral de un presunto linfoma cerebeloso. J Med Insight. 2024; 2024(139). doi:10.24296/jomi/139.