Riparazione dell'aneurisma aortico toracoaddominale
Main Text
Table of Contents
Gli aneurismi toracoaddominali dell'aorta (TAAA) sono generalmente asintomatici e vengono scoperti incidentalmente durante immagini toraciche o addominali. Quando vengono identificati, la gestione è spesso prevedibile, a seconda della dimensione dell'aneurisma e del suo tasso di crescita. L'intervento chirurgico è indicato per aneurismi di grande entità e per quelli che si espandono rapidamente, al fine di evitare la rottura catastrofica dell'aneurisma. Qui presentiamo il caso di una donna di 70 anni con una TAAA, che avevamo seguito con scansioni di angiografia computerizzata seriali. La decisione di operare fu presa quando l'aneurisma iniziò a mostrare una crescita del diametro. La sua anatomia non era favorevole al trattamento endovascolare; Pertanto, abbiamo riparato il suo aneurisma utilizzando un approccio tradizionale aperto.
Malattie cardiovascolari; malattie vascolari; aneurisma; aneurisma aortico; toracoaddominale.
Gli aneurismi aortici sono dilatazioni focali dell'aorta che possono verificarsi in qualsiasi punto lungo la sua lunghezza dalla radice, appena sopra la valvola aortica, fino alla biforcazione nel bacino. La classificazione avviene per localizzazione anatomica e suddivisa in aneurismi toracici, addominali o toracoaddominali. Gli aneurismi toracici si suddividono ulteriormente in quelli che coinvolgono la radice e l'aorta ascendente, quelli che coinvolgono l'arco aortico e quelli che coinvolgono l'aorta toracica discendente. Gli aneurismi toracoaddominali dell'aorta (TAAA) sono classificati secondo la classificazione di Crawford: l'estensione I comprende la maggior parte dell'aorta toracica discendente, che si estende dall'arteria succlavia sinistra all'aorta addominale suprarenale. L'estensione II è la più estesa, coinvolgendo l'aorta dall'arteria succlavia sinistra fino alla biforcazione aortoiliaca. L'estensione III include l'aorta toracica distale ed estende fino alla biforcazione aortoiliaca. L'estensione IV è confinata all'aorta addominale sotto il diaframma. Il gruppo di Safi ha introdotto l'Extent V, che coinvolge l'aorta toracica distale, includendo le origini delle arterie celiaca e mesenterica superiore ma escludendo le arterie renali (Figura 1). 57
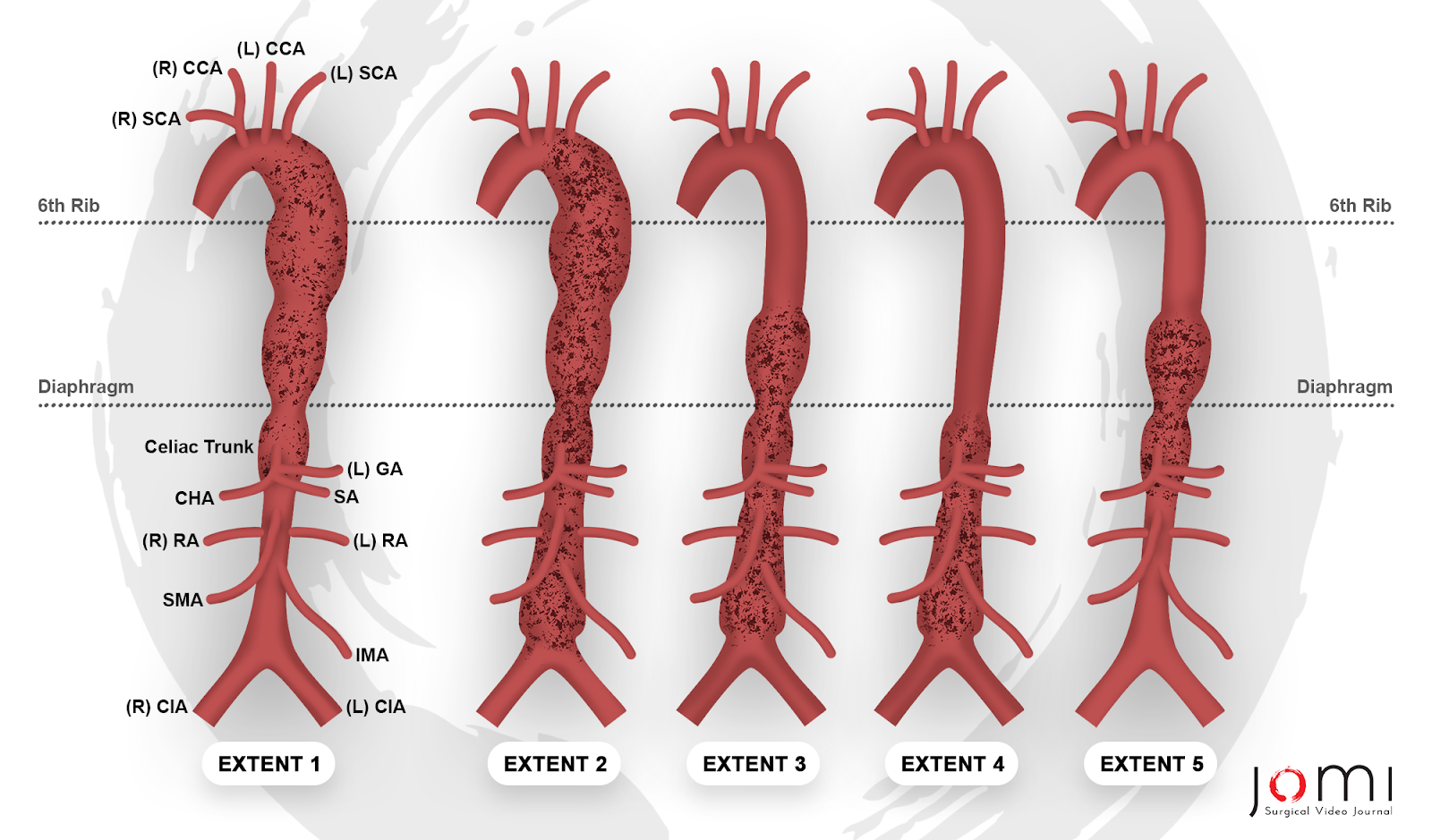
Figura 1. Classificazione Crawford dell'aneurisma toracoaddominale dell'aorta, modificata dal gruppo di Safi. Leggenda: (R) SCA - Arteria Subclavia Destra, (R) CCA - Arteria Carotidea Comune Destra, (L) CCA - Arteria Carotidea Comune Sinistra, (L) SCA - Arteria Subclavia Sinistra, (L) GA - Arteria Gastrica Sinistra, CHA - Arteria Epatica Comune, SA - Arteria Splenica, (R) RA - Arteria Renale Destra (L) AR - Arteria Renale Sinistra, SMA - Arteria Mesentica Superiore, IMA - Arteria Mesenterica Inferiore, (R) CIA - Arteria Iliaca Comune Destra, (A sinistra) CIA - Arteria iliaca comune sinistra.
L'eziologia della dilatazione è tipicamente multifattoriale ed è il risultato sia di fattori ereditari che ambientali, il cui percorso comune finale porta al degrado delle fibre di collagene ed elastina e/o all'inibizione della loro corretta sintesi. Queste due proteine della matrice extracellulare della parete aortica sono principalmente responsabili della sua resistenza alla trazione e dell'elasticità. 1 Oltre a collagene ed elastina, altri componenti della matrice extracellulare della parete aortica (come i glicosaminoglicani) risultano diminuiti nei pazienti con aneurismi aortici, cosa che si propone sia dovuta a un'attività della metalloproteinasi della matrice aberrante. 2 Altri fattori come l'angiotensina II, i mineralocorticoidi, le specie reattive dell'ossigeno e le cellule classicamente presenti nella risposta infiammatoria sistemica sono stati anch'essi implicati nella formazione degli aneurismi aortici. 3,4,5 Le cause secondarie della formazione degli aneurismi sono traumi e infezioni, queste ultime classificate come aneurismi micotici. Infine, mutazioni genetiche ereditarie e spontanee che codificano per i componenti del pozzo aortico sopra menzionati possono portare alla formazione di aneurisma in associazione a sindromi specifiche come Ehlers-Danlos tipo IV e sindrome di Marfan. 6
I fattori di rischio tradizionalmente associati alla patogenesi della degenerazione aneurismatica aortica includono il sesso maschile, la storia familiare e il fumo di sigaretta. Le differenze di genere nella prevalenza degli aneurismi aortici sono significative, con un rapporto maschile-femmine di 5:1 tra i pazienti colpiti, anche se non è ancora stato chiarito un singolo meccanismo unificante per queste differenze di sesso. 7,8 La patogenesi esatta del fumo di sigaretta nella formazione degli aneurisma è complessa dato il numero eterogeneo di costituenti del fumo di tabacco, anche se l'associazione con l'aumento dell'espressione di metalloproteinasi nella matrice è ben supportata dalla letteratura. 9,10
La riparazione dell'aneurisma aortico viene effettuata per evitare la rottura, che nella maggior parte dei casi è fatale se non trattata con urgenza o urgenza. 11
Come già detto, gli aneurismi aortici sono comunemente insidiosi per natura e si presentano in modo asintomaticamente, con la diagnosi spesso fatta incidentalmente tramite tomografia computerizzata (TC) per un'altra indicazione. Gli aneurismi che sono cresciuti possono causare dolore alla schiena o al petto, o sintomi secondari alla compressione delle strutture circostanti. Alcuni pazienti possono anche sottolineare la sensazione di una "massa pulsante", a livello dell'aneurisma. Gli stimmi embolici causati da trombo murale che si separano dalla parete dell'aneurisma possono manifestarsi come infarti all'interno degli organi addominali o lesioni purpuriche agli arti inferiori, la cosiddetta sindrome del "dito trash-toe" o "blue-toe". Come discusso, i pazienti con aneurisma possono presentare elementi della loro storia che aumentano il rischio di sviluppare aneurisma, come la storia del fumo, la storia di ipertensione non controllata o la storia di malattia cardiovascolare aterosclerotica. Se ci sono complicazioni secondarie dell'aneurisma, come un'infezione, il paziente può presentarsi con febbre soggettiva e altri sintomi sistemici.
Sono rilevanti due scenari distinti di esame fisico: la rilevazione incidentale di un aneurisma non rotto e l'esame al momento della rottura imminente o attiva. Il primo può presentarsi come una massa particolarmente prominente e pulsabile nella regione addominale sopra e leggermente a sinistra dell'ombelico. L'habitus corporeo del paziente e la dimensione dell'aneurisma influenzeranno notevolmente la capacità di apprezzare questo risultato. A volte si possono osservare stimmi embolici negli arti inferiori, soprattutto se i pulsi degli arti inferiori sono palpabili attraverso il livello del pedale. Nei casi di aneurismi micotici o infiammatori, possono essere presenti sintomi costituzionali associati come febbri e rigori.
A differenza dei loro corrispettivi asintomatici, la rottura o la rottura imminente si manifestano più comunemente con dolore in qualsiasi punto lungo la distribuzione dell'aneurisma. La rottura contenuta può causare compressione di organi o strutture adiacenti come l'uretere, causando idronefrosi. La fistulizzazione in strutture luminali come l'intestino provoca sanguinamento gastrointestinale, mentre la rottura delle strutture circostanti come la vena cava può causare l'insorgenza acuta di insufficienza cardiaca e un classico brusco rumoroso di macchinari nell'addome. La rottura contenuta nel retroperitoneo può manifestarsi esternamente come segni di Grey Turner (eccimosi sul fianco) o Cullen (eccimosi peri-ombelicale).
La maggior parte degli aneurismi viene scoperta incidentalmente durante altri studi; tuttavia, in coloro che non hanno mai effettuato tali esami di immagini, il Gruppo di Lavoro per i Servizi Preventivi degli Stati Uniti (USPSTF) raccomanda un'ecografia addominale una tantum in uomini tra i 65 e i 75 anni con precedenti di fumo per lo screening dell'aneurisma dell'aorta addominale (AAA) (raccomandazione B). Queste raccomandazioni non sono le stesse per donne della stessa fascia d'età e della stessa storia di uso di sostanze (affermazione I). 12
I pazienti identificati con aneurismi aortici vengono seguiti in base alla dimensione della dilatazione. Secondo le raccomandazioni dell'American Academy of Family Physicians, i pazienti con AAA di diametro da 3,0 a 3,9 cm dovrebbero essere monitorati tramite ecografia dell'addome ogni due o tre anni (raccomandazione C). I pazienti con AAA di diametro da 4,0 a 5,4 cm devono essere seguiti tramite ecografia o TAC ogni sei-dodici mesi (raccomandazione C).13, 14 I pazienti con diametri aortici superiori a 5,5 cm vengono indirizzati per una riparazione chirurgica elettiva. Negli aneurismi dell'aorta toracica (TAA), la sorveglianza consiste tipicamente in ripetizione dell'imaging assiale sei mesi dopo la diagnosi e la diagnosi iniziale per valutare la crescita o la stabilità. La gestione e le modalità specifiche di imaging per la sorveglianza continua delle TAA dipendono dall'estensione, dalla dimensione e dal tasso di crescita. Anche l'ecocardiografia e l'imaging a risonanza magnetica possono essere opzioni. 15 Lo screening per l'ATA è appropriato nei pazienti con una forte storia familiare. 16,17
Grazie alle raccomandazioni di screening dell'USPSTF, della Society for Vascular Surgery e dell'American College of Radiology, gli aneurismi dell'aorta addominale possono essere rilevati e adeguatamente seguiti dove altrimenti avrebbero potuto continuare a crescere. Ciò consente una mitigazione pianificata a seconda dell'entità della dimensione o del tasso di crescita dell'aneurisma, tramite la gestione dei fattori di rischio o la consulenza chirurgica.
I pazienti che non rientrano nelle categorie di rischio per lo screening possono comunque sviluppare aneurismi aortici e potrebbero non averli mai visualizzati, dove possono essere asintomatici fino al punto di rompersi. Alcuni studi hanno suggerito che si stima che il 70–80% dei pazienti portati al pronto soccorso per aneurismi aortici rotti non avesse una storia o conoscenza conosciuta di un aneurisma aortico diagnosticato. 18,19
Gli aneurismi aortici asintomatici che non soddisfano i criteri appropriati di diametro/espansione per la riparazione vengono gestiti tramite la riduzione dei fattori di rischio cardiovascolare. Questo si ottiene tramite terapia antiipertensiva e statinica, oltre che attraverso la cessazione del fumo. Altre terapie farmacologiche come la doxiciclina sono in fase di studio per le loro proprietà anti-MMP, ma al momento non ci sono dati che suggeriscano benefici sostanziali per la mitigazione del rischio di aneurisma al di fuori di quelli già menzionati. 20, 21, 22
Gli aneurismi aortici in cui il rischio di rottura supera quello di un intervento chirurgico vengono inviati a una consulenza chirurgica per riparare l'aneurisma. Sebbene considerata profilassi, la riparazione di un aneurisma aortico ad alto rischio ha un tasso di sopravvivenza significativamente migliore a 5 anni rispetto alla riparazione di un aneurisma aortico rotto. 23 opzioni chirurgiche per la riparazione degli aneurismi includono aperto, endovascolare o un ibrido dei due. La scelta tra le modalità procedurali dipende dalle specifiche del caso del paziente, come la posizione lungo l'aorta o altre considerazioni anatomiche, oltre che dall'estensione dell'aneurisma. Altre considerazioni più sfumate, come l'eziologia esatta dell'aneurisma (degenerativo vs. parte di una sindrome genetica), influenzano la decisione, poiché pazienti che altrimenti sarebbero buoni candidati per la terapia endovascolare vengono invece trattati chirurgicamente se si ritiene che l'eziologia dell'aneurisma sia di natura genetica.
Naturalmente, vengono prese in considerazione anche le comorbidità mediche del paziente che potrebbero influenzare la sua candidatura chirurgica.
La riparazione endovascolare consiste nel posizionare un tubo di tessuto collassato intrecciato su uno stent, un innesto di stent, nell'aorta da una o entrambe le arterie femori. L'innesto dello stent viene posizionato attraverso l'aneurisma tramite fluoroscopia e poi dispiegato in modo che possa espandersi e colmare dall'aorta normale prossimalmente all'aorta normale o alle arterie iliache distalmente. L'aneurisma viene effettivamente "sigillato" dalla pressione sanguigna sistemica e il flusso viene mantenuto attraverso l'aorta. Gli aneurismi che coinvolgono l'aorta toracoaddominale, tuttavia, sono molto più complessi perché i principali vasi sanguigni che alimentano gli organi addominali nascono dall'aneurisma stesso. Tradizionalmente, il dispiegamento degli innesti dello stent attraverso l'area avrebbe causato un disturbo del flusso sanguigno verso questi organi. Sebbene esistano tecniche endovascolari avanzate e molto eleganti per affrontare e mantenere il flusso sanguigno verso questi vasi sigillando contemporaneamente l'aneurisma, i dettagli sono al di fuori dell'ambito di questo capitolo. Piuttosto, qui l'attenzione è rivolta alla riparazione chirurgica aperta della TAAA. L'operazione prevede l'esposizione dell'aorta accedendo sia al torace che all'addome, mobilitando gli organi e i tessuti adiacenti dall'aorta, controllando l'aorta sopra e sotto l'aneurisma, controllando tutti i vasi ramificati derivanti dall'aneurisma, arrestando il flusso sanguigno attraverso il segmento aneurismatico e sostituendo tutta l'aorta aneurismatica con un innesto di tessuto e ripristinando il flusso verso le arterie ramificate. Addetti come il bypass atrio-femorale sono utilizzati per aiutare a minimizzare e mitigare gli effetti dell'ischemia degli organi durante la riparazione.
La terapia endovascolare è stata dimostrata in studi osservazionali e prospettici di conferire un beneficio sulla mortalità perioperatoria, anche se la superiorità della terapia endovascolare rispetto alla terapia chirurgica rimane controversa quando si considera la mortalità a breve termine, specialmente per quanto riguarda la riparazione dell'aorta toracica. 24-31 Le conclusioni degli studi DREAM, EVAR-1, OVER e ACE, che valutano la gestione dell'AAA infrarenale, sembrano corroborare con studi precedenti che identificano un beneficio sulla mortalità a breve termine rispetto alla chirurgia aperta, anche se questi studi non mostrano differenze significative negli esiti a lungo termine fino a 10 anni. 32-42 Questi dati hanno aiutato i fornitori a identificare il percorso procedurale più appropriato per i pazienti che rientrano in queste categorie. I pazienti anziani a rischio perioperatorio sono candidati più appropriati per la terapia endovascolare, anche se il rischio per pazienti più giovani, altrimenti sani e con un rischio perioperatorio più basso è meno chiaro e richiede ulteriori indagini. 43-47
Il paziente in questo caso è stato diagnosticato con TAAA di tipo I, cioè coinvolgimento aortico esteso dall'aorta discendente all'aorta addominale suprarenale. Nel caso specifico di questo paziente, il loro aneurisma inizia poco oltre l'origine dell'arteria succlavia sinistra e si estende attraverso l'aorta toracica che termina nel segmento viscerale. Il piano per l'intervento chirurgico prevede l'esposizione dell'aorta toracica, addominale e infrarenale prossimale, il controllo dei vasi viscerali, la collocazione del paziente in bypass atriale femorale sinistro, la collocazione dell'innesto e la chiusura addominale.
Il paziente viene posizionato in una posizione di decubito laterale destro (come è consuetudine nella riparazione TAAA di tipo I–III) per consentire un facile accesso sia al torace che all'addome. Durante tutta la procedura vengono inoltre inseriti drenaggi spinali e cavi motori evocati per la valutazione del midollo spinale. L'incisione primaria viene effettuata lungo la base del collo tra la colonna vertebrale e la scapola ad angolo obliquo, passando sotto la punta della scapola e parallela alle costole, terminando in uno spazio tra l'ombelico del paziente e la simfisi pubica.
Durante l'incisione primaria viene prestata molta attenzione a non penetrare la fascia prima che sia completamente esposta lungo l'intera incisione. Vengono identificati piccoli vasi sanguinanti ed elettrocauterizzati per prevenire il sanguinamento quando viene somministrata l'eparina più avanti nella procedura. Dopo l'esposizione della fascia, la divisione della muscolatura sovrapposta, inclusi il dorsale largo, il trapezio, il serrato anteriore e i romboidi, avviene separatamente, con la formazione di lembi che consente una ricostruzione più facile alla fine della procedura. Vengono inoltre inserite suture di marcatura per aiutare a identificare i bordi anatomici per la ricostruzione muscolare. La sesta costola è identificata e segnata, poiché sarà il punto d'ingresso nella cavità toracica. L'ingresso inizia con la divisione dei muscoli intercostali, la liberazione della costola posteriore dal diaframma e l'osteotomia della sesta costola. I punti di marcatura sono posizionati ovunque per riferimento anatomico.
Una volta esposto il diaframma, si utilizza una cucitrice GIA per dividere il diaframma. Le aderenze polmonari all'aneurisma toracico vengono quindi lisate. Il rene sinistro è stato quindi identificato e mobilitato. Il diaframma viene ulteriormente suddiviso e il pericardio viene esposto. L'arteria e vena renale sinistra e l'arteria mesenterica superiore vengono identificate in preparazione alla dissezione dall'aorta. I rami del tronco celiaco vengono quindi legati e divisi. L'aorta viene seguita verso l'alto, continuando a esporla insieme ai suoi rami per la dissezione e la legatura prima della canulazione all'anastomosi prossimale per bypass atrio-femorale.
I punti di pinzatura per l'anastomosi prossimale sono identificati nell'aorta toracica discendente, e la vena polmonare inferiore sinistra e il legamento vengono mobilitati prima che venga inserita una sutura a cordone per la vena polmonare inferiore sinistra prima della cannulazione prossimale. Viene praticata un'incisione all'estremità inferiore per sezionare e posizionare un cordone per l'arteria femorale, il sito distale del bypass anastomotico. La collocazione di una cannula dalla vena polmonare inferiore sinistra all'arteria femorale permette la perfusione degli arti inferiori mentre l'aorta viene riparata. Una volta raggiunta la corretta esposizione, l'arteria femorale sinistra viene dilatata e vengono cannulate sia la vena polmonare inferiore sinistra che l'arteria femorale sinistra.
La riparazione aortica dopo la canulazione inizia con il clampaggio dell'aorta prossimale prima dell'anastomosi dell'innesto. Durante questa fase, gestiamo il flusso della pompa a 500 mL/h per garantire una perfusione adeguata. L'innesto viene quindi suturato all'estremità prossimale pinzata dell'aorta e, dopo il completamento dell'anastomosi prossimale, viene valutato per eventuali perdite nel sito della sutura. Una volta fissata l'anastomosi prossimale, viene posizionata una seconda pinza sull'aorta toracica discendente media e l'aorta viene divisa longitudinalmente, con la legatura di eventuali vasi luminali sanguinanti. Durante tutta la procedura, manteniamo la pressione distale media a 70 mmHg per garantire una corretta perfusione degli organi, aggiustando se necessario in base al monitoraggio intraoperatorio. Questa tecnica viene proseguita mentre la pinza viene spostata sequenzialmente verso il basso verso il segmento distale dell'aneurisma aortico, con incisione longitudinale continua e legatura dei vasi intraluminali sanguinanti. L'innesto viene quindi misurato alla lunghezza appropriata in preparazione all'anastomosi distale.
La parte successiva dell'intervento riguarda il tempo dell'ischemia viscerale, una parte sensibile al tempo della procedura in cui il segmento viscerale è ischemico a causa della legatura dell'arteria celiachica. Similmente ai passaggi precedenti, l'aorta viene divisa longitudinalmente e intersectata sotto l'arteria renale destra, mentre i vasi sanguinanti intraluminali vengono legati. L'aorta viene quindi trascinata nel sito di impianto e l'innesto viene anastomizzato al segmento distale, con i pledgets suturati nel sito dell'anastomosi per minimizzare il rischio di perdite dopo che l'innesto è stato completamente suturato e valutato. Una volta valutate, le pinze distali vengono rimosse in sequenza, permettendo la perfusione degli arti inferiori e delle visceri. Il tempo totale di pinza per questo intervento è stato di 21 minuti.
Dopo che l'innesto è stato anastomizzato sia prossimalmente che distalmente, il paziente viene decanulato nel sito della vena polmonare inferiore sinistra con la chiusura della sutura a corda della borsa sulla vena polmonare inferiore sinistra, seguita dalla decanulazione dell'arteria femorale sinistra e dalla chiusura dell'incisione all'arteria femorale. Quando l'incisione per l'accesso all'arteria femorale è chiusa, l'innesto aortico viene clampato longitudinalmente e inciso per facilitare l'anastomosi di un punto di uscita laterale. L'anastomosi laterale viene valutata per eventuali perdite una volta completamente suturata. L'arteria celiaca viene quindi anastomizzata capo a capo al segmento distale dell'innesto laterale e valutata per eventuali perdite.
A questo punto, tutte le strutture devascolarizzate transitoriamente vengono rivascolarizzate e il sacco dell'aneurisma viene cucito insieme con l'innesto patente che contiene sangue aortico all'interno. Da lì, vengono riparati l'emisiaframma sinistro e la toracotomia e vengono posizionati drenaggi toracici. La pelle è chiusa, concludendo così la procedura.
Per accennare brevemente alle cure post-operatorie di questi pazienti, i pazienti vengono tenuti intubati per 24 ore fino a raggiungere l'eutermia e essere adeguatamente rianimati. Dopo questo periodo, viene prestata un'attenzione estremamente attenta alla valutazione neurologica del paziente (flessione dell'anca/estensione della gamba), ai parametri vitali (pressione sanguigna) e ai valori ematici completi (Hgb), poiché il rischio di lesioni intraoperatorie del midollo spinale viene valutato con meticolosità dettagliata. Inoltre, lo scarico del liquido cerebrospinale in posizione deve essere gestito con attenzione per garantire una pressione di perfusione arteriosa adeguata al midollo spinale, che normalmente corrisponde a una bassa pressione del liquido cerebrospinale. Lo sdraino del liquido cerebrospinale viene normalmente mantenuto in posizione per i primi due giorni postoperatori, seguito da una prova di clampaggio il secondo o terzo giorno postoperatorio e (supponendo che la prova di clampaggio abbia successo) il drenaggio viene rimosso il terzo o quarto giorno postoperatorio.
Oltre alla morte, la paraplegia secondaria a una cattiva perfusione del midollo spinale è un evento avverso significativo che può verificarsi dopo questo tipo di riparazione aneurismatica aortica. Crawford e colleghi hanno dimostrato che il tempo di pinzatura incrociata e l'estensione aneurismatica sono direttamente associati a questo rischio, e che una lesione completa e permanente del midollo spinale garantisce una mortalità quasi del 100% a cinque annidall'operazione. A causa di questa potenziale morbilità, sono state condotte indagini e ricerche significative per ottimizzare la strategia e proteggere la perfusione. Sebbene fosse stata data molta attenzione all'arteria spinale anteriore (di Adamkiewicz) come principale determinante della perfusione del midollo spinale, il paradigma si è spostato verso un "concetto di rete collaterale" come descritto da Backes, Jacobs, Griepp, Wynn e Acher. 49-52 Queste reti collaterali includono anastomosi delle sottoclavie, segmentari (intercostali e lombari) e interne iliache. In questo modello, finché si mantiene una perfusione adeguata da due di queste arterie, la rottura di una di queste ridurrà minimamente il rischio di danni ischemici permanenti. 53 I tassi di paraplegia differiscono tra la riparazione TAAA aperta e endovascolare, con incidenze riportate di circa l'8,5% per la riparazione aperta e dell'1,7% per le tecniche endovascolari in alcuni studi. Si incoraggia ulteriori ricerche per confermare gli esiti tra le popolazioni, poiché l'approccio dipende dall'anatomia, dalle circostanze e dalle competenze. 55,56
L'aumento delle tecniche endovascolari per la riparazione TAAA ha ridotto le opportunità di formazione per la riparazione chirurgica aperta. Con meno casi aperti eseguiti, i tirocinanti hanno un'esposizione limitata alle competenze complesse richieste per la dissezione aortica e il posizionamento di trapianto. Questa tendenza comporta una carenza di chirurghi esperti nella riparazione aperta, in particolare per i pazienti non adatti agli approcci endovascolari. Affrontare questo problema richiede strategie di addestramento alternative, come simulazioni ad alta fedeltà e programmi centralizzati in centri ad alto volume.
Storicamente, la riparazione degli aneurismi aortici si è evoluta da Rudolph Matas che eseguiva un'endoaneurismorrafia per lesioni arteriose nel 1888, al 1951 con DeBakey e colleghi che tentavano l'escissione e l'aortorrafia su pazienti con aneurismi, fino all'istituzione di programmi attivi di chirurgia aortica in centri medici di tutto il paese. L'innovazione medica nel campo degli aneurismi aortici è recentemente esplosa, con progressi individuali nelle modalità di imaging, innesti, farmaci anticoagulanti e bypass cardiopolmonare che contribuiscono tutti a migliori approcci per risolvere un problema medico con conseguenze quasi fatali in caso di rottura. Inoltre, gli approcci endovascolari sono entrati in primo piano come considerazioni principali nella pianificazione della riparazione di aneurisma aortico senza controindicazioni. 54 Man mano che la nostra imaging, i farmaci, gli strumenti chirurgici e altri attori nella chirurgia aortica continuano a evolversi, continuerà anche la nostra capacità di eseguire queste procedure in modo sicuro ed efficace per i nostri pazienti.
Cucitrice GIA; Innesto protesico.
Niente da rivelare.
Il paziente citato in questo video ha dato il suo consenso informato per essere filmato ed è consapevole che informazioni e immagini saranno pubblicate online.
References
- Tokgoz A, Wang S, Sastry P, et al. Associazione di collagene, elastina, glicosaminoglicani e macrofagi con la resistenza e l'elasticità del materiale tessutale negli aneurismi aortici toracici umani: uno studio uniaxiale sulla tensione. J Biomeccanica Ingegneria. 2022; 144(10):101001. doi:10.1115/1.4054060.
- Kadoglou NP, Liapis CD. Metalloproteinasi della matrice: contributo alla patogenesi, diagnosi, sorveglianza e trattamento degli aneurismi dell'aorta addominale. Curr Med Res Opinion. 2004; 20(4):419-432. doi:10.1185/030079904125003143.
-
Savoia C, Burger D, Nishigaki N, Montezano A, Touyz RM. Angiotensina II e il fenotipo vascolare nell'ipertensione. Esperto Rev Mol Med. 30 marzo 2011; 13:e11. doi:10.1017/S1462399411001815.
- Montezano AC, Touyz RM. Stress ossidativo, Noxs e ipertensione: evidenze sperimentali e controversie cliniche [correzione pubblicata pubblicata pubblicata su Ann Med. 2012 dicembre; 44(8):854-8]. Ann Med. 2012; 44 Supporto 1:S2-S16. doi:10.3109/07853890.2011.653393.
- Garrido AM, KK Lutante. NADPH ossidasi e segnalazione del recettore dell'angiotensina II. Endocrinolo a cellule mol. 2009; 302(2):148-158. doi:10.1016/j.mce.2008.11.003.
- Saratzis A, Bown MJ. La base genetica della malattia aneurismatica aortica. Heart. 2014; 100(12):916-922. doi:10.1136/heartjnl-2013-305130.
- Pleumeekers HJ, Hoes AW, van der Does E, et al. Aneurismi dell'aorta addominale negli anziani. Lo Studio di Rotterdam. Am J Epidemiol. 1995; 142(12):1291-1299. doi:10.1093/oxfordjournals.aje.a117596.
- Boese AC, Chang L, Yin KJ, Chen YE, Lee JP, Hamblin MH. Differenze di sesso negli aneurismi dell'aorta addominale. Am J Physiol Heart Circ Physiol. 2018; 314(6):H1137-H1152. doi:10.1152/ajpheart.00519.2017.
- Ghosh A, Pechota A, Coleman D, Upchurch GR Jr, Eliason JL. La secrezione di MMP2 e MMP9 indotta dal fumo di sigaretta dalle cellule lisci vascolari aortiche è mediata tramite la via Jak/Stat. Hum Pathol. 2015; 46(2):284-294. doi:10.1016/j.humpath.2014.11.003.
-
Wang S, Zhang C, Zhang M, et al. L'attivazione della proteina chinasi α2 attivata da AMP da parte della nicotina innesca la formazione di aneurismi dell'aorta addominale in vivo. Medicina naturale. giugno 2012; 18(6):902-10. doi:10.1038/nm.2711.
- Johansson G, Markström U, Swedenborg J. Aneurismi aortici toracici rotti: uno studio sui tassi di incidenza e mortalità. J Vasc Surg. 1995; 21(6):985-988. doi:10.1016/s0741-5214(95)70227-x.
- Task Force dei Servizi Preventivi degli Stati Uniti. Screening per l'aneurisma dell'aorta addominale: dichiarazione di raccomandazione della Task Force dei Servizi Preventivi degli Stati Uniti. JAMA. 2019; 322(22):2211–2218. doi:10.1001/jama.2019.18928.
- Keisler B, Carter C. Aneurisma aortico addominale. Sono un medico familiare. 2015; 91(8):538-543.
- Hirsch AT, Haskal ZJ, Hertzer NR, et al. ACC/AHA 2005 Linee guida di pratica per la gestione dei pazienti con malattia arteriosa periferica (arti inferiori, renale, mesenterica e aortica addominale): un rapporto collaborativo dell'American Association for Vascular Surgery/Society for Vascular Surgery, Society for Cardiovascular Angiography and Interventions, Society for Vascular Medicine and Biology, Society of Interventional Radiology, e il Gruppo di Lavoro ACC/AHA sulle Linee Guida di Pratica (Comitato di Redazione per Sviluppare Linee Guida per la Gestione dei Pazienti con Malattie Arteriali Periferiche): approvato dall'American Association of Cardiovascular and Pulmonary Rehabilitation; Istituto Nazionale per il Cuore, i Polmoni e il Sangue; Società per l'Infermieristica Vascolare; Consenso Inter-Società Transatlantico; e Vascolar Disease Foundation. Tiraggio. 2006; 113(11):e463-e654. doi:10.1161/CIRCULATIONAHA.106.174526.
- Hiratzka LF, Bakris GL, Beckman JA, et al. 2010 linee guida ACCF/AHA/AATS/ACR/ASA/SCA/SCAI/SIR/STS/SVM per la diagnosi e gestione dei pazienti con malattia aortica toracica: un rapporto del gruppo di lavoro sulla pratica delle linee guida della American College of Cardiology Foundation/American Heart Association, American Association for Thoracic Surgery, American College of Radiology, American Stroke Association, Society of Cardiovascular Anesthesiologists, Society for Cardiovascular Angiography and Interventions, Society of Interventional Radiology, Society of Thoracic Surgeons e Society for Vascular Medicine [correzione pubblicata pubblicata pubblicata su Circulation. 27 luglio 2010; 122(4):e410]. Tiraggio. 2010; 121(13):e266-e369. doi:10.1161/CIR.0b013e3181d4739e.
- Coady MA, Davies RR, Roberts M, et al. Modelli familiari degli aneurismi aortici toracici. Archichirurgia. 1999; 134(4):361-367. doi:10.1001/archsurg.134.4.361.
- Albornoz G, Coady MA, Roberts M, et al. Aneurismi aortici toracici familiari e dissecazioni—incidenza, modalità di ereditarietà e schemi fenotipici. Ann Thorac Surg. 2006; 82(4):1400-1405. doi:10.1016/j.athoracsur.2006.04.098.
- Akkersdijk GJ, van Bockel JH. Aneurisma aortico addominale rotto: diagnosi iniziale errata e effetto sul trattamento. Eur J Surg. 1998; 164(1):29-34. doi:10.1080/110241598750004922.
- Gloviczki P, Pairolero PC, Mucha P Jr, et al. Aneurismi aortici addominali rotti: la riparazione non va negata. J Vasc Surg. 1992; 15(5):851-859.
- Meijer CA, Stijnen T, Wasser MN, et al. Doxiciclina per la stabilizzazione degli aneurismi dell'aorta addominale: uno studio randomizzato. Ann Intern Med. 2013; 159(12):815-823. doi:10.7326/0003-4819-159-12-201312170-00007.
- Baxter BT, Matsumura J, Curci JA, et al. Effetto della Doxiciclina sulla crescita degli aneurismi tra pazienti con piccoli aneurismi dell'aorta addominale infrarenale: uno studio clinico randomizzato. JAMA. 2020; 323(20):2029-2038. doi:10.1001/jama.2020.5230.
- Baxter BT, Matsumura J, Curci J, et al. Trattamento non invasivo dell'aneurisma aortico addominale (N-TA(3)CT): progettazione di uno studio clinico randomizzato di fase IIb, controllato con placebo, in doppio cieco, con doxiciclina per la riduzione della crescita di un piccolo aneurisma aortico addominale. Processi contemporanei sul Clin. 2016;48:91-98. doi:10.1016/j.cct.2016.03.008.
- Davies RR, Goldstein LJ, Coady MA, et al. Tassi annuali di rottura o dissezione per aneurismi aortici toracici: previsione semplice basata sulla dimensione. Ann Thorac Surg. 2002; 73(1):17-28. doi:10.1016/s0003-4975(01)03236-2.
- Walsh SR, Tang TY, Sadat U, et al. Stent endovascolare versus chirurgia aperta per la malattia aortica toracica: revisione sistematica e meta-analisi dei risultati perioperatori. J Vasc Surg. 2008; 47(5):1094-1098. doi:10.1016/j.jvs.2007.09.062.
- Cheng D, Martin J, Shennib H, et al. Riparazione aortica endovascolare versus riparazione chirurgica aperta per la malattia aortica toracica discendente: una revisione sistematica e meta-analisi di studi comparativi. J Am Coll Cardiol. 2010; 55(10):986-1001. doi:10.1016/j.jacc.2009.11.047.
- Abraha I, Romagnoli C, Montedori A, Cirocchi R. Innesto dello stent toracico contro chirurgia per aneurisma toracico. Cochrane Database Syst Rev. 2013; (9):CD006796. Pubblicato l'11 settembre 2013. doi:10.1002/14651858.CD006796.pub3.
- Matsumura JS, Cambria RP, Dake MD, et al. Studio clinico controllato internazionale sulla riparazione endovascolare dell'aneurisma endovascolare toracico con l'innesto endovascolare Zenith TX2: risultati di 1 anno. J Vasc Surg. 2008; 47(2):247-257. doi:10.1016/j.jvs.2007.10.032.
- Bavaria JE, Appoo JJ, Makaroun MS, et al. Innesto endovascolare dello stent versus riparazione chirurgica aperta degli aneurismi dell'aorta toracica discendente in pazienti a basso rischio: uno studio comparativo multicentrico. J Thorac Cardiovasc Surg. 2007; 133(2):369-377. doi:10.1016/j.jtcvs.2006.07.040.
- Svensson LG, Crawford ES, Hess KR, Coselli JS, Safi HJ. Esperienza con 1509 pazienti sottoposti a interventi di toracoaddominale dell'aorta. Giudice Vasc Surg. 1993; 17(2):357-370.
- Greenberg RK, Lu Q, Roselli EE, et al. Analisi contemporanea della riparazione degli aneurisma toracico e toracoaddominale discendente: un confronto tra tecniche endovascolari e aperte. Circolazione. 2008; 118(8):808-817. doi:10.1161/CIRCULATIONAHA.108.769695.
- Jackson BM, Carpenter JP, Fairman RM, et al. Esclusione anatomica dalla riparazione endovascolare dell'aneurisma aortico toracico. J Vasc Surg. 2007; 45(4):662-666. doi:10.1016/j.jvs.2006.12.062.
- Gli investigatori del processo EVAR nel Regno Unito, Greenhalgh RM, Brown LC, et al. Riparazione endovascolare vs riparazione aperta dell'aneurisma aortico addominale. N Engl J Med. 2010; 362(20):1863-1871. doi:10.1056/NEJMoa0909305.
- Bulder RMA, Bastiaannet E, Hamming JF, Lindeman JHN. Meta-analisi della sopravvivenza a lungo termine dopo la riparazione endovascolare o aperta elettiva dell'aneurisma dell'aorta addominale. Br J Surg. 2019; 106(5):523-533. doi:10.1002/bjs.11123.
- Powell JT, Sweeting MJ, Ulug P, e altri. Meta-analisi dei dati individuali di pazienti provenienti da studi EVAR-1, DREAM, OVER e ACE confrontando gli esiti della riparazione endovascolare o aperta per aneurisma aortico addominale su 5 anni [correzione pubblicata appare su Br J Surg. 2018 agosto 2018; 105(9):1222. doi:10.1002/bjs.10928]. Br J Surg. 2017; 104(3):166-178. doi:10.1002/bjs.10430.
- Paravastu SC, Jayarajasingam R, Cottam R, Palfreyman SJ, Michaels JA, Thomas SM. Riparazione endovascolare dell'aneurisma dell'aorta addominale. Cochrane Database Syst Rev. 2014; 2014(1):CD004178. Pubblicato il 23 gennaio 2014. doi:10.1002/14651858.CD004178.pub2.
- Stather PW, Sidloff D, Dattani N, Choke E, Bown MJ, Sayers RD. Revisione sistematica e meta-analisi degli esiti precoci e tardi della riparazione aperta ed endovascolare dell'aneurisma aortico addominale. Br J Surg. 2013; 100(7):863-872. doi:10.1002/bjs.9101.
- Lederle FA, Freischlag JA, Kyriakides TC, et al. Confronto a lungo termine tra la riparazione endovascolare e aperta dell'aneurisma dell'aorta addominale. N Engl J Med. 2012; 367(21):1988-1997. doi:10.1056/NEJMoa1207481.
- Partecipanti allo studio EVAR. Riparazione endovascolare dell'aneurisma versus riparazione aperta in pazienti con aneurisma dell'aorta addominale (studio EVAR 1): studio controllato randomizzato. Lancet. 2005; 365(9478):2179-2186. doi:10.1016/S0140-6736(05)66627-5.
- De Bruin JL, Baas AF, Buth J, et al. Esito a lungo termine della riparazione aperta o endovascolare dell'aneurisma aortico addominale. N Engl J Med. 2010; 362(20):1881-1889. doi:10.1056/NEJMoa0909499.
- Blankensteijn JD, de Jong SE, Prinssen M, et al. Esiti a due anni dopo la riparazione convenzionale o endovascolare degli aneurismi dell'aorta addominale. N Engl J Med. 2005; 352(23):2398-2405. doi:10.1056/NEJMoa051255.
- Brown LC, Thompson SG, Greenhalgh RM, Powell JT; Partecipanti allo studio di riparazione dell'aneurisma endovascolare. Incidenza di eventi cardiovascolari e morte dopo la riparazione aperta o endovascolare dell'aneurisma dell'aorta addominale nello studio randomizzato EVAR 1. Br J Surg. 2011; 98(7):935-942. doi:10.1002/bjs.7485.
- Becquemin JP, Pillet JC, Lescalie F, e altri. Uno studio controllato randomizzato sulla riparazione endovascolare di aneurisma rispetto alla chirurgia aperta per aneurismi aortici addominali in pazienti a basso o moderato rischio. J Vasc Surg. 2011; 53(5):1167-1173.e1. doi:10.1016/j.jvs.2010.10.124.
- Siracuse JJ, Gill HL, Graham AR, et al. Sicurezza comparativa della riparazione chirurgica endovascolare e aperta degli aneurismi dell'aorta addominale in pazienti maschi a basso rischio. J Vasc Surg. 2014; 60(5):1154-1158. doi:10.1016/j.jvs.2014.05.018.
- Vallabhaneni R, Farber MA, Schneider F, Ricco JB. Dibattito: se i pazienti giovani e a buon rischio debbano essere trattati con la riparazione endovascolare dell'aneurisma aortico addominale. J Vasc Surg. 2013; 58(6):1709-1715. doi:10.1016/j.jvs.2013.09.017.
- Sandford RM, Choke E, Bown MJ, Sayers RD. Qual è la migliore opzione per la riparazione elettiva di un aneurisma dell'aorta addominale in un paziente giovane in forma? Eur J Vasc Endovasc Surg. 2014; 47(1):13-18. doi:10.1016/j.ejvs.2013.09.014.
- Lee K, Tang E, Dubois L, Power AH, DeRose G, Forbes TL. La durata e la sopravvivenza sono simili dopo la riparazione endovascolare elettiva e aperta degli aneurismi dell'aorta addominale nei pazienti più giovani. J Vasc Surg. 2015; 61(3):636-641. doi:10.1016/j.jvs.2014.10.012.
- Siracuse JJ, Schermerhorn ML, Meltzer AJ, et al. Confronto degli esiti dopo la riparazione endovascolare e aperta degli aneurismi dell'aorta addominale in pazienti a basso rischio. Br J Surg. 2016; 103(8):989-994. doi:10.1002/bjs.10139.
- Crawford ES, Crawford JL, Safi HJ, et al. Aneurismi toracoaddominali dell'aorta: fattori preoperatori e intraoperatori che determinano i risultati immediati e a lungo termine delle operazioni in 605 pazienti. J Vasc Surg. 1986; 3(3):389-404. doi:10.1067/mva.1986.avs0030389.
- Backes WH, Nijenhuis RJ, Mess WH, Wilmink FA, Schurink GW, Jacobs MJ. Angiografia a risonanza magnetica dell'apporto collaterale di sangue al midollo spinale in pazienti con aneurisma toracico e toracoaddominale dell'aorta. J Vasc Surg. agosto 2008; 48(2):261–271. doi:10.1016/j.jvs.2008.03.015.
- Jacobs MJ, de Mol BA, Elenbaas T, e altri. Apporto di sangue al midollo spinale in pazienti con aneurismi aortico-aortico-toracoaddominali. J Vasc Surg. Gennaio 2002; 35(1):30–37. doi:10.1067/mva.2002.120041.
- Griepp EB, Griepp RB. Il concetto di rete collaterale: minimizzare la paraplegia secondaria alla resezione dell'aneurisma aortico toracoaddominale. Tex Heart Inst J. 2010; 37(6):672–674.
- Wynn MM, Acher CW. Una teoria moderna dell'ischemia/lesione del midollo spinale nella chirurgia aortica toracoaddominale e le sue implicazioni per la prevenzione della paralisi. J Cardiotoracico Anesto vasco. 2014; 28(4):1088-1099. doi:10.1053/j.jvca.2013.12.015.
- Eagleton MJ, Shah S, Petkosevek D, Mastracci TM, Greenberg RK. La patenza delle arterie ipogastriche e succlavie influisce sull'insorgenza e il recupero dell'ischemia midollare associata all'endoinnesto aortico. J Vasc Surg. 2014; 59(1):89-94. doi:10.1016/j.jvs.2013.07.007.
- Cooley, procuratore distrettuale. Una breve storia di chirurgia per aneurisma aortico. Aorta (Stamford). 2013; 1(1):1-3. Pubblicato il 1° giugno 2013. doi:10.12945/j.aorta.2013.12.006.
- Wongkornrat W, Yamamoto S, Sekine Y, et al. Predictori della paraplegia con riparazione attuale dell'aneurisma aortico toracoaddominale. Cardiovasco Asiatico Thorac Ann. 2015; 23(4):406-411. doi:10.1177/0218492314549563.
- Kotelis D, Geisbüsch P, von Tengg-Kobligk H, Allenberg JR, Böckler D. Paraplegie nach endovaskulärer therapie der thorakalen und thorakoabdominellen [Paraplegia dopo la riparazione endovascolare dell'aorta toracica e toracoaddominale]. Zentralbl Chir. 2008; 133(4):338-343. doi:10.1055/s-2008-1076903.
- Frederick JR, Woo YJ. Aneurisma toracoaddominale dell'aorta. Ann Cardiotoracica Chirurgica. 2012; 1(3):277-285. doi:10.3978/j.issn.2225-319X.2012.09.01.
Cite this article
Del Re A, Mohebali J, Patel VI. Riparazione dell'aneurisma toracoaddominale dell'aorta. J Med Insight. 2024; 2024(109). doi:10.24296/jomi/109.


